Nhà sản xuất
Janssen-Cilag
Nhà phân phối
DKSH
Thành phần
Mỗi lọ: Bortezomib (dưới dạng mannitol boronic ester) 1mg hoặc 3,5mg.
Mô tả
Bột hoặc bánh màu trắng đến trắng ngà.
Dược lực học
Nhóm dược lý trị liệu: Thuốc chống ung thư, các thuốc chống ung thư khác, mã ATC: L01XX32.
Cơ chế tác dụng
Bortezomib là một chất ức chế proteasome. Thuốc được thiết kế đặc biệt để ức chế hoạt tính kiểu-chymotrypsin của proteasome 26S trong tế bào động vật có vú. Proteasome 26S là một phức hợp protein lớn gây tiêu hủy các protein được ubiquitin hóa. Con đường proteasome - ubiquitin đóng vai trò thiết yếu trong việc điều hòa số lượng các protein cụ thể, do đó duy trì ổn định nội môi trong tế bào. Ức chế proteasome 26S làm ngăn ngừa sự ly giải các protein đích này và ảnh hưởng đến nhiều dòng thác tín hiệu bên trong tế bào, cuối cùng dẫn đến chết tế bào ung thư.
Bortezomib có tính chọn lọc cao với proteasome. Ở nồng độ 10 μM, bortezomib không ức chế bất kỳ loại receptor và protease nào trên một phổ rộng các loại được sàng lọc và tác dụng trên proteasome chọn lọc hơn 1.500 lần so với enzyme ưu tiên tiếp theo của thuốc. Động học của quá trình ức chế proteasome đã được đánh giá in vitro, và cho thấy bortezomib tách ra khỏi proteasome với t½ là 20 phút, do đó chứng minh sự ức chế proteasome bởi bortezomib là có thể hồi phục.
Sự ức chế proteasome qua trung gian của bortezomib ảnh hưởng đến các tế bào ung thư bằng nhiều cách, bao gồm nhưng không giới hạn, trong việc thay đổi các protein điều hòa, là những protein điều khiển tiến triển của chu trình tế bào và hoạt hóa yếu tố nhân kappa B (NF-kB). Ức chế proteasome dẫn đến việc ngừng chu trình tế bào và chết tế bào theo chương trình (apoptosis). NF- kB là một yếu tố sao mã mà sự hoạt hóa yếu tố này là cần thiết trên nhiều phương diện của quá trình sinh khối u, bao gồm sự tăng trưởng và sống còn của tế bào, sự hình thành mạch máu, sự tương tác tế bào - tế bào và sự di căn. Trong u tủy xương, bortezomib ảnh hưởng đến khả năng các tế bào u tủy xương tương tác với vi môi trường ở tủy xương.
Các thí nghiệm đã chứng minh rằng bortezomib có độc tính với nhiều loại tế bào ung thư và so với các tế bào bình thường, các tế bào ung thư này nhạy cảm hơn với tác dụng ức chế proteasome dẫn đến chết tế bào theo chương trình. Bortezomib làm giảm sự phát triển khối u in vivo ở nhiều mô hình tiền lâm sàng trên khối u, bao gồm đa u tủy xương.
Dữ liệu từ các mô hình thực nghiệm in vitro, ex-vivo và trên động vật với bortezomib cho thấy rằng thuốc làm tăng biệt hóa và hoạt động của tế bào tạo xương và ức chế chức năng tế bào hủy xương. Những tác dụng này đã được quan sát ở những bệnh nhân đa u tủy xương bị ảnh hưởng bởi một tình trạng hủy xương bệnh lý tiến triển và được điều trị với bortezomib.
Hiệu quả lâm sàng ở bệnh đa u tủy chưa được điều trị trước đó
Một nghiên cứu lâm sàng nhãn mở pha III, tiến cứu, quốc tế, ngẫu nhiên (tỷ lệ 1:1), (MMY-3002 VISTA) trên 682 bệnh nhân đã được tiến hành để xác định liệu VELCADE (1,3 mg/m2 tiêm tĩnh mạch) kết hợp với melphalan (9 mg/m2) và prednisone (60 mg/m2) có cải thiện thời gian đến khi tiến triển bệnh (time to progression - TTP) khi so sánh với melphalan (9 mg/m2) và prednisone (60 mg/m2) ở bệnh nhân đa u tủy không được điều trị trước đó. Điều trị được thực hiện tối đa 9 chu kỳ (khoảng 54 tuần) và được ngừng sớm khi có tiến triển bệnh hoặc độc tính không chấp nhận được. Trung vị tuổi bệnh nhân trong nghiên cứu là 71 tuổi, 50% là nam giới, 88% là người da trắng và trung vị chỉ số thể trạng Karnofsky của bệnh nhân là 80. Các bệnh nhân có u tủy IgG/IgA/chuỗi nhẹ ở 63%/25%/ 8% các trường hợp, trung vị hemoglobin là 105 g/L, và trung vị số lượng tiểu cầu là 221,5 x 109/L. Tỷ lệ bệnh nhân có độ thanh thải creatinine ≤ 30 mL/phút là tương tự nhau (3% ở mỗi nhóm).
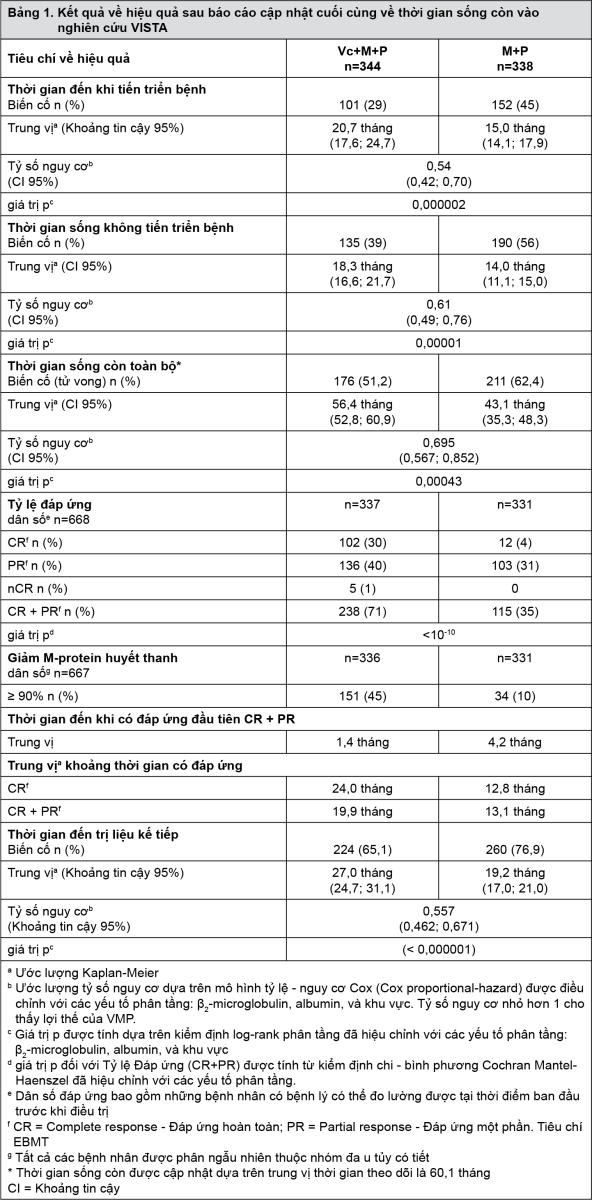
Tại thời điểm thực hiện phân tích tạm thời được xác định trước trong đề cương nghiên cứu, tiêu chí chính, thời gian đến khi tiến triển bệnh, đã đạt được và bệnh nhân ở nhóm M+P được đề nghị điều trị với phác đồ Vc+M+P. Trung vị thời gian theo dõi là 16,3 tháng. Báo cáo cập nhật cuối cùng về thời gian sống còn được thực hiện với trung vị thời gian theo dõi là 60,1 tháng. Đã quan sát thấy lợi ích về thời gian sống còn có ý nghĩa thống kê ở nhóm điều trị Vc+M+P (HR = 0,695; p = 0,00043) mặc dù các trị liệu tiếp sau đó bao gồm phác đồ có VELCADE. Trung vị thời gian sống còn của nhóm điều trị Vc+M+P là 56,4 tháng so với 43,1 tháng ở nhóm điều trị M+P. Các kết quả về hiệu quả được trình bày trong Bảng 1.
- xem Bảng 1.
Bệnh nhân đủ điều kiện để ghép tế bào gốc
Hai thử nghiệm lâm sàng pha III ngẫu nhiên, nhãn mở, đa trung tâm (IFM- 2005-01, MMY- 3010) được tiến hành để chứng minh hiệu quả và an toàn của VELCADE phối hợp với các thuốc khác trong phác đồ hai và ba thuốc, như là điều trị tấn công trước khi ghép tế bào gốc ở những bệnh nhân đa u tủy chưa được điều trị trước đó.
Trong nghiên cứu IFM- 2005-01 VELCADE kết hợp với dexamethasone [VcDx, n = 240] được so sánh với vincristine – doxorubicin - dexamethasone [VDDx, n = 242]. Bệnh nhân trong nhóm VcDx đã được điều trị 4 chu kỳ 21 ngày, mỗi chu kỳ gồm VELCADE (1,3 mg/m2 dùng đường tĩnh mạch hai lần mỗi tuần vào các ngày 1, 4, 8 và 11) và dexamethasone uống (40 mg/ngày trong các ngày 1 đến 4 và các ngày 9 đến 12, ở các Chu kỳ 1 và 2, và trong các ngày 1 đến 4 trong các Chu kỳ 3 và 4).
Trong các nhóm dùng VDDx và VcDx, tương ứng có 198 (82%) bệnh nhân và 208 (87%) bệnh nhân được ghép tế bào gốc tự thân; phần lớn bệnh nhân đã trải qua một lần ghép. Đặc điểm nhân khẩu học và đặc điểm bệnh lý trước điều trị của bệnh nhân là tương tự nhau giữa các nhóm điều trị. Trung vị tuổi của bệnh nhân trong nghiên cứu là 57 tuổi, 55% là nam giới và 48% bệnh nhân có nguy cơ cao về di truyền tế bào. Trung vị thời gian điều trị là 13 tuần đối với nhóm VDDx và 11 tuần đối với nhóm VcDx. Trung vị số chu kỳ nhận được cho cả hai nhóm là 4 chu kỳ.
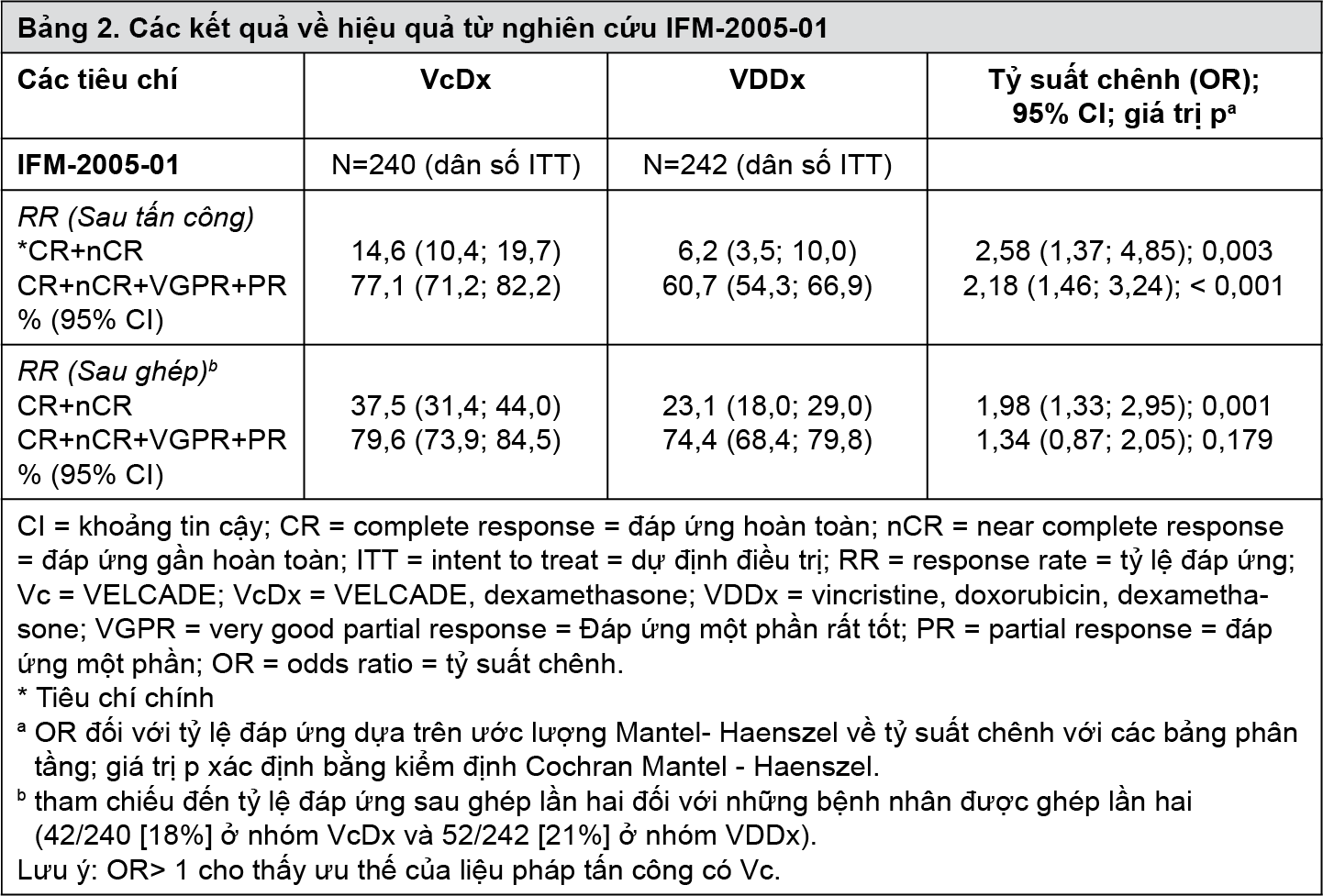
Tiêu chí hiệu quả chính của nghiên cứu là tỷ lệ đáp ứng sau điều trị tấn công (CR + nCR). Sự khác biệt có ý nghĩa thống kê về CR + nCR được quan sát thấy có lợi cho nhóm VELCADE kết hợp với dexamethasone. Các tiêu chí hiệu quả phụ bao gồm tỷ lệ đáp ứng sau ghép (CR + nCR, CR + nCR + VGPR + PR), sống không tiến triển bệnh và sống còn toàn bộ. Các kết quả về hiệu quả chính được trình bày trong Bảng 2.
- xem Bảng 2.
Trong nghiên cứu MMY-3010 điều trị tấn công bằng VELCADE kết hợp với thalidomide và dexamethasone [VcTDx, n = 130] được so sánh với kết hợp thalidomide- dexamethasone [TDx, n = 127]. Bệnh nhân trong nhóm VcTDx nhận được 6 chu kỳ điều trị 4 tuần, mỗi chu kỳ gồm VELCADE (1,3 mg/m2 dùng hai lần mỗi tuần vào các ngày 1, 4, 8 và 11, sau đó là 17 ngày nghỉ từ ngày 12 đến ngày 28), dexamethasone (40 mg dùng đường uống vào các ngày 1 đến 4 và các ngày 8 đến 11), và thalidomide (dùng đường uống 50 mg mỗi ngày vào các ngày 1 - 14, tăng lên đến 100 mg trong các ngày 15 - 28 và sau đó đến 200 mg mỗi ngày).
105 (81%) bệnh nhân và 78 (61%) bệnh nhân được ghép tế bào gốc tự thân một lần tương ứng trong các nhóm VcTDx và TDx . Đặc điểm nhân khẩu học và bệnh lý trước điều trị của bệnh nhân là tương tự giữa các nhóm điều trị. Bệnh nhân trong nhóm VcTDx và TDx lần lượt có giá trị trung vị tuổi là 57 so với 56 tuổi, 99% so với 98% bệnh nhân là người da trắng, và 58% so với 54% là nam giới. Trong nhóm VcTDx, 12% bệnh nhân được phân loại nguy cơ cao về di truyền tế bào so với 16% bệnh nhân trong nhóm TDx. Trung vị thời gian điều trị là 24,0 tuần và trung vị số chu kỳ điều trị nhận được là 6,0 và nhất quán giữa các nhóm điều trị.
Tiêu chí hiệu quả chính của nghiên cứu là tỷ lệ đáp ứng sau điều trị tấn công và sau ghép (CR + nCR). Sự khác biệt có ý nghĩa thống kê về CR + nCR được quan sát thấy có lợi cho nhóm VELCADE kết hợp với dexamethasone và thalidomide. Các tiêu chí hiệu quả phụ bao gồm sống không tiến triển bệnh và sống còn toàn bộ. Các kết quả về hiệu quả chính được trình bày trong Bảng 3.
- xem Bảng 3.

Hiệu quả lâm sàng trong điều trị đa u tủy tái phát hoặc kháng trị
An toàn và hiệu quả của VELCADE (tiêm tĩnh mạch) được đánh giá trong 2 nghiên cứu ở liều khuyến cáo là 1,3 mg/m2: một nghiên cứu pha III ngẫu nhiên so sánh (APEX), so với dexamethasone (Dex), trên 669 bệnh nhân đa u tủy tái phát hoặc kháng trị đã dùng 1 - 3 trị liệu trước đó và một nghiên cứu pha II đơn nhóm trên 202 bệnh nhân bị đa u tủy tái phát và kháng trị, những người đã dùng ít nhất 2 trị liệu trước đó và đang tiến triển bệnh trong liệu trình điều trị gần nhất.
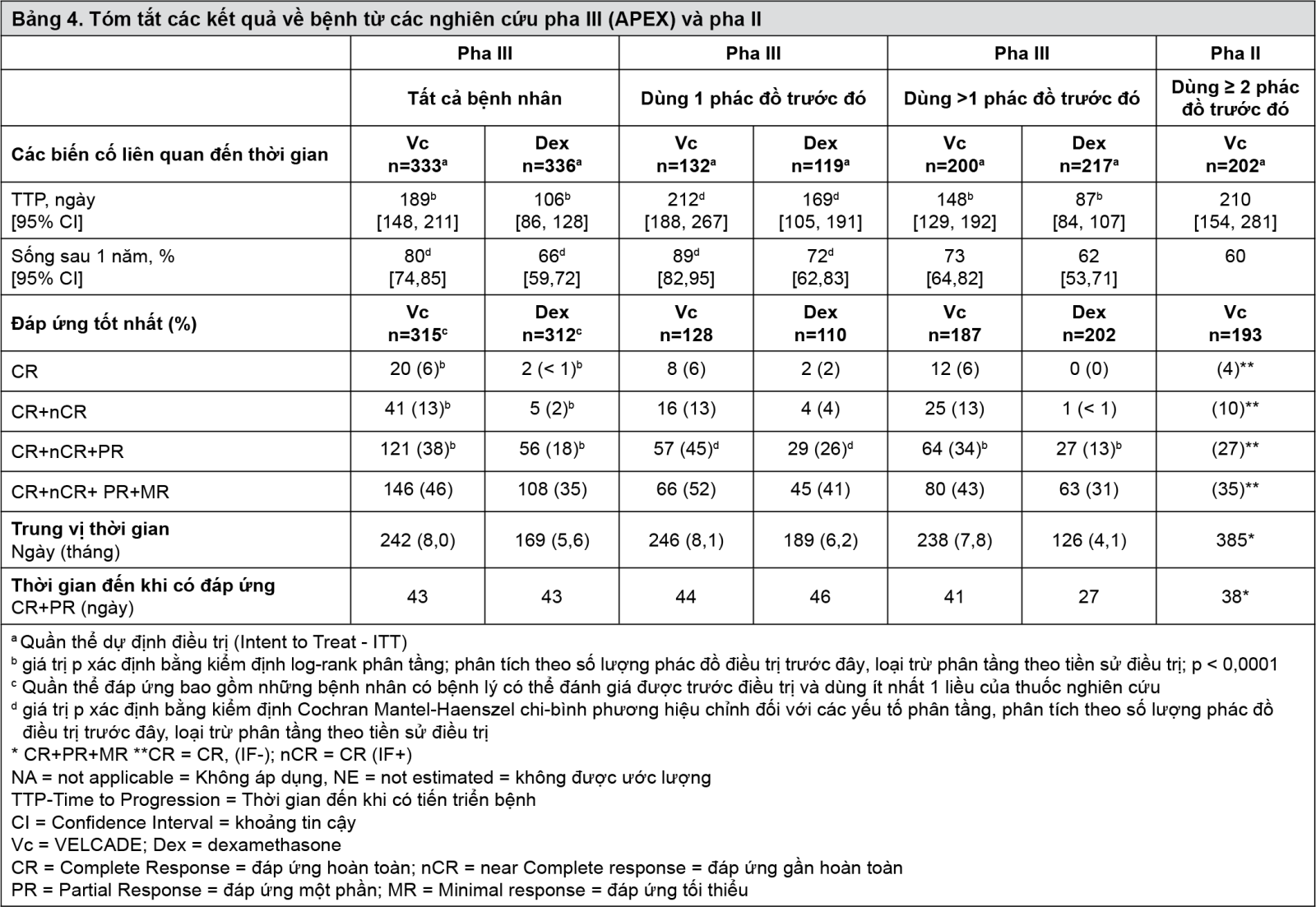
Trong nghiên cứu pha III, điều trị bằng VELCADE đã kéo dài đáng kể thời gian đến khi bệnh tiến triển, thời gian sống còn kéo dài đáng kể và tỷ lệ đáp ứng cao hơn đáng kể so với điều trị bằng dexamethasone (xem Bảng 4), ở tất cả bệnh nhân cũng như ở bệnh nhân dùng 1 trị liệu trước đó. Theo kết quả của một phân tích tạm thời theo kế hoạch, nhóm dexamethasone bị ngừng điều trị theo đề nghị của ủy ban giám sát dữ liệu và tất cả bệnh nhân được phân ngẫu nhiên vào nhóm dùng dexamethasone sau đó được cho dùng VELCADE, bất kể tình trạng bệnh lý. Do sự bắt chéo nhóm sớm này, trung vị thời gian theo dõi sống còn ở bệnh nhân là 8,3 tháng. Cả những bệnh nhân kháng trị với phác đồ trước đó và những người không kháng trị, thời gian sống còn toàn bộ lâu hơn đáng kể và tỷ lệ đáp ứng cao hơn đáng kể ở nhóm VELCADE.
Trong số 669 bệnh nhân tham gia nghiên cứu, 245 (37%) có tuổi từ 65 tuổi trở lên. Các thông số về đáp ứng cũng như TTP vẫn tốt hơn đáng kể ở nhóm VELCADE, không phụ thuộc vào tuổi. Bất kể nồng độ β2- microglobulin ở thời điểm ban đầu, tất cả các thông số về hiệu quả (thời gian đến khi có tiến triển bệnh và sống còn toàn bộ, cũng như tỷ lệ đáp ứng) được cải thiện đáng kể trên nhóm dùng VELCADE.
Trong nhóm kháng trị của một nghiên cứu pha II, các đáp ứng được xác định bởi một hội đồng đánh giá độc lập và tiêu chuẩn xác định đáp ứng là của Nhóm Ghép Tủy Châu Âu (European Bone Marrow Transplant Group). Trung vị thời gian sống còn của tất cả bệnh nhân tham gia nghiên cứu là 17 tháng (trong khoảng <1 đến 36+ tháng). Thời gian sống còn này lớn hơn trung vị thời gian sống còn mà được các nghiên cứu viên lâm sàng cố vấn dự đoán cho một dân số bệnh nhân tương tự từ 6 đến 9 tháng. Bằng cách phân tích đa biến, tỷ lệ đáp ứng là độc lập với thể u tủy, chỉ số toàn trạng, tình trạng mất nhiễm sắc thể số 13, hoặc số lượng hoặc loại trị liệu trước đây. Bệnh nhân đã được điều trị 2 đến 3 phác đồ điều trị trước có tỷ lệ đáp ứng là 32% (10/32) và những bệnh nhân được điều trị trước đó trên 7 phác đồ có tỷ lệ đáp ứng là 31% (21/67).
- xem Bảng 4.
Trong một nghiên cứu pha II, những bệnh nhân không có đáp ứng tối ưu với đơn trị liệu bằng VELCADE đã có thể nhận được liều cao dexamethasone kết hợp với VELCADE. Phác đồ này cho phép bệnh nhân dùng dexamethasone nếu họ không có đáp ứng tối ưu với VELCADE. Tổng cộng có 74 bệnh nhân có thể đánh giá được, đã dùng dexamethasone phối hợp với VELCADE. 18 phần trăm bệnh nhân đạt được đáp ứng, hoặc đã có đáp ứng cải thiện [MR (11%) hoặc PR (7%)] với điều trị kết hợp.
Hiệu quả lâm sàng của VELCADE tiêm dưới da ở bệnh nhân u đa tủy tái phát/kháng trị
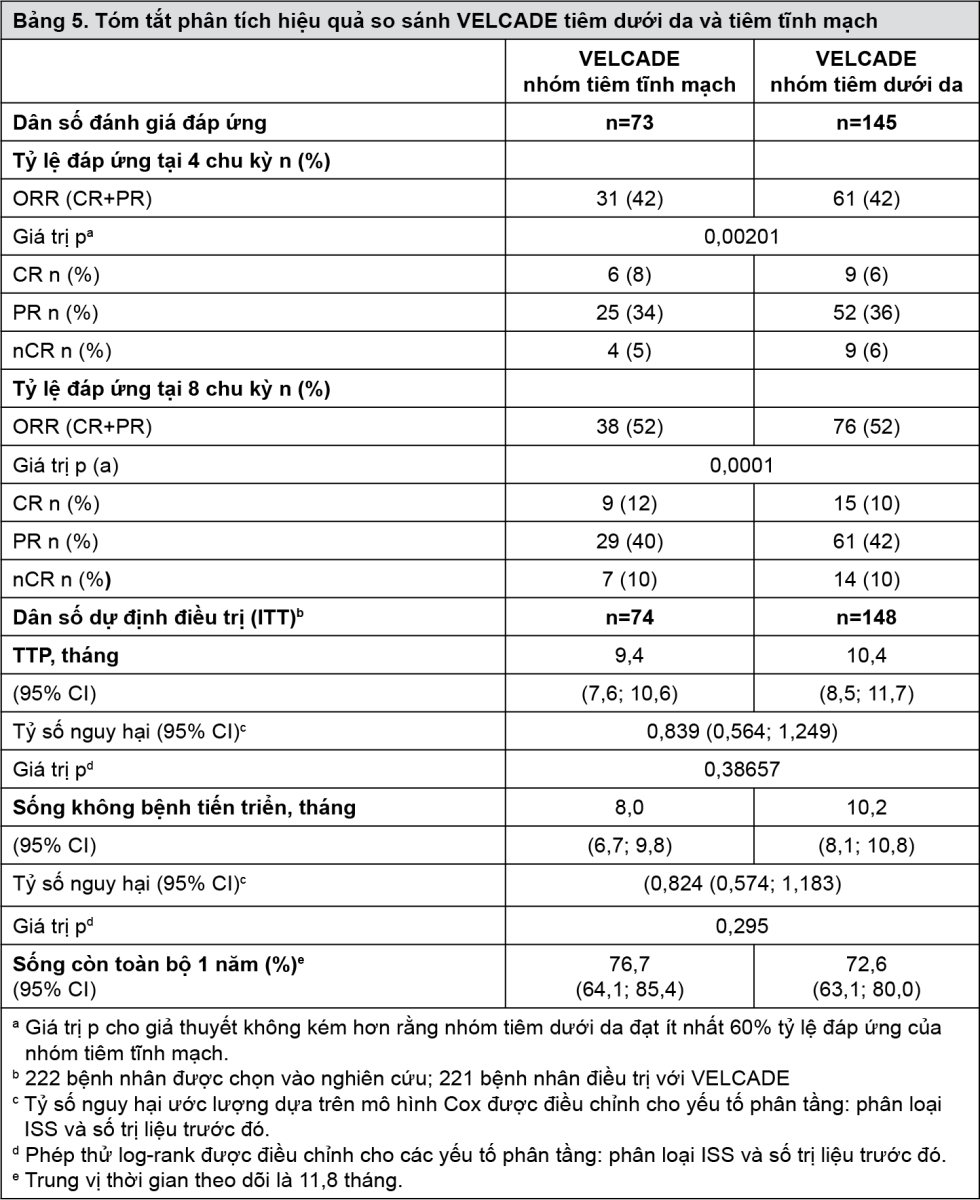
Trong một nghiên cứu không so sánh kém hơn (non-inferiority study) pha III, nhãn mở, ngẫu nhiên so sánh hiệu quả và an toàn của VELCADE tiêm dưới da với tiêm tĩnh mạch. Nghiên cứu bao gồm 222 bệnh nhân u đa tủy tái phát/kháng trị đã được chọn ngẫu nhiên với tỷ lệ 2:1 để nhận VELCADE 1,3 mg/m2 qua đường tiêm dưới da hoặc tiêm tĩnh mạch trong 8 chu kỳ. Bệnh nhân mà không đạt được đáp ứng tối ưu (thấp hơn đáp ứng hoàn toàn [CR]) với VELCADE đơn trị liệu sau 4 chu kỳ đã được dùng dexamethasone 20 mg mỗi ngày vào ngày dùng VELCADE và ngày sau đó. Bệnh nhân có bệnh lý thần kinh ngoại vi Độ ≥ 2 hoặc số lượng tiểu cầu <50.000/μL tại thời điểm trước điều trị đã bị loại khỏi nghiên cứu. Đã đánh giá đáp ứng trên tổng số 218 bệnh nhân.
Nghiên cứu này đáp ứng tiêu chí chính về tỷ lệ đáp ứng không so sánh kém hơn (CR+PR) sau 4 chu kỳ đơn trị liệu với VELCADE tiêm dưới da và tiêm tĩnh mạch, 42% trong hai nhóm. Hơn nữa, đánh giá tiêu chí hiệu quả liên quan đến đáp ứng thứ phát và thời gian đến khi có biến cố cho thấy kết quả nhất quán đối với tiêm dưới da và tiêm tĩnh mạch (Bảng 5).
- xem Bảng 5.
Điều trị VELCADE kết hợp với doxorubicin liposome pegylat hóa (nghiên cứu DOXIL MMY-3001)
Một nghiên cứu pha III ngẫu nhiên, nhóm song song, nhãn mở, đa trung tâm được thực hiện trên 646 bệnh nhân so sánh an toàn và hiệu quả của VELCADE phối hợp doxorubicin liposome pegylate hóa so với VELCADE đơn trị liệu ở bệnh nhân đa u tủy dùng ít nhất 1 trị liệu trước đó và những bệnh nhân không tiến triển trong khi đang dùng trị liệu có anthracycline. Tiêu chí đánh giá hiệu quả chính là TTP, còn các tiêu chí đánh giá hiệu quả phụ là OS và ORR (CR + PR), sử dụng các tiêu chí của Nhóm Ghép Tủy và Máu Châu Âu (European Group for Blood and Marrow Transplantation - EBMT).
Một phân tích tạm thời xác định trước trong đề cương (dựa trên 249 biến cố TTP) đã kích hoạt việc ngừng nghiên cứu sớm trước thời hạn do đạt hiệu quả. Phân tích tạm thời này cho thấy giảm nguy cơ TTP là 45% (khoảng tin cậy 95%, 29- 57%, p <0,0001) đối với những bệnh nhân điều trị VELCADE kết hợp doxorubicin liposome pegylate hóa. Trung vị TTP là 6,5 tháng đối với bệnh nhân đơn trị liệu VELCADE so với 9,3 tháng đối với bệnh nhân trị liệu VELCADE kết hợp doxorubicin liposome pegylate hóa. Các kết quả này, mặc dù chưa hoàn toàn đầy đủ, đã làm nên phân tích cuối cùng xác định trước trong đề cương.
Phân tích cuối cùng về OS được tiến hành sau trung vị thời gian theo dõi là 8,6 năm cho thấy không có sự khác biệt đáng kể về OS giữa hai nhóm điều trị. Trung vị OS là 30,8 tháng (khoảng tin cậy 95%, 25,2- 36,5 tháng) đối với bệnh nhân đơn trị liệu VELCADE và 33,0 tháng (khoảng tin cậy 95%, 28,9 - 37,1 tháng) đối với bệnh nhân trị liệu VELCADE kết hợp doxorubicin liposome pegylate hóa.
Điều trị phối hợp VELCADE với dexamethasone
Do không có bất kỳ so sánh trực tiếp nào giữa VELCADE và VELCADE kết hợp với dexamethasone ở bệnh nhân đa u tủy tiến triển, một phân tích thống kê ghép cặp đã được tiến hành để so sánh kết quả từ nhóm không được phân ngẫu nhiên của VELCADE kết hợp với dexamethasone (nghiên cứu nhãn mở pha II MMY- 2045), với kết quả thu được ở các nhóm dùng đơn trị liệu VELCADE từ các nghiên cứu pha III ngẫu nhiên khác nhau (M34101-039 [APEX] và DOXIL MMY-3001) trong cùng một chỉ định.
Phân tích ghép cặp là một phương pháp thống kê, trong đó các bệnh nhân ở nhóm điều trị (ví dụ như VELCADE phối hợp với dexamethasone) và bệnh nhân trong nhóm so sánh (ví dụ như VELCADE) có đặc điểm tương tự về các yếu tố gây nhiễu bằng cách ghép cặp từng đối tượng nghiên cứu riêng lẻ. Điều này giảm thiểu các tác động của yếu tố gây nhiễu quan sát được khi ước tính hiệu quả điều trị mà sử dụng dữ liệu trên các bệnh nhân không được phân ngẫu nhiên.
Một trăm hai mươi bảy cặp bệnh nhân phù hợp được xác định. Phân tích cho thấy có cải thiện ORR (CR + PR) (tỉ suất chênh 3,769, khoảng tin cậy 95%: 2,045-6,947, p <0,001), PFS (tỷ số nguy cơ 0,511; khoảng tin cậy 95%: 0,309 - 0,845, p = 0,008), TTP (tỷ số nguy cơ 0,385; khoảng tin cậy 95%: 0,212 - 0,698; p = 0,001) đối với VELCADE kết hợp với dexamethasone tốt hơn so với đơn trị liệu VELCADE.
Hiện thông tin còn hạn chế về tái điều trị VELCADE ở bệnh đa u tủy tái phát.
Một nghiên cứu Pha II, MMY- 2036 (RETRIEVE), một nhánh, nhãn mở đã được tiến hành để xác định hiệu quả và an toàn của tái điều trị với VELCADE. Một trăm ba mươi bệnh nhân (≥18 tuổi) bị đa u tủy, những người trước đây đã có ít nhất đáp ứng một phần với phác đồ có VELCADE, đã được tái điều trị khi bệnh tiến triển. Ít nhất 6 tháng sau trị liệu trước đó, VELCADE được bắt đầu ở liều đã dung nạp gần nhất là 1,3 mg/m2 (n = 93) hoặc ≤1,0 mg/m2 (n = 37) và được dùng vào các ngày 1, 4, 8 và 11 mỗi 3 tuần trong tối đa 8 chu kỳ với phác đồ đơn trị liệu hoặc kết hợp với dexamethasone dùng phù hợp theo điều trị chuẩn. Dexamethasone đã được dùng kết hợp với VELCADE cho 83 bệnh nhân trong Chu kỳ 1 và thêm 11 bệnh nhân dùng dexamethasone trong suốt các chu kỳ tái điều trị với VELCADE.
Tiêu chí chính là đáp ứng tốt nhất được xác nhận với việc tái điều trị đánh giá theo tiêu chí của EBMT. Tỷ lệ đáp ứng chung tốt nhất (CR + PR), với tái điều trị ở 130 bệnh nhân là 38,5% (khoảng tin cậy 95%: 30,1; 47,4).
Hiệu quả lâm sàng trên u lympho tế bào vỏ (MCL) chưa được điều trị trước đó
Nghiên cứu LYM 3002 là một nghiên cứu pha III, ngẫu nhiên và nhãn mở, so sánh hiệu quả và an toàn của VELCADE kết hợp rituximab, cyclophosphamide, doxorubicin và prednisone (VcR-CAP; n = 243) so với rituximab, cyclophosphamide, doxorubicin, vincristine và prednisone (R - CHOP; n = 244) ở bệnh nhân người lớn bị MCL chưa được điều trị trước đó (Giai đoạn II, III hoặc IV). Bệnh nhân trong nhóm điều trị VcR-CAP được dùng VELCADE (1,3 mg/m2; vào ngày 1, 4, 8, 11, giai đoạn nghỉ là các ngày 12 - 21), rituximab 375 mg/m2 đường tĩnh mạch vào ngày 1; cyclophosphamide 750 mg/m2 đường tĩnh mạch vào ngày 1; doxorubicin 50 mg/m2 đường tĩnh mạch vào ngày 1; và prednisone 100 mg/m2 dùng đường uống vào ngày 1 đến ngày 5 của chu kỳ điều trị VELCADE 21 ngày. Đối với những bệnh nhân có đáp ứng đầu tiên được ghi nhận ở chu kỳ 6, được điều trị thêm hai chu kỳ.
Tiêu chí đánh giá hiệu quả chính là sống không tiến triển bệnh dựa trên đánh giá của Hội đồng Đánh giá Độc lập (Independent Review Committee -IRC). Các tiêu chí phụ bao gồm thời gian đến khi bệnh tiến triển (TTP), thời gian đến điều trị kháng u lympho tiếp theo (time to next anti-lymphoma treatment - TNT), khoảng thời gian không điều trị (treatment free interval - TFI), tỷ lệ đáp ứng chung (overall response rate - ORR) và tỷ lệ đáp ứng hoàn toàn (complete response -CR/CRu), sống còn toàn bộ (overall survival - OS) và khoảng thời gian đạt đáp ứng.
Đặc điểm nhân khẩu học và bệnh lý trước điều trị nhìn chung là cân bằng giữa hai nhóm điều trị: trung vị tuổi là 66 tuổi, 74% là nam giới, 66% là người da trắng và 32% người Châu Á, 69% bệnh nhân có kết quả chọc hút tủy và/hoặc sinh thiết tủy xương dương tính với MCL, 54% bệnh nhân có Chỉ số Tiên lượng Quốc tế (International Prognostic Index - IPI) ≥ 3, và 76% bệnh nhân ở giai đoạn IV. Thời gian điều trị (trung vị = 17 tuần) và thời gian theo dõi (trung vị = 40 tháng) là tương tự nhau ở cả hai nhóm điều trị. Bệnh nhân ở cả hai nhóm điều trị có trung vị 6 chu kỳ điều trị với 14% đối tượng trong nhóm VcR-CAP và 17% bệnh nhân trong nhóm R-CHOP được điều trị thêm 2 chu kỳ. Phần lớn bệnh nhân ở cả hai nhóm đã hoàn thành điều trị, 80% ở nhóm VcR-CAP và 82% ở nhóm R-CHOP. Các kết quả về hiệu quả được trình bày trong Bảng 6.
- xem Bảng 6.
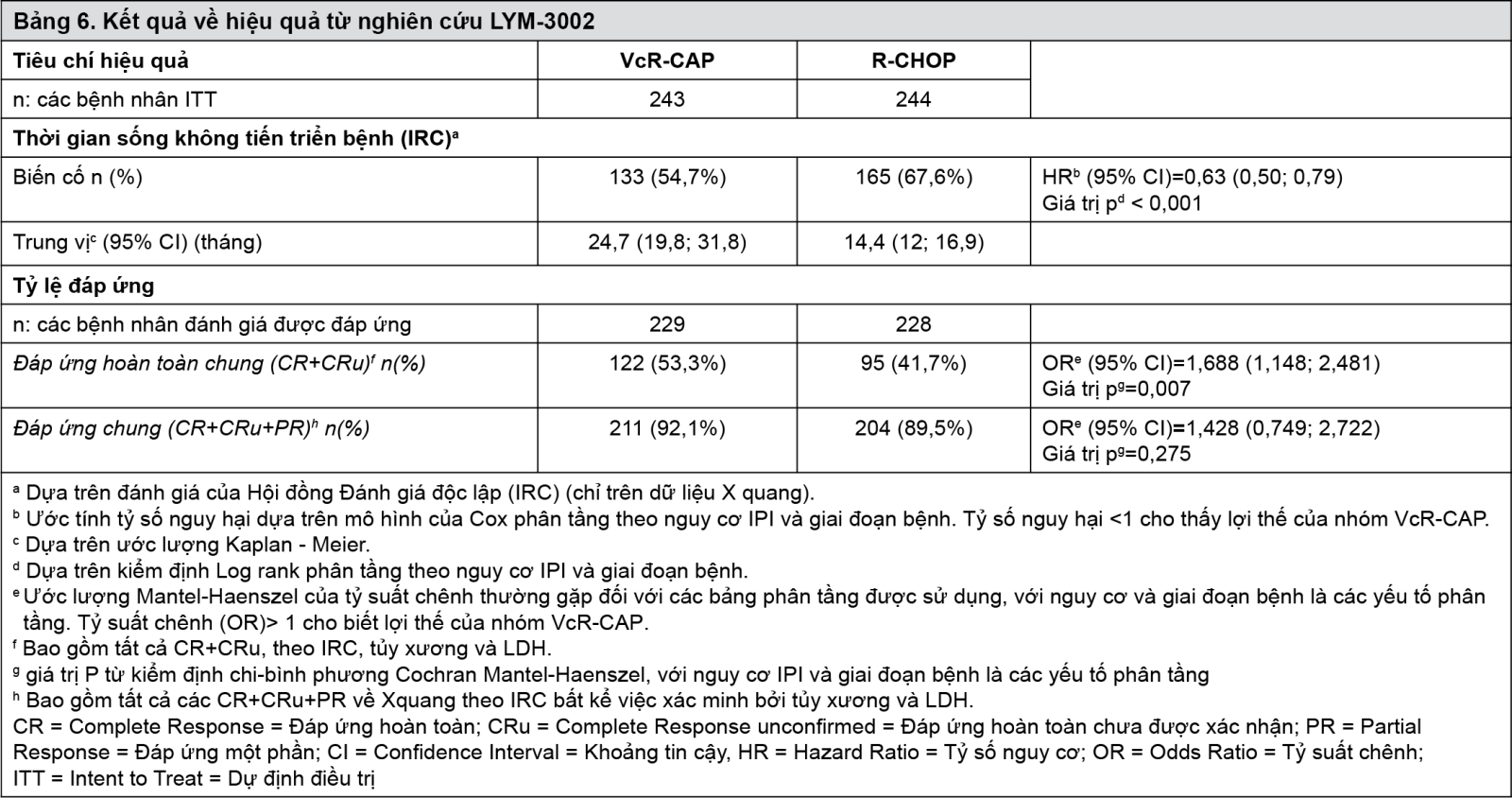
Trung vị của PFS theo đánh giá của nghiên cứu viên là 30,7 tháng trong nhóm VcR-CAP và 16,1 tháng ở nhóm R-CHOP (Tỷ số nguy hại [HR] = 0,51; p <0,001). Đã ghi nhận lợi ích đáng kể có ý nghĩa thống kê (p <0,001) đối với nhóm điều trị VcR-CAP so với nhóm R-CHOP về TTP (trung vị là 30,5 so với 16,1 tháng), TNT (trung vị 44,5 so với 24,8 tháng) và TFI (trung vị 40,6 so với 20,5 tháng). Trung vị khoảng thời gian có đáp ứng hoàn toàn là 42,1 tháng ở nhóm VcR-CAP so với 18 tháng ở nhóm R-CHOP. Khoảng thời gian có đáp ứng chung ở nhóm VcR-CAP dài hơn 21,4 tháng (trung vị là 36,5 tháng so với 15,1 tháng ở nhóm R-CHOP). Với trung vị thời gian theo dõi là 40 tháng, trung vị thời gian sống còn (56,3 tháng trong nhóm R-CHOP và chưa xác định được trong nhóm VcR-CAP) ưu thế cho nhóm VcR-CAP (HR ước tính = 0,80, p = 0,173). Có một xu hướng kéo dài thời gian sống còn ưu thế cho nhóm VcR-CAP; tỷ lệ bệnh nhân sống còn 4 năm ước tính là 53,9% ở nhóm R-CHOP và 64,4% ở nhóm VcR-CAP.
Bệnh nhân bị bệnh bột hóa chuỗi nhẹ (light-chain Amyloidosis – AL) đã được điều trị trước đó
Một nghiên cứu giai đoạn I/II nhãn mở, không ngẫu nhiên được tiến hành để xác định an toàn và hiệu quả của VELCADE ở bệnh nhân trước đó đã điều trị bệnh bột hóa chuỗi nhẹ (AL). Không có lo ngại mới nào về an toàn được quan sát trong quá trình nghiên cứu, và đặc biệt là VELCADE không làm gia tăng tổn thương cơ quan đích (tim, thận và gan). Trong một phân tích thăm dò hiệu quả, tỷ lệ đáp ứng 67,3% (bao gồm tỷ lệ CR 28,6%) được đo bằng đáp ứng huyết học (M-protein) đã được báo cáo ở 49 bệnh nhân có thể đánh giá được và được điều trị với liều tối đa cho phép là 1,6 mg/m2 mỗi tuần và 1,3 mg/m2 hai lần mỗi tuần. Đối với những nhóm liều này, tỷ lệ sống còn sau 1 năm là 88,1%.
Dân số bệnh nhân trẻ em
Cơ quan Quản lý Dược phẩm Châu Âu đã miễn nghĩa vụ nộp các kết quả nghiên cứu của VELCADE trên tất cả các phân nhóm của dân số bệnh nhân trẻ em bị đa u tủy xương và u lympho tế bào vỏ (xem Liều lượng và cách dùng về thông tin sử dụng thuốc trên trẻ em).
Một thử nghiệm pha II, đơn nhánh, nghiên cứu về an toàn và dược động học được tiến hành bởi Nhóm Ung thư Trẻ em (Children’s Oncology Group) đánh giá tác dụng của việc bổ sung bortezomib vào phác đồ hóa trị liệu nhiều thuốc tái tấn công trên bệnh nhân trẻ em và thanh niên bị bệnh lý ác tính dòng lympho (lơ xê mi cấp dòng lympho tế bào tiền B- pre-B cell acute lymphoblastic leukemia -ALL], ALL tế bào T [T-cell ALL], và lơ xê mi dòng lympho tế bào T [T-cell lymphoblastic lymphoma -LL]). Chế độ hóa trị liệu nhiều thuốc tái tấn công được thực hiện theo 3 giai đoạn. VELCADE chỉ được sử dụng trong Giai đoạn 1 và 2 để tránh các độc tính tiềm tàng chồng lấp với các thuốc dùng đồng thời trong Giai đoạn 3.
Đáp ứng hoàn toàn (CR) được đánh giá vào cuối Giai đoạn 1. Trên các bệnh nhân B-ALL tái phát trong vòng 18 tháng sau khi chẩn đoán (n = 27) tỷ lệ CR là 67% (khoảng tin cậy 95%: 46, 84); tỷ lệ sống không có biến cố sau 4 tháng là 44% (khoảng tin cậy 95%: 26, 62). Trên các bệnh nhân B-ALL tái phát trong khoảng 18 - 36 tháng kể từ khi chẩn đoán (n = 33), tỷ lệ CR là 79% (khoảng tin cậy 95%: 61, 91) và tỷ lệ sống không biến cố sau 4 tháng là 73% (khoảng tin cậy 95%: 54, 85). Tỷ lệ CR ở bệnh nhân ALL tế bào T tái phát lần đầu tiên (n = 22) là 68% (khoảng tin cậy 95%: 45, 86) và tỷ lệ sống không có biến cố sau 4 tháng là 67% (khoảng tin cậy 95%: 42, 83). Các dữ liệu hiệu quả đã báo cáo được xem là chưa đủ để kết luận (xem Liều lượng và cách dùng).
Có 140 bệnh nhân bị ALL hoặc LL được tuyển chọn và đánh giá về an toàn; trung vị tuổi là 10 tuổi (khoảng từ 1 đến 26). Không có mối quan ngại mới nào về an toàn được quan sát thấy khi VELCADE được bổ sung vào phác đồ hóa trị liệu cốt lõi tiêu chuẩn điều trị ALL tế bào tiền B (pre-B cell ALL) trên trẻ em. Các phản ứng bất lợi sau đây (Độ ≥ 3) được quan sát thấy tần suất cao hơn trong phác đồ điều trị có chứa VELCADE so với nghiên cứu có đối chứng trước đây, trong đó phác đồ cốt lõi được dùng đơn độc: ở giai đoạn 1 bệnh lý thần kinh cảm giác ngoại biên (3% so với 0%); liệt ruột (2,1% so với 0%); giảm oxy mô (8% so với 2%). Không có thông tin về hậu quả có thể xảy ra hoặc tỷ lệ hồi phục bệnh lý thần kinh ngoại vi đã có trong nghiên cứu này. Tần suất cao hơn cũng được ghi nhận về các nhiễm trùng với giảm bạch cầu Độ ≥ 3 (24% so với 19% ở giai đoạn 1 và 22% so với 11% ở giai đoạn 2), tăng ALT (17% so với 8% ở giai đoạn 2), hạ kali máu (18% so với 6% trong giai đoạn 1 và 21% so với 12% ở giai đoạn 2) và hạ natri máu (12% so với 5% ở giai đoạn 1 và 4% so với 0 ở giai đoạn 2).
Dược động học
Hấp thu
Sau khi tiêm tĩnh mạch nhanh với liều 1,0 mg/m2 và 1,3 mg/m2 cho 11 bệnh nhân đa u tủy và độ thanh thải creatinine lớn hơn 50 mL/phút, nồng độ tối đa trung bình trong huyết tương của liều đầu tiên bortezomib tương ứng là 57 và 112 ng/mL. Trong các liều tiếp theo, nồng độ tối đa trung bình trong huyết tương quan sát thấy dao động từ 67 đến 106 ng/mL đối với liều 1,0 mg/m2 và 89 đến 120 ng/mL đối với liều 1,3 mg/m2.
Sau khi tiêm tĩnh mạch nhanh hoặc tiêm dưới da liều 1,3 mg/m2 cho bệnh nhân đa u tủy (n = 14 cho nhóm tiêm tĩnh mạch, n = 17 cho nhóm tiêm dưới da), tổng nồng độ toàn thân sau liều lặp lại (AUClast) là tương tự khi tiêm tĩnh mạch hoặc tiêm dưới da. Cmax sau khi tiêm dưới da (20,4 ng/mL) là thấp hơn so với tiêm tĩnh mạch (223 ng/mL). Tỷ lệ phân bố biểu kiến trung bình là 0,99 và khoảng tin cậy 90% là 80,18%-122,80%.
Phân bố
Thể tích phân bố trung bình (Vd) của bortezomib dao động từ 1659 L đến 3294 L sau khi tiêm tĩnh mạch đơn liều hoặc liều lặp lại 1,0 mg/m2 hoặc 1,3 mg/m2 cho bệnh nhân đa u tủy. Điều này gợi ý rằng bortezomib phân bố rộng rãi vào các mô ngoại vi. Trong dải nồng độ bortezomib từ 0,01 đến 1,0 μg/mL, sự liên kết protein in vitro trung bình là 82,9% trong huyết tương người. Tỷ lệ bortezomib gắn với protein huyết tương không phụ thuộc vào nồng độ.
Chuyển dạng sinh học
Các nghiên cứu in vitro với microsome gan người và các phân typ enzym cytochrome P450 được biểu hiện cDNA của người cho thấy bortezomib được chuyển hóa chủ yếu bằng cách oxy hoá thông qua các enzyme cytochrome P450, 3A4, 2C19 và 1A2. Con đường chuyển hóa chính là deboron để tạo thành hai chất chuyển hóa deboron hóa mà những chất này sau đó được hydroxyl hóa thành nhiều chất chuyển hóa. Các chất chuyển hóa bortezomib deboron hóa không có hoạt tính ức chế proteasome 26S.
Thải trừ
Thời gian bán thải trung bình (t1/2) của bortezomib khi dùng đa liều dao động từ 40-193 giờ. Bortezomib được thải trừ nhanh hơn sau liều đầu tiên so với những liều tiếp theo. Thanh thải toàn bộ là 102 và 112 L/giờ sau liều đầu tiên lần lượt ở các mức liều 1,0 mg/m2 và 1,3 mg/m2 và dao động tương ứng trong khoảng từ 15 đến 32 L/giờ và 18 đến 32 L/giờ sau khi dùng đa liều 1,0 mg/m2 và 1,3 mg/m2.
Các quần thể bệnh nhân đặc biệt
Suy gan: Tác dụng của tình trạng suy gan đối với dược động học của bortezomib đã được đánh giá trong một nghiên cứu pha I trong chu kỳ điều trị đầu tiên, bao gồm 61 bệnh nhân chủ yếu bị các khối u rắn và có các mức độ suy gan khác nhau ở các liều bortezomib từ 0,5 đến 1,3 mg/m2.
Khi so sánh với những bệnh nhân có chức năng gan bình thường, suy gan nhẹ không làm thay đổi AUC chuẩn hóa theo liều của bortezomib. Tuy nhiên, các giá trị AUC trung bình chuẩn hóa theo liều đã tăng lên khoảng 60% ở những bệnh nhân suy gan mức độ trung bình hoặc nặng. Khuyến cáo liều khởi đầu thấp hơn ở những bệnh nhân suy gan mức độ trung bình hoặc nặng, và những bệnh nhân này cần được theo dõi chặt chẽ (xem Liều lượng và cách dùng, Bảng 12).
Suy thận: Một nghiên cứu dược động học đã được thực hiện ở những bệnh nhân có mức độ suy thận khác nhau, được phân loại theo các giá trị thanh thải creatinine (CrCl) của họ vào các nhóm sau: Bình thường (CrCl ≥ 60 mL/phút/1,73 m2, n = 12), Suy thận nhẹ (CrCL = 40-59 mL/phút/1,73 m2, n = 10), Suy thận trung bình (CrCl = 20-39 mL/phút/1,73 m2, n = 9) và Suy thận nặng (CrCl <20 mL/phút/1,73 m2, n = 3). Một nhóm bệnh nhân thẩm phân thận đã được dùng thuốc sau khi thẩm phân thận cũng được đưa vào nghiên cứu (n = 8). Bệnh nhân được dùng các liều tiêm tĩnh mạch từ 0,7 đến 1,3 mg/m2 của VELCADE hai lần mỗi tuần. Nồng độ của VELCADE (AUC và Cmax chuẩn hóa theo liều) là tương tự giữa tất cả các nhóm (xem Liều lượng và cách dùng).
Tuổi: Dược động học của bortezomib được mô tả sau khi dùng tiêm tĩnh mạch liều 1,3 mg/m2 hai lần mỗi tuần cho 104 bệnh nhân nhi (từ 2-16 tuổi) mắc bệnh lơ xê mi dòng lympho cấp tính (ALL) hoặc bệnh lơ xê mi dòng tủy cấp tính (AML). Dựa trên phân tích dược động học quần thể, thanh thải của bortezomib tăng lên khi diện tích bề mặt cơ thể (BSA) tăng lên. Các giá trị trung bình của thanh thải (%CV) là 7,79 (25%) L/giờ/m2, thể tích phân bố ở trạng thái ổn định là 834 (39%) L/m2 và thời gian bán thải là 100 (44%) giờ. Sau khi hiệu chỉnh theo BSA, các đặc điểm nhân khẩu học khác như tuổi, cân nặng và giới tính không ảnh hưởng đáng kể về mặt lâm sàng đối với thanh thải của bortezomib.
Thanh thải chuẩn hóa theo BSA của bortezomib ở bệnh nhân trẻ em cũng tương tự như ở người lớn.
An toàn tiền lâm sàng
Bortezomib có kết quả dương tính với tác dụng gây đột biến nhiễm sắc thể (sai lệch về cấu trúc nhiễm sắc thể) trong thử nghiệm sai lệch nhiễm sắc thể in vitro sử dụng tế bào trứng của chuột lang hamster Trung Quốc (Chinese hamster ovary -CHO) ở nồng độ thấp 3,125 μg/mL, là nồng độ thấp nhất được đánh giá. Bortezomib không có độc tính trên gen khi được đánh giá trong thử nghiệm gây đột biến in vitro (thử nghiệm Ames) và thử nghiệm vi nhân in vivo ở chuột nhắt.
Các nghiên cứu độc tính trên sự phát triển ở chuột cống và thỏ cho thấy phôi thai chết ở liều có độc tính trên động vật mẹ, nhưng không có độc tính phôi - thai trực tiếp ở liều dưới liều có độc tính trên con mẹ. Các nghiên cứu về khả năng sinh sản chưa được thực hiện nhưng đánh giá các mô sinh sản đã được thực hiện trong các nghiên cứu độc tính chung. Trong nghiên cứu ở chuột cống kéo dài 6 tháng, đã quan sát thấy các tác dụng thoái hóa ở cả tinh hoàn và buồng trứng. Do đó, có thể bortezomib có tác dụng tiềm tàng đến khả năng sinh sản ở cả nam giới hay nữ giới. Các nghiên cứu về sự phát triển ở giai đoạn trong và sau sinh chưa được tiến hành.
Trong các nghiên cứu độc tính chung đa chu kỳ được thực hiện ở chuột cống và khỉ, các cơ quan đích chủ yếu bao gồm đường tiêu hóa, dẫn đến nôn và/hoặc tiêu chảy; các mô tạo máu và bạch huyết, dẫn đến giảm các tế bào máu ngoại biên, teo mô bạch huyết và giảm tế bào tạo máu tủy xương; bệnh lý thần kinh ngoại biên (quan sát thấy ở khỉ, chuột nhắt và chó) liên quan đến các sợi trục thần kinh cảm giác; và những thay đổi nhẹ ở thận. Tất cả các cơ quan đích này đều đã phục hồi một phần hoặc hoàn toàn sau khi ngừng điều trị.
Dựa trên các nghiên cứu trên động vật, sự xâm nhập, nếu có, của bortezomib qua hàng rào máu não dường như bị giới hạn và mối liên quan đến người là chưa rõ.
Các nghiên cứu dược lý học an toàn trên tim mạch ở khỉ và chó cho thấy các liều tiêm tĩnh mạch cao khoảng 2-3 lần so với liều được khuyến cáo trên lâm sàng tính theo mg/m2, có liên quan đến tăng nhịp tim, giảm sức co bóp, hạ huyết áp và tử vong. Ở chó, sự giảm co bóp tim và hạ huyết áp đã đáp ứng với sự can thiệp cấp tính bằng các thuốc hướng cơ tim dương tính hoặc các thuốc làm tăng huyết áp. Hơn nữa, trong nghiên cứu trên chó, quan sát thấy tăng nhẹ về khoảng QT hiệu chỉnh.
Chỉ định/Công dụng
VELCADE đơn trị liệu hoặc phối hợp với doxorubicin liposom pegylat hóa hoặc dexamethasone được chỉ định để điều trị cho bệnh nhân người lớn bị đa u tủy tiến triển đã được dùng ít nhất 1 trị liệu trước đó và đã trải qua hoặc không thích hợp để ghép tế bào gốc tạo máu.
VELCADE kết hợp với melphalan và prednisone được chỉ định để điều trị cho bệnh nhân người lớn bị đa u tủy chưa được điều trị trước đó, những người không đủ điều kiện để điều trị hóa trị liệu liều cao với ghép tế bào gốc tạo máu.
VELCADE kết hợp với dexamethasone, hoặc với dexamethasone và thalidomide, được chỉ định để điều trị tấn công cho bệnh nhân người lớn bị đa u tủy chưa được điều trị trước đó, những người đủ điều kiện để hóa trị liệu liều cao với ghép tế bào gốc tạo máu.
VELCADE kết hợp với rituximab, cyclophosphamide, doxorubicin và prednisone được chỉ định để điều trị cho bệnh nhân người lớn bị u lympho tế bào vỏ chưa được điều trị trước đó mà không thích hợp để ghép tế bào gốc tạo máu.
Liều lượng & Cách dùng
Điều trị VELCADE phải được bắt đầu dưới sự giám sát của bác sĩ có kinh nghiệm trong điều trị các bệnh nhân ung thư, tuy nhiên VELCADE có thể được sử dụng bởi một chuyên gia y tế có kinh nghiệm sử dụng các chất hoá trị liệu. VELCADE phải được hoàn nguyên bởi một cán bộ y tế (xem Thận trọng đặc biệt về hủy thuốc và xử lý khác).
Liều dùng để điều trị bệnh đa u tủy tiến triển (những bệnh nhân đã được dùng ít nhất một trị liệu trước đó)
Đơn trị liệu
VELCADE 3,5 mg bột để pha dung dịch tiêm được dùng qua đường tiêm tĩnh mạch hoặc tiêm dưới da với liều khuyến cáo là 1,3 mg/m2 diện tích bề mặt cơ thể hai lần mỗi tuần trong hai tuần vào các ngày 1, 4, 8 và 11 của một chu kỳ điều trị 21 ngày. Giai đoạn 3 tuần này được coi là một chu kỳ điều trị. Khuyến cáo bệnh nhân dùng 2 chu kỳ VELCADE sau khi xác nhận đáp ứng hoàn toàn. Cũng khuyến cáo những bệnh nhân đang có đáp ứng nhưng không đạt được đáp ứng hoàn toàn dùng tổng cộng 8 chu kỳ điều trị bằng VELCADE. Cần ít nhất 72 giờ giữa các liều liên tiếp của VELCADE.
Điều chỉnh liều trong quá trình điều trị và tái khởi trị đối với đơn trị liệu
Điều trị VELCADE phải được tạm ngừng ngay khi có bất kỳ độc tính không thuộc huyết học nào ở Độ 3 hoặc bất kỳ độc tính huyết học nào ở Độ 4, ngoại trừ bệnh lý thần kinh như đã bàn luận dưới đây (cũng xem thêm Cảnh báo). Khi các triệu chứng độc tính đã được giải quyết, điều trị VELCADE có thể được bắt đầu lại với liều giảm 25% (1,3 mg/m2 giảm xuống còn 1,0 mg/m2; liều 1,0 mg/m2 giảm xuống 0,7 mg/m2). Nếu độc tính không được giải quyết hoặc nếu độc tính tái phát ở liều thấp nhất thì phải cân nhắc ngừng sử dụng VELCADE trừ khi lợi ích của điều trị rõ ràng lớn hơn nguy cơ.
Đau thần kinh và/hoặc bệnh lý thần kinh ngoại biên
Bệnh nhân bị đau thần kinh và/hoặc bệnh lý thần kinh ngoại biên liên quan đến bortezomib được quản lý như trình bày trong Bảng 7 (xem Cảnh báo). Bệnh nhân bị bệnh lý thần kinh nặng trước đó có thể được điều trị bằng VELCADE chỉ sau khi đánh giá cẩn thận nguy cơ/lợi ích.
- xem Bảng 7.

Điều trị kết hợp với doxorubicin liposome pegylate hóa
VELCADE 3,5 mg bột pha dung dịch tiêm được dùng qua đường tiêm tĩnh mạch hoặc tiêm dưới da với liều khuyến cáo là 1,3 mg/m2 diện tích bề mặt cơ thể hai lần mỗi tuần trong hai tuần vào các ngày 1, 4, 8 và 11 của một chu kỳ điều trị 21 ngày. Giai đoạn 3 tuần này được coi là một chu kỳ điều trị. Cần ít nhất 72 giờ giữa các liều liên tiếp của VELCADE.
Doxorubicin liposome pegylate hóa được dùng vào ngày 4 của chu kỳ điều trị VELCADE với liều 30 mg/m2 truyền tĩnh mạch trong 1 giờ sau khi tiêm VELCADE.
Liệu pháp kết hợp này có thể được điều trị cho đến 8 chu kỳ miễn là bệnh nhân không tiến triển bệnh và dung nạp điều trị. Bệnh nhân đạt được đáp ứng hoàn toàn có thể tiếp tục điều trị trong ít nhất là 2 chu kỳ sau khi có bằng chứng đầu tiên của đáp ứng hoàn toàn, ngay cả khi liệu trình này cần được điều trị dài hơn 8 chu kỳ. Bệnh nhân có nồng độ paraprotein tiếp tục giảm sau 8 chu kỳ cũng có thể tiếp tục miễn là dung nạp với điều trị và tiếp tục có đáp ứng.
Để biết thêm thông tin liên quan đến doxorubicin liposome pegylate hóa, xem Tóm tắt đặc tính sản phẩm của thuốc này.
Kết hợp với dexamethasone
VELCADE 3,5 mg bột pha dung dịch tiêm được dùng qua đường tiêm tĩnh mạch hoặc tiêm dưới da với liều khuyến cáo là 1,3 mg/m2 diện tích bề mặt cơ thể hai lần mỗi tuần trong hai tuần vào các ngày 1, 4, 8 và 11 của chu kỳ điều trị 21 ngày. Giai đoạn 3 tuần này được coi là một chu kỳ điều trị. Cần ít nhất 72 giờ giữa các liều liên tiếp của VELCADE.
Dexamethasone được dùng đường uống với liều 20 mg vào các ngày 1, 2, 4, 5, 8, 9, 11, và 12 của chu kỳ điều trị VELCADE.
Bệnh nhân đạt đáp ứng hoặc bệnh ổn định sau 4 chu kỳ điều trị kết hợp này có thể tiếp tục dùng phác đồ này cho tối đa thêm 4 chu kỳ nữa.
Để biết thêm thông tin liên quan đến dexamethasone, xem Tóm tắt đặc tính sản phẩm của thuốc này.
Điều chỉnh liều cho trị liệu kết hợp trên bệnh nhân đa u tủy tiến triển
Để điều chỉnh liều VELCADE cho trị liệu kết hợp, thực hiện theo hướng dẫn điều chỉnh liều được mô tả trong mục đơn trị liệu ở trên.
Liều dùng cho bệnh nhân đa u tủy chưa được điều trị trước đây mà không đủ điều kiện để ghép tế bào gốc tạo máu
Liệu pháp phối hợp với melphalan và prednisone
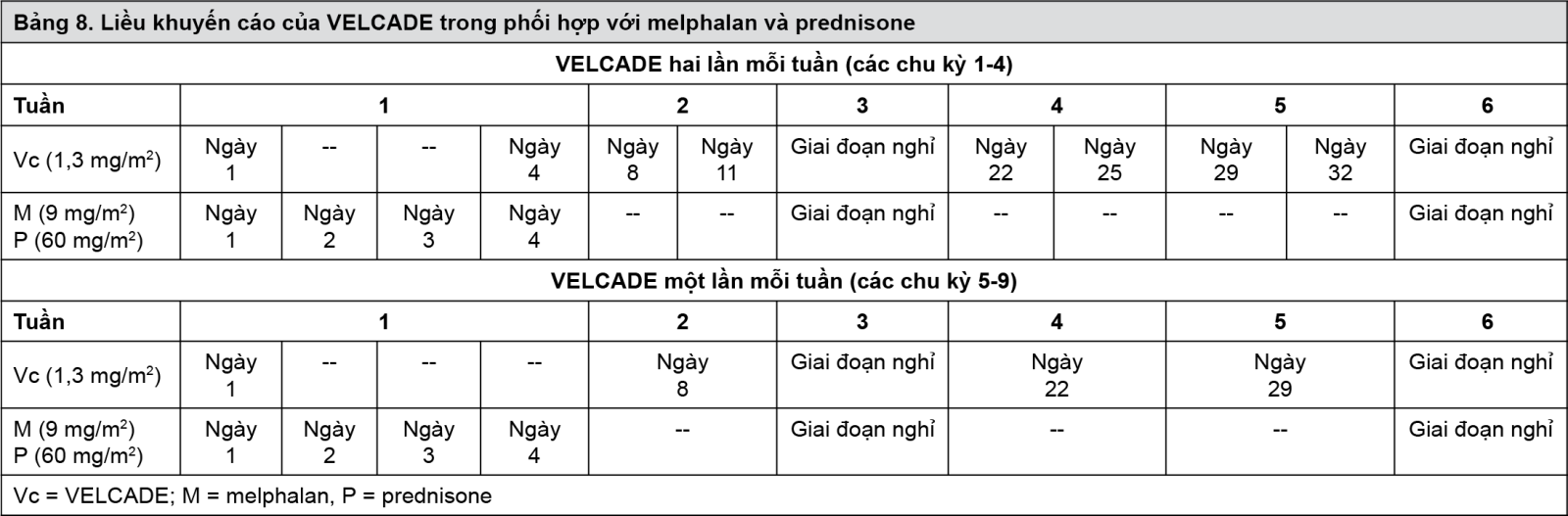
VELCADE 3,5 mg bột pha dung dịch tiêm được dùng qua đường tiêm tĩnh mạch hoặc tiêm dưới da phối hợp với melphalan dùng đường uống và prednisone dùng đường uống như trong Bảng 8. Giai đoạn 6 tuần được coi là một chu kỳ điều trị. Trong các chu kỳ 1- 4, VELCADE được dùng hai lần mỗi tuần vào các ngày 1, 4, 8, 11, 22, 25, 29 và 32. Trong các chu kỳ 5 - 9, VELCADE được dùng mỗi tuần một lần vào các ngày 1, 8, 22 và 29. Cần ít nhất 72 giờ giữa các liều liên tiếp của VELCADE.
Cần uống cả melphalan và prednisone vào các ngày 1, 2, 3 và 4 của tuần đầu tiên trong mỗi chu kỳ điều trị của VELCADE.
Chín chu kỳ điều trị của liệu pháp phối hợp này được sử dụng.
- xem Bảng 8.
Điều chỉnh liều trong thời gian điều trị và tái khởi trị khi phối hợp với melphalan và prednisone
Trước khi bắt đầu một chu kỳ điều trị mới:
• Số lượng tiểu cầu cần ≥ 70 x 109/L và số lượng bạch cầu trung tính tuyệt đối (ANC) phải ≥ 1,0 x 109/L
• Các độc tính không thuộc huyết học cần được điều trị về Độ 1 hoặc như thời điểm trước khi điều trị
- xem Bảng 9.

Để biết thêm thông tin về melphalan và prednisone, xem Tóm tắt các đặc tính sản phẩm tương ứng.
Liều dùng cho bệnh nhân đa u tủy chưa được điều trị trước đó, đủ điều kiện để ghép tế bào gốc tạo máu (điều trị tấn công)
Phối hợp với dexamethasone
VELCADE 3,5 mg bột pha dung dịch tiêm được dùng qua đường tiêm tĩnh mạch hoặc tiêm dưới da với liều khuyến cáo là 1,3 mg/m2 diện tích bề mặt cơ thể hai lần mỗi tuần trong hai tuần vào các ngày 1, 4, 8 và 11 của chu kỳ điều trị 21 ngày. Giai đoạn 3 tuần được coi là một chu kỳ điều trị. Cần ít nhất 72 giờ giữa các liều liên tiếp của VELCADE.
Dexamethasone được dùng đường uống với liều 40 mg vào các ngày 1, 2, 3, 4, 8, 9, 10 và 11 của chu kỳ điều trị VELCADE.
Sử dụng bốn chu kỳ điều trị với liệu pháp phối hợp này.
Phối hợp với dexamethasone và thalidomide
VELCADE 3,5 mg bột pha dung dịch tiêm được dùng qua đường tiêm tĩnh mạch hoặc tiêm dưới da với liều khuyến cáo là 1,3 mg/m2 diện tích bề mặt cơ thể hai lần mỗi tuần trong hai tuần vào các ngày 1, 4, 8 và 11 của chu kỳ điều trị 28 ngày. Giai đoạn 4 tuần này được coi là một chu kỳ điều trị. Cần ít nhất 72 giờ giữa các liều liên tiếp của VELCADE.
Dexamethasone được dùng đường uống với liều 40 mg vào ngày 1, 2, 3, 4, 8, 9, 10 và 11 của chu kỳ điều trị VELCADE.
Thalidomide được dùng đường uống với liều 50 mg mỗi ngày vào các ngày 1-14 và nếu dung nạp được, tăng liều đến 100 mg vào các ngày 15-28, và sau đó có thể tăng đến 200 mg mỗi ngày từ chu kỳ 2 (xem Bảng 10).
Sử dụng bốn chu kỳ điều trị của phối hợp này. Khuyến cáo những bệnh nhân đạt ít nhất đáp ứng một phần, cần điều trị thêm 2 chu kỳ.
- xem Bảng 10.

Điều chỉnh liều cho bệnh nhân đủ điều kiện ghép
Để điều chỉnh liều VELCADE, cần tuân theo hướng dẫn điều chỉnh liều cho đơn trị liệu.
Ngoài ra, khi sử dụng VELCADE phối hợp với các thuốc hóa trị liệu khác, cần xem xét giảm liều phù hợp cho các thuốc này trong trường hợp có độc tính, theo khuyến cáo trong Tóm tắt đặc tính sản phẩm.
Liều dùng cho bệnh nhân u lympho tế bào vỏ chưa được điều trị trước đó
Điều trị phối hợp với rituximab, cyclophosphamide, doxorubicin và prednisone (VcR-CAP)
VELCADE 3,5 mg bột pha dung dịch tiêm được dùng qua đường tiêm tĩnh mạch hoặc tiêm dưới da với liều khuyến cáo là 1,3 mg/m2 diện tích bề mặt cơ thể hai lần mỗi tuần trong hai tuần vào các ngày 1, 4, 8 và 11, tiếp theo là khoảng thời gian nghỉ 10 ngày vào các ngày 12-21. Giai đoạn 3 tuần này được coi là một chu kỳ điều trị. Sáu chu kỳ VELCADE được khuyến cáo, mặc dù đối với những bệnh nhân có đáp ứng đầu tiên được ghi nhận ở chu kỳ 6, có thể điều trị thêm hai chu kỳ VELCADE nữa. Cần ít nhất 72 giờ giữa các liều liên tiếp của VELCADE.
Các thuốc sau được dùng theo đường truyền tĩnh mạch vào ngày 1 của mỗi chu kỳ điều trị 3 tuần của VELCADE: rituximab liều 375 mg/m2, cyclophosphamide liều 750 mg/m2 và doxorubicin liều 50 mg/m2.
Prednisone được dùng đường uống ở liều 100 mg/m2 vào các ngày 1, 2, 3, 4 và 5 của mỗi chu kỳ điều trị VELCADE.
Điều chỉnh liều trong quá trình điều trị cho bệnh nhân bị u lympho tế bào vỏ chưa được điều trị trước đó
Trước khi bắt đầu một chu kỳ điều trị mới:
• Số lượng tiểu cầu cần ≥ 100.000 tế bào/μL và số lượng bạch cầu trung tính tuyệt đối (ANC) cần ≥ 1.500 tế bào/μL
• Số lượng tiểu cầu cần ≥ 75.000 tế bào/μL ở những bệnh nhân bị thâm nhiễm tủy xương hoặc tích tụ tiểu cầu tại lách (splenic sequestration)
• Hemoglobin ≥ 8 g/dL
• Các độc tính không phải huyết học cần được điều trị về Độ 1 hoặc mức độ ban đầu trước khi điều trị.
Phải tạm ngừng điều trị VELCADE khi xuất hiện bất kỳ độc tính không phải huyết học Độ ≥ 3 liên quan đến VELCADE (ngoại trừ bệnh lý thần kinh) hoặc độc tính huyết học Độ ≥ 3 (xem thêm Cảnh báo). Để điều chỉnh liều, xem Bảng 11.
Các yếu tố kích thích bạch cầu hạt có thể được sử dụng đối với độc tính huyết học theo thực hành chuẩn tại cơ sở điều trị/địa phương. Sử dụng dự phòng các yếu tố kích thích bạch cầu hạt cần được xem xét trong trường hợp lặp lại việc trì hoãn điều trị trong chu kỳ sử dụng. Nên xem xét truyền tiểu cầu để điều trị giảm tiểu cầu khi thích hợp về mặt lâm sàng.
- xem Bảng 11.

Ngoài ra, khi sử dụng VELCADE phối hợp với các thuốc hóa trị liệu khác, cần xem xét giảm liều thích hợp cho các thuốc này trong trường hợp có độc tính, theo khuyến cáo trong Tóm tắt đặc tính sản phẩm tương ứng.
Quần thể bệnh nhân đặc biệt
Người cao tuổi
Không có bằng chứng cho thấy cần điều chỉnh liều ở bệnh nhân trên 65 tuổi bị đa u tủy hoặc bị u lympho tế bào vỏ.
Không có nghiên cứu về việc sử dụng VELCADE ở bệnh nhân cao tuổi đa u tủy chưa được điều trị trước đó mà có đủ điều kiện để được hóa trị liệu liều cao với ghép tế bào gốc tạo máu. Do đó không có khuyến cáo liều trong quần thể này.
Trong một nghiên cứu trên bệnh nhân u lympho tế bào vỏ chưa được điều trị trước đó, 42,9% bệnh nhân dùng VELCADE ở trong khoảng 65-74 tuổi và 10,4% bệnh nhân dùng VELCADE ≥ 75 tuổi. Ở bệnh nhân có độ tuổi ≥ 75, cả hai phác đồ điều trị, VcR-CAP và R-CHOP, đều ít dung nạp (xem Tác dụng ngoại ý).
Suy gan
Bệnh nhân suy gan nhẹ không cần điều chỉnh liều và nên điều trị theo liều khuyến cáo. Bệnh nhân suy gan trung bình hoặc nặng nên bắt đầu dùng VELCADE với liều giảm còn 0,7 mg/m2 mỗi lần tiêm trong chu kỳ điều trị đầu tiên, và tăng liều sau đó lên đến 1,0 mg/m2 hoặc có thể xem xét tiếp tục giảm liều tới 0,5 mg/m2 dựa trên khả năng dung nạp của bệnh nhân (xem Bảng 12 và Cảnh báo và Dược động học).
- xem Bảng 12.

Suy thận
Dược động học của bortezomib không bị ảnh hưởng ở bệnh nhân suy thận nhẹ đến trung bình (độ thanh thải creatinine [Creatinine Clearance - CrCL]> 20 mL/phút/1,73 m2); do đó, không cần thiết phải điều chỉnh liều cho những bệnh nhân này. Không rõ dược động học của bortezomib có bị ảnh hưởng ở bệnh nhân suy thận nặng không được thẩm phân máu hay không (CrCl <20 mL/phút/1,73 m2). Do thẩm phân máu có thể làm giảm nồng độ bortezomib, nên dùng VELCADE sau khi thẩm phân máu (xem Dược động học).
Dân số bệnh nhân trẻ em
An toàn và hiệu quả của VELCADE ở trẻ em dưới 18 tuổi chưa được thiết lập (xem Dược lực học và Dược động học). Dữ liệu hiện có được mô tả trong phần Dược lực học nhưng không có khuyến cáo nào về liều dùng.
Cách dùng
VELCADE 3,5 mg bột để pha dung dịch tiêm có thể dùng theo đường tĩnh mạch hoặc dưới da.
VELCADE 1 mg bột để pha dung dịch tiêm chỉ để dùng theo đường tĩnh mạch.
Không dùng VELCADE theo các đường dùng khác. Dùng theo đường tiêm tủy sống đã dẫn đến tử vong.
Tiêm tĩnh mạch
VELCADE 3,5 mg dung dịch sau khi hoàn nguyên được tiêm tĩnh mạch nhanh trong 3 - 5 giây thông qua catheter tĩnh mạch ngoại vi hoặc trung tâm, sau đó rửa bằng dung dịch tiêm natri chlorid 9 mg/mL (0,9%). Cần nghỉ ít nhất 72 giờ giữa các liều liên tiếp của VELCADE.
Tiêm dưới da
VELCADE 3,5 mg dung dịch sau khi hoàn nguyên được tiêm dưới da đùi (phải hoặc trái) hoặc bụng (phải hoặc trái). Dung dịch nên được tiêm dưới da với góc nghiêng 45-90o. Nên thay đổi vị trí tiêm cho lần tiêm kế tiếp.
Nếu xuất hiện phản ứng tại chỗ tiêm dưới da VELCADE thì nên tiêm dưới da với dung dịch VELCADE pha loãng hơn (VELCADE 3,5 mg được pha loãng thành 1 mg/mL thay vì 2,5 mg/mL) hoặc đổi sang tiêm tĩnh mạch.
Khi sử dụng VELCADE phối hợp với các thuốc khác, hãy tham khảo Tóm tắt Đặc tính sản phẩm của các thuốc này về hướng dẫn sử dụng.
THẬN TRỌNG ĐẶC BIỆT VỀ HỦY THUỐC VÀ XỬ LÝ KHÁC
Thận trọng chung
Bortezomib là một chất gây độc tế bào. Do đó, cần thận trọng khi xử lý và pha chế VELCADE. Khuyến cáo sử dụng găng tay và quần áo bảo hộ khác để tránh thuốc tiếp xúc với da.
Phải tuân thủ nghiêm ngặt kỹ thuật vô khuẩn trong suốt quá trình xử lý VELCADE vì thuốc này không chứa chất bảo quản.
Đã có trường hợp tử vong do vô ý tiêm VELCADE vào khoang dưới nhện của tủy sống. VELCADE 1 mg bột pha dung dịch tiêm chỉ dùng cho đường tĩnh mạch, trong khi VELCADE 3,5 mg bột pha dung dịch tiêm dùng cho đường tiêm tĩnh mạch hoặc tiêm dưới da. Không tiêm VELCADE vào khoang dưới nhện của tủy sống.
Hướng dẫn hoàn nguyên thuốc
VELCADE phải được hoàn nguyên bởi cán bộ y tế.
Mỗi lọ 10 mL của VELCADE phải được hoàn nguyên một cách cẩn thận với 3,5 mL dung dịch natri chloride 9 mg/mL (0,9%) để tiêm, bằng cách sử dụng một ống tiêm có dung tích phù hợp, mà không mở nắp lọ thuốc. Hòa tan bột đông khô được hoàn thành trong vòng chưa đến 2 phút.
Sau khi hoàn nguyên, mỗi mL dung dịch chứa 1 mg bortezomib. Dung dịch đã được hoàn nguyên trong suốt và không màu, có pH từ 4 đến 7.
Phải kiểm tra bằng mắt dung dịch đã hoàn nguyên về các tiểu phân và sự biến màu trước khi sử dụng. Nếu quan sát thấy sự biến màu hoặc tiểu phân, phải loại bỏ dung dịch đã hoàn nguyên.
Tiêm dưới da
Mỗi lọ 10 mL VELCADE phải được hoàn nguyên cẩn thận với 1,4 mL dung dịch natri chloride 9 mg/mL (0,9%) để tiêm, bằng cách sử dụng một bơm tiêm với dung tích phù hợp mà không mở nắp lọ thuốc. Hòa tan bột đông khô được hoàn thành trong vòng chưa đến 2 phút.
Sau khi hoàn nguyên, mỗi mL dung dịch chứa 2,5 mg bortezomib. Dung dịch đã được hoàn nguyên trong suốt và không màu, có pH từ 4 đến 7. Phải kiểm tra bằng mắt dung dịch đã hoàn nguyên về các tiểu phân và sự biến màu trước khi sử dụng. Nếu quan sát thấy sự biến màu hoặc tiểu phân, phải loại bỏ dung dịch đã hoàn nguyên.
Hủy thuốc
Chỉ dùng VELCADE cho một lần tiêm.
Phải xử lý bất kỳ lượng thuốc nào chưa sử dụng hoặc vật liệu phế thải theo yêu cầu của địa phương.
Cảnh báo
Khi sử dụng VELCADE kết hợp với các thuốc khác, phải tham khảo Tóm tắt Đặc tính sản phẩm của các thuốc này trước khi bắt đầu điều trị bằng VELCADE. Khi sử dụng thalidomide, cần đặc biệt chú ý tới xét nghiệm có thai và cần sử dụng các biện pháp ngừa thai (xem Sử dụng ở phụ nữ có thai và cho con bú).
Tiêm vào khoang dưới nhện của tủy sống
Đã có các trường hợp tử vong do vô ý sử dụng VELCADE tiêm vào khoang dưới nhện của tủy sống. VELCADE 1 mg bột pha dung dịch tiêm chỉ dùng cho đường tĩnh mạch, trong khi VELCADE 3,5 mg bột pha dung dịch tiêm dùng cho tiêm tĩnh mạch hoặc tiêm dưới da. Không tiêm VELCADE vào khoang dưới nhện của tủy sống.
Độc tính trên đường tiêu hóa
Độc tính trên đường tiêu hóa, bao gồm buồn nôn, tiêu chảy, nôn và táo bón rất phổ biến khi điều trị bằng VELCADE. Các trường hợp liệt ruột đã được báo cáo là ít gặp (xem Tác dụng ngoại ý). Do đó, những bệnh nhân bị táo bón cần được theo dõi chặt chẽ.
Độc tính huyết học
Điều trị VELCADE rất thường gặp các độc tính huyết học (giảm tiểu cầu, giảm bạch cầu trung tính và thiếu máu). Trong những nghiên cứu trên bệnh nhân đa u tủy tái phát được điều trị bằng VELCADE và ở bệnh nhân MCL chưa được điều trị trước đó khi được điều trị bằng phác đồ phối hợp VELCADE với rituximab, cyclophosphamide, doxorubicin và prednisone (VcR-CAP), một trong những độc tính huyết học phổ biến nhất là giảm tiểu cầu thoáng qua. Tiểu cầu ở mức thấp nhất vào ngày thứ 11 của mỗi chu kỳ điều trị VELCADE và thường hồi phục đến ngưỡng ban đầu trước điều trị vào chu kỳ kế tiếp. Không có bằng chứng về giảm tiểu cầu tích lũy. Số lượng tiểu cầu trung bình lúc thấp nhất đo được là khoảng 40% so với trước điều trị trong các nghiên cứu đa u tủy sử dụng đơn trị liệu và bằng 50% trong nghiên cứu MCL. Ở bệnh nhân đa u tủy tiến triển, mức độ nặng của tình trạng giảm tiểu cầu có liên quan đến số lượng tiểu cầu trước khi điều trị: với số lượng tiểu cầu ban đầu <75.000/μL, 90% trong số 21 bệnh nhân có số lượng ≤25.000/μL trong thời gian nghiên cứu, bao gồm 14% <10.000/μL; ngược lại, với số lượng tiểu cầu ban đầu >75.000/μL, chỉ có 14% trong số 309 bệnh nhân có số lượng ≤25.000/μL trong thời gian nghiên cứu.
Ở những bệnh nhân MCL (nghiên cứu LYM-3002), tần suất giảm tiểu cầu Độ ≥ 3 ở nhóm điều trị VELCADE (VcR-CAP) cao hơn so với nhóm điều trị không có VELCADE (rituximab, cyclophosphamide, doxorubicin, vincristine, và prednisone [R-CHOP]) (56,7% so với 5,8%). Hai nhóm điều trị tương tự nhau về tần suất chung biến cố xuất huyết ở tất cả các mức độ (6,3% ở nhóm VcR-CAP và 5,0% ở nhóm R-CHOP) cũng như các biến cố xuất huyết Độ 3 và cao hơn (VcR-CAP: 4 bệnh nhân [ 1,7%], R-CHOP: 3 bệnh nhân [1,2%]). Trong nhóm VcR-CAP, 22,5% bệnh nhân được truyền tiểu cầu so với 2,9% bệnh nhân trong nhóm R-CHOP.
Xuất huyết tiêu hóa và nội sọ đã được báo cáo có liên quan đến điều trị bằng VELCADE. Do đó, số lượng tiểu cầu phải được theo dõi trước mỗi liều VELCADE. Cần tạm ngừng điều trị VELCADE khi số lượng tiểu cầu <25.000/μL, hoặc trong trường hợp kết hợp với melphalan và prednisone, khi số lượng tiểu cầu là ≤30.000/μL (xem Liều lượng và cách dùng). Lợi ích tiềm tàng của điều trị cần được cân nhắc kỹ lưỡng trước những nguy cơ, đặc biệt trong trường hợp giảm tiểu cầu từ trung bình đến nặng và có các yếu tố nguy cơ chảy máu.
Thường xuyên theo dõi công thức máu toàn phần (Complete blood counts - CBC) có phân biệt các loại và bao gồm đếm số lượng tiểu cầu trong suốt quá trình điều trị với VELCADE. Có thể xem xét truyền tiểu cầu khi thích hợp về mặt lâm sàng (xem Liều lượng và cách dùng).
Ở những bệnh nhân MCL, đã thấy có giảm bạch cầu trung tính thoáng qua có thể hồi phục giữa các chu kỳ, không có bằng chứng của giảm bạch cầu trung tính tích lũy. Bạch cầu trung tính thấp nhất vào Ngày 11 của mỗi chu kỳ điều trị VELCADE và thường hồi phục đến mức ban đầu vào chu kỳ kế tiếp. Trong nghiên cứu LYM-3002, điều trị hỗ trợ bằng yếu tố kích thích bạch cầu hạt đã được dùng cho 78% bệnh nhân trong nhóm VcR-CAP và 61% ở bệnh nhân nhóm R-CHOP. Vì bệnh nhân giảm bạch cầu trung tính có nguy cơ gia tăng bị mắc nhiễm trùng nên cần theo dõi các dấu hiệu và triệu chứng của nhiễm trùng và điều trị kịp thời. Các yếu tố kích thích bạch cầu hạt có thể được sử dụng cho độc tính huyết học phù hợp với thực hành chuẩn tại cơ sở/địa phương. Cần xem xét sử dụng dự phòng các yếu tố kích thích bạch cầu hạt trong trường hợp lặp lại việc trì hoãn trong chu kỳ dùng thuốc (xem Liều lượng và cách dùng).
Tái hoạt virus Herpes zoster
Dự phòng bằng thuốc kháng virus được khuyến cáo ở những bệnh nhân đang điều trị bằng VELCADE.
Trong nghiên cứu pha III ở bệnh nhân đa u tủy chưa được điều trị trước đó, tỉ lệ chung về tái hoạt Herpes zoster là thường gặp hơn ở nhóm bệnh nhân điều trị bằng VELCADE + Melphalan + Prednisone so với nhóm Melphalan + Prednisone (tương ứng là 14% so với 4%).
Ở những bệnh nhân MCL (nghiên cứu LYM-3002), tỷ lệ mắc Herpes zoster là 6,7% ở nhóm VcR-CAP và 1,2% ở nhóm R-CHOP (xem Tác dụng ngoại ý).
Nhiễm trùng và tái hoạt virus viêm gan B (HBV)
Khi dùng rituximab kết hợp với VELCADE, phải luôn kiểm tra HBV ở những bệnh nhân có nguy cơ nhiễm HBV trước khi bắt đầu điều trị. Những người mang virus viêm gan B và những bệnh nhân có tiền sử bị viêm gan virus B phải được theo dõi chặt chẽ về các dấu hiệu lâm sàng và xét nghiệm của tình trạng nhiễm HBV hoạt động, trong và sau khi điều trị phối hợp rituximab với VELCADE. Nên xem xét điều trị dự phòng thuốc kháng virus. Tham khảo Tóm tắt Đặc tính sản phẩm của rituximab để biết thêm thông tin.
Bệnh não chất trắng đa ổ tiến triển (PML - progressive multifocalleukoencephalopathy)
Đã có báo cáo về một số rất hiếm các trường hợp nhiễm virus John Cunningham (JC) mà không rõ nguyên nhân, dẫn đến PML và tử vong, ở những bệnh nhân điều trị bằng VELCADE. Bệnh nhân được chẩn đoán PML đã điều trị ức chế miễn dịch trước đó hoặc đồng thời. Hầu hết các trường hợp PML được chẩn đoán trong vòng 12 tháng kể từ lần đầu tiên dùng VELCADE. Bệnh nhân cần được theo dõi thường xuyên định kỳ về bất kỳ triệu chứng hoặc dấu hiệu thần kinh mới hoặc bị trầm trọng hơn mà có thể gợi ý bị PML, như là một phần của chẩn đoán phân biệt với các vấn đề trên thần kinh trung ương. Nếu chẩn đoán nghi ngờ PML, bệnh nhân nên được chuyển đến một chuyên gia về PML và nên bắt đầu tiến hành các biện pháp chẩn đoán thích hợp đối với PML. Ngừng VELCADE nếu PML được chẩn đoán.
Bệnh lý thần kinh ngoại biên
Bệnh lý thần kinh ngoại biên, chủ yếu là bệnh lý thần kinh cảm giác, rất thường gặp khi điều trị bằng VELCADE. Tuy nhiên, đã có báo cáo về các trường hợp bệnh lý thần kinh vận động nặng có hoặc không kèm theo bệnh lý thần kinh cảm giác ngoại biên. Tỷ lệ mắc bệnh lý thần kinh ngoại biên tăng lên trong giai đoạn đầu điều trị và đã được quan sát thấy đạt đỉnh điểm trong chu kỳ 5.
Khuyến cáo bệnh nhân nên được theo dõi cẩn thận về các triệu chứng của bệnh lý thần kinh như cảm giác bỏng rát, chứng tăng cảm giác, giảm cảm giác, dị cảm, khó chịu, đau thần kinh hoặc cảm giác yếu.
Trong nghiên cứu giai đoạn III so sánh VELCADE tiêm tĩnh mạch với tiêm dưới da, tỉ lệ mắc phải các biến cố bệnh lý thần kinh ngoại biên Độ ≥ 2 là 24% ở nhóm dùng đường tiêm dưới da và 41% ở nhóm dùng đường tiêm tĩnh mạch (p = 0,0124). Bệnh lý thần kinh ngoại biên Độ ≥ 3 xảy ra ở 6% bệnh nhân trong nhóm tiêm dưới da, so với 16% trong nhóm tiêm tĩnh mạch (p = 0,0264). Tỉ lệ bệnh lý thần kinh ngoại biên ở mọi mức độ khi dùngVELCADE đường tiêm tĩnh mạch trong các nghiên cứu trước đây đều được ghi nhận thấp hơn so với nghiên cứu MMY-3021.
Bệnh nhân mới bị bệnh lý thần kinh ngoại biên hoặc bệnh tiến triển xấu thì nên được đánh giá về thần kinh và có thể cần thay đổi liều hoặc đường dùng VELCADE thành tiêm dưới da (xem Liều lượng và cách dùng). Bệnh lý thần kinh đã được điều trị bằng chăm sóc hỗ trợ và các liệu pháp khác.
Cần cân nhắc theo dõi sớm và thường xuyên các triệu chứng của bệnh lý thần kinh liên quan đến điều trị với đánh giá về thần kinh ở các bệnh nhân dùng VELCADE kết hợp với các thuốc được biết là có liên quan đến bệnh lý thần kinh (ví dụ như thalidomide) và cần phải cân nhắc giảm liều phù hợp hoặc ngừng thuốc.
Ngoài bệnh lý thần kinh ngoại biên, có thể có sự góp phần của bệnh lý thần kinh tự động vào một số phản ứng bất lợi như hạ huyết áp tư thế và táo bón nặng kèm theo liệt ruột. Thông tin về bệnh lý thần kinh tự động và sự liên quan của nó đối với những tác dụng không mong muốn này còn hạn chế.
Co giật
Co giật đã được báo cáo ít gặp ở những bệnh nhân không có tiền sử cơn động kinh hoặc co giật trước đó. Cần lưu ý đặc biệt khi điều trị bệnh nhân có bất kỳ yếu tố nguy cơ co giật nào.
Hạ huyết áp
Điều trị VELCADE thường liên quan đến hạ huyết áp thế đứng/tư thế. Hầu hết phản ứng bất lợi có bản chất từ nhẹ đến trung bình và được quan sát thấy trong suốt quá trình điều trị. Bệnh nhân xuất hiện hạ huyết áp tư thế khi đang dùng VELCADE (tiêm tĩnh mạch) đã không có bằng chứng bị hạ huyết áp tư thế trước khi điều trị bằng VELCADE. Hầu hết bệnh nhân bị hạ huyết áp tư thế đều cần điều trị. Một số ít bệnh nhân bị hạ huyết áp tư thế đã có biến cố ngất. Hạ huyết áp thế đứng/tư thế không liên quan ngay đến việc truyền nhanh VELCADE. Cơ chế của biến cố này chưa được biết, mặc dù một phần có thể là do bệnh lý thần kinh tự động. Bệnh lý thần kinh tự động có thể liên quan đến bortezomib hoặc bortezomib có thể làm trầm trọng thêm một tình trạng nền như bệnh lý thần kinh do tiểu đường hoặc bệnh lý thần kinh thoái hóa bột (amyloidotic neuropathy). Cần thận trọng khi điều trị cho bệnh nhân có tiền sử ngất khi dùng các thuốc có liên quan đến hạ huyết áp; hoặc những người bị mất nước do tiêu chảy tái phát hoặc nôn. Điều trị hạ huyết áp thế đứng/tư thế có thể bao gồm điều chỉnh các thuốc điều trị tăng huyết áp, bù nước hoặc dùng các thuốc nhóm mineralocorticosteroid và/hoặc các thuốc giống giao cảm. Bệnh nhân cần được hướng dẫn để đi khám nếu họ gặp các triệu chứng chóng mặt, choáng váng hoặc ngất xỉu.
Hội chứng bệnh não tuần hoàn sau có hồi phục (Posterior Reversible Encephalopathy Syndrome -PRES)
Đã có báo cáo về PRES ở những bệnh nhân dùng VELCADE. PRES là một bệnh lý thần kinh hiếm gặp, thường hồi phục, tiến triển nhanh, có thể biểu hiện với co giật, tăng huyết áp, đau đầu, ngủ lịm, lú lẫn, mù lòa, và các rối loạn thị giác và thần kinh khác. Chẩn đoán hình ảnh não, thường dùng nhất, là chụp cộng hưởng từ (MRI), được sử dụng để chẩn đoán xác định. Ở bệnh nhân đang có PRES, nên ngừng dùng VELCADE.
Suy tim
Suy tim sung huyết cấp tính hoặc cơn kịch phát, và/hoặc khởi phát mới tình trạng giảm phân suất tống máu thất trái đã được báo cáo trong quá trình điều trị bortezomib. Giữ nước có thể là một yếu tố tiền triệu cho các dấu hiệu và triệu chứng của suy tim. Bệnh nhân có các yếu tố nguy cơ hoặc đang có bệnh tim nên được theo dõi chặt chẽ.
Thăm dò điện tim
Đã có những trường hợp riêng lẻ kéo dài khoảng QT trong các nghiên cứu lâm sàng, mối quan hệ nhân quả chưa được thiết lập.
Rối loạn hô hấp
Hiếm có báo cáo về bệnh phổi thâm nhiễm lan tỏa cấp tính không rõ nguyên nhân, như bệnh viêm phế nang (pneumonitis), viêm phổi kẽ, thâm nhiễm phổi, và hội chứng suy hô hấp cấp (ARDS) ở bệnh nhân đang dùng VELCADE (xem Tác dụng ngoại ý). Một số biến cố này đã gây tử vong. Khuyến cáo chụp X quang phổi trước khi điều trị để làm cơ sở ban đầu đánh giá những thay đổi tiềm tàng ở phổi sau điều trị.
Trong trường hợp có các triệu chứng ở phổi mới xuất hiện hoặc trở nên trầm trọng hơn (ví dụ, ho, khó thở), cần tiến hành đánh giá chẩn đoán ngay và bệnh nhân được điều trị thích hợp. Tỷ số lợi ích/nguy cơ cần được xem xét trước khi tiếp tục điều trị bằng VELCADE.
Trong một thử nghiệm lâm sàng, hai bệnh nhân (một trong số 2 bệnh nhân) dùng cytarabine liều cao (2 g/m2/ngày) bằng cách truyền liên tục trong 24 giờ với daunorubicin và VELCADE để điều trị bệnh bạch cầu cấp dòng tủy tái phát đã tử vong do ARDS trong giai đoạn đầu của quá trình điều trị, và nghiên cứu đã bị ngừng. Vì vậy, không khuyến cáo phác đồ cụ thể này với việc dùng đồng thời liều cao cytarabine (2 g/m2/ngày) bằng cách truyền liên tục trong 24 giờ.
Suy thận
Các biến chứng trên thận thường xảy ra ở bệnh nhân đa u tủy. Bệnh nhân suy thận cần được theo dõi chặt chẽ (xem Liều lượng và cách dùng và Dược động học).
Suy gan
Bortezomib được chuyển hóa bởi các enzym gan. Nồng độ bortezomib tăng ở những bệnh nhân suy gan trung bình hoặc nặng; những bệnh nhân này nên giảm liều điều trị của VELCADE và theo dõi chặt chẽ về độc tính (xem Liều lượng và cách dùng và Dược động học).
Phản ứng trên gan
Các trường hợp hiếm gặp bị suy gan đã được báo cáo ở bệnh nhân dùng VELCADE và các thuốc dùng đồng thời với các tình trạng bệnh lý nền nghiêm trọng. Các phản ứng khác của gan được báo cáo bao gồm tăng các enzym gan, tăng bilirubin máu, và viêm gan. Những thay đổi này có thể hồi phục khi ngừng dùng bortezomib (xem Tác dụng ngoại ý).
Hội chứng ly giải khối u
Do bortezomib là một tác nhân gây độc tế bào và có thể nhanh chóng tiêu diệt các tế bào ác tính và tế bào MCL, nên có thể xảy ra các biến chứng của hội chứng ly giải khối u. Bệnh nhân có nguy cơ hội chứng ly giải khối u là những người có khối u lớn/nhiều trước khi điều trị. Những bệnh nhân này nên được theo dõi chặt chẽ và áp dụng các biện pháp phòng ngừa thích hợp.
Các thuốc dùng đồng thời
Bệnh nhân nên được theo dõi chặt chẽ khi dùng bortezomib kết hợp với các thuốc ức chế CYP3A4 mạnh. Cần thận trọng khi phối hợp bortezomib với các cơ chất của CYP3A4 hoặc CYP2C19 (xem Tương tác).
Cần xác nhận chức năng gan bình thường và cần thận trọng khi dùng thuốc ở những bệnh nhân đang dùng thuốc hạ đường huyết đường uống (xem Tương tác).
Phản ứng tiềm tàng qua trung gian phức hợp miễn dịch
Các phản ứng tiềm tàng qua trung gian phức hợp miễn dịch, như phản ứng kiểu bệnh huyết thanh, viêm đa khớp với phát ban và viêm thận cầu thận tăng sinh đã được báo cáo ít gặp. Nên ngừng bortezomib nếu phản ứng nghiêm trọng xảy ra.
Ảnh hưởng trên khả năng lái xe và vận hành máy móc
VELCADE có thể gây ảnh hưởng trung bình đến khả năng lái xe và sử dụng máy móc. VELCADE có thể gây ra mệt mỏi với tần suất rất thường gặp, chóng mặt với tần suất thường gặp, ngất với tần suất không thường gặp, hạ huyết áp tư thế/ hạ huyết áp thế đứng hoặc nhìn mờ với tần suất thường gặp. Do đó, bệnh nhân phải thận trọng khi lái xe hoặc sử dụng máy móc và cần được khuyên không lái xe hoặc vận hành máy móc nếu gặp các triệu chứng này (xem Tác dụng ngoại ý).
Quá Liều
Ở các bệnh nhân, dùng quá liều gấp hai lần liều khuyến cáo có liên quan đến triệu chứng hạ huyết áp và giảm tiểu cầu cấp tính gây tử vong. Đối với các nghiên cứu tiền lâm sàng về an toàn trên tim mạch, xem An toàn tiền lâm sàng.
Chưa có thuốc giải độc đặc hiệu khi quá liều bortezomib. Trong trường hợp dùng thuốc quá liều, cần theo dõi các dấu hiệu sinh tồn của bệnh nhân và chăm sóc hỗ trợ thích hợp để duy trì huyết áp (như truyền dịch, các thuốc tăng huyết áp, và/hoặc các thuốc tăng co bóp cơ tim) và nhiệt độ cơ thể (xem Liều lượng và cách dùng và Cảnh báo).
Chống chỉ định
Mẫn cảm với hoạt chất, với boron hoặc với bất kỳ tá dược nào (mannitol, nitrogen).
Bệnh phổi và màng ngoài tim thâm nhiễm lan tỏa cấp tính.
Khi sử dụng VELCADE phối hợp với các thuốc khác, hãy tham khảo Tóm tắt Đặc tính sản phẩm các thuốc này về các chống chỉ định khác.
Sử dụng ở phụ nữ có thai và cho con bú
Tránh thai ở nam và nữ
Bệnh nhân nam và nữ có khả năng sinh đẻ phải sử dụng các biện pháp tránh thai hiệu quả trong thời gian điều trị và đến 3 tháng sau điều trị.
Mang thai
Hiện không có dữ liệu lâm sàng về phơi nhiễm bortezomib trong thai kỳ. Chưa nghiên cứu đầy đủ tiềm năng gây quái thai của bortezomib.
Trong các nghiên cứu tiền lâm sàng, bortezomib không có ảnh hưởng đến sự phát triển của phôi/thai ở chuột cống và thỏ với liều cao nhất dung nạp được ở con mẹ. Các nghiên cứu trên động vật để xác định ảnh hưởng của bortezomib trên quá trình sinh đẻ và phát triển sau khi sinh chưa được tiến hành (xem An toàn tiền lâm sàng). Không nên dùng VELCADE trong thời gian mang thai trừ khi tình trạng lâm sàng của người phụ nữ đòi hỏi cần điều trị bằng VELCADE.
Nếu VELCADE được sử dụng trong thời kỳ mang thai, hoặc nếu bệnh nhân có thai trong khi đang dùng thuốc, bệnh nhân cần được thông báo về khả năng gây hại cho thai nhi.
Thalidomide là một hoạt chất có đặc tính gây quái thai, mà gây ra dị tật bẩm sinh nặng đe dọa tính mạng. Chống chỉ định sử dụng thalidomide trong thời kỳ mang thai và ở phụ nữ có khả năng sinh đẻ trừ khi tất cả các điều kiện của chương trình ngừa thai khi dùng thalidomide được đáp ứng. Bệnh nhân dùng VELCADE phối hợp với thalidomide cần tuân thủ chương trình ngừa thai của thalidomide. Tham khảo Tóm tắt Đặc tính sản phẩm của thalidomide để biết thêm thông tin.
Cho con bú
Không rõ liệu bortezomib có bài tiết vào sữa mẹ hay không. Vì có thể gặp phản ứng có hại nghiêm trọng ở trẻ bú sữa mẹ, nên ngừng cho con bú khi đang điều trị bằng VELCADE.
Khả năng sinh sản
Các nghiên cứu về khả năng sinh sản chưa được tiến hành với VELCADE (xem An toàn tiền lâm sàng).
Tương tác
Các nghiên cứu in vitro cho thấy bortezomib là một chất ức chế yếu các isozyme cytochrome P450 (CYP) 1A2, 2C9, 2C19, 2D6 và 3A4. Dựa trên sự đóng góp hạn chế (7%) của CYP2D6 đến chuyển hóa của bortezomib, kiểu hình chất chuyển hóa CYP2D6 yếu không được cho là gây ảnh hưởng đến phân bố chung của bortezomib.
Một nghiên cứu tương tác thuốc-thuốc đã đánh giá ảnh hưởng của ketoconazole, một chất ức chế CYP3A4 mạnh, trên dược động học của bortezomib (tiêm tĩnh mạch) cho thấy AUC của bortezomib tăng trung bình 35% (CI 90% [1,032 đến 1,772]), dựa trên dữ liệu từ 12 bệnh nhân. Do đó, bệnh nhân nên được theo dõi chặt chẽ khi dùng bortezomib kết hợp với các chất ức chế CYP3A4 mạnh (ví dụ ketoconazole, ritonavir).
Trong một nghiên cứu tương tác thuốc-thuốc đánh giá ảnh hưởng của omeprazole, một chất ức chế CYP2C19 mạnh, trên dược động học của bortezomib (tiêm tĩnh mạch), không thấy ảnh hưởng đáng kể đến dược động học của bortezomib, dựa trên dữ liệu từ 17 bệnh nhân.
Một nghiên cứu tương tác thuốc - thuốc đánh giá tác dụng của rifampicin, một thuốc gây cảm ứng CYP3A4 mạnh, trên dược động học của bortezomib (tiêm tĩnh mạch) cho thấy AUC của bortezomib giảm trung bình 45%, dựa trên dữ liệu của 6 bệnh nhân. Do đó, không khuyến cáo sử dụng đồng thời bortezomib với các thuốc cảm ứng CYP3A4 mạnh (như rifampicin, carbamazepine, phenytoin, phenobarbital và St John's Wort) vì có thể giảm hiệu quả.
Trong cùng nghiên cứu tương tác thuốc - thuốc đánh giá ảnh hưởng của dexamethasone, một thuốc gây cảm ứng CYP3A4 yếu hơn, trên dược động học của bortezomib (tiêm tĩnh mạch), không thấy có ảnh hưởng đáng kể đến dược động học của bortezomib, dựa trên dữ liệu từ 7 bệnh nhân.
Một nghiên cứu tương tác thuốc - thuốc đánh giá ảnh hưởng của melphalan - prednisone trên dược động học của bortezomib (tiêm tĩnh mạch), cho thấy AUC của bortezomib tăng trung bình 17%, dựa trên dữ liệu của 21 bệnh nhân. Tác dụng này được xem là không có ý nghĩa lâm sàng.
Trong các thử nghiệm lâm sàng, ít gặp báo cáo hạ đường huyết và thường gặp báo cáo tăng đường huyết ở những bệnh nhân tiểu đường đang dùng thuốc hạ đường huyết đường uống. Bệnh nhân uống thuốc điều trị tiểu đường mà dùng VELCADE có thể cần phải theo dõi chặt chẽ nồng độ đường trong máu và điều chỉnh liều thuốc tiểu đường của họ.
Tương kỵ
Không được trộn lẫn thuốc này với các thuốc khác trừ những thuốc được đề cập đến trong phần "Hướng dẫn sử dụng''.
Tác dụng ngoại ý
Tóm tắt hồ sơ an toàn
Các phản ứng bất lợi nghiêm trọng ít được báo cáo trong quá trình điều trị bằng VELCADE bao gồm suy tim, hội chứng ly giải khối u, tăng huyết áp động mạch phổi, hội chứng bệnh não tuần hoàn sau có thể hồi phục (posterior reversible encephalopathy syndrome-PRES), rối loạn phổi thâm nhiễm lan tỏa cấp tính và hiếm gặp bệnh lý thần kinh tự động.
Các phản ứng bất lợi thường gặp nhất khi điều trị với VELCADE là buồn nôn, tiêu chảy, táo bón, nôn, mệt mỏi, sốt, giảm tiểu cầu, thiếu máu, giảm bạch cầu trung tính, bệnh lý thần kinh ngoại biên (bao gồm thần kinh cảm giác), đau đầu, dị cảm, giảm ngon miệng, khó thở, phát ban, Herpes zoster và đau cơ.
Bảng tóm tắt phản ứng bất lợi
Đa u tủy
Tác dụng không mong muốn trong Bảng 7 được đánh giá bởi các nghiên cứu viên có ít nhất một mối quan hệ nhân quả ở mức có thể hoặc có khả năng xảy ra với VELCADE. Những phản ứng bất lợi này dựa trên một bộ dữ liệu tích hợp trên 5476 bệnh nhân, trong đó 3996 bệnh nhân được điều trị bằng VELCADE với liều 1,3 mg/m2 và được đưa vào Bảng 7.
Nhìn chung, VELCADE được dùng để điều trị đa u tủy trên 3974 bệnh nhân.
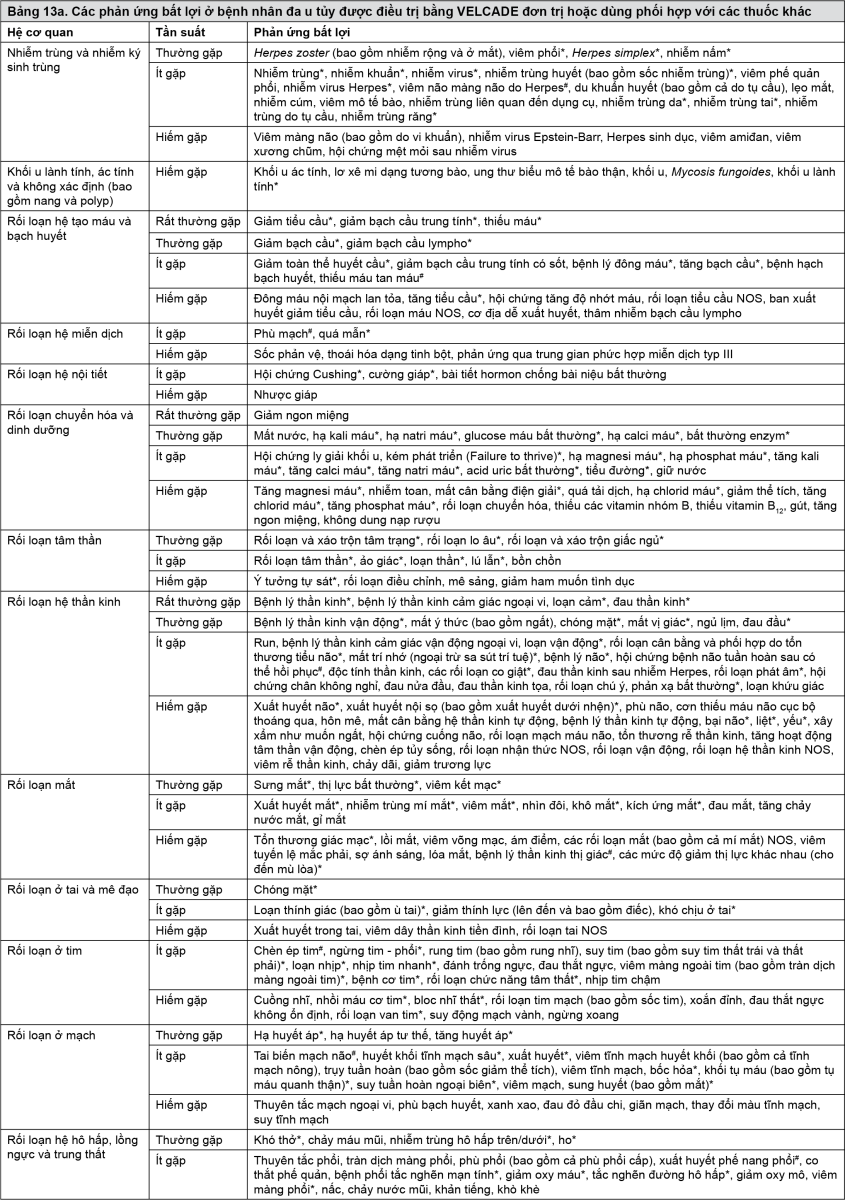
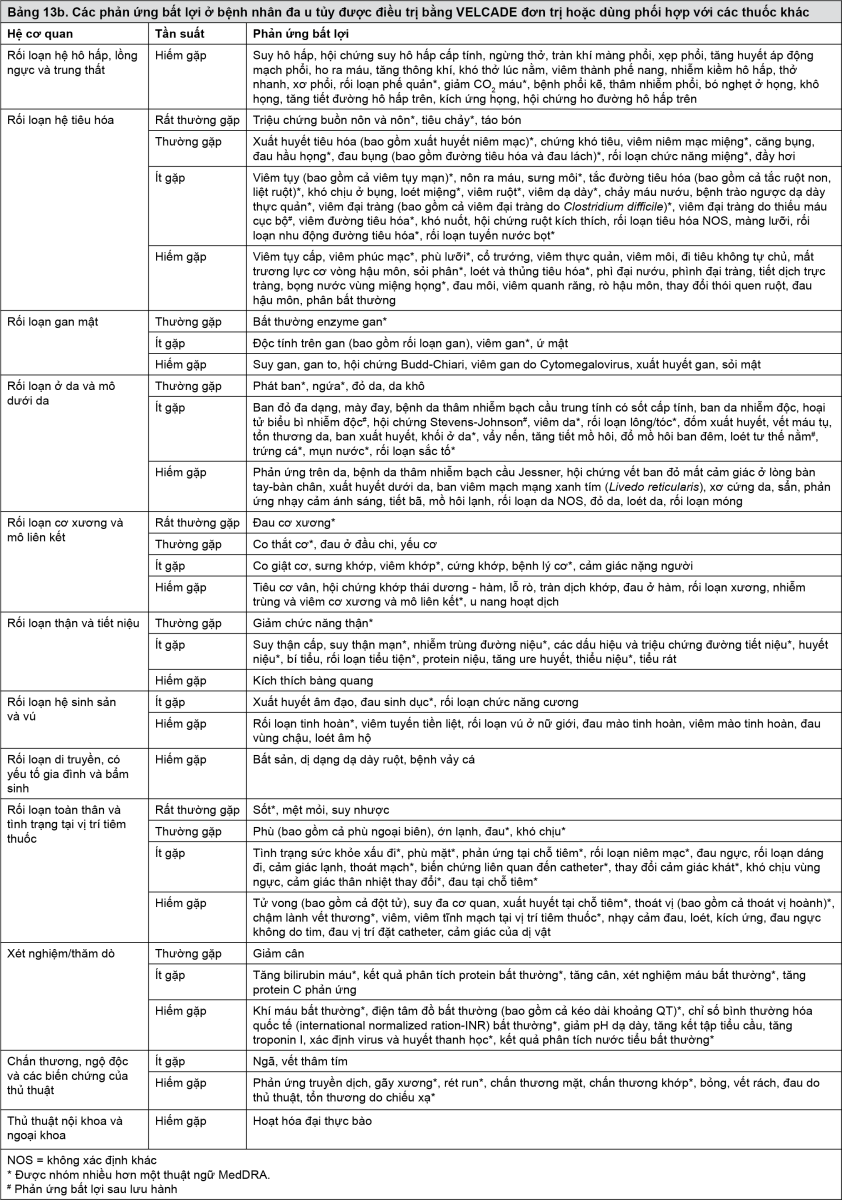
Phản ứng bất lợi được liệt kê dưới đây theo hệ cơ quan và nhóm tần suất. Các tần suất được định nghĩa là: Rất thường gặp (≥1/10); thường gặp (≥1/100 đến <1/10); ít gặp (≥ 1/1.000 đến <1/100); hiếm gặp (≥1/10.000 đến <1/1.000); rất hiếm gặp (<1/10.000); chưa biết (không thể ước lượng tần suất từ dữ liệu sẵn có). Trong mỗi nhóm tần suất, tác dụng không mong muốn được trình bày theo thứ tự giảm dần về mức độ nghiêm trọng. Bảng 13a & 13b đã được tạo ra dựa trên phiên bản 14.1 của MedDRA. Các phản ứng bất lợi xuất hiện trong giai đoạn sau khi thuốc lưu hành mà không gặp trong các thử nghiệm lâm sàng cũng được đưa vào.
- xem Bảng 13a & 13b.
U lympho tế bào vỏ (MCL)
Hồ sơ an toàn của VELCADE trên 240 bệnh nhân MCL điều trị bằng VELCADE với liều 1,3 mg/m2 phối hợp với rituximab, cyclophosphamide, doxorubicin và prednisone (phác đồ VcR-CAP) so với 242 bệnh nhân điều trị bằng rituximab, cyclophosphamide, doxorubicin, vincristine, và prednisone [phác đồ R-CHOP] tương đối nhất quán những gì được quan sát thấy ở bệnh nhân đa u tủy với những khác biệt chính được mô tả dưới đây. Các phản ứng bất lợi bổ sung được xác định là có liên quan đến việc sử dụng liệu pháp kết hợp (VcR-CAP) là nhiễm virus viêm gan B (<1%) và thiếu máu cục bộ cơ tim (1,3%). Tần suất tương tự của các biến cố này ở cả hai nhóm điều trị, chỉ ra rằng các phản ứng bất lợi này không chỉ do VELCADE. Sự khác biệt đáng chú ý trong nhóm bệnh nhân MCL so với các bệnh nhân trong các nghiên cứu đa u tủy là tần suất xuất hiện các phản ứng bất lợi về huyết học cao hơn ≥ 5% (giảm bạch cầu trung tính, giảm tiểu cầu, giảm bạch cầu, thiếu máu, giảm bạch cầu lympho), bệnh thần kinh cảm giác ngoại biên, tăng huyết áp, sốt, viêm phổi, viêm miệng, và rối loạn tóc/lông.
Các phản ứng bất lợi được xác định có tần suất mắc ≥1%, tương tự hoặc cao hơn ở nhóm VcR-CAP và ít nhất có mối quan hệ nhân quả ở mức có thể hoặc có khả năng với các thành phần của nhóm VcR-CAP, được liệt kê trong Bảng 8. Bảng này cũng bao gồm phản ứng bất lợi của thuốc được xác định trong nhóm VcR-CAP mà đã được các nghiên cứu viên đánh giá là có ít nhất một mối quan hệ nhân quả ở mức có thể hoặc có khả năng với VELCADE dựa trên dữ liệu lịch sử trong các nghiên cứu đa u tủy.
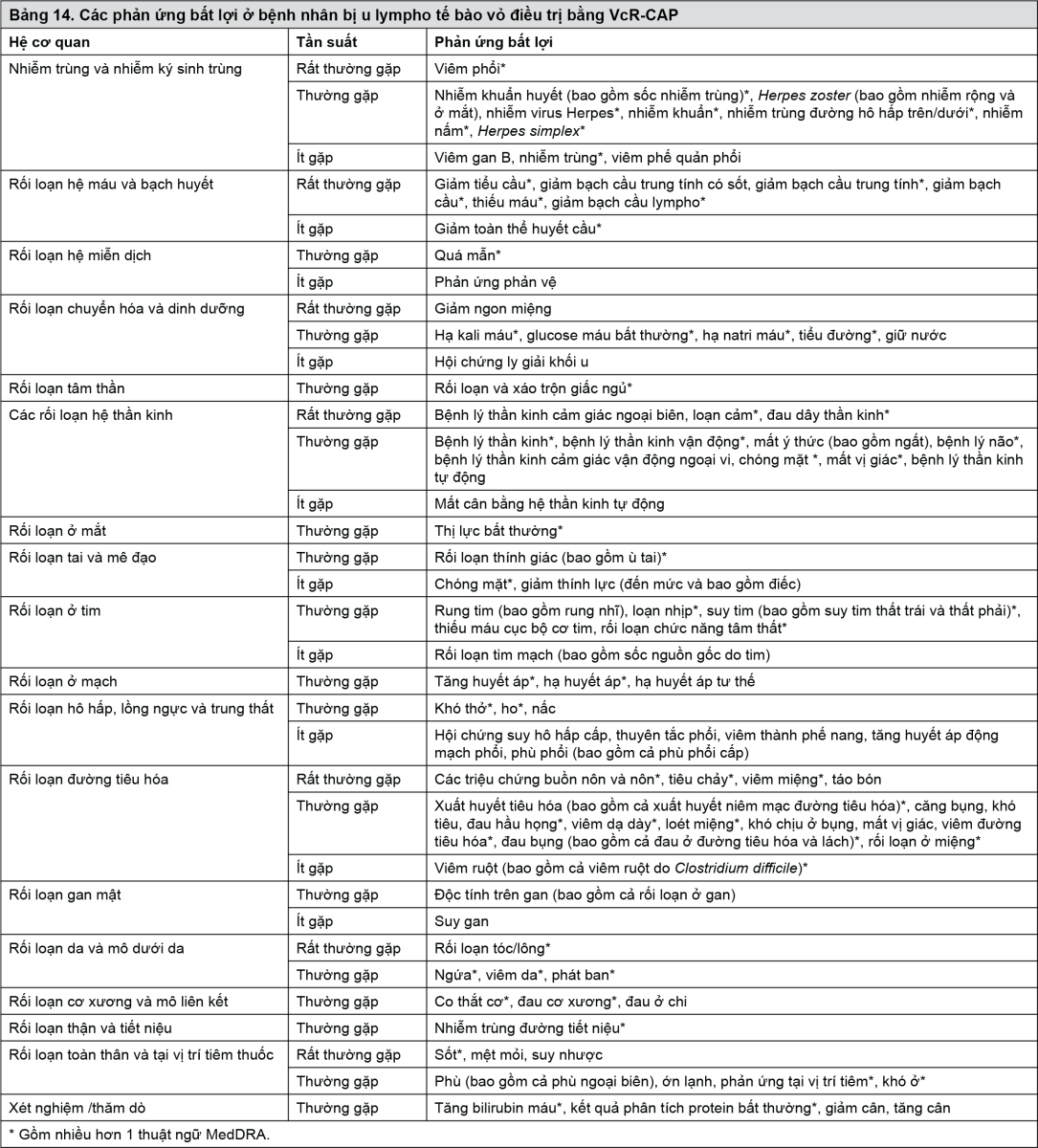
Phản ứng bất lợi được liệt kê dưới đây theo hệ cơ quan và nhóm tần suất. Các tần suất được định nghĩa là: Rất thường gặp (≥1/10); thường gặp (≥1/100 đến <1/10); ít gặp (≥1/1.000 đến <1/100); hiếm gặp (≥1/10.000 đến <1/1.000); rất hiếm gặp (<1/10.000), chưa biết (không thể ước lượng tần suất từ dữ liệu sẵn có). Trong mỗi nhóm tần suất, tác dụng không mong muốn được trình bày theo thứ tự giảm dần về mức độ nghiêm trọng. Bảng 14 đã được tạo ra dựa trên phiên bản 16 của MedDRA.
- xem Bảng 14.
Mô tả một số phản ứng bất lợi
Tái hoạt hóa virus Herpes zoster
Đa u tủy: Đã dùng thuốc kháng virus dự phòng cho 26% bệnh nhân trong nhóm Vc+M+P. Tỷ lệ mắc Herpes zoster trong số bệnh nhân ở nhóm điều trị Vc+M+P là 17% đối với bệnh nhân không điều trị dự phòng bằng thuốc kháng virus so với 3% đối với bệnh nhân được điều trị dự phòng bằng thuốc kháng virus.
U lympho tế bào vỏ: Dự phòng bằng thuốc kháng virus được dùng cho 137 trong số 240 bệnh nhân (57%) trong nhóm VcR-CAP. Tỷ lệ mắc Herpes zoster trong số các bệnh nhân trong nhóm VcR-CAP là 10,7% đối với bệnh nhân không điều trị dự phòng bằng thuốc kháng virus so với 3,6% đối với bệnh nhân điều trị dự phòng bằng thuốc kháng virus (xem Cảnh báo).
Tái hoạt hóa và nhiễm virus viêm gan B (HBV)
U lympho tế bào vỏ: Nhiễm HBV với kết cục tử vong xuất hiện ở 0,8% (n=2) bệnh nhân trong nhóm điều trị không dùng VELCADE (rituximab, cyclophosphamide, doxorubicin, vincristine, prednisone; R-CHOP) và 0,4% (n = 1) các bệnh nhân dùng VELCADE phối hợp với rituximab, cyclophosphamide, doxorubicin, và prednisone (VcR-CAP). Tỷ lệ chung nhiễm virus viêm gan B cũng tương tự ở những bệnh nhân được điều trị bằng VcR-CAP hoặc với R-CHOP (lần lượt là 0,8% so với 1,2%).
Bệnh lý thần kinh ngoại biên trong phác đồ phối hợp
Đa u tủy: Trong các thử nghiệm với VELCADE được điều trị như là một thuốc điều trị tấn công phối hợp với dexamethasone (nghiên cứu IFM-2005-01) và dexamethasone-thalidomide (nghiên cứu MMY-3010), tỷ lệ mắc bệnh lý thần kinh ngoại biên trong phác đồ phối hợp được trình bày trong Bảng 15:
- xem Bảng 15.

U lympho tế bào vỏ: Trong nghiên cứu LYM-3002, VELCADE được dùng với rituximab, cyclophosphamide, doxorubicin và prednisone (R-CAP), tỷ lệ mắc bệnh lý thần kinh ngoại biên trong phác đồ phối hợp được trình bày trong Bảng 16:
- xem Bảng 16.

Bệnh nhân MCL cao tuổi
42,9% bệnh nhân trong nhóm VcR-CAP trong độ tuổi 65-74 tuổi và 10,4% bệnh nhân ≥ 75 tuổi. Mặc dù ở bệnh nhân ≥ 75 tuổi, cả VcR-CAP và R-CHOP đều kém dung nạp hơn, tỷ lệ biến cố bất lợi nghiêm trọng ở nhóm VcR-CAP là 68%, so với 42% ở nhóm R-CHOP.
Khác biệt đáng chú ý trong dữ liệu an toàn của VELCADE tiêm dưới da so với tiêm tĩnh mạch khi đơn trị liệu
Trong một nghiên cứu pha III, những bệnh nhân dùng VELCADE tiêm dưới da so với tiêm tĩnh mạch, tỷ lệ chung về phản ứng ngoại ý liên quan đến điều trị ở Độ ≥ 3 là thấp hơn 13%, và tỷ lệ ngừng điều trị VELCADE là thấp hơn 5%. Tỷ lệ chung về tiêu chảy, đau dạ dày ruột và đau bụng, suy nhược cơ thể, nhiễm trùng đường hô hấp trên và bệnh lý thần kinh ngoại biên là thấp hơn 12% - 15% ở nhóm tiêm dưới da so với nhóm tiêm tĩnh mạch. Ngoài ra tỷ lệ bệnh lý thần kinh ngoại biên ở Độ ≥ 3 là thấp hơn 10% và tỷ lệ ngừng thuốc do bệnh lý thần kinh ngoại biên thấp hơn 8% ở nhóm tiêm dưới da so với nhóm tiêm tĩnh mạch.
6% bệnh nhân có phản ứng bất lợi tại chỗ tiêm dưới da, phần lớn là đỏ da. Các trường hợp hồi phục trung bình trong 6 ngày, cần điều chỉnh liều trên hai bệnh nhân. Hai bệnh nhân (1%) có phản ứng nghiêm trọng; 1 trường hợp bị ngứa và 1 trường hợp đỏ da.
Tỉ lệ tử vong khi điều trị ở nhóm tiêm dưới da là 5% và ở nhóm tiêm tĩnh mạch là 7%. Tỷ lệ tử vong do "bệnh tiến triển" ở nhóm tiêm dưới da là 18% và ở nhóm tiêm tĩnh mạch là 9%.
Điều trị lại cho bệnh nhân đa u tuỷ tái phát
Trong một nghiên cứu với VELCADE được điều trị lại cho 130 bệnh nhân đa u tủy tái phát, những người trước đây có ít nhất đáp ứng một phần với phác đồ có chứa VELCADE, các biến cố bất lợi thường gặp nhất ở tất cả các mức độ, xảy ra ít nhất ở 25% số bệnh nhân là giảm tiểu cầu (55%), bệnh lý thần kinh (40%), thiếu máu (37%), tiêu chảy (35%) và táo bón (28%). Bệnh lý thần kinh ngoại biên tất cả mức độ và độ ≥ 3 được ghi nhận lần lượt ở 40% và 8,5% số bệnh nhân.
Báo cáo các trường hợp nghi ngờ phản ứng bất lợi
Báo cáo các trường hợp nghi ngờ phản ứng bất lợi sau khi cấp phép lưu hành sản phẩm là rất quan trọng. Nó cho phép tiếp tục theo dõi cân bằng lợi ích/nguy cơ của sản phẩm. Các cán bộ y tế được yêu cầu báo cáo bất kỳ trường hợp nghi ngờ phản ứng bất lợi nào thông qua hệ thống báo cáo quốc gia.
Bảo quản
Không bảo quản thuốc ở nhiệt độ trên 30oC.
Giữ thuốc trong hộp để tránh ánh sáng.
Dung dịch hoàn nguyên phải được sử dụng ngay sau khi pha. Nếu không được sử dụng ngay, thời gian và điều kiện bảo quản trong quá trình sử dụng trước khi dùng thuốc là trách nhiệm của người sử dụng. Tuy nhiên, dung dịch hoàn nguyên trong quá trình sử dụng đã được chứng minh là ổn định về hóa học và vật lý trong vòng 8 giờ khi bảo quản ở 25°C trong lọ ban đầu và/hoặc một bơm tiêm. Tổng thời gian bảo quản thuốc sau khi hoàn nguyên không được vượt quá 8 giờ trước khi dùng.
Phân loại ATC
L01XX32 - bortezomib
Trình bày/Đóng gói
Bột đông khô pha tiêm: hộp 1 lọ.
- Abacavir
- Abernil
- Abiiogran
- Acarbose
- ACC
- Acebutolol
- Acenocoumarol
- Acetate Ringer's
- Acetazolamide
- Acetylcystein
- Acetylsalicylic acid
- Aciclovir
- Acid acetylsalicylic
- Acid aminocaproic
- Acid ascorbic
- Acid boric
- Acid chenodeoxycholic
- Acid ethacrynic
- Acid folic
- Acid fusidic
- Acid iopanoic
- Acid ioxaglic
- Acid nalidixic
- Acid pantothenic
- Acid para-aminobenzoic
- Acid salicylic
- Acid tranexamic
- Acid valproic
- Acid zoledronic
- Acitretin
- Aclasta
- Aclon
- Actapulgite
- Actelsar
- Actelsar HCT
- Actemra
- Actilyse
- Acular
- Acupan
- Acuvail
- Acyclovir STADA
- Acyclovir STADA Cream
- Adalat
- Adenosin
- Adenosin Ebewe
- Adipiodon
- Advagraf
- Aerius
- Afinitor
- Agicarvir
- Agifovir-E
- Agilosart
- Agilosart-H
- Agimepzol
- Agimosarid
- Agimstan
- Agimstan-H
- Agiremid
- Agivastar
- Aibezym
- Air-X
- Alaxan
- Albendazol
- Albiomin
- Albumin
- Albumin người Grifols 20%
- Albuminar
- AlbuRx
- Albutein
- Alcuronium chloride
- Aldesleukin
- Alendronat
- Alertin
- Alfa-Lipogamma 600 Oral
- Alfuzosin hydrochlorid
- Algotra
- Alimemazin
- Alimta
- Allipem
- Allopurinol
- Allopurinol STADA
- Aloxi
- Alprazolam
- Alpha Chymotrypsin
- Alpha tocopherol
- Alphachymotrypsin Glomed
- Alphagan-P
- Aluvia
- Alzental
- Amaryl
- Ambroco
- Ambroxol
- Amcinol-Paste
- Amigold
- Amikacin
- Aminocaproic acid
- Aminoleban
- Aminoleban Oral
- Aminosteril N-Hepa
- Amiparen
- Amitriptyline
- Amiyu
- Amlodipine
- Amlor
- Amoxicillin
- Amoxicillin & clavulanate
- Ampicillin
- Amquitaz
- Anaferon for children
- Anargil
- Anaropin
- Andriol Testocaps
- Anepzil
- Anyfen
- Apaisac
- Apidra SoloStar
- Apitim 5
- Aprovel
- Aquaphil
- Arcalion
- Arcoxia
- Aricept Evess
- Arimidex
- Arnetine
- Artrodar
- A-Scabs
- Ascorbic acid
- Asperlican/Candinazol
- Aspilets EC
- Aspirin
- Asthmatin
- Atelec
- Atocib 120
- Atocib 90
- Atosiban PharmIdea
- Atozet
- Attapulgite
- Atussin
- Atropin
- Augbactam
- Augmentin Sachet
- Augmentin SR
- Augmentin Tablets
- Augmex
- Avamys
- Avastin
- Avelox Dịch truyền
- Avelox Viên nén
- Avodart
- Axcel Cefaclor-125 Suspension
- Axcel Cetirizine Syrup
- Axcel Chlorpheniramine
- Axcel Dexchlorpheniramine
- Axcel Dicyclomine-S Syrup
- Axcel Diphenhydramine Paediatric Syrup
- Axcel Erythromycin ES
- Axcel Eviline
- Axcel Fungicort Cream
- Axcel Fusidic acid Cream
- Axcel Fusidic acid-B Cream
- Axcel Hydrocortisone Cream
- Axcel Lignocaine 2% Sterile Gel
- Axcel Loratadine
- Axcel Miconazole Cream
- Axcel Paracetamol
- Axcel Urea Cream
- Axitan
- Azenmarol
- Azicine
- Aziphar
- Azithromycin