Nhà sản xuất
AbbVie
Thành phần
Mỗi viên: Lopinavir 200mg, ritonavir 50mg.
Mô tả
ALUVIA (lopinavir/ritonavir) là một công thức phối hợp của lopinavir và ritonavir. Lopinavir là một chất ức chế HIV protease. Khi dùng phối hợp trong ALUVIA, ritonavir ức chế sự chuyển hóa qua trung gian CYP3A của lopinavir, do đó làm tăng nồng độ lopinavir trong huyết tương.
Lopinavir có công thức hóa học là [1S-[1R*,(R*), 3R*, 4R*]]-N-[4-[[(2,6-dimethylphenoxy) acetyl] amino] -3-hydroxy-5-phenyl-1-(phenylmethyl)pentyl]telrahydro-alpha-(1-methylethyl)-2-oxo-1(2H)-pyrimidinacetamid.
Công thức phân tử là C37H48N4O5, và phân tử lượng là 628,80.
Ritonavir có công thức hóa học là 10-Hydroxy-2-methyl-5-(1-methylethyl)-1-[2-(1-methylethyl)-4-thiazolyl]-3,6-dioxo-8,11-bis(phenylmethyl)-2,4,7,12-tetraazatridecan-13-oic acid, 5-thiazolylmethyl ester, [5S-(5R*,8R*,10R*,11R*)].
Công thức phân tử là C37H48N6O5S2 và phân tử lượng là 720,95.
Lopinavir là bột trắng đến nâu nhạt, tan tự do trong methanol và ethanol, tan trong isopropanol và thực tế không tan trong nước.
Viên nén bao film ALUVIA dùng để uống chứa 200 mg lopinavir và 50 mg ritonavir với các tá dược sau đây: copovidon, sorbitan monolaurat, colloidal silicon dioxid và natri stearyl fumarat. Các tá dược bao phim gồm: hypromellos, titan dioxid, macrogol 400, hydroxypropyl cellulose, bột talc, colloidal silicon dioxid, macrogol 3350, oxid sắt E172 và polysorbat 80.
Dược lý
Dược lực học
Nhóm trị liệu: Thuốc kháng virus đường dùng toàn thân, ức chế protease, điều trị nhiễm HIV, dạng thuốc phối hợp, mã ATC: J05AR10
Cơ chế tác dụng: Hoạt chất kháng virus của Aluvia là lopinavir. Lopinavir là chất ức chế enzym protease của virus HIV-1 và HIV-2. Sự ức chế protease của HIV ngăn cản thủy phân gag-pol polyprotein dẫn đến hình thành ra các virus không hoàn chỉnh và không lây nhiễm.
Ảnh hưởng trên điện tâm đồ: Ảnh hưởng của thuốc lên khoảng QTcF được đánh giá trong một nghiên cứu ngẫu nhiên, có kiểm soát, chéo đôi, dùng đối chứng placebo và moxifloxacin 400 mg 1 lần mỗi ngày, tiến hành trên 39 người tình nguyện khỏe mạnh với 10 lần ghi điện tâm đồ trong vòng 12 giờ vào ngày thứ 3. Giá trị trung bình khác biệt (khoảng tin cậy 95%) của khoảng QTcF so với placebo là 3,6 (6,3) với liều 400/100mg 2 lần mỗi ngày và 13,1 (15,8) với liều lớn hơn liều điều trị 800/200mg 2 lần mỗi ngày. Liponavir/ritonavir liều cao (800/200mg 2 lần mỗi ngày) làm kéo dài khoảng QRS từ 6 mili giây lên 9,5 mili giây góp phần kéo dài khoảng QT. Giá trị khoảng QTcF ghi nhận được trong ngày thứ 3 tương ứng với 2 chế độ liều trên cao hơn gấp 1,5 lần và 3 lần so với liều khuyến cáo của liponavir/ritonavir sử dụng 1 lần mỗi ngày hoặc 2 lần mỗi ngày ở trạng thái cân bằng. Không bệnh nhân nào có mức tăng QTcF ≥60 mili giây so với giá trị nền hoặc khoảng QTcF vượt quá ngưỡng có thể gây biểu hiện trên lâm sàng là 500 mili giây.
Cùng trong nghiên cứu này, sự tăng nhẹ khoảng PR cũng được ghi nhận ở các bệnh nhân dùng liponavir/ritonavir vào ngày thứ 3. Mức thay đổi trung bình so với giá trị nền của khoảng PR nằm trong khoảng 11,6 đến 24,4 mili giây được ghi nhận trong vòng 12 giờ sau khi dùng thuốc. Khoảng PR tối đa ghi nhận được là 286 mili giây và không ghi nhận được trường hợp nào có giá trị hàng giây trong hay block tim độ 2 hoặc độ 3 nào (xem phần Cảnh báo).
Hoạt tính kháng virus trên in vitro: Hoạt tính kháng virus trên in vitro của lopinavir với chủng HIV phòng thí nghiệm và phân lập từ lâm sàng đã được đánh giá tương ứng trên các dòng nguyên bào lympho và các tế bào lympho máu ngoại biên gây nhiễm. Trong trường hợp không có mặt huyết thanh người, IC50 trung bình của lopinavir với 5 chủng HIV-1 phòng thí nghiệm là 19 nM. Trong trường hợp không có mặt và có 50% huyết thanh người thì giá trị IC50 trung bình của lopinavir với chúng HIV-1IIIB trên dòng tế bào MT4 tương ứng là 17 nM và 102 nM. Ở trường hợp không có mặt huyết thanh người, giá trị EC50 trung bình của lopinavir với một số chủng HIV-1 được phân lập từ lâm sàng là 6,5 nM.
Kháng thuốc
Chọn lọc kháng thuốc trên in vitro: Một số chủng phân lập HIV-1 giảm nhạy cảm với lopinavir đã được chọn lọc trên in vitro. HIV-1 được nuôi cấy trong môi trường có chứa lopinavir đơn độc và chứa liponavir kết hợp ritonavir ở các tỷ lệ nồng độ tương ứng với khoảng nồng độ được ghi nhận trong quá trình điều trị bằng Aluvia. Phân tích kiểu gen và kiểu hình các virus được chọn lọc trong môi trường này cho thấy sự có mặt của ritonavir, với các nồng độ thử không ảnh hưởng đến việc chọn lọc virus kháng lopinavir. Nhìn chung, phân tích đặc điểm kiểu hình đề kháng chéo trên in vitro giữa lopinavir và các thuốc ức chế protease khác cho thấy sự giảm nhạy cảm với lopinavir có mối tương quan chặt chẽ với sự giảm nhạy cảm với ritonavir và indinavir, nhưng không có mối tương quan chặt chẽ nào với sự giảm nhạy cảm với amprenavir, saquinavir và nelfinavir.
Phân tích kháng thuốc ở bệnh nhân chưa điều trị thuốc ARV: Trong các nghiên cứu lâm sàng với số lượng hạn chế chủng phân lập được lựa chọn đề kháng lopinavir chưa được ghi nhận ở bệnh nhân mới không có kháng ức chế protease ở mức nền (xem thêm thông tin chi tiết trong các thử nghiệm lâm sàng).
Phân tích kháng thuốc ở bệnh nhân đã điều trị thuốc ức chế protease
Chọn lọc đề kháng với lopinavir ở bệnh nhân bị thất bại với phác đồ điều trị bằng thuốc ức chế protease trước đó được mô tả bằng phân tích dọc các chủng phân lập được từ 19 bệnh nhân đã điều trị với thuốc ức chế protease trong 2 nghiên cứu pha II và một nghiên cứu pha III, đối tượng nghiên cứu bao gồm những bệnh nhân không ức chế được hoàn toàn sự phát triển của virus hoặc có sự tăng số lượng virus bật lại sau khi đã có đáp ứng ban đầu với thuốc và những bệnh nhân có tăng kháng thuốc trên in vitro giữa mức nền và mức bật lại (được định nghĩa là sự xuất hiện đột biến mới hoặc thay đổi 2 lần nhạy cảm kiểu hình với lopinavir). Sự kháng thuốc tăng lên phổ biến nhất ở bệnh nhân mà chủng phân lập nền đã có một số đột biến khác liên quan đến các thuốc ức chế protease, nhưng mức độ nhạy cảm với lopinavir < 40 lần so với mức nền. Những đột biến thường gặp nhất là V82A, I54V và M46I. Các đột biến L33F, I50V và V32I phối hợp với I47V/A cũng đã được ghi nhận. 19 chủng phân lập có IC50 tăng 4,3 lần so với các chủng phân lập nền (từ 6,2 đến 43 lần so với virus hoang dại).
Kiểu gen liên quan đến kiểu hình giảm nhạy cảm với lopinavir ở những virus được chọn lọc bởi các thuốc ức chế protease khác. Hoạt tính kháng virus trên in vitro của lopinavir trên đã được đánh giá trên 112 chủng phân lập từ các bệnh nhân đã được đánh giá thất bại điều trị với một hoặc nhiều thuốc ức chế protease. Trong phạm vi các chủng này, các đột biến trên HIV protease liên quan đến giảm nhạy cảm với lopinavir trên in vitro là: L10F/I/R/V, K20M/R, L24I, M46I/L, F53L, I54L/T/V, L63P, A71I/L/T/V, V82A/F/T, I84V và L90M. Giá trị EC50 trung bình của lopinavir với các chủng phân lập đột biến ở các vị trí acid amin 0-3, 4-5, 6-7, và 8-10 trên amino acid tương ứng cao hơn gấp 0,8; 2,7; 13,5 và 44,0 lần so với EC50 của chủng HIV hoang dại. Trên 16 virus có sự thay đổi lớn hơn 20 lần đều chứa các đột biến ở các vị trí 10, 54, 63 cộng 82 và/hoặc 84. Ngoài ra, chúng còn chứa trung bình khoảng 3 đột biến tại các vị trí acid amin số 20, 24, 46, 53, 71 và 90. Ngoài các đột biến được mô tả ở trên, đột biến V32I và I47A đã được ghi nhận ở các chủng bật lại có giảm nhạy cảm với lopinavir ở bệnh nhân đã sử dụng thuốc ức chế protease đang sử dụng lopinavir/ritonavir. Các đột biến I47A, L76V đã được ghi nhận ở các chủng bật lại giảm nhạy cảm với lopinavir ở bệnh nhân đang sử dụng lopinavir/ritonavir.
Kết luận liên quan đến ý nghĩa của các đột biến riêng biệt hoặc các đột biến chung có thể thay đổi với các dữ liệu bổ sung do đó nên tham khảo các hệ thống phân tích hiện tại kiểm tra kháng thuốc.
Hoạt tính kháng virus của lopinavir/ritonavir ở những bệnh nhân đã thất bại điều trị với thuốc ức chế protease: Ý nghĩa lâm sàng của sự giảm nhạy cảm với lopinavir trên in vitro được đánh giá thông qua đáp ứng virus với liệu pháp lopinavir/ritonavir so với giá trị nền kiểu gen và kiểu hình virus ở 56 bệnh nhân đã thất bại điều trị với nhiều thuốc ức chế protease trước đó. Giá trị EC50 của lopinavir với 56 chủng virus phân lập nền cao hơn từ 0,6 đến 96 lần giá trị EC50 với chủng HIV hoang dại. Sau 48 tuần điều trị với lopinavir/ritonavir, efavirenz và các thuốc ức chế enzym phiên mã ngược có nguồn gốc nucleosid, tại lượng ARN của virus HIV ≤ 400 phiên bản/mL đã được ghi nhận 93% (25/27), 73% (11/15) và 25% (2/8) số bệnh nhân có sự giảm nhạy cảm với lopinavir so với giá trị nền tương ứng ≤ 10 lần, từ 10 đến 40 lần và ≥ 40 lần. Ngoài ra, đáp ứng virus đã được ghi nhận ở 91% (21/23), 71% (15/21) và 33% (2/6) bệnh nhân có 0-5, 6-7 và 8-10 đột biến trên HIV protease liên quan đến giảm nhạy cảm với lopinavir trên in vitro. Do những bệnh nhân không phơi nhiễm với Aluvia hoặc efavirenz trước đó, một phần đáp ứng có thể do hoạt tính kháng virus của efavirenz, đặc biệt ở bệnh nhân mang virus có đề kháng cao với lopinavir. Nghiên cứu này không có nhóm bệnh nhân đối chứng không sử dụng lopinavir/ritonavir.
Kháng chéo: Hoạt tính của các thuốc ức chế protease với các chủng phân lập có sự tăng đề kháng với lopinavir sau khi điều trị lopinavir/ritonavir ở bệnh nhân đã từng sử dụng thuốc ức chế protease: Sự có mặt của hiện tượng kháng chéo với các thuốc ức chế protease khác đã được phân tích trên 18 chủng phân lập bật lại cho thấy có sự tiến triển của đề kháng lopinavir trong 3 nghiên cứu pha II và 1 nghiên cứu pha III của lopinavir/ritonavir trên bệnh nhân đã từng sử dụng thuốc ức chế protease. Giá trị IC50 trung bình của lopinavir với 18 chủng phân lập nền và bật lại tương ứng gấp 6,9 và 63 lần so với chủng HIV hoang dại. Nhìn chung, các chủng phân lập bật lại đều lưu giữ được (nếu kháng chéo ở mức nền) hoặc phát triển kháng chéo đáng kể với indinavir, saquinavir và atazanavir. Giảm nhẹ sinh hoạt tính của amprenavir giảm nhẹ đã được ghi nhận với giá trị IC50 trung bình tăng từ 3,7 đến 8 lần tương ứng với các chủng nền và chủng bật lại. Những chủng phân lập còn nhạy cảm với tipranavir tăng giá trị IC50 trung bình tương ứng 1,9 và 1,8 lần với các chủng nền và chủng bật lại so với chủng virus hoang dại. Nên tham khảo tóm tắt đặc tính sản phẩm của Aptivus để bổ sung thêm thông tin sử dụng tipranavir bao gồm các yếu tố kiểu hình dự đoán đáp ứng trong điều trị HIV-1 đã kháng lại lopinavir.
Kết quả nghiên cứu lâm sàng: Tác dụng của lopinavir/ritonavir (phối hợp với các thuốc kháng retrovirus khác) lên các chất chỉ điểm sinh học (hàm lượng ARN của virus HIV trong huyết tương và số lượng tế bào T CD4+) đã được đánh giá trong các nghiên cứu đối chứng có kiểm soát có sử dụng lopinavir/ritonavir trong khoảng thời gian từ 48 đến 360 tuần.
Sử dụng thuốc cho người lớn
Với bệnh nhân chưa từng điều trị thuốc kháng virus
Nghiên cứu M98-863 có phân nhóm ngẫu nhiên, mù đôi tiến hành trên 653 bệnh nhân chưa từng điều trị thuốc kháng virus được sử dụng lopinavir/ritonavir (400/100mg 2 lần mỗi ngày) được so sánh với nelfinavir (750 mg 3 lần mỗi ngày), stavudin và lamivudin. Số lượng tế bào T CD4+ trung bình ở mức nền là 259 tế bào/mm3 (dao động từ 2 đến 949 tế bào/mm3) và hàm lượng ARN của virus HIV-1 ở mức nền là 4,9 log10 phiên bản/mL (dao động từ 2,6 đến 6,8 log10 phiên bản/mL).
- xem Bảng 1.

113 bệnh nhân điều trị bằng nelfinavir và 74 bệnh nhân điều trị bằng lopinavir/ritonavir có hàm lượng ARN của HIV trên 400 phiên bản/mL trong khoảng thời gian điều trị từ tuần 24 đến tuần 96. Trong số đó, các chủng phân lập từ 96 bệnh nhân điều trị với nelfinavir và 51 bệnh nhân điều trị lopinavir/ritonavir có thể được khuyếch đại để đánh giá kháng thuốc. Kháng nelfinavir được định nghĩa bởi sự có mặt của gen đột biến D30N hoặc L90M đã được ghi nhận ở 41/96 bệnh nhân (43%). Kháng lopinavir được định nghĩa bởi sự có mặt của bất kỳ đột biến ở vị trí khởi đầu hoặc ở vị trí hoạt động trên protease (xem phần trên) đã được ghi nhận 0/50 bệnh nhân (0%). Sự vắng mặt của virus kháng lopinavir đã được xác nhận qua phân tích kiểu hình.
Nghiên cứu M05-730 là thử nghiệm phân nhóm ngẫu nhiên, mở, đa trung tâm tiến hành so sánh điều trị với lopinavir/ritonavir 800/200mg 1 lần mỗi ngày kết hợp tenofovir DF, emtricitabin và lopinavir/ritonavir 400/100mg 2 lần mỗi ngày kết hợp tenofovir DF, emtricitabin trên 664 bệnh nhân chưa từng điều trị thuốc kháng virus. Do tương tác dược động học đã công bố giữa lopinavir/ritonavir và tenofovir (xem phần Tương tác thuốc), kết quả của nghiên cứu này không thể ngoại suy hoàn toàn khi sử dụng các phác đồ khác của lopinavir/rotinavir. Bệnh nhân được phân nhóm ngẫu nhiên theo tỷ lệ 1:1 để sử dụng lopinavir/ritonavir liều 800/200mg 1 lần mỗi ngày (n=333) hoặc sử dụng lopinavir/ritonavir 400/100mg 2 lần mỗi ngày (n=331). Hơn nữa sự phân thành từng nhóm (viên nén và viên nang mềm) là theo tỷ lệ 1:1. Bệnh nhân được điều trị bằng thuốc dạng viên nén hoặc viên nang mềm trong 8 tuần sau đó tất cả các bệnh nhân được điều trị bằng thuốc dạng viên nén 1 lần hoặc 2 lần mỗi ngày trong phần sau của nghiên cứu. Bệnh nhân được điều trị bằng emtricitabin 200 mg 1 lần mỗi ngày và tenofovir DF 300 mg 1 lần mỗi ngày. Nghiên cứu đã định nghĩa sự không thua kém của chế độ liều dùng 1 lần mỗi ngày so với liều 2 lần mỗi ngày được chứng minh nếu cận dưới của khoảng tin cậy 95% về sự khác biệt của tỷ lệ đối tượng đáp ứng (liều 1 lần mỗi ngày trừ đi liều 2 lần mỗi ngày) thấp hơn -12% ở tuần 48.
Độ tuổi trung bình của các bệnh nhân là 39 (dao động từ 19 đến 71), 75% là người Cap-ca-dơ, nam giới chiếm78%. Số lượng tế bào T CD4+ trung bình ở mức nền là 216 tế bào/mm3 (dao động từ 20 đến 775 tế bào/mm3) và hàm lượng ARN của HIV-1 trung bình ở mức nền là 5,0 log10 phiên bản/mL (dao động từ 1,7 đến 7,0 log10 phiên bản/mL).
- xem Bảng 2.
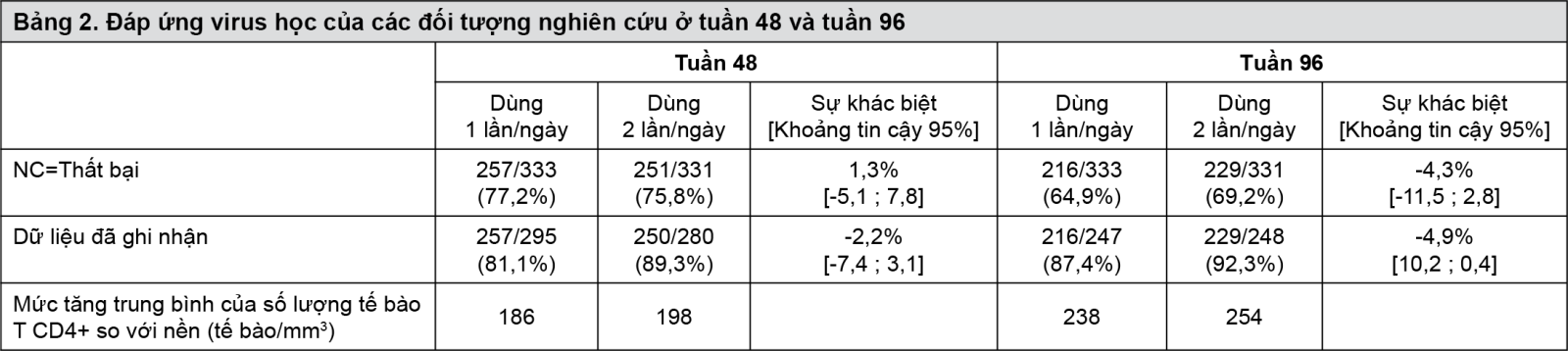
Sau 96 tuần, kết quả xét nghiệm kiểu gen kháng thuốc thu được từ các bệnh nhân đáp ứng virus không hoàn chỉnh gồm 25 bệnh nhân trong nhóm sử dụng liều 1 lần mỗi ngày và 26 bệnh nhân trong nhóm sử dụng liều 2 lần mỗi ngày. Trong nhóm sử dụng liều 1 lần mỗi ngày không có bệnh nhân nào có đề kháng lopinavir và trong nhóm sử dụng thuốc liều 2 lần mỗi ngày có 1 bệnh nhân có kháng ức chế protease rõ rệt ở mức nền đã giải thích sự xuất hiện đề kháng với lopinavir trong nghiên cứu.
Sự duy trì đáp ứng virus với lopinavir/ritonavir (phối hợp với thuốc ức chế enzym phiên mã ngược có nguồn gốc nucleosid/nucleotid) cũng đã được ghi nhận trong 1 nghiên cứu nhỏ ở pha II (M97-720) trong suốt 360 tuần điều trị. Nghiên cứu gồm 100 bệnh nhân được bắt đầu điều trị với lopinavir/ritonavir (bao gồm 51 bệnh nhân sử dụng liều 400/100mg 2 lần mỗi ngày và 49 bệnh nhân sử dụng liều 200/100mg 2 lần mỗi ngày hoặc 400/200mg 2 lần mỗi ngày). Tất cả bệnh nhân được công khai đổi liều lopinavir/ritonavir ở mức liều 400/100mg 2 lần mỗi ngày vào khoảng giữa tuần 48 và tuần 72. Có 39 bệnh nhân (39%) không tiếp tục nghiên cứu, trong đó 16 bệnh nhân (16%) dừng điều trị do gặp các biến cố bất lợi, một bệnh nhân trong số đó đã tử vong. Có 61 bệnh nhân hoàn thành nghiên cứu (35 bệnh nhân sử dụng liều khuyến cáo 400/100mg 2 lần mỗi ngày trong suốt quá trình nghiên cứu).
- xem Bảng 3.

Sau 360 tuần, phân tích kiểu gen của các chủng virus phân lập đã được tiến hành ở 19 trong 28 bệnh nhân được xác nhận có hàm lượng ARN của HIV trên 400 phiên bản/mL cho thấy không có đột biến ở vị trí khởi đầu hay ở vị trí hoạt động trên protease (amino acid ở các vị trí 8, 30, 32, 46, 47, 48, 50, 82, 84 và 90) hoặc sự kháng thể hiện trên kiểu hình của thuốc ức chế protease.
Bệnh nhân đã điều trị thuốc kháng retrovirus trước đó
Một nghiên cứu mở có phân nhóm ngẫu nghiên M06-802 so sánh tính an toàn, khả năng dung nạp và hoạt tính kháng virus của viên nén lopinavir/ritonavir với liều dùng 1 lần mỗi ngày và 2 lần mỗi ngày trên 599 bệnh nhân có tải lượng virus phát hiện được khi điều trị kháng virus hiện tại. Những bệnh nhân chưa điều trị với lopinavir/ritonavir trước đó được phân nhóm ngẫu nhiên theo tỷ lệ 1:1 vào nhóm sử dụng lopinavir/ritonavir liều 800/200mg 1 lần mỗi ngày (n=300) hoặc liều 400/100mg 2 lần mỗi ngày (n=299). Bằng ít nhất 2 thuốc ức chế enzym phiên mã ngược tương tự nucleosid/nucleo 3 lần/ngày được các nghiên cứu viên kê đơn thêm cho bệnh nhân. Các bệnh nhân tham gia phơi nhiễm ở mức đó. Trung bình với thuốc ức chế protease có nhiều hơn nửa bệnh nhân chưa bao giờ sử dụng thuốc ức chế protease trước đó và khoảng 80% bệnh nhân mang 1 chủng virus có ít hơn 3 đột biến trên protease. Độ tuổi trung bình của bệnh nhân đưa vào nghiên cứu là 41 tuổi (dao động từ 21 đến 73 tuổi); 51% là người Cap-ca-dơ và 66% là nam giới. Số lượng tế bào T CD4+ trung bình ở mức nền là 254 tế bào/mm3 (dao động từ 4 đến 952 tế bào/mm3) và hàm lượng ARN của HIV-1 trung bình ở mức nền là 4,3 log10 phiên bản/mL (dao động từ 1,7 đến 6,6 log10 phiên bản/mL). Khoảng 85% bệnh nhân có tải lượng virus < 100.000 phiên bản/mL.
- xem Bảng 4.

Sau 48 tuần, kết quả xét nghiệm gen kháng thuốc có được từ những bệnh nhân đáp ứng virus không hoàn chỉnh gồm 75 bệnh nhân trong nhóm sử dụng thuốc 1 lần mỗi ngày và 75 bệnh nhân trong nhóm sử dụng thuốc 2 lần mỗi ngày. Ở nhóm sử dụng thuốc 1 lần mỗi ngày 6/75 bệnh nhân (8%) có xuất hiện các đột biến mới trên protease (các vị trí mã hóa 30, 32, 48, 50, 82, 84, 90), 12/77 (16%) bệnh nhân trong nhóm sử dụng liều 2 lần mỗi ngày cũng xuất hiện các đột biến tương tự.
Sử dụng thuốc cho bệnh nhân nhi: Một nghiên cứu mở M98-940 về dạng bào chế lỏng của lopinavir/ritonavir tiến hành trên 100 bệnh nhi trong đó có 44% bệnh nhi chưa điều trị với thuốc kháng retrovirus và 56% bệnh nhi đã điều trị với thuốc kháng retrovirus. Tất cả các bệnh nhân đều chưa từng sử dụng thuốc ức chế enzym phiên mã ngược không có nguồn gốc nucleosid. Bệnh nhân được lựa chọn ngẫu nhiên vào 1 trong 2 nhóm sử dụng liều 230mg lopinavir/57,5mg ritonavir trên 1m2 diện tích bề mặt cơ thể và nhóm sử dụng liều 300mg lopinavir/75mg ritonavir trên 1m2 diện tích bề mặt cơ thể. Những bệnh nhân chưa điều trị với thuốc kháng retrovirus được sử dụng thuốc ức chế enzym phiên mã ngược nguồn gốc nucleosid. Còn những bệnh nhân đã từng điều trị với thuốc kháng virus thì được sử dụng nevirapin kết hợp với 2 thuốc ức chế enzym phiên mã ngược nguồn gốc nucleosid. Tính an toàn, hiệu quả và các đặc tính dược động học của hai chế độ liều được đánh giá sau 3 tuần điều trị ở mỗi bệnh nhân. Sau đó, tất cả các bệnh nhân được tiếp tục sử dụng liều 300/75mg trên 1m2 diện tích bề mặt cơ thể. Độ tuổi trung bình của bệnh nhân là 5 tuổi (dao động từ 6 tháng đến 12 tuổi), trong đó 14 bệnh nhân dưới 2 tuổi và 6 bệnh nhân 1 tuổi. Số lượng tế bào T CD4+ trung bình ở mức nền là 838 tế bào/mm3 và hàm lượng ARN của HIV-1 trung bình ở mức nền là 4,7 log10 phiên bản/mL.
- xem Bảng 5.

KONCERT/PENTA 18 là một nghiên cứu nhãn mở, ngẫu nhiên, đa trung tâm nhằm đánh giá dược động học, hiệu lực và tính an toàn của viên nén lopinavir/ritonavir 100/25mg tính liều theo cân nặng dùng 2 lần/ngày so với 1 lần/ngày trong phác đồ điều trị phối hợp với các thuốc kháng HIV (cART) ở trẻ em nhiễm HIV-1 đã ức chế được virus (n=173). Trẻ nhiễm đủ tiêu chuẩn tham gia vào nghiên cứu khi dưới 18 tuổi, cân nặng ≥ 15kg, đang điều trị cART bao gồm lopinavir/ritonavir, tải lượng virus ARN HIV-1 < 50 bản sao/mL trong ít nhất 24 tuần và có thể nuốt được viên thuốc. Tại tuần thứ 24, hiệu lực và tính an toàn ở bệnh nhi sử dụng viên nén lopinavir/ritonavir 100/25mg liều 2 lần/ngày (n=87) cho kết quả tương đồng với hiệu lực và tính an toàn thấy được ở các nghiên cứu trước đây trên bệnh nhân trưởng thành và bệnh nhân nhi dùng lopinavir/ritonavir liều 2 lần/ngày. Cũng tại tuần 24, phần trăm bệnh nhân có tải lượng virus ARN HIV-1 < 50 bản sao/mL ở bệnh nhi sử dụng viên nén lopinavir/ritonavir liều 1 lần/ngày (88,2%) thấp hơn ở bệnh nhân sử dụng liều 2 lần/ngày (96,6%, p=0,040), chủ yếu là do sự gắn thấp hơn của nhóm 1 lần/ngày. Hiệu quả của chế độ liều 2 lần/ngày tăng lên do có sự khác biệt rõ rệt về các thông số dược động học của chế độ liều này (xem phần Dược động học).
Dược động học
Các đặc tính dược động học của lopinavir phối hợp với ritonavir được đánh giá trên người tình nguyện khỏe mạnh và trên bệnh nhân bị nhiễm HIV, không có sự khác biệt đáng kể được ghi nhận giữa hai nhóm này. Lopinavir được chuyển hóa chủ yếu hoàn toàn qua CYP3A. Ritonavir ức chế quá trình chuyển hóa của lopinavir, do đó làm tăng nồng độ của lopinavir trong huyết tương. Các nghiên cứu cho thấy, điều trị bằng Aluvia 400/100mg 2 lần mỗi ngày tạo nồng độ lopinavir ở trạng thái ổn định trong huyết tương cao hơn gấp 15 đến 20 lần nồng độ của ritonavir ở bệnh nhân bị nhiễm HIV. Nồng độ ritonavir ít hơn 7% so với nồng độ thu được sau khi dùng ritonavir liều 600 mg 2 lần mỗi ngày. Nghiên cứu kháng virus trên in vitro cho thấy giá trị EC50 của lopinavir thấp hơn gần 10 lần so với ritonavir. Do đó hoạt tính kháng virus của Aluvia là do lopinavir.
Hấp thu
Dùng đa liều 400/100mg lopinavir/ritonavir 2 lần mỗi ngày trong 2 tuần với điều kiện không hạn chế về chế độ ăn cho thấy nồng độ đỉnh của lopinavir trong huyết tương (Cmax) (giá trị trung bình ± SD) là 12,3±5,4 μg/mL, xuất hiện khoảng 4 giờ sau khi dùng thuốc. Nồng độ đáy ở trạng thái ổn định thu được trước khi sử dụng liều buổi sáng là 8,1±5,7 μg/mL. Giá trị AUC của lopinavir với khoảng cách liều là 12 giờ đạt trung bình là 113,2±60,5 μg.giờ/mL. Sinh khả dụng tuyệt đối của lopinavir khi phối hợp với ritonavir chưa được thiết lập trên người.
Ảnh hưởng của thức ăn đến hấp thu qua đường uống: Sử dụng liều đơn viên nén Aluvia 400/100mg với chế độ ăn đầy đủ (giàu chất béo, 872kCal, 56% lượng calo được cung cấp từ chất béo) được so sánh với khi dùng thuốc lúc đói cho thấy không có sự thay đổi đáng kể giá trị về Cmax và AUCinf. Do đó, viên nén Aluvia có thể sử dụng cùng hoặc không cùng với thức ăn. Viên nén Aluvia ít bị biến đổi dược động học do điều kiện ăn uống hơn so với viên nang mềm Aluvia.
Phân bố: Ở trạng thái ổn định, tỷ lệ lopinavir gắn với protein trong huyết tương khoảng 98-99%. Lopinavir gắn với cả alpha-1-acid glycoprotein (AAG) và albumin, tuy nhiên lopinavir có ái lực cao hơn với AAG. Ở trạng thái ổn định, liên kết lopinavir với protein vẫn hằng định trong khoảng nồng độ đã được ghi nhận sau khi sử dụng Aluvia liều 400/100mg 2 lần mỗi ngày và tỷ lệ này là tương tự giữa nhóm người tình nguyện khỏe mạnh và nhóm bệnh nhân nhiễm HIV.
Chuyển hóa: Thử nghiệm in vitro tiến hành trên microsom gan người cho thấy lopinavir chủ yếu được chuyển hóa bằng quá trình oxy hóa khử. Lopinavir chuyển hóa chủ yếu bởi hệ thống cytochrom P450 tại gan, phần lớn là do nhóm isozym CYP3A. Ritonavir là một thuốc ức chế mạnh CYP3A, ức chế quá trình chuyển hóa của lopinavir vì vậy làm tăng nồng độ của lopinavir trong huyết tương. Một nghiên cứu sử dụng liponavir gắn đồng vị phóng xạ 14C-lopinavir tiến hành trên người cho thấy 89% hoạt tính phóng xạ trong huyết tương sau khi dùng 1 liều Aluvia 400/100mg là do chất mẹ. Có ít nhất 13 dẫn chất chuyển hóa chất oxy hóa từ liponavir được tìm thấy trên người. Cặp đồng phân epime của chất chuyển hóa tại các vị trí 4-oxo và 4-hydro là chất chuyển hóa chính có hoạt tính kháng virus nhưng hoạt tính phóng xạ trong huyết tương rất thấp. Ritonavir có tác dụng cảm ứng enzym dẫn đến tự cảm ứng chuyển hóa của chính nó và có thể cảm ứng sự chuyển hóa của lopinavir. Nồng độ lopinavir từ liều dùng trước giảm trong suốt thời gian dùng đa liều và nồng độ này ổn định sau khoảng 10 ngày đến 2 tuần.
Thải trừ
Sau khi sử dụng 14C-lopinavir/ritonavir liều 400/100mg có khoảng 10,4±2,3% và 82,6±2,5% liều dùng của 14C-lopinavir được phát hiện trong nước tiểu và phân. Lượng lopinavir không bị biến đổi chiếm khoảng 2,2% và 19,8% liều dùng xuất hiện tương ứng trong nước tiểu và phân. Sau khi sử dụng đa liều, có ít hơn 3% lượng lopinavir bài tiết trong nước tiểu dưới dạng không bị biến đổi. Thời gian bán thải của lopinavir với khoảng cách đưa liều 12 giờ trung bình khoảng 5-6 giờ, độ thanh thải đường uống biểu kiến (CL/F) của lopinavir là 6 đến 7 L/giờ.
Chế độ dùng 1 lần mỗi ngày: dược động học của lopinavir/ritonavir liều dùng 1 lần mỗi ngày được đánh giá trên bệnh nhân bị nhiễm HIV chưa từng điều trị với thuốc kháng retrovirus. Lopinavir/ritonavir liều 800/200mg được dùng phối hợp với emtricitabin 200mg và tenofovir DF 300mg thành một chế độ liều dùng 1 lần mỗi ngày. Sử dụng đa liều lopinavir/ritonavir 800/200mg 1 lần mỗi ngày trong 2 tuần trong điều kiện hạn chế về chế độ ăn cho nồng độ đỉnh của lopinavir trong huyết tương (Cmax) (giá trị trung bình ± SD) là 14,8±3,5 μg/mL, xuất hiện khoảng 6 giờ sau khi bắt đầu điều trị. Nồng độ đáy ở trạng thái ổn định trước khi sử dụng liều buổi sáng là 5,5±5,4 μg/mL. Giá trị AUC của lopinavir với khoảng cách liều 24 giờ trung bình là 206,5±89,7 μg.giờ/mL.
So với chế độ liều 2 lần mỗi ngày, liều dùng một lần mỗi ngày làm giảm giá trị Cmin/Ctrough xấp xỉ khoảng 50%.
Những đối tượng đặc biệt
Bệnh nhân nhi: Dữ liệu về dược động học của viên nén Aluvia ở trẻ em dưới 2 tuổi còn hạn chế. Dược động học của dung dịch uống lopinavir/ritonavir liều 300/75 mg/m2 2 lần mỗi ngày và 230/57,5 mg/m2 2 lần mỗi ngày được nghiên cứu trên 53 bệnh nhân nhi, có tuổi dao động từ 6 tháng đến 12 tuổi. Ở trạng thái ổn định giá trị các thông số AUC, Cmax và Cmin của lopinavir tương ứng là 72,6±31,1 μg.giờ/mL; 8,2±2,9 μg/mL và 3,4±2,1 μg/mL sau khi uống dung dịch lopinavir/ritonavir liều 230/57,5 mg/m2 2 lần mỗi ngày không phối hợp nevirapin (n=12); giá trị các thông số tương ứng là 85,8±36,9 μg.giờ/mL, 10,0±3,3 μg/mL và 3,6±3,5 μg/mL sau khi uống dung dịch lopinavir/ritonavir liều 300/75 mg/m2, 2 lần mỗi ngày có phối hợp nevirapin (n=12). Chế độ liều 230/57,5 mg/m2, 2 lần mỗi ngày không phối hợp nevirapin và chế độ liều 300/75 mg/m2, 2 lần mỗi ngày có phối hợp nevirapin đều cho nồng độ lopinavir trong huyết tương tương tự như giá trị thu được ở bệnh nhân người lớn trưởng thành sử dụng liều 400/100mg 2 lần mỗi ngày không phối hợp nevirapin.
Giới tính, chủng tộc và tuổi: Dược động học của Aluvia chưa được nghiên cứu ở người cao tuổi. Không có mối liên quan giữa tuổi, giới tính với sự khác nhau về dược động học được ghi nhận ở bệnh nhân trưởng thành. Không nhận thấy có sự khác nhau về dược động học do chủng tộc.
Phụ nữ thời kỳ có thai và sau sinh
Trong nghiên cứu nhãn mở, 12 phụ nữ nhiễm HIV đang mang thai dưới 20 tuần bắt đầu điều trị phối hợp thuốc ARV dùng lopinavir/ritonavir 400mg/100mg (2 viên nén 200mg/50mg) 2 lần/ngày cho tới 30 tuần thai. Tại thời điểm thai 30 tuần, liều lopinavir/ritonavir được tăng lên tới 500/125mg (2 viên 200mg/50mg và 1 viên 100mg/25mg), 2 lần/ngày cho tới khi sau sinh 2 tuần. Nồng độ lopinavir huyết tương được đo trên 4 lần, chu kỳ 12 giờ trong 3 tháng giữa thai kỳ (tuổi thai 20-24 tuần), 3 tháng cuối thai kỳ trước khi tăng liều (tuổi thai 30 tuần), 3 tháng cuối thai kỳ sau khi tăng liều (tuổi thai 32 tuần) và tại thời điểm tuần thứ 8 sau khi sinh. Việc tăng liều dùng này không làm tăng đáng kể nồng độ lopinavir huyết tương.
Trong một nghiên cứu nhãn mở khác, 19 phụ nữ nhiễm HIV sử dụng lopinavir/ritonavir 400mg/100mg, 2 lần/ngày từ trước khi có thai như là một phần của liệu trình điều trị phối hợp thuốc ARV cho phụ nữ có thai. Một loạt các mẫu máu đã được thu thập trước khi dùng thuốc, tại các thời điểm chu kỳ 12 giờ trong 3 tháng giữa và 3 tháng cuối thai kỳ, tại thời điểm sinh, và 4-6 tuần sau khi sinh (đối với phụ nữ tiếp tục điều trị sau khi sinh) để phân tích dược động học của nồng độ lopinavir huyết tương.
Dữ liệu dược động học của các bệnh nhân có thai nhiễm HIV dùng lopinavir/ritonavir 400mg/100mg, 2 lần/ngày được trình bày trong bảng 6 (xem phần Liều lượng và Cách dùng).
- xem Bảng 6.

Suy giảm chức năng thận: Dược động học của Aluvia chưa được nghiên cứu trên bệnh nhân suy giảm chức năng thận; tuy nhiên do độ thanh thải thận của lopinavir không đáng kể nên có ít khả năng độ thanh thải toàn phần của cơ thể bị giảm ở bệnh nhân suy thận.
Suy giảm chức năng gan: Các thông số dược động học ở trạng thái ổn định của lopinavir trên bệnh nhân nhiễm HIV có suy giảm chức năng gan nhẹ đến trung bình được so sánh với bệnh nhân bị nhiễm HIV có chức năng gan bình thường trong một nghiên cứu đa liều sử dụng lopinavir/ritonavir 400/100mg, 2 lần mỗi ngày. Nồng độ trong máu của lopinavir tăng khoảng 30% đã được ghi nhận nhưng sự tăng này không được coi là có ý nghĩa lâm sàng.
Dữ liệu an toàn tiền lâm sàng
Các nghiên cứu về độc tính của liều lặp lại tiến hành trên động vật gặm nhấm và chó đã xác định được những cơ quan đích chính là gan, thận, tuyến giáp, lách và hồng cầu lưu hành trong máu. Sự thay đổi tại gan cho thấy có sự phồng lên của tế bào kèm theo thoái hóa trung tâm. Mặc dù phơi nhiễm gây ra những thay đổi trên là tương đương hoặc thấp hơn nồng độ trên lâm sàng ở người, nhưng liều dùng trên động vật cao hơn 6 lần liều khuyến cáo trên lâm sàng. Thoái hóa nhẹ ống thận đã quan sát được trên nồng độ chuột nhắt đã phơi nhiễm gấp ít nhất 2 lần so với nồng độ khuyến cáo trên người; trong khi đó thận không bị ảnh hưởng ở chuột cống và chó. Nồng độ thyroxin trong huyết thanh giảm dẫn đến tăng giải phóng TSH làm phì đại các tế bào nang tuyến dù được quan sát ở chuột cống. Sự thay đổi này có tính chất thuận nghịch khi ngừng dùng thuốc và không xuất hiện ở chuột nhắt và chó. Xét nghiệm Coomb âm tính hồng cầu không đều và hồng cầu biến dạng được quan sát thấy ở chuột cống nhưng không thấy ở chuột nhắt và chó. Lách to kết hợp với chứng mô bào huyết đã được phát hiện ở chuột cống nhưng không thấy ở các loài khác. Nồng độ cholesterol trong huyết thanh tăng lên ở động vật gặm nhấm nhưng không tăng ở chó, trong khi đó nồng độ triglycerid lại chỉ tăng ở chuột nhắt.
Trên in vitro, kênh kali ở dòng tế bào tim người (HERG) đã bị ức chế 30% với nồng độ cao nhất của lopinavir/ritonavir được thử tương ứng gấp 7 lần nồng độ trong huyết thanh toàn phần và 15 lần nồng độ đỉnh của dạng tự do trong huyết tương đạt được ở người với liều khuyến cáo cao nhất. Ngược lại, nồng độ tương tự của lopinavir/ritonavir không làm chậm lại sự tái cực ở các sợi Purkinje của cơ tim. Nồng độ thấp hơn lopinavir/ritonavir không gây phong bế rõ rệt dòng kali (HERG). Nghiên cứu phân bố mô được tiến hành trên chuột cống cho thấy khả năng lưu giữ của thuốc trong tim là không đáng kể. Sau 72 giờ giá trị AUC trong tim đạt xấp xỉ 50% giá trị AUC đo được trong huyết tương. Do đó, có thể cho rằng nồng độ lopinavir trong tim cao hơn không đáng kể nồng độ trong huyết tương.
Ở chó, các sóng U cao trên điện tâm đồ đã được xác nhận là có liên quan đến kéo dài khoảng PR và làm chậm nhịp tim. Tác động này là do khả năng ảnh hưởng đến nồng độ các chất điện giải.
Ý nghĩa lâm sàng của các dữ liệu tiền lâm sàng nói trên chưa được biết đến, tuy nhiên không thể loại trừ tác động trên tim người của thuốc (xem phần Cảnh báo, Tác dụng ngoại ý).
Ở chuột cống, độc tính trên phôi thai (sẩy thai, giảm khả năng sống của bào thai, giảm cân nặng bào thai, tăng sự biến đổi bộ xương) và độc tính tăng trưởng sau khi sinh (giảm khả năng sống sót của chó con) đã được ghi nhận liều gây độc cho cá thể mẹ. Nồng độ toàn thân của lopinavir/ritonavir ở cá thể mẹ và liều gây độc ảnh hưởng đến phát triển của cá thể con thấp hơn nồng độ điều trị mong đợi ở người.
Nghiên cứu về khả năng gây ung thư của lopinavir/ritonavir trên chuột nhắt cho thấy thuốc không độc hại gen, không kích thích phân bào khởi tạo khối u gan, do đó được coi là không có nguy cơ trên người.
Nghiên cứu khả năng sinh ung thư trên chuột cống không tìm thấy khả năng sinh khối u của thuốc. Lopinavir/ritonavir không gây đột biến gen trong các thử nghiệm in vitro và in vivo bao gồm thử nghiệm đảo ngược đột biến trên vi khuẩn Ames, xét nghiệm u lympho ở chuột nhắt, xét nghiệm vi nhân trên chuột nhắt và xét nghiệm sự sai lệch nhiễm sắc thể ở tế bào lympho của người.
Chỉ định/Công dụng
Aluvia được chỉ định phối hợp với các thuốc kháng retrovirus khác điều trị cho bệnh nhân nhiễm virus gây suy giảm miễn dịch ở người (HIV-1) trên các đối tượng người lớn, trẻ vị thành niên và trẻ em từ 2 tuổi trở lên.
Lựa chọn Aluvia để điều trị cho bệnh nhân nhiễm HIV-1 đã từng sử dụng thuốc ức chế protease nên dựa vào xét nghiệm đề kháng virus và tiền sử điều trị của bệnh nhân (xem phần Cảnh báo, Dược lực học).
Liều lượng & Cách dùng
Nên sử dụng Aluvia theo chỉ định của bác sĩ đã có kinh nghiệm điều trị nhiễm HIV.
Viên nén Aluvia được nuốt trực tiếp, không nhai, bẻ vỡ hoặc nghiền nát.
LIỀU LƯỢNG: Điều trị theo phác đồ hướng dẫn của chương trình phòng chống HIV/AIDS - Bộ Y tế.
Sử dụng cho người lớn và trẻ vị thành niên: Aluvia được chỉ định với liều chuẩn là 400/100mg (2 viên 200/50mg) 2 lần mỗi ngày dùng cùng hoặc không cùng với thức ăn. Ở bệnh nhân trưởng thành, trong những trường hợp cần thiết dùng liều 1 lần mỗi ngày, Aluvia có thể được chỉ định với liều 800/200mg (4 viên 200/50mg) 1 lần mỗi ngày dùng cùng hoặc không cùng với thức ăn. Cần hạn chế sử dụng liều 1 lần mỗi ngày cho những bệnh nhân có rất ít đột biến liên quan đến thuốc ức chế protease (nghĩa là ít hơn 3 đột biến liên quan đến thuốc ức chế protease được mô tả trong kết quả của thử nghiệm lâm sàng, xem phần Dược lực học để biết thông tin đầy đủ về các đối tượng bệnh nhân) và nên chú ý đến những nguy cơ giảm khả năng duy trì hiệu quả tiêu diệt virus (xem phần Dược lực học) và nguy cơ cao bị tiêu chảy (xem phần Tác dụng ngoại ý) so với phác đồ chuẩn được khuyến cáo là dùng 2 lần mỗi ngày.
Sử dụng cho bệnh nhân nhi (trẻ từ 2 tuổi trở lên): Liều dùng của Aluvia được chỉ định cho người lớn (400/100mg 2 lần mỗi ngày) có thể áp dụng cho trẻ có cân nặng từ 40kg trở lên hoặc diện tích bề mặt cơ thể lớn hơn 1,4m2 (BSA)*. Trường hợp trẻ em có cân nặng dưới 40kg hoặc diện tích bề mặt từ 0,5 đến 1,4m2 và có thể dùng thuốc dạng viên nén xin tham khảo thêm tờ tóm tắt đặc tính sản phẩm của viên nén Aluvia 100mg/25mg. Theo các dữ liệu sẵn có còn hạn chế, không nên dùng lopinavir/ritonavir phác đồ 1 lần mỗi ngày cho bệnh nhân nhi (xem phần Dược lực học).
*Cách tính diện tích bề mặt cơ thể (BSA) như sau:

Trẻ em dưới 2 tuổi: Tính an toàn và hiệu quả của viên nén Aluvia chưa được thiết lập cho trẻ dưới 2 tuổi. Dữ liệu hiện có được trình bày trong phần Dược động học nhưng không có bất cứ khuyến cáo về liều dùng có thể được đưa ra.
Liệu pháp kết hợp Efavirenz hoặc Nevirapin
Bảng hướng dẫn chuyển đổi liều Aluvia dựa trên diện tích bề mặt cơ thể khi sử dụng phối hợp với efavirenz hoặc nevirapin cho trẻ em.
- xem Bảng 7.

Bệnh nhân suy gan: Ở bệnh nhân nhiễm HIV bị suy gan mức độ nhẹ và trung bình, nồng độ lopinavir tăng khoảng 30% nhưng sự tăng này không đem lại sự thay đổi nào có ý nghĩa lâm sàng (xem phần Dược động học). Không có dữ liệu về bệnh nhân suy gan nặng. Không nên sử dụng Aluvia cho bệnh nhân suy gan nặng (xem phần Chống chỉ định).
Bệnh nhân suy thận: Độ thanh thải tại thận của lopinavir và ritonavir không đáng kể nên có ít khả năng nồng độ thuốc trong huyết thanh tăng ở bệnh nhân suy thận. Do lopinavir và ritonavir gắn mạnh với protein nên ít có khả năng thuốc có thể được loại bỏ đáng kể bằng thẩm tích máu hoặc thẩm phân phúc mạc.
Phụ nữ có thai và sau sinh
• Không cần điều chỉnh liều lopinavir/ritonavir cho phụ nữ có thai và sau sinh
• Không khuyến cáo dùng phác đồ lopinavir/ritonavir 1 lần/mỗi ngày cho phụ nữ có thai do thiếu dữ liệu lâm sàng và dược động học.
CÁCH DÙNG: Viên nén Aluvia được dùng đường uống và phải nuốt trực tiếp, không được nhai, bẻ vỡ hoặc nghiền nát. Viên nén Aluvia có thể dùng cùng hoặc không cùng với thức ăn.
Cảnh báo
Bệnh nhân có các bệnh mắc kèm
Suy gan: Tính an toàn và hiệu quả của Aluvia chưa được thiết lập ở bệnh nhân rối loạn đáng kể chức năng gan. Aluvia chống chỉ định với bệnh nhân suy gan nặng (xem phần Chống chỉ định). Bệnh nhân bị viêm gan B hoặc viêm gan C mạn tính điều trị với liệu pháp phối hợp thuốc kháng retrovirus có nguy cơ cao gặp các phản ứng có hại nghiêm trọng đe dọa tính mạng liên quan đến gan. Khi sử dụng phối hợp các thuốc kháng virus điều trị viêm gan B, C, cần tham khảo các thông tin liên quan của các chế phẩm này.
Bệnh nhân có tiền sử rối loạn chức năng gan bao gồm viêm gan mạn tính có các bất thường về chức năng gan tăng trong suốt quá trình điều trị bằng phác đồ phối hợp các thuốc kháng retrovirus và cần phải theo dõi theo các hướng dẫn thực hành điều trị chuẩn. Nếu dấu hiệu bệnh gan trở nên trầm trọng hơn thì cần phải xem xét tạm dừng hoặc ngừng hẳn thuốc.
Tăng nồng độ enzym transaminase kèm theo có/hoặc không tăng nồng độ bilirubin đã được báo cáo ở bệnh nhân nhiễm đơn HIV-1 đơn thuần và ở bệnh nhân điều trị dự phòng sau 7 ngày sử dụng lopinavir/ritonavir phối hợp với các thuốc kháng retrovirus khác. Một số trường hợp rối loạn chức năng gan nghiêm trọng cũng đã được ghi nhận.
Các xét nghiệm phù hợp nên được tiến hành trước khi bắt đầu điều trị với lopinavir/ritonavir và theo dõi chặt chẽ trong suốt quá trình điều trị.
Suy thận: Do độ thanh thải tại thận của lopinavir và ritonavir không đáng kể nên có ít khả năng nồng độ thuốc trong huyết thanh tăng ở bệnh nhân suy thận. Do lopinavir và ritonavir gắn mạnh với protein nên ít có khả năng thuốc được loại bỏ đáng kể bằng thẩm tích máu hoặc thẩm phân phúc mạc.
Bệnh máu khó đông: Đã có những báo cáo về sự gia tăng tình trạng chảy máu bao gồm tụ máu dưới da tự phát, tụ máu khớp ở bệnh nhân mắc bệnh máu khó đông tuýp A và tuýp B sử dụng các thuốc ức chế protease. Một số bệnh nhân đã được bổ sung yếu tố VIII. Trong hơn một nửa số trường hợp được báo cáo, bệnh nhân vẫn tiếp tục được điều trị hoặc bắt đầu điều trị lại với các các thuốc ức chế protease nếu thuốc đã bị dừng trước đó. Mối quan hệ nhân quả đã được xác định mặc dù cơ chế tác dụng vẫn chưa được làm sáng tỏ. Vì vậy những bệnh nhân mắc bệnh máu khó đông cần thận trọng với khả năng gia tăng tình trạng chảy máu.
Viêm tụy
Viêm tụy đã được ghi nhận ở bệnh nhân điều trị với Aluvia bao gồm cả những bệnh nhân có tăng triglycerid máu tiến triển. Đa số các trường hợp đã có tiền sử viêm tụy và/hoặc sử dụng đồng thời với các thuốc khác có thể gây viêm tụy. Nồng độ triglycerid tăng rõ rệt là một nhân tố nguy cơ gây viêm tụy. Bệnh nhân nhiễm HIV tiến triển có thể có nguy cơ tăng triglycerid máu và bị viêm tụy.
Nên cân nhắc đến viêm tụy khi xuất hiện các triệu chứng lâm sàng (buồn nôn, nôn, đau bụng) hoặc các xét nghiệm cận lâm sàng bất thường (nồng độ amylase hoặc lipase trong huyết thanh tăng). Cần tiến hành đánh giá những bệnh nhân có các dấu hiệu và triệu chứng trên, nên ngừng sử dụng Aluvia nếu bệnh nhân được chẩn đoán viêm tụy (xem phần Tác dụng ngoại ý).
Hội chứng hoạt hóa lại hệ miễn dịch
Các bệnh nhân nhiễm HIV bị suy giảm miễn dịch nặng khi bắt đầu liệu pháp phối hợp các thuốc kháng retrovirus (CART) có thể bị gia tăng phản ứng viêm đối với các tác nhân nhiễm trùng cơ hội không triệu chứng hoặc các nhiễm trùng cơ hội còn sót lại và gây ra tình trạng lâm sàng nghiêm trọng hoặc làm nặng thêm các triệu chứng. Thông thường những phản ứng này xảy ra trong vài tuần hoặc vài tháng đầu khi bắt đầu liệu pháp CART. Các bệnh thường gặp là viêm võng mạc do Cytomegalovirus, nhiễm trực khuẩn Mycobacterium tại chỗ và/hoặc toàn thân, viêm phổi do Pneumocystis jiroveci. Bất kỳ triệu chứng viêm nào nên được đánh giá và điều trị nếu cần thiết.
Đã có báo cáo về các rối loạn tự miễn dịch (như bệnh Graves’) xảy ra trong khi kích hoạt hệ miễn dịch; tuy nhiên, thời gian bắt đầu xuất hiện các rối loạn này là khác nhau và có thể xảy ra sau vài tháng điều trị.
Hoại tử xương: Mặc dù bệnh nguyên có sự tham gia của nhiều yếu tố (bao gồm việc sử dụng corticoid, rượu, suy giảm miễn dịch nặng, chỉ số khối cơ thể cao) nhưng các trường hợp hoại tử xương đã được ghi nhận ở bệnh nhân nhiễm HIV tiến triển và/hoặc sử dụng phối hợp các thuốc kháng retrovirus (CART). Cần tham khảo ý kiến bác sĩ nếu có các triệu chứng đau, nhức, cứng khớp hoặc khó di chuyển.
Kéo dài khoảng PR: Lopinavir/ritonavir được ghi nhận gây kéo dài khoảng PR ở mức vừa phải không có triệu chứng ở người tình nguyện khỏe mạnh. Đã ghi nhận rất ít báo cáo về block nhĩ thất độ 2 hoặc độ 3 ở bệnh nhân mắc bệnh tim cấu trúc hoặc có bất thường hệ thống dẫn truyền trước đó hoặc ở bệnh nhân sử dụng các thuốc gây kéo dài khoảng PR (chẳng hạn verapamil hay atazanavir) khi họ sử dụng lopinavir/ritonavir. Nên thận trọng khi sử dụng Aluvia cho những đối tượng bệnh nhân này (xem phần Dược lực học).
Các thông số về trọng lượng và chuyển hóa: Trong quá trình điều trị thuốc kháng virus có thể xuất hiện sự tăng trọng lượng và tăng nồng độ lipid và glucose huyết. Sự thay đổi này có thể là một phần liên quan đến việc kiểm soát bệnh và chế độ sinh hoạt. Với lipid, có một vài trường hợp cho thấy có ảnh hưởng đến việc điều trị, trong khi đó không có bằng chứng rõ ràng cho thấy việc tăng trọng lượng liên quan đến bất kỳ việc điều trị cụ thể nào. Sự kiểm tra nồng độ lipid và glucose huyết là căn cứ tham khảo cho việc xây dựng hướng dẫn điều trị HIV. Nên xử trí tình trạng rối loạn lipid bằng các biện pháp lâm sàng phù hợp.
Tương tác với các thuốc khác
Aluvia chứa lopinavir và ritonavir đều có tác dụng ức chế CYP3A của hệ thống enzym chuyển hóa thuốc CYP450. Aluvia có khả năng làm tăng nồng độ trong huyết tương của các thuốc được chuyển hóa chủ yếu bởi CYP3A. Sự tăng nồng độ trong huyết tương của các thuốc dùng kèm có thể làm tăng hoặc kéo dài hiệu quả điều trị và các tác dụng không mong muốn của các thuốc này (xem phần Chống chỉ định và Tương tác thuốc).
Sử dụng đồng thời delamanid với chất ức chế CYP3A mạnh (như lopinavir/ritonavir) có thể làm tăng đáng kể sự chuyển hóa của delamanid, dẫn đến làm kéo dài khoảng QT. Vì vậy, nếu việc sử dụng đồng thời delamanid và lopinavir/ritonavir đã được đánh giá là cần thiết, thì khuyến cáo cần theo dõi điện tâm đồ (ECG) thường xuyên trong suốt quá trình sử dụng delamanid (xem mục Tương tác thuốc và tham khảo ''Tóm tắt đặc tính sản phẩm của delamanid'').
Chất ức chế CYP3A4 mạnh như thuốc ức chế protease có thể làm tăng nồng độ bedaquilin dẫn đến làm tăng nguy cơ của các tác dụng không mong muốn liên quan đến bedaquilin. Vì vậy, nên tránh dùng đồng thời bedaquilin với lopinavir/ritonavir. Tuy nhiên, có thể sử dụng thận trọng sự kết hợp này khi lợi ích được đánh giá cao hơn nguy cơ. Khuyến cáo theo dõi điện tâm đồ thường xuyên và kiểm soát các enzym transaminase (xem phần Tương tác thuốc và tham khảo "Tóm tắt đặc tính sản phẩm của bedaquilin'').
Đã có báo cáo trong tương tác thuốc nguy hiểm đe dọa tính mạng và tử vong ở bệnh nhân được điều trị với colchicin và thuốc ức chế CYP3A mạnh như ritonavir. Chống chỉ định sử dụng đồng thời với colchicine ở bệnh nhân suy thận và/hoặc suy gan (xem phần Chống chỉ định và Tương tác thuốc).
Không khuyến cáo sử dụng đồng thời Aluvia với:
- Tadalafil, chỉ định điều trị tăng huyết áp động mạch phổi (xem phần Tương tác thuốc).
- Acid fusidic, chỉ định điều trị các nhiễm khuẩn xương khớp (xem phần Tương tác thuốc).
- Salmeterol (xem phần Tương tác thuốc).
- Rivaroxaban (xem phần Tương tác thuốc).
Không khuyến cáo sử dụng đồng thời Aluvia với atorvastatin. Nếu việc sử dụng atorvastatin là thực sự cần thiết thì nên sử dụng liều thấp nhất có thể và phải theo dõi cẩn thận tính an toàn. Cần thận trọng và cân nhắc giảm liều khi sử dụng phối hợp Aluvia với rosuvastatin. Nếu cần điều trị bằng thuốc ức chế HMG-CoA reductase, nên lựa chọn pravastatin hoặc fluvastatin (xem phần Tương tác thuốc).
Thuốc ức chế PDE5
Thận trọng đặc biệt khi chỉ định sildenafil, tadalafil hoặc vardenafil để điều trị rối loạn cương dương cho bệnh nhân đang sử dụng Aluvia. Sử dụng đồng thời Aluvia với các thuốc này làm tăng nồng độ của các thuốc và có thể gây ra các phản ứng có hại liên quan như hạ huyết áp, ngất, thay đổi thị giác và cương dương kéo dài (xem phần Tương tác thuốc). Chống chỉ định sử dụng đồng thời avanafil hoặc vardenafil và lopinavir/ritonavir (xem phần Chống chỉ định). Chống chỉ định sử dụng đồng thời sildenafil để điều trị tăng áp lực động mạch phổi với Aluvia (xem phần Chống chỉ định).
Thận trọng đặc biệt khi kê đơn Aluvia và các thuốc gây kéo dài khoảng QT như: chlorpheniramin, quinidin, erythromycin, clarithromycin. Thực vậy, Aluvia làm tăng nồng độ của các thuốc này khi dùng phối hợp và có thể làm tăng phản ứng có hại liên quan đến tim. Các biến cố trên tim đã được ghi nhận với Aluvia trong nghiên cứu tiền lâm sàng; do đó những ảnh hưởng trên tim của Aluvia không thể loại trừ (xem phần Tác dụng ngoại ý và Dữ liệu an toàn tiền lâm sàng).
Không khuyến cáo sử dụng đồng thời Aluvia với rifampicin. Rifampicin khi phối hợp với Aluvia làm giảm nồng độ lopinavir dẫn đến giảm đáng kể hiệu quả điều trị của lopinavir. Nồng độ thích hợp của lopinavir/ritonavir có thể đạt được khi sử dụng Aluvia liều cao hơn nhưng điều này có liên quan đến nguy cơ cao gây độc trên gan và trên tiêu hóa. Do đó, nên tránh sử dụng phối hợp trừ khi thực sự cần thiết (xem phần Tương tác thuốc).
Việc sử dụng đồng thời Aluvia và fluticason hoặc các glucocorticoid khác chuyển hóa qua CYP3A4 như budesonid và triamcinolon không được khuyến cáo trừ khi lợi ích điều trị vượt trội nguy cơ tác dụng toàn thân của corticoid bao gồm cả hội chứng Cushing và ức chế tuyến thượng thận (xem phần Tương tác thuốc).
Lưu ý khác: Aluvia không phải thuốc điều trị tận gốc nhiễm virus HIV hay bệnh AIDS. Do đó vẫn có nguy cơ lây nhiễm HIV cho người khác qua quan hệ tình dục hoặc qua đường máu khi dùng Aluvia. Vì vậy, nên có những biện pháp thận trọng phù hợp. Những bệnh nhân đang sử dụng Aluvia vẫn có thể tiến triển tình trạng nhiễm trùng hoặc các bệnh khác liên quan đến HIV và bệnh AIDS.
Ảnh hưởng lên khả năng lái xe và vận hành máy móc: Chưa có nghiên cứu nào về tác dụng đối với khả năng lái xe và vận hành máy móc được công bố. Bệnh nhân nên được thông báo về tác dụng không mong muốn buồn nôn đã được báo cáo khi sử dụng Aluvia (xem phần Tác dụng ngoại ý).
Quá Liều
Cho đến nay, dữ liệu về quá liều Aluvia cấp tính ở người còn hạn chế.
Những triệu chứng lâm sàng đã được ghi nhận trên chó bao gồm tăng tiết nước bọt, nôn và tiêu chảy/phân bất thường. Các dấu hiệu ngộ độc đã được ghi nhận trên chuột nhắt, chuột cống và chó bao gồm giảm hoạt động, mất điều hòa, gầy mòn, mất nước và run.
Không có thuốc giải độc đặc hiệu cho trường hợp quá liều Aluvia. Nên xử trí quá liều Aluvia bằng các biện pháp hỗ trợ chung bao gồm theo dõi dấu hiệu sinh tồn và tình trạng lâm sàng của bệnh nhân. Khi có chỉ định cần loại bỏ lượng thuốc chưa hấp thu qua niêm mạc ruột bằng cách gây nôn hoặc rửa dạ dày. Sử dụng than hoạt cũng có thể giúp loại bỏ phần thuốc chưa được hấp thu. Aluvia gắn mạnh với protein vì vậy thẩm tích có thể không hiệu quả trong việc loại bỏ đáng kể thành phần có hoạt tính.
Chống chỉ định
Aluvia chống chỉ định với bệnh nhân có tiền sử mẫn cảm với lopinavir, ritonavir hay với bất kỳ thành phần nào của thuốc.
Bệnh nhân bị suy gan nặng.
Aluvia chứa lopinavir và ritonavir là những chất ức chế CYP3A của hệ thống enzym chuyển hóa thuốc CYP450. Không nên phối hợp Aluvia với các thuốc có độ thanh thải phụ thuộc cao vào CYP3A vì nồng độ thuốc trong huyết tương cao liên quan đến những biến cố nghiêm trọng hoặc đe dọa tính mạng. Các thuốc này bao gồm (xem Bảng 8):

Sử dụng ở phụ nữ có thai và cho con bú
Phụ nữ có thai
Theo nguyên tắc, khi quyết định sử dụng thuốc kháng retrovirus để điều trị nhiễm HIV ở phụ nữ có thai và để hạn chế nguy cơ lây nhiễm HIV trực tiếp sang trẻ sơ sinh, các dữ liệu về sử dụng thuốc trên động vật cũng như kinh nghiệm lâm sàng trên phụ nữ có thai cần được đưa vào để mô tả tính an toàn cho thai nhi.
Lopinavir/ritonavir đã được đánh giá trên bệnh nhân mang thai với số lượng lớn hơn 3000 người, trong đó có trên 1000 người ở giai đoạn ba tháng đầu thai kỳ.
Theo dõi hậu maketing thông qua Dữ liệu đăng ký sử dụng thuốc kháng retrovirus ở phụ nữ có thai – được thành lập từ tháng 01 năm 1989 cho thấy không có báo cáo nào về sự tăng nguy cơ dị tật bẩm sinh ở hơn 1000 phụ nữ sử dụng Aluvia trong ba tháng đầu thai kỳ. Tỷ lệ dị tật bẩm sinh sau khi sử dụng lopinavir ở bất kỳ giai đoạn thai kỳ nào ngang bằng với tỷ lệ dị tật bẩm sinh quan sát được trong quần thể chung. Không có trường hợp dị tật bẩm sinh gợi ý nguyên nhân gây ra bởi thuốc. Nghiên cứu trên động vật cho thấy có độc tính trên sinh sản (xem phần Dữ liệu an toàn tiền lâm sàng). Dựa vào những dữ liệu hạn chế đã mô tả ở trên, nguy cơ dị tật không chắc chắn xảy ra trên người. Lopinavir có thể sử dụng cho phụ nữ mang thai nếu cần thiết.
Phụ nữ cho con bú: Nghiên cứu trên chuột cho thấy lopinavir được bài tiết qua sữa. Hiện chưa rõ thuốc có bài tiết qua sữa mẹ hay không. Theo nguyên tắc, người mẹ nhiễm HIV nên được khuyến cáo không cho con bú dưới bất kỳ hình thức nào để tránh lây nhiễm HIV.
Ảnh hưởng lên khả năng sinh sản: Nghiên cứu trên động vật cho thấy thuốc không ảnh hưởng đến khả năng sinh sản. Hiện không có dữ liệu nào về ảnh hưởng của lopinavir/ritonavir trên khả năng sinh sản ở người.
Tương tác
Aluvia chứa lopinavir và ritonavir đều có tác dụng ức chế CYP3A của hệ thống enzym chuyển hóa thuốc CYP450 trên in vitro. Sử dụng đồng thời Aluvia với các thuốc chuyển hóa chủ yếu qua CYP3A có thể làm tăng nồng độ các thuốc này trong huyết tương dẫn tới tăng tác dụng điều trị và phản ứng có hại của chúng. Aluvia không ức chế CYP2D6, CYP2C9, CYP2C19, CYP2E1, CYP2B6 hoặc CYP1A ở nồng độ được ghi nhận trên lâm sàng (xem phần Chống chỉ định).
Nghiên cứu in vivo cho thấy Aluvia tự cảm ứng chuyển hóa của chính mình và làm tăng chuyển hóa sinh học của một số thuốc chuyển hóa qua enzym cytochrom P450 (bao gồm CYP2C9 và CYP2C19) và qua phản ứng liên hợp với acid glucuronic. Điều này làm giảm nồng độ trong huyết tương và giảm hiệu quả điều trị của các thuốc sử dụng đồng thời.
Các thuốc chống chỉ định đặc biệt do gây tương tác nghiêm trọng và có khả năng gây biến cố bất lợi nghiêm trọng được liệt kê trong phần Chống chỉ định.
Tất cả các nghiên cứu về tương tác, nếu không có mô tả đặc biệt nào khác đều được tiến hành với viên nang lopinavir/ritonavir thì nồng độ của lopinavir thấp hơn khoảng 20% so với khi dùng viên nén 200/50mg.
Những tương tác lý thuyết và những tương tác đã được ghi nhận giữa các thuốc kháng retrovirus và các thuốc khác được liệt kê trong bảng dưới đây.
Bảng tương tác
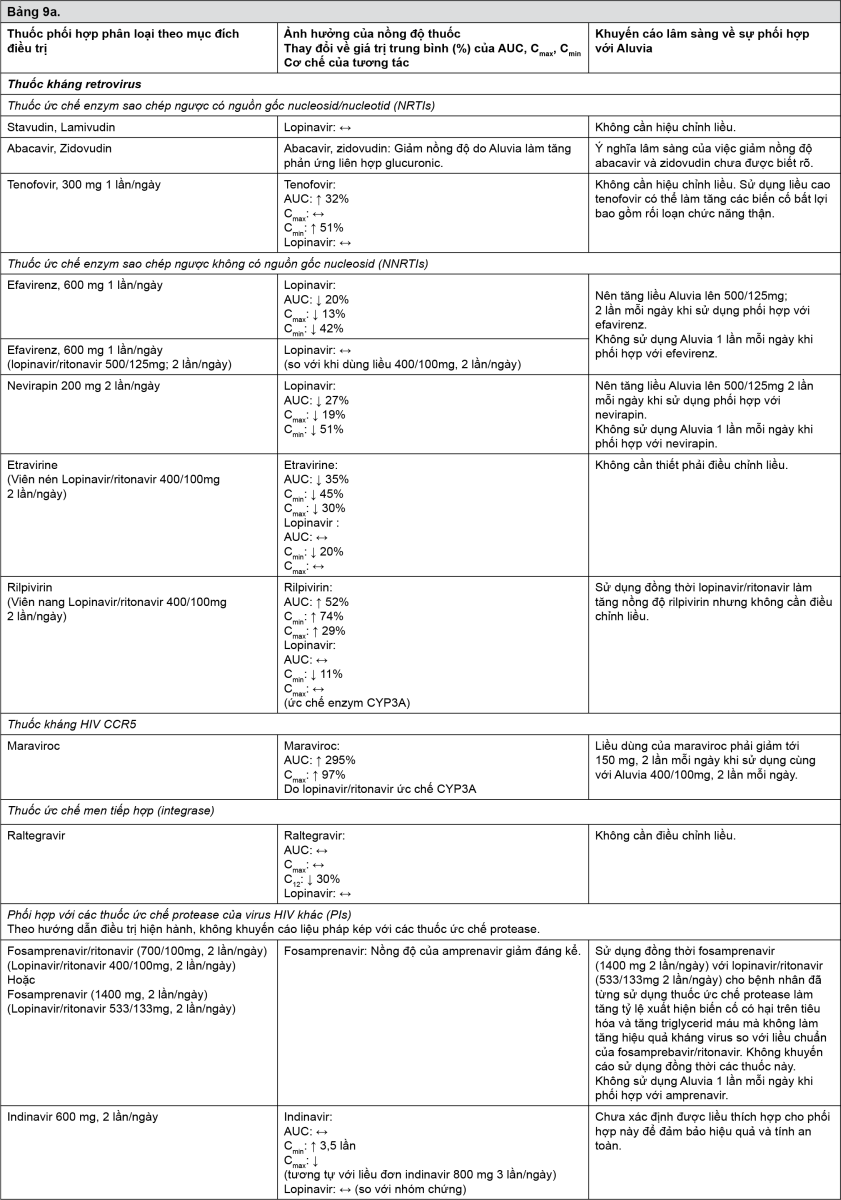
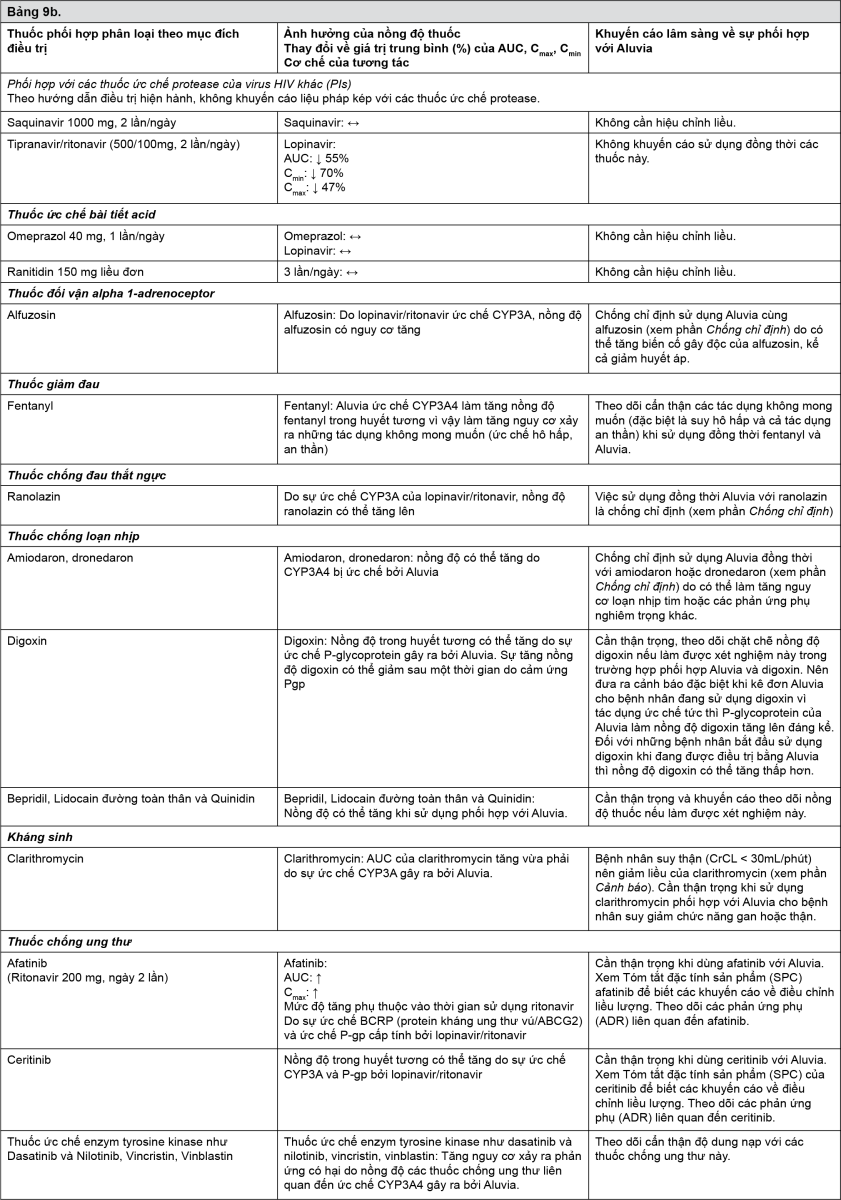
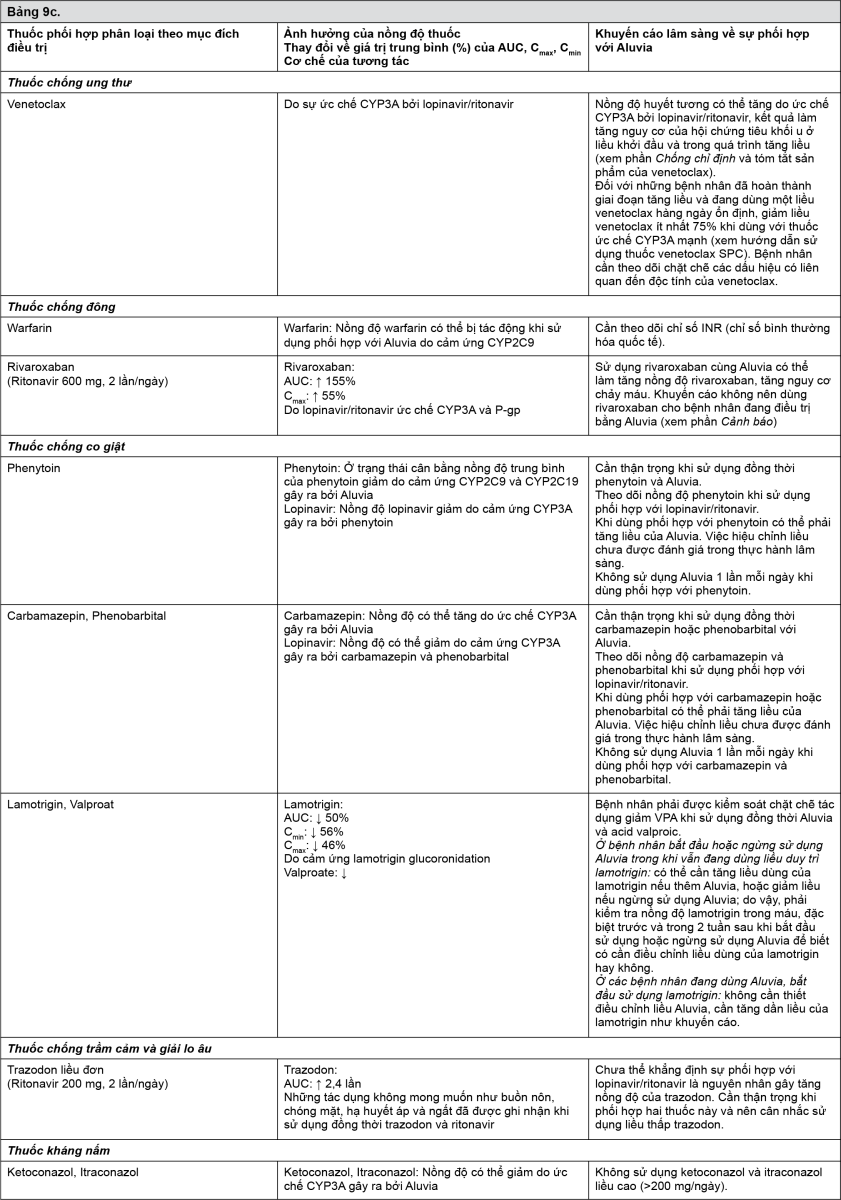
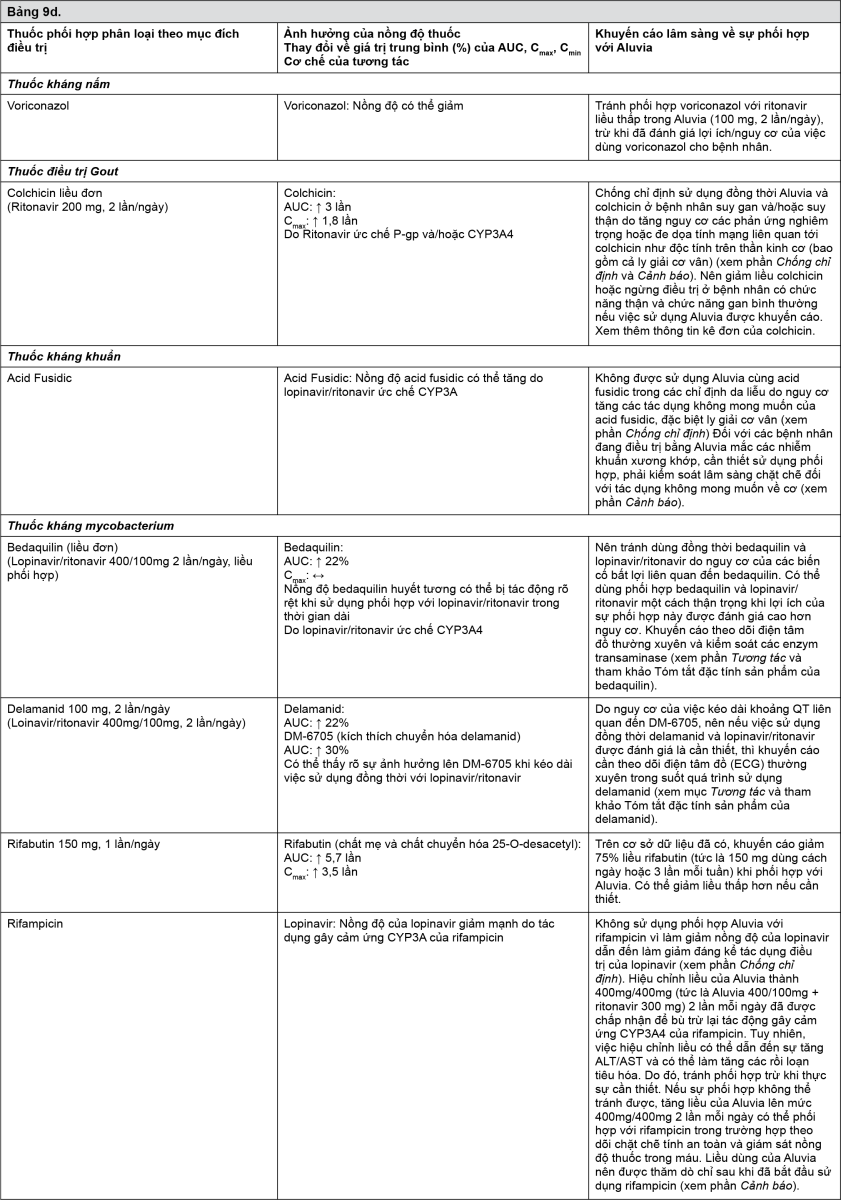
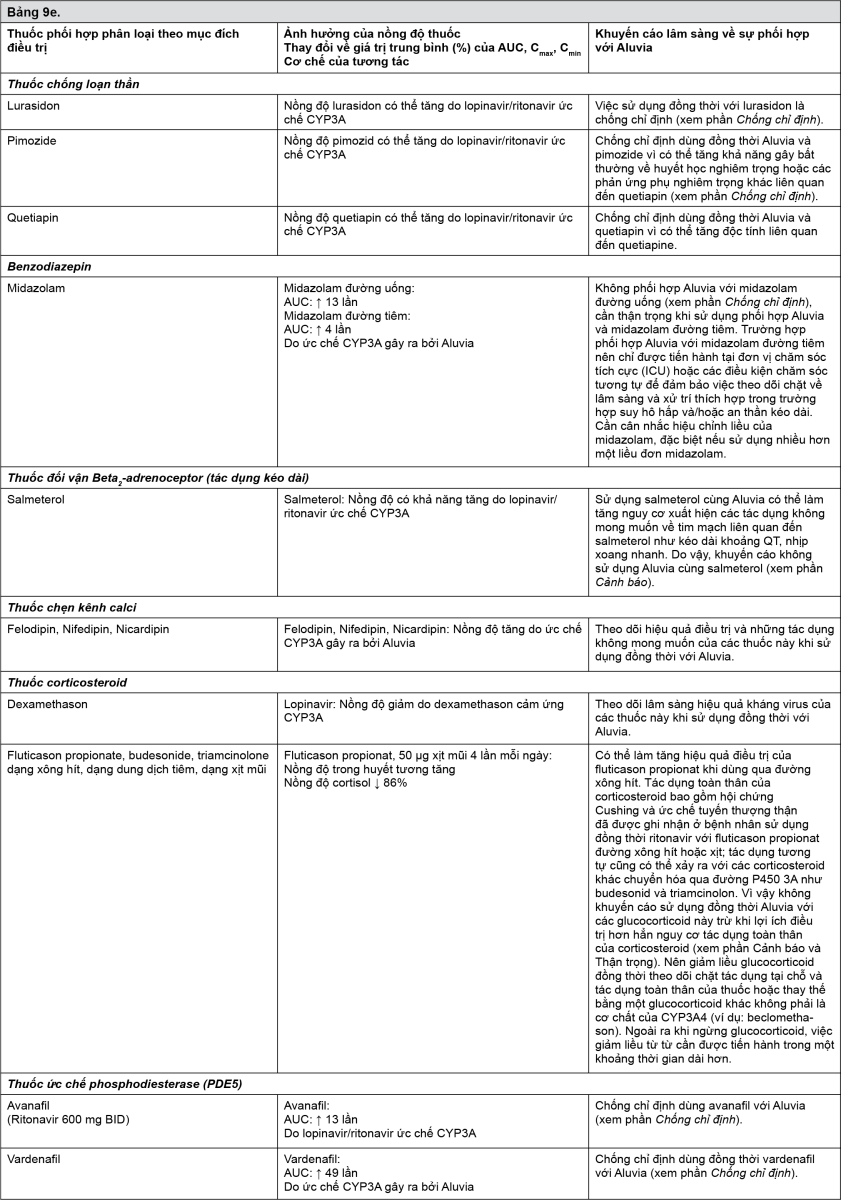
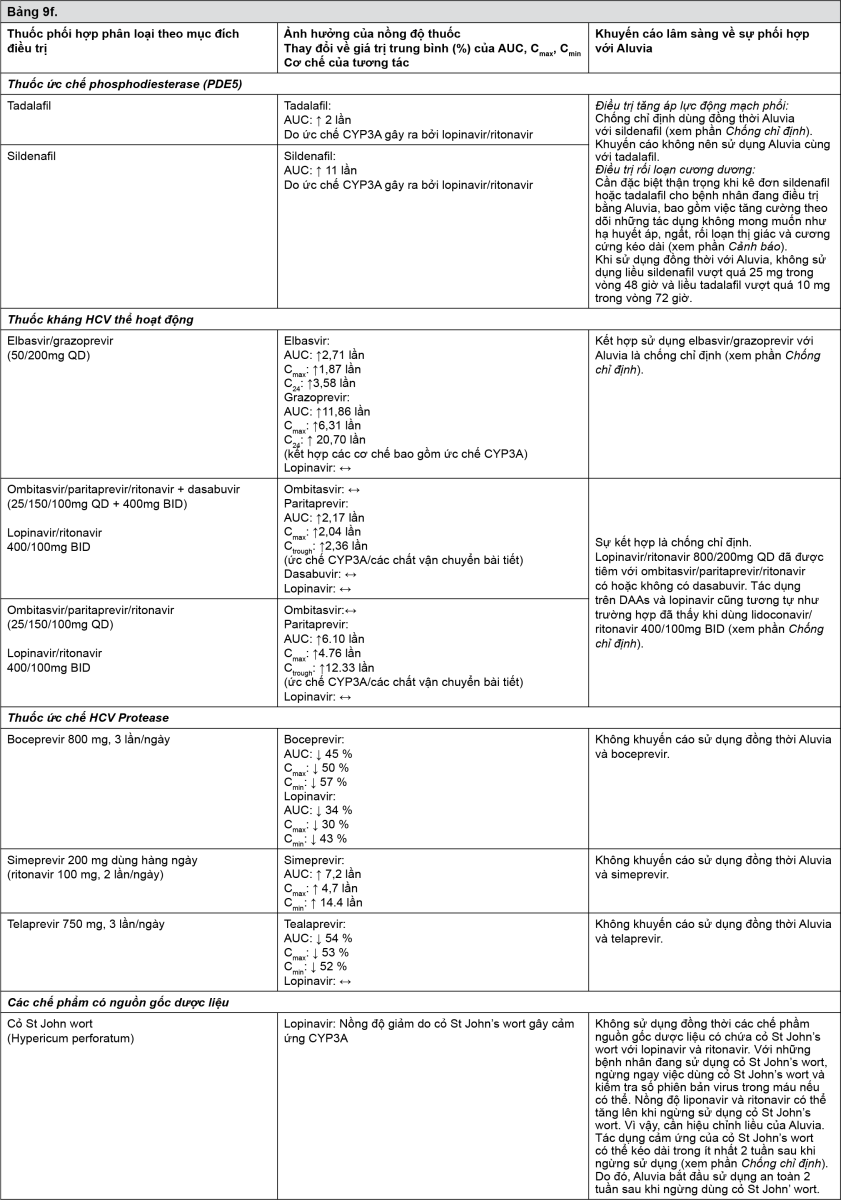
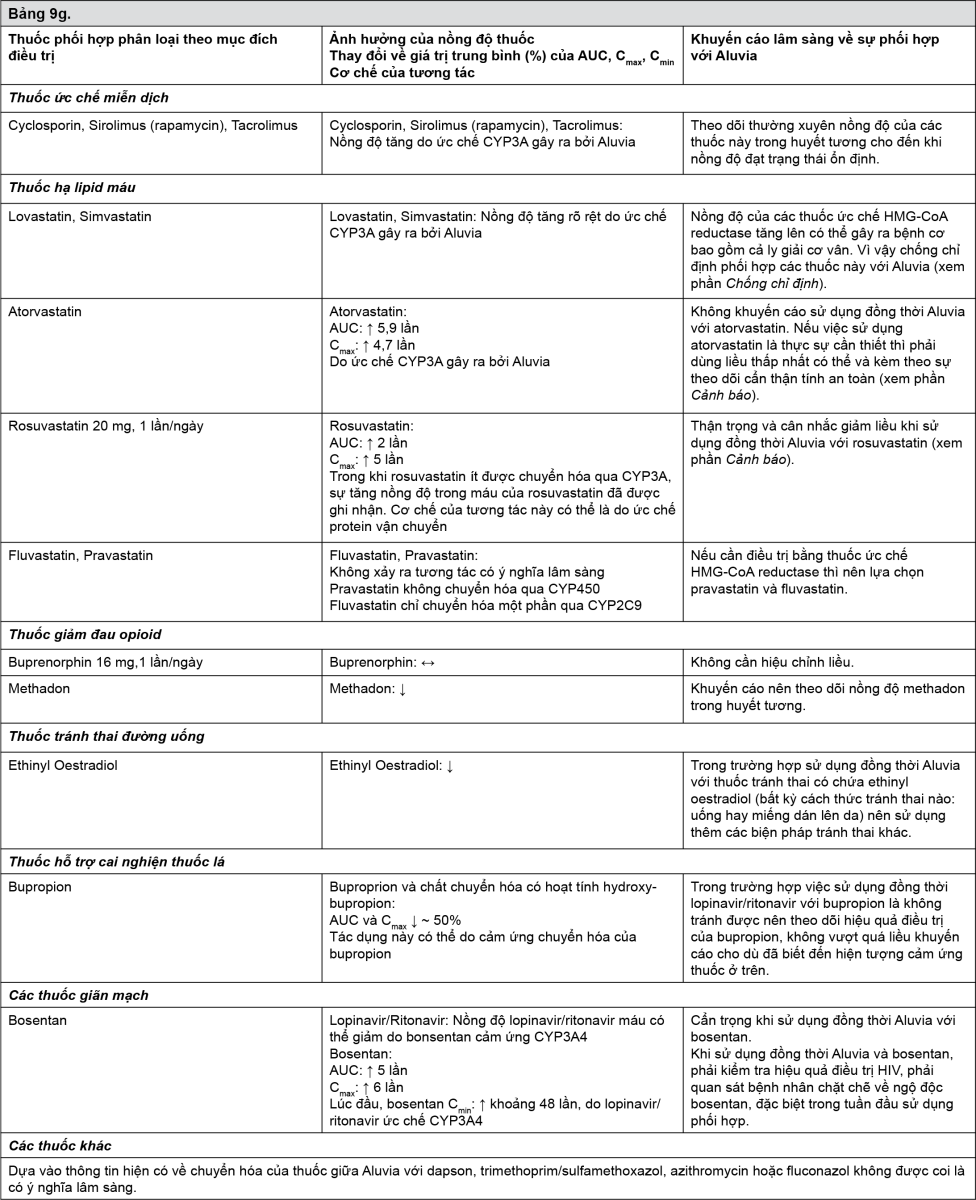
Tương tác giữa Aluvia với các thuốc sử dụng đồng thời được liệt kê trong bảng dưới đây (ký hiệu: “↑” là tăng,“↓” là giảm, “↔” là không thay đổi).
Trừ các trường hợp có chú thích đặc biệt, các nghiên cứu mô tả dưới đây đã được thực hiện với liều khuyến cáo của lopinavir/ritonavir (tức là 400/100mg 2 lần mỗi ngày).
- xem Bảng 9a-9g.
Tác dụng ngoại ý
Tóm tắt hồ sơ về độ an toàn
Tính an toàn của lopinavir/ritonavir được đánh giá trên hơn 2600 bệnh nhân trong các nghiên cứu lâm sàng pha II-IV, trong đó có hơn 700 bệnh nhân sử dụng liều 800/200mg 1 lần mỗi ngày (6 viên nang hoặc 4 viên nén). Cùng với các thuốc ức chế enzym phiên mã ngược có nguồn gốc nucleosid (NRTIs), trong một số nghiên cứu lopinavir/ritonavir được sử dụng phối hợp với efavirenz hoặc nevirapin.
Các phản ứng có hại thường gặp nhất liên quan đến liệu pháp lopinavir/ritonavir trong các thử nghiệm lâm sàng là tiêu chảy, buồn nôn, nôn, tăng triglycerid máu và tăng cholesterol máu. Nguy cơ tiêu chảy cao hơn khi dùng Aluvia liều 1 lần mỗi ngày. Tiêu chảy, buồn nôn, nôn có thể xảy ra ở giai đoạn đầu điều trị, trong khi tăng triglycerid máu và tăng cholesterol máu có thể xảy ra muộn hơn. Có 7% số bệnh nhân đã phải ngừng tham gia trước hạn các nghiên cứu pha II-IV do xuất hiện các biến cố bất lợi cần phải điều trị.
Cần lưu ý rằng một số trường hợp viêm tụy đã được báo cáo ở bệnh nhân đang sử dụng lopinavir/ritonavir, bao gồm cả những bệnh nhân tăng triglycerid tiến triển. Hơn nữa, kéo dài khoảng PR cũng được báo cáo trong khi điều trị với lopinavir/ritonavir (xem phần Cảnh báo).
Bảng phân loại phản ứng có hại
Các phản ứng có hại từ thử nghiệm lâm sàng và theo dõi hậu mãi ở bệnh nhân trưởng thành và bệnh nhân nhi
Những biến cố sau đây đã được xác định là phản ứng có hại. Tất cả các biến cố từ mức độ trung bình đến nặng đã được đưa vào để tính tần suất, cho dù mối quan hệ nhân quả đã được đánh giá hay không. Các phản ứng có hại được trình bày theo nhóm cơ quan hệ thống. Trong mỗi nhóm, tác dụng không mong muốn được liệt kê theo thứ tự giảm dần của độ nghiêm trọng: hay gặp (≥1/10), thường gặp (≥1/100 đến <1/10), ít gặp (≥1/1000 đến <1/100) và không rõ (không thể ước lượng được từ các dữ liệu sẵn có).
Các biến cố được ghi chú tần suất là “Không rõ” được xác định thông qua theo dõi hậu mãi.
- xem Bảng 10.
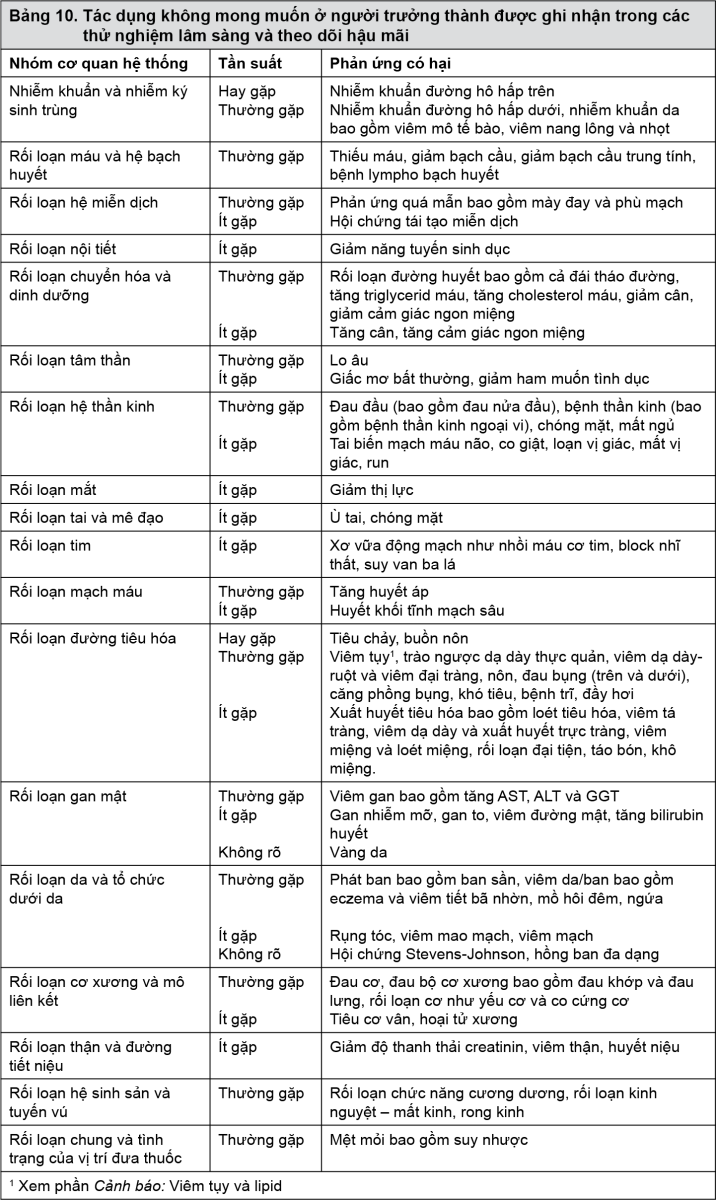
Mô tả một số phản ứng có hại
Hội chứng Cushing đã được ghi nhận ở bệnh nhân sử dụng đồng thời ritonavir và fluticason propionat đường xông hít hoặc xịt mũi; tác dụng tương tự cũng có thể xảy ra với các corticosteroid khác chuyển hóa qua con đường CYP3A4 như budesonid (xem phần Cảnh báo, Tương tác thuốc).
Tăng creatine phosphokinase (CPK), đau cơ, viêm cơ và hiếm gặp hơn là ly giải cơ vân đã được ghi nhận với các thuốc ức chế protease, đặc biệt trong trường hợp sử dụng phối hợp với các thuốc ức chế enzym phiên mã ngược có nguồn gốc nucleosid.
Các thông số chuyển hóa: Trọng lượng cơ thể và nồng độ lipid và glucose huyết có thể tăng trong quá trình điều trị thuốc kháng vius (xem phần Cảnh báo).
Bệnh nhân nhiễm HIV bị suy giảm miễn dịch nặng có thể tăng phản ứng viêm đối với các nhiễm trùng cơ hội không triệu chứng hoặc các nhiễm trùng cơ hội còn sót lại khi bắt đầu điều trị với liệu pháp phối hợp các thuốc kháng retrovirus. Cũng đã có báo cáo về các rối loạn tự miễn dịch (như bệnh Graves) xảy ra, tuy nhiên, thời gian bắt đầu khác nhau, và có thể xảy ra nhiều tháng sau thời điểm bắt đầu điều trị (xem phần Cảnh báo).
Một số trường hợp hoại tử xương đã được báo cáo, đặc biệt ở bệnh nhân có những yếu tố nguy cơ đã biết, nhiễm HIV tiến triển hoặc thời gian điều trị bằng liệu pháp phối hợp thuốc kháng retrovirus (CART) kéo dài. Tần suất của tác dụng không mong muốn này vẫn chưa được rõ (xem phần Cảnh báo).
Trẻ em: Trẻ em từ 2 tuổi trở lên, tính an toàn tương tự như đã quan sát được trên người lớn.
Báo cáo tác dụng không mong muốn: Việc báo cáo tác dụng không mong muốn sau khi thuốc được lưu hành là quan trọng, giúp tiếp tục theo dõi cán cân lợi ích/nguy cơ khi sử dụng thuốc. Nhân viên y tế cần báo cáo bất kỳ tác dụng không mong muốn nào của thuốc theo hệ thống báo cáo của quốc gia.
Bảo quản
Bảo quản viên nén bao phim ALUVIA ở nhiệt độ không quá 30oC.
Phân loại ATC
J05AR10 - lopinavir and ritonavir
Trình bày/Đóng gói
Viên nén bao phim: chai 120 viên.
- Abacavir
- Abernil
- Abiiogran
- Acarbose
- ACC
- Acebutolol
- Acenocoumarol
- Acetate Ringer's
- Acetazolamide
- Acetylcystein
- Acetylsalicylic acid
- Aciclovir
- Acid acetylsalicylic
- Acid aminocaproic
- Acid ascorbic
- Acid boric
- Acid chenodeoxycholic
- Acid ethacrynic
- Acid folic
- Acid fusidic
- Acid iopanoic
- Acid ioxaglic
- Acid nalidixic
- Acid pantothenic
- Acid para-aminobenzoic
- Acid salicylic
- Acid tranexamic
- Acid valproic
- Acid zoledronic
- Acitretin
- Aclasta
- Aclon
- Actapulgite
- Actelsar
- Actelsar HCT
- Actemra
- Actilyse
- Acular
- Acupan
- Acuvail
- Acyclovir STADA
- Acyclovir STADA Cream
- Adalat
- Adenosin
- Adenosin Ebewe
- Adipiodon
- Advagraf
- Aerius
- Afinitor
- Agicarvir
- Agifovir-E
- Agilosart
- Agilosart-H
- Agimepzol
- Agimosarid
- Agimstan
- Agimstan-H
- Agiremid
- Agivastar
- Aibezym
- Air-X
- Alaxan
- Albendazol
- Albiomin
- Albumin
- Albumin người Grifols 20%
- Albuminar
- AlbuRx
- Albutein
- Alcuronium chloride
- Aldesleukin
- Alendronat
- Alertin
- Alfa-Lipogamma 600 Oral
- Alfuzosin hydrochlorid
- Algotra
- Alimemazin
- Alimta
- Allipem
- Allopurinol
- Allopurinol STADA
- Aloxi
- Alprazolam
- Alpha Chymotrypsin
- Alpha tocopherol
- Alphachymotrypsin Glomed
- Alphagan-P
- Aluvia
- Alzental
- Amaryl
- Ambroco
- Ambroxol
- Amcinol-Paste
- Amigold
- Amikacin
- Aminocaproic acid
- Aminoleban
- Aminoleban Oral
- Aminosteril N-Hepa
- Amiparen
- Amitriptyline
- Amiyu
- Amlodipine
- Amlor
- Amoxicillin
- Amoxicillin & clavulanate
- Ampicillin
- Amquitaz
- Anaferon for children
- Anargil
- Anaropin
- Andriol Testocaps
- Anepzil
- Anyfen
- Apaisac
- Apidra SoloStar
- Apitim 5
- Aprovel
- Aquaphil
- Arcalion
- Arcoxia
- Aricept Evess
- Arimidex
- Arnetine
- Artrodar
- A-Scabs
- Ascorbic acid
- Asperlican/Candinazol
- Aspilets EC
- Aspirin
- Asthmatin
- Atelec
- Atocib 120
- Atocib 90
- Atosiban PharmIdea
- Atozet
- Attapulgite
- Atussin
- Atropin
- Augbactam
- Augmentin Sachet
- Augmentin SR
- Augmentin Tablets
- Augmex
- Avamys
- Avastin
- Avelox Dịch truyền
- Avelox Viên nén
- Avodart
- Axcel Cefaclor-125 Suspension
- Axcel Cetirizine Syrup
- Axcel Chlorpheniramine
- Axcel Dexchlorpheniramine
- Axcel Dicyclomine-S Syrup
- Axcel Diphenhydramine Paediatric Syrup
- Axcel Erythromycin ES
- Axcel Eviline
- Axcel Fungicort Cream
- Axcel Fusidic acid Cream
- Axcel Fusidic acid-B Cream
- Axcel Hydrocortisone Cream
- Axcel Lignocaine 2% Sterile Gel
- Axcel Loratadine
- Axcel Miconazole Cream
- Axcel Paracetamol
- Axcel Urea Cream
- Axitan
- Azenmarol
- Azicine
- Aziphar
- Azithromycin





