Nhà sản xuất
Baxter / Cilag AG
Nhà tiếp thị
Janssen-Cilag
Thành phần
Mỗi 0,5mL: Ustekinumab 45mg.
Thành phần tá dược: L-histidine, L-histidine monohydrochloride monohydrate, polysorbate 80, sucrose, nước cất pha tiêm.
Mô tả
Ustekinumab là một kháng thể đơn dòng IgG1κ hoàn toàn của người tác động lên đích interleukin (IL)-12/23 được sản xuất bằng phương pháp tái tổ hợp DNA dòng tế bào ung thư tủy xương của chuột.
Dung dịch trong đến vẩn sữa, từ không màu đến màu vàng nhạt.
Dược lý
Đặc tính dược lực học
Nhóm dược lý: chất ức chế miễn dịch, ức chế interleukin, mã ATC: L04AC05.
Cơ chế tác dụng
Ustekinumab là một kháng thể hoàn toàn đơn dòng IgG1κ của người có ái lực gắn kết đặc hiệu đối với tiểu đơn vị p40 protein chung của cytokin interleukin (IL)-12 và (IL)-23 ở người. Ustekinumab ức chế hoạt tính sinh học của IL-12 và IL-23 bằng cách ngăn cản p40 gắn với thụ thể IL-12Rβ1 trên bề mặt của các tế bào miễn dịch. Ustekinumab không thể gắn với IL-12 hoặc IL-23 đã liên kết trước với IL-12Rβ1 ở bề mặt tế bào. Do đó, ustekinumab không tham gia vào phản ứng gây độc tế bào qua trung gian bổ thể hoặc kháng thể với các thụ thể IL-12 và/hoặc IL-23. IL-12 và IL-23 là những cytokine được cấu tạo bởi 2 đơn phân khác nhau và được tiết bởi tế bào trình diện kháng nguyên bị hoạt hóa, như đại thực bào và tế bào đuôi gai [tế bào tua], và cả hai cytokine này đều tham gia vào các hoạt động miễn dịch; IL-12 kích thích các tế bào diệt tự nhiên (NK) và gây biệt hóa các tế bào T có CD4+ thành kiểu hình tế bào T hỗ trợ 1 (Th1), trong khi đó IL-23 làm đẩy mạnh quá trình biệt hóa tạo tế bào T hỗ trợ 17 (Th17). Tuy nhiên, sự điều tiết bất thường của IL-12 và IL-23 thường gắn liền với các bệnh mắc phải qua trung gian miễn dịch, như bệnh vẩy nến, viêm khớp vẩy nến và bệnh Crohn.
Bằng cách gắn kết với tiểu đơn vị p40 chung của IL-12 và IL-23, ustekinumab có thể phát huy các tác dụng lâm sàng trong bệnh vẩy nến, viêm khớp vẩy nến và bệnh Crohn vì làm gián đoạn các quá trình biệt hóa Th1 và Th17 do cytokine tác động, mà các quá trình này có vai trò chủ yếu trong bệnh sinh của các căn bệnh này.
Điều trị ustekinumab trên bệnh nhân bị bệnh Crohn cho thấy giảm các chỉ số viêm bao gồm Protein phản ứng C (CRP) và calprotectin trong phân trong giai đoạn điều trị tấn công và sau đó được duy trì trong suốt giai đoạn điều trị duy trì.
Tiêm chủng
Trong Nghiên cứu vẩy nến 2 (PHOENIX 2) điều trị mở rộng và dài hạn, bệnh nhân người lớn điều trị với STELARA ít nhất 3,5 năm đã có đáp ứng kháng thể với vaccine polysaccharide phế cầu khuẩn và cả vaccine uốn ván tăng cao tương tự như ở nhóm chứng bệnh nhân vẩy nến không dùng liệu pháp điều trị toàn thân. Tỷ lệ bệnh nhân người lớn sinh các kháng thể chống phế cầu khuẩn và kháng thể chống uốn ván ở mức bảo vệ đều như nhau và hiệu giá kháng thể cũng bằng nhau giữa nhóm bệnh nhân dùng STELARA và nhóm bệnh nhân đối chứng.
Hiệu quả lâm sàng
Vẩy nến thể mảng (Người lớn)
Tính an toàn và hiệu quả của ustekinumab được đánh giá ở 1.996 bệnh nhân trong hai nghiên cứu có đối chứng với giả dược, mù đôi, phân nhóm ngẫu nhiên trên bệnh nhân bị vẩy nến thể mảng mức độ trung bình đến nặng cần dùng quang trị liệu hoặc trị liệu toàn thân. Ngoài ra, một nghiên cứu có đối chứng với hoạt chất, thiết kế mù đơn đối với người giám định, phân nhóm điều trị ngẫu nhiên cũng đã tiến hành so sánh ustekinumab với etanercept trên bệnh nhân bị vẩy nến thể mảng mức độ trung bình đến nặng không đáp ứng đủ, không dung nạp, hoặc có chống chỉ định dùng ciclosporin, MTX, hoặc liệu pháp PUVA.
Nghiên cứu vẩy nến 1 (PHOENIX 1) đã đánh giá 766 bệnh nhân. 53% số bệnh nhân này hoặc không đáp ứng, không dung nạp, hoặc có chống chỉ định dùng trị liệu toàn thân khác. Bệnh nhân được phân ngẫu nhiên vào nhóm ustekinumab sẽ dùng liều 45 mg hoặc 90 mg tại Tuần 0 và Tuần 4 và tiếp tục với cùng liều mỗi 12 tuần. Bệnh nhân được phân ngẫu nhiên vào nhóm giả dược cũng dùng giả dược tại Tuần 0 và Tuần 4, sau đó chuyển sang sử dụng ustekinumab (liều 45 mg hoặc 90 mg) tại Tuần 12 và Tuần 16, và tiếp tục với cùng liều điều trị mỗi 12 tuần. Bệnh nhân ban đầu được phân ngẫu nhiên dùng ustekinumab, khi có đáp ứng PASI 75 (cải thiện điểm số PASI [chỉ số về diện tích da bị vẩy nến và độ nặng của bệnh] ít nhất 75% so với ban đầu) ở cả hai Tuần 28 và Tuần 40 thì được chia nhóm ngẫu nhiên lại để nhận ustekinumab mỗi 12 tuần hoặc nhận giả dược (nghĩa là, ngừng dùng thuốc). Các bệnh nhân được chia nhóm ngẫu nhiên lại vào nhóm dùng giả dược tại tuần 40 sẽ dùng lại ustekinumab với chế độ liều ban đầu khi bị giảm ít nhất 50% mức cải thiện điểm số PASI tại tuần 40. Tất cả bệnh nhân đều được theo dõi cho tới 76 tuần tính từ lần đầu dùng thuốc nghiên cứu.
Nghiên cứu vẩy nến 2 (PHOENIX 2) đã đánh giá 1.230 bệnh nhân. 61% số bệnh nhân này hoặc không đáp ứng, không dung nạp, hoặc có chống chỉ định dùng trị liệu toàn thân khác. Những bệnh nhân được phân ngẫu nhiên vào nhóm ustekinumab sẽ dùng liều 45 mg hoặc 90 mg tại tuần 0 và tuần 4, tiếp theo là một liều bổ sung lúc 16 tuần. Những bệnh nhân được phân ngẫu nhiên vào nhóm giả dược cũng dùng giả dược tại tuần 0 và tuần 4, sau đó chuyển sang sử dụng ustekinumab (liều 45 mg hoặc 90 mg) tại tuần 12 và tuần 16. Tất cả bệnh nhân đều được theo dõi cho tới 52 tuần tính từ lần đầu dùng thuốc nghiên cứu.
Nghiên cứu vẩy nến 3 (ACCEPT) đã đánh giá 903 bệnh nhân bị bệnh vẩy nến mức độ trung bình đến nặng không đáp ứng đầy đủ, không dung nạp, hoặc có chống chỉ định dùng trị liệu toàn thân khác. Nghiên cứu này đã so sánh hiệu quả và đánh giá tính an toàn của ustekinumab với etanercept. Trong suốt 12 tuần của giai đoạn đối chứng với hoạt chất của nghiên cứu này, các bệnh nhân được phân ngẫu nhiên dùng etanercept (50 mg, hai lần mỗi tuần), ustekinumab 45 mg tại tuần 0 và tuần 4, hoặc ustekinumab 90 mg tại Tuần 0 và Tuần 4.
Các đặc điểm bệnh lúc ban đầu nhìn chung đều như nhau ở tất cả các nhóm điều trị trong Nghiên cứu vẩy nến 1 và Nghiên cứu vẩy nến 2, với trung vị của điểm số PASI ban đầu có giá trị từ 17 đến 18, trung vị của thang điểm Diện tích bề mặt cơ thể (BSA) ban đầu có giá trị ≥20, và trung vị của thang điểm Chất lượng cuộc sống của người có bệnh ngoài da (DLQI) dao động từ 10 đến 12. Khoảng 1/3 (trong Nghiên cứu vẩy nến 1) và 1/4 (trong Nghiên cứu vẩy nến 2) các đối tượng bị viêm khớp vẩy nến (PsA). Mức độ nặng tương tự của bệnh cũng được ghi nhận trong Nghiên cứu vẩy nến 3.
Tiêu chí đánh giá chính của các nghiên cứu này là tỷ lệ bệnh nhân đạt đáp ứng PASI 75 tại tuần 12 khi so với điểm số ban đầu (xem Bảng 1 và 2).
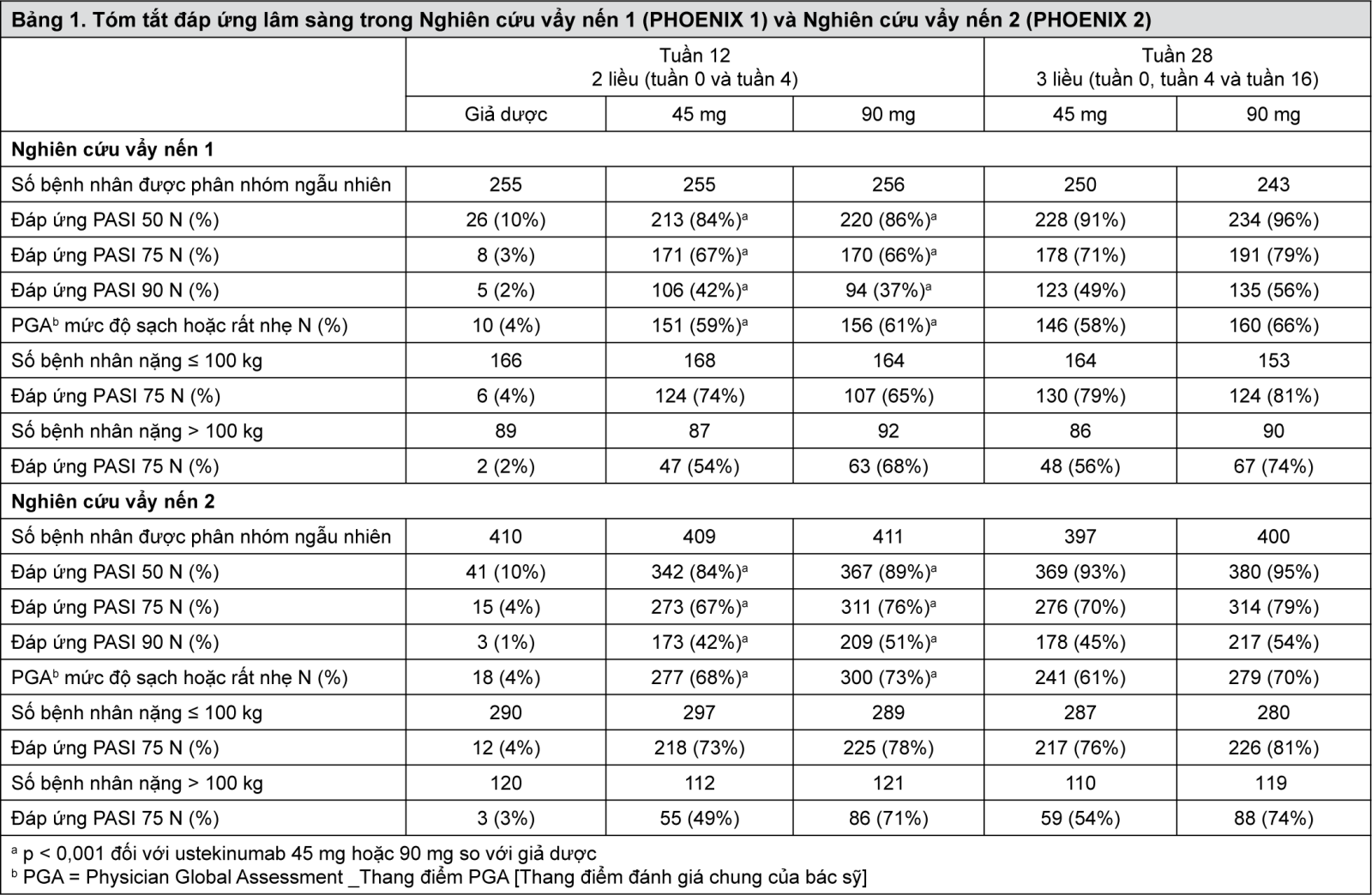

Trong Nghiên cứu vẩy nến 1, duy trì đáp ứng PASI 75 ở nhóm bệnh nhân tiếp tục điều trị được ghi nhận cao hơn rõ rệt so với nhóm ngừng điều trị (p < 0,001). Cũng quan sát thấy các kết quả tương tự với từng chế độ liều ustekinumab. Tại thời điểm 1 năm (tuần 52), 89% bệnh nhân được phân ngẫu nhiên lại vào nhóm duy trì điều trị đều là người có đáp ứng PASI 75 so với 63% ở nhóm bệnh nhân được phân ngẫu nhiên lại để dùng giả dược (ngừng điều trị) (p < 0,001). Tại thời điểm 18 tháng (tuần 76), 84% bệnh nhân được phân ngẫu nhiên lại vào nhóm duy trì điều trị đều là người có đáp ứng PASI 75 so với 19% ở nhóm bệnh nhân được phân ngẫu nhiên lại để dùng giả dược (ngừng điều trị). Tại thời điểm 3 năm (tuần 148), 82% bệnh nhân được phân ngẫu nhiên lại vào nhóm duy trì điều trị đều là người có đáp ứng PASI 75. Tại thời điểm 5 năm (tuần 244), 80% bệnh nhân được phân ngẫu nhiên lại vào nhóm duy trì điều trị đã có đáp ứng PASI 75.
Ở nhóm bệnh nhân được phân ngẫu nhiên lại dùng giả dược, và các bệnh nhân dùng lại phác đồ điều trị ustekinumab ban đầu sau khi mất ≥50% mức cải thiện điểm số PASI; và 85% số bệnh nhân này đã có lại đáp ứng PASI 75 trong vòng 12 tuần sau khi dùng lại thuốc nghiên cứu.
Trong Nghiên cứu vẩy nến 1, tại tuần 2 và tuần 12, điểm số DLQI đã cải thiện đáng kể so với giá trị ban đầu trong mỗi nhóm dùng ustekinumab so với nhóm giả dược. Sự cải thiện điểm số vẫn duy trì đến tuần 28. Tương tự, cũng quan sát thấy cải thiện đáng kể điểm số DLQI trong Nghiên cứu vẩy nến 2 tại tuần 4 và tuần 12, và vẫn duy trì đến tuần 24. Trong Nghiên cứu vẩy nến 1, sự cải thiện có ý nghĩa trong điểm số về vẩy nến móng (Chỉ số đánh giá mức độ nặng của bệnh vẩy nến móng), trong điểm số SF-36 đánh giá tổng hợp tình trạng thể chất và tâm thần của bệnh nhân và trong giá trị VAS (thang thị giác đánh giá mức độ ngứa) cũng quan sát thấy trong mỗi nhóm điều trị với ustekinumab so với giả dược. Trong Nghiên cứu vẩy nến 2, thang điểm về lo âu và trầm cảm (HADS) và bộ câu hỏi đánh giá mức độ hạn chế công việc (WLQ) cũng có điểm số cải thiện có ý nghĩa trong mỗi nhóm dùng ustekinumab so với giả dược.
Viêm khớp vẩy nến (PsA) (Người lớn)
Ustekinumab đã cho thấy cải thiện các dấu hiệu và triệu chứng, hoạt động thể chất và chất lượng cuộc sống liên quan đến sức khỏe, và làm giảm mức độ tiến triển của tổn thương khớp ngoại biên ở bệnh nhân người lớn có viêm khớp vẩy nến đang hoạt động.
Tính an toàn và hiệu quả của ustekinumab được đánh giá trong hai nghiên cứu có đối chứng với giả dược, mù đôi, phân nhóm điều trị ngẫu nhiên trên 927 bệnh nhân có viêm khớp vẩy nến đang hoạt động (≥5 khớp sưng và ≥5 khớp đau) mặc dù đã dùng thuốc kháng viêm không steroid (NSAID) hoặc thuốc chống thấp khớp làm cải thiện bệnh (DMARD). Bệnh nhân trong các nghiên cứu này đã được chẩn đoán viêm khớp vẩy nến ít nhất 6 tháng. Bệnh nhân với mỗi thể bệnh viêm khớp vẩy nến đã được thu nhận vào nghiên cứu, bao gồm viêm đa khớp không có các nốt dạng thấp (39%), viêm cột sống có viêm khớp ngoại biên (28%), viêm khớp ngoại biên không đối xứng (21%), viêm khớp liên đốt xa (12%) và viêm khớp biến dạng nặng (0,5%). Hơn 70% và 40% tương ứng số bệnh nhân trong cả hai nghiên cứu đã có tình trạng viêm điểm bám gân và viêm sưng ngón ở thời điểm ban đầu. Bệnh nhân được phân nhóm ngẫu nhiên để điều trị với ustekinumab 45 mg, 90 mg, hoặc giả dược tiêm dưới da tại Tuần 0 và Tuần 4, sau đó dùng thuốc mỗi 12 tuần (q12w). Khoảng 50% bệnh nhân tiếp tục dùng các liều MTX ổn định (≤ 25 mg/tuần).
Trong Nghiên cứu PsA 1 (PSUMMIT I) và Nghiên cứu PsA 2 (PSUMMIT II), 80% và 86% bệnh nhân tương ứng đã được điều trị trước đó với các DMARD. Trong Nghiên cứu 1, không cho phép thu nhận bệnh nhân đã điều trị từ trước với thuốc kháng yếu tố hoại tử khối u - alpha (TNFα). Trong Nghiên cứu 2, đa số bệnh nhân (58%, n=180) đã điều trị trước đó với một hoặc nhiều thuốc kháng TNFα, trong đó có hơn 70% bệnh nhân đã ngừng dùng thuốc kháng TNFα vì thiếu hiệu quả hoặc không dung nạp thuốc ở bất kỳ thời điểm nào.
Các dấu hiệu và triệu chứng
Điều trị bằng ustekinumab dẫn đến cải thiện đáng kể các chỉ số đánh giá mức độ bệnh tiến triển khi so với giả dược tại tuần 24. Tiêu chí đánh giá chính là tỷ lệ bệnh nhân đạt đáp ứng ACR 20 của Hội Thấp khớp học Hoa kỳ tại tuần 24. Các kết quả quan trọng về hiệu quả của thuốc được thể hiện trong Bảng 3 dưới đây.
- xem Bảng 3.
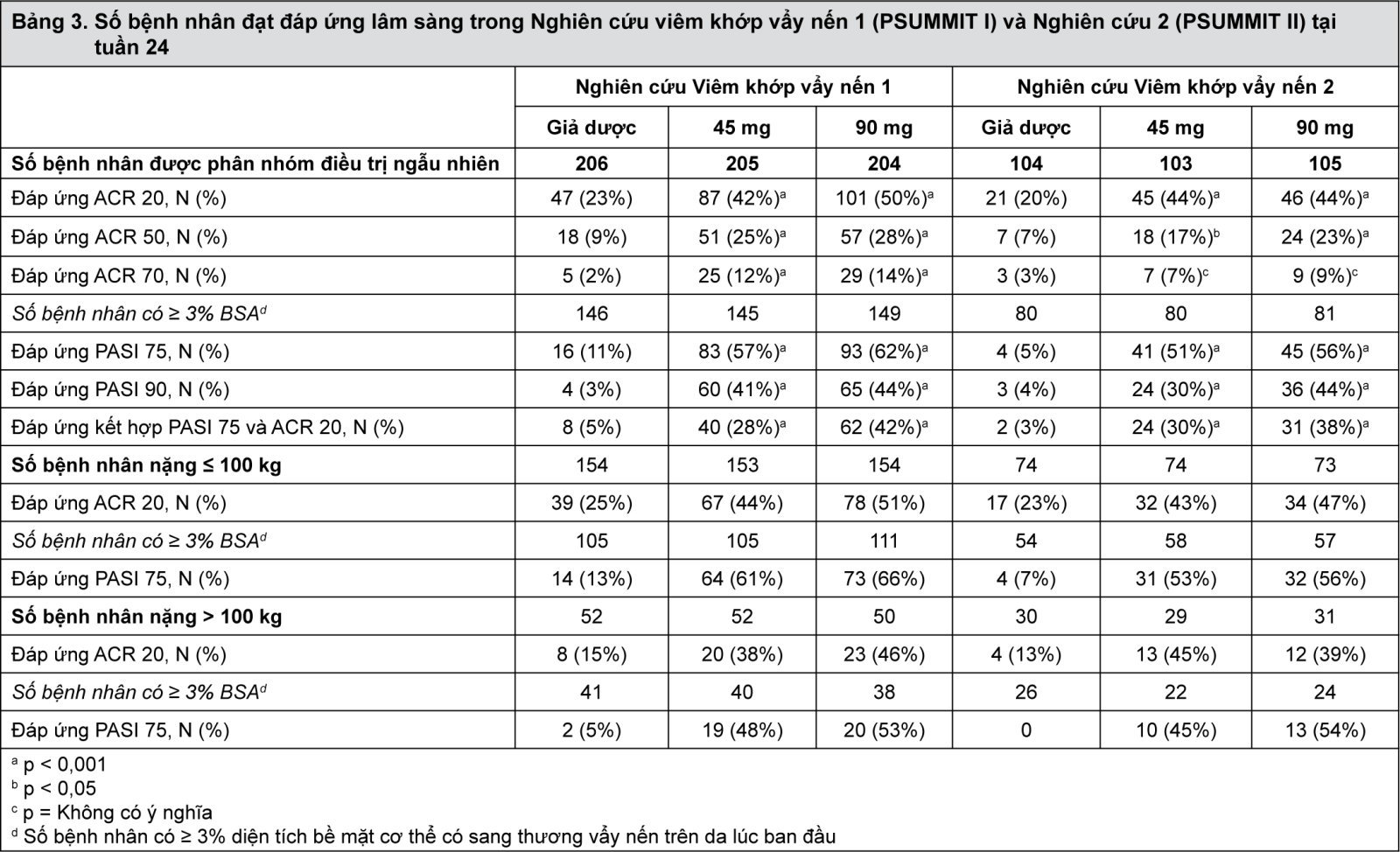
Các đáp ứng ACR 20, 50 và 70 tiếp tục cải thiện hoặc duy trì đến tuần 52 (Nghiên cứu PsA 1 và 2) và tuần 100 (Nghiên cứu PsA 1). Trong Nghiên cứu PsA 1, đáp ứng ACR 20 tại tuần 100 đã đạt đến 57% và 64%, cho liều 45 mg và 90 mg tương ứng. Trong Nghiên cứu PsA 2, đáp ứng ACR 20 tại tuần 52 đã đạt đến 47% và 48%, cho liều 45 mg và 90 mg tương ứng.
Tỷ lệ bệnh nhân đạt tiêu chuẩn đáp ứng sửa đổi trong viêm khớp vẩy nến (PsARC) cũng cao hơn đáng kể ở các nhóm dùng ustekinumab so với giả dược tại tuần 24. Các đáp ứng PsARC cũng được duy trì đến tuần 52 và tuần 100. Tỷ lệ bệnh nhân có biểu hiện viêm cột sống kèm viêm khớp ngoại biên tại thời điểm ban đầu, dùng ustekinumab đạt cải thiện 50% và 70% về điểm BASDAI (chỉ số tiến triển bệnh Viêm cột sống dính khớp) tại tuần 24, cao hơn so với giả dược.
Các đáp ứng quan sát được trong các nhóm dùng ustekinumab tương tự nhau giữa nhóm bệnh nhân dùng và không dùng MTX đồng thời, và được duy trì đến tuần 52 và tuần 100. Bệnh nhân trước đó được điều trị bằng các thuốc kháng TNFα đã đạt đáp ứng tốt hơn tại tuần 24 với trị liệu ustekinumab, so với bệnh nhân dùng giả dược (đáp ứng ACR 20 tại tuần 24 cho liều 45 mg và 90 mg lần lượt là 37% và 34%, so với giả dược là 15%; p<0,05), và các đáp ứng này được duy trì đến tuần 52.
Đối với các bệnh nhân bị viêm điểm bám gân và/hoặc viêm ngón tại thời điểm bắt đầu nghiên cứu, trong Nghiên cứu PsA 1, đã thấy sự cải thiện đáng kể về điểm số đánh giá tình trạng viêm điểm bám gân và viêm ngón ở các nhóm dùng ustekinumab so với nhóm giả dược tại tuần 24. Trong Nghiên cứu PsA 2, cũng thấy có sự cải thiện đáng kể của điểm số về viêm điểm bám gân và cải thiện giá trị (nhưng không có ý nghĩa thống kê) của điểm số về viêm ngón trong nhóm dùng ustekinumab 90 mg so với nhóm giả dược tại tuần 24. Sự cải thiện điểm số về viêm điểm bám gân và viêm ngón vẫn duy trì đến tuần 52 và tuần 100.
Đáp ứng trên hình ảnh X quang
Tổn thương cấu trúc ở cả bàn tay và bàn chân được thể hiện qua sự thay đổi về tổng điểm van der Heijde-Sharp (điểm số vdH-S) so với thời điểm bắt đầu nghiên cứu, thang điểm này được điều chỉnh cho phù hợp với bệnh viêm khớp vẩy nến bằng cách bổ sung đánh giá các khớp liên đốt xa của bàn tay. Một phân tích tích hợp với mục tiêu định trước đã được tiến hành trên dữ liệu tổng hợp từ 927 đối tượng trong cả hai Nghiên cứu PsA 1 và Nghiên cứu PsA 2. Ustekinumab đã cho thấy mức độ tiến triển tổn thương cấu trúc đã giảm đáng kể, có ý nghĩa thống kê khi so với giả dược, qua đánh giá sự thay đổi tổng điểm tại tuần 24 của thang điểm vdH-S đã điều chỉnh khi so với giá trị ban đầu (điểm số trung bình ± SD là 0,97±3,85 ở nhóm dùng giả dược so với 0,40±2,11 và 0,39±2,40 ở nhóm dùng ustekinumab liều 45 mg (p<0,05) và liều 90 mg (p<0,001), tương ứng). Tác dụng này được thấy rõ trong Nghiên cứu PsA 1. Tác dụng này đã được chứng minh xảy ra cho dù có sử dụng MTX đồng thời hay không, và vẫn được duy trì đến tuần 52 (phân tích tích hợp) và tuần 100 (Nghiên cứu PsA 1).
Hoạt động thể chất và chất lượng cuộc sống liên quan đến sức khỏe
Bệnh nhân dùng trị liệu ustekinumab đã cải thiện đáng kể về hoạt động thể chất, được đánh giá qua Chỉ số tàn tật của bộ câu hỏi đánh giá sức khỏe (HAQ-DI) tại tuần 24. Tỷ lệ bệnh nhân đạt cải thiện có ý nghĩa trên lâm sàng ≥ 0,3 điểm số HAQ-DI so với giá trị ban đầu trong các nhóm ustekinumab cũng cao hơn đáng kể khi so với nhóm giả dược. Sự cải thiện điểm số HAQ-DI so với giá trị ban đầu đã được duy trì đến tuần 52 và tuần 100.
Tại tuần 24, có sự cải thiện có ý nghĩa điểm số DLQI ở các nhóm dùng ustekinumab so với giả dược và cải thiện này vẫn duy trì đến tuần 52 và tuần 100. Trong Nghiên cứu PsA 2, có sự cải thiện đáng kể các điểm số Đánh giá chức năng của phương pháp điều trị bệnh mạn tính - Mức độ mệt mỏi (FACIT-F) ở các nhóm dùng ustekinumab so với giả dược tại tuần 24. Tỷ lệ bệnh nhân có cải thiện đáng kể về mặt lâm sàng về mức độ mệt mỏi (4 điểm trong thang điểm FACIT-F) cao hơn đáng kể trong các nhóm dùng ustekinumab khi so với nhóm giả dược. Cải thiện điểm số FACIT được duy trì đến tuần 52.
Đối tượng trẻ em
Cơ quan quản lý dược phẩm Châu Âu đã hoãn nghĩa vụ nộp kết quả các nghiên cứu liên quan đến ustekinumab trên một hoặc nhiều phân nhóm của đối tượng trẻ em từ 6 đến 11 tuổi bị vẩy nến thể mảng mức độ trung bình đến nặng và viêm khớp tự phát thiếu niên (xem mục Liều lượng và cách dùng để có thông tin về việc dùng thuốc trên trẻ em).
* Bệnh vẩy nến thể mảng trên trẻ em
Ustekinumab được chứng minh là giúp cải thiện các dấu hiệu, triệu chứng và chất lượng cuộc sống liên quan đến sức khỏe của bệnh nhân trẻ em từ 12 tuổi trở lên mắc bệnh vẩy nến thể mảng.
Hiệu quả của ustekinumab đã được nghiên cứu trên 110 bệnh nhân trẻ em từ 12 đến 17 tuổi mắc vẩy nến thể mảng mức độ trung bình đến nặng trong một nghiên cứu ngẫu nhiên, mù đôi, có đối chứng giả dược, đa trung tâm, Pha 3 (CADMUS). Bệnh nhân được phân nhóm ngẫu nhiên để sử dụng giả dược (n = 37), hoặc liều khuyến cáo của ustekinumab (xem mục Liều lượng và cách dùng; n = 36) hoặc một nửa liều khuyến cáo của ustekinumab (n = 37) bằng đường tiêm dưới da vào thời điểm tuần 0 và 4 sau đó dùng chế độ liều mỗi 12 tuần. Vào tuần 12, các bệnh nhân điều trị bằng giả dược được chuyển chéo sang sử dụng ustekinumab.
Các bệnh nhân có điểm PASI ≥ 12, PGA ≥ 3 và mức độ bề mặt da tổn thương tối thiểu là 10%, đây là những đối tượng cần sử dụng liệu trình toàn thân hoặc quang trị liệu, thỏa mãn để lựa chọn vào nghiên cứu. Khoảng 60% bệnh nhân trước đó đã được sử dụng liệu trình toàn thân theo phác đồ thông thường hoặc quang trị liệu. Khoảng 11% bệnh nhân trước đó đã được sử dụng chế phẩm sinh học.
Tiêu chí chính của nghiên cứu là tỷ lệ bệnh nhân đạt điểm PGA ở mức sạch (0) hoặc rất ít (1) vào tuần 12. Tiêu chí phụ bao gồm PASI 75, PASI 90, sự thay đổi chỉ số chất lượng cuộc sống về da trên trẻ em (Children’s Dermatology Life Quality Index-CDLQI) so với giá trị ban đầu, sự thay đổi thang đo chất lượng sống trên trẻ em (PedsQL-Paediatric Quality of Life Inventory) vào tuần 12 so với giá trị ban đầu. Tại tuần 12, nhóm bệnh nhân được điều trị bằng ustekinumab ghi nhận sự cải thiện cao hơn có ý nghĩa về tình trạng vẩy nến và chất lượng cuộc sống liên quan đến sức khỏe khi so sánh với nhóm dùng giả dược (Bảng 4).
Tất cả các bệnh nhân được theo dõi hiệu quả điều trị trong thời gian lên tới 52 tuần sau lần đầu tiên sử dụng hoạt chất nghiên cứu. Tỷ lệ bệnh nhân có điểm PGA mức sạch (0) hoặc rất ít (1) và tỷ lệ bệnh nhân đạt PASI 75 cho thấy sự khác biệt giữa nhóm điều trị bằng ustekinumab và nhóm sử dụng giả dược trong lần khám đầu tiên tại tuần 4, khác biệt lớn nhất được ghi nhận vào tuần 12. Sự cải thiện điểm số trong các thang PGA, PASI, CDLQI và PedsQL được duy trì đến tuần 52.
- xem Bảng 4.
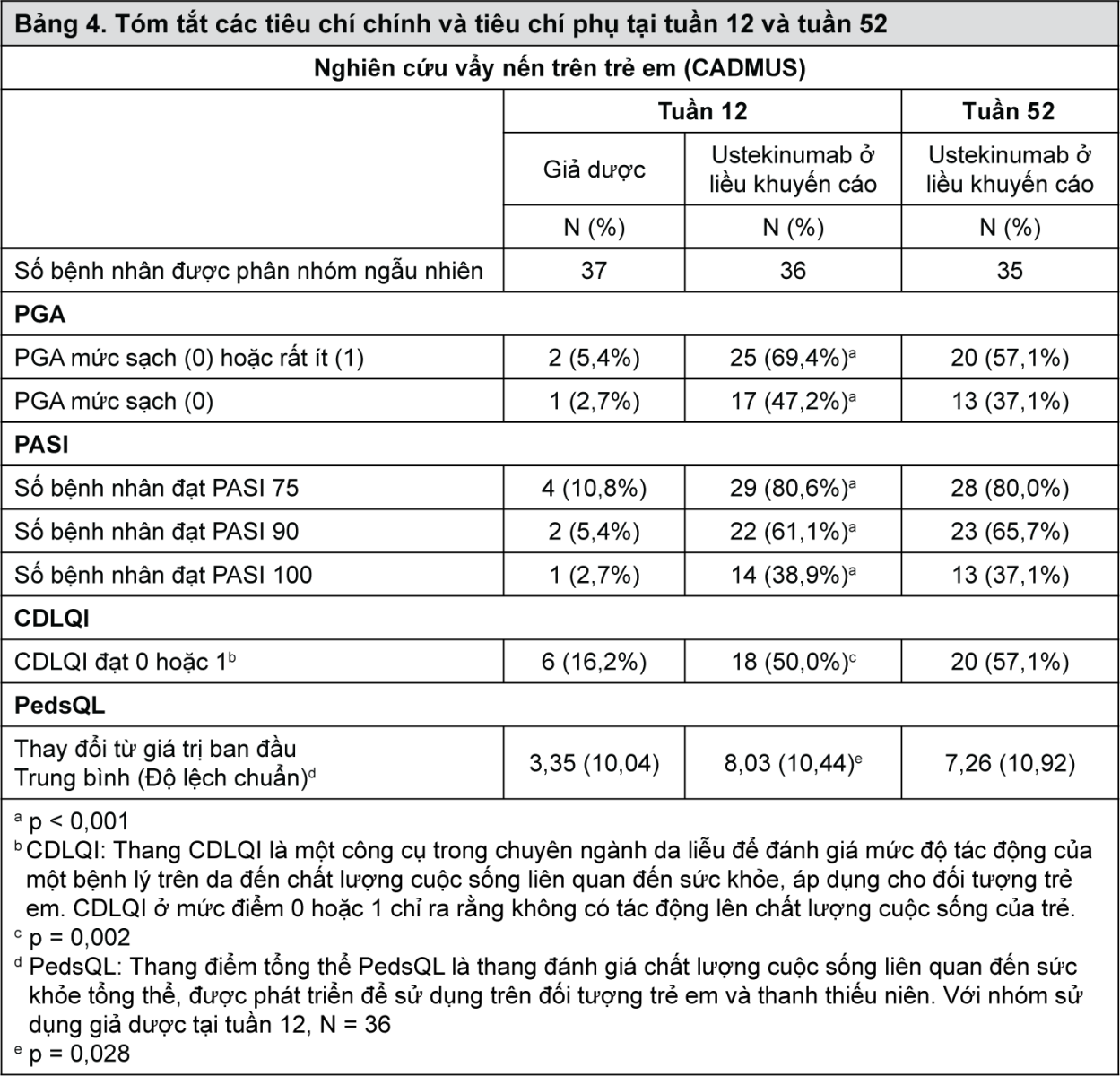
Trong giai đoạn đối chứng giả dược đến tuần 12, hiệu quả ghi nhận trên nhóm dùng liều khuyến cáo và nửa liều khuyến cáo tương đối tương đồng, xét trên tiêu chí chính (lần lượt là 69,4% và 67,6%) mặc dù có bằng chứng cho thấy đáp ứng phụ thuộc liều khi xét trên các tiêu chí hiệu quả ở mức độ cao hơn (ví dụ PGA mức sạch (0), PASI 90). Sau tuần 12, hiệu quả nhìn chung cao hơn và duy trì tốt hơn trên nhóm sử dụng liều khuyến cáo so với nhóm sử dụng nửa liều khuyến cáo, trong đó nhóm dùng nửa liều khuyến cáo đã ghi nhận tình trạng mất hiệu lực của thuốc ở mức độ nhẹ phổ biến hơn trong giai đoạn cuối của mỗi khoảng đưa liều 12 tuần. Dữ liệu an toàn của liều khuyến cáo và nửa liều khuyến cáo được ghi nhận tương tự nhau.
* Bệnh Crohn
Tính an toàn và hiệu quả của ustekinumab đã được đánh giá trong ba nghiên cứu ngẫu nhiên, mù đôi, đối chứng giả dược, đa trung tâm trên bệnh nhân người lớn có tình trạng bệnh Crohn đang hoạt động ở mức độ trung bình đến nặng (chỉ số điểm đánh giá mức độ hoạt động của bệnh Crohn [CDAI] ở giá trị ≥ 220 và ≤ 450). Chương trình phát triển lâm sàng bao gồm hai nghiên cứu điều trị tấn công theo đường tĩnh mạch kéo dài 8 tuần (UNITI-1 và UNITI-2), sau đó là nghiên cứu về giai đoạn điều trị duy trì có phân nhóm bệnh nhân ngẫu nhiên ngừng dùng thuốc, sử dụng theo đường tiêm dưới da, kéo dài 44 tuần (IM-UNITI), tổng thời gian các nghiên cứu này là 52 tuần điều trị.
Các nghiên cứu điều trị tấn công đã thu nhận 1409 bệnh nhân (UNITI-1, n = 769; UNITI-2 n = 640). Tiêu chí chính trong cả hai nghiên cứu điều trị tấn công là tỷ lệ bệnh nhân ghi nhận đáp ứng lâm sàng (được định nghĩa là sự giảm điểm CDAI ≥ 100 điểm) vào tuần 6. Các dữ liệu liên quan đến hiệu quả đã được thu thập và phân tích đến tuần 8 trong cả hai nghiên cứu. Nghiên cứu cho phép sử dụng đồng thời các thuốc corticosteroid đường uống, thuốc điều hòa miễn dịch, các thuốc aminosalicylate và kháng sinh và 75% bệnh nhân vẫn tiếp tục sử dụng ít nhất một thuốc trong số này. Trong cả hai nghiên cứu, bệnh nhân được phân ngẫu nhiên vào các nhóm để sử dụng một liều đơn theo đường tĩnh mạch của hoặc ustekinumab với liều khuyến cáo theo các mức cân nặng, khoảng 6 mg/kg (xem mục Liều lượng và cách dùng trong tờ Tóm tắt Đặc tính Sản phẩm của STELARA 130 mg dung dịch đậm đặc để pha dịch truyền), hoặc ustekinumab liều cố định 130 mg, hoặc giả dược ở tuần 0.
Bệnh nhân trong nghiên cứu UNITI-1 là những bệnh nhân trước đó đã thất bại hoặc không dung nạp với phác đồ kháng TNFα. Khoảng 48% bệnh nhân đã thất bại với 1 phác đồ kháng TNFα và 52% đã thất bại với 2 hoặc 3 phác đồ kháng TNFα. Trong nghiên cứu này, 29,1% bệnh nhân có đáp ứng ban đầu không đủ (bệnh nhân không đáp ứng nguyên phát), 69,4% đã có đáp ứng nhưng sau đó mất đáp ứng (bệnh nhân không đáp ứng thứ phát), và 36,4% không dung nạp với các phác đồ kháng TNFα.
Các bệnh nhân trong nghiên cứu UNITI-2 là bệnh nhân đã thất bại với ít nhất một phác đồ trị liệu thông thường, bao gồm các corticosteroid hoặc các thuốc điều hòa miễn dịch, hoặc chưa từng sử dụng phác đồ kháng TNF-α (68,6%) hoặc đã từng sử dụng trước đó nhưng chưa có dấu hiệu thất bại với phác đồ kháng TNFα (31,4%).
Trong cả nghiên cứu UNITI-1 và UNITI-2, nhóm điều trị bằng ustekinumab có tỷ lệ bệnh nhân đáp ứng lâm sàng và thuyên giảm cao hơn có ý nghĩa so với nhóm dùng giả dược (Bảng 5). Nhóm bệnh nhân điều trị bằng ustekinumab đã ghi nhận đáp ứng và thuyên giảm lâm sàng có ý nghĩa ngay từ tuần 3 và tiếp tục tăng lên cho đến tuần 8. Trong các nghiên cứu điều trị tấn công này, hiệu quả được ghi nhận cao hơn và duy trì tốt hơn trên nhóm bệnh nhân dùng liều theo các mức cân nặng so với nhóm dùng liều 130 mg, và do đó chế độ liều theo các mức cân nặng được coi là liều tấn công dùng đường tĩnh mạch được khuyến cáo.
- xem Bảng 5.

Nghiên cứu duy trì (IM-UNITI), đánh giá 388 bệnh nhân đã đạt mức đáp ứng lâm sàng 100 điểm tại tuần 8 sau khi điều trị tấn công bằng ustekinumab trong nghiên cứu UNITI-1 và UNITI-2. Bệnh nhân được phân nhóm ngẫu nhiên để sử dụng liều duy trì theo đường tiêm dưới da với chế độ liều 90 mg ustekinumab mỗi 8 tuần, 90 mg ustekinumab mỗi 12 tuần hoặc giả dược trong 44 tuần (để biết thêm thông tin về chế độ liều duy trì khuyến cáo, xem phần Liều lượng và cách dùng).
Tỷ lệ bệnh nhân duy trì được sự thuyên giảm lâm sàng và đáp ứng lâm sàng trong nhóm điều trị bằng ustekinumab cao hơn đáng kể so với nhóm sử dụng giả dược tại tuần 44.
- xem Bảng 6.

Trong nghiên cứu IM-UNITI, 29 trong số 129 bệnh nhân không duy trì đáp ứng với ustekinumab khi điều trị mỗi 12 tuần và được phép chỉnh liều để dùng ustekinumab mỗi 8 tuần. Tình trạng mất đáp ứng được định nghĩa là điểm CDAI ≥ 220 và mức tăng ≥ 100 điểm từ điểm CDAI ban đầu. Trên những bệnh nhân này, sự thuyên giảm lâm sàng đã ghi nhận được ở 41,4% bệnh nhân tại thời điểm 16 tuần sau khi chỉnh liều.
Các bệnh nhân không có đáp ứng lâm sàng với phác đồ tấn công ustekinumab tại tuần 8 của nghiên cứu giai đoạn tấn công UNITI-1 và UNITI-2 (476 bệnh nhân) được tham gia vào nhóm không được ngẫu nhiên hóa trong nghiên cứu duy trì (IM-UNITI) và được sử dụng 90 mg ustekinumab đường tiêm dưới da tại thời điểm này. Tám tuần sau đó, 50,5% bệnh nhân đã ghi nhận đáp ứng lâm sàng và tiếp tục được sử dụng liều duy trì mỗi 8 tuần; trong số các bệnh nhân dùng chế độ liều duy trì này, phần lớn duy trì đáp ứng (68,1%) và đạt thuyên giảm (50,2%) vào tuần 44, các tỷ lệ này tương tự với nhóm bệnh nhân đã đáp ứng ngay với phác đồ tấn công ustekinumab.
Trong số 131 bệnh nhân đáp ứng với phác đồ tấn công ustekinumab, và được phân ngẫu nhiên vào nhóm dùng giả dược tại thời điểm bắt đầu nghiên cứu duy trì, 51 bệnh nhân sau đó đã mất đáp ứng và được sử dụng 90 mg ustekinumab tiêm dưới da mỗi 8 tuần. Phần lớn bệnh nhân đã mất đáp ứng và được sử dụng lại ustekinumab trong vòng 24 tuần sử dụng chế độ truyền tấn công. Trong số 51 bệnh nhân này, 70,6% đã ghi nhận đáp ứng lâm sàng và 39,2% ghi nhận thuyên giảm lâm sàng 16 tuần sau khi sử dụng liều tiêm dưới da ustekinumab đầu tiên.
* Nội soi
Hình ảnh nội soi niêm mạc đã được đánh giá trên 252 bệnh nhân có tình trạng bệnh lý nền ghi nhận trên nội soi trong một nghiên cứu nhánh. Tiêu chí chính là sự thay đổi từ mức ban đầu tính theo thang đánh giá rút gọn mức độ nặng trên nội soi áp dụng cho bệnh Crohn (Simplified Endoscopic Disease Severity Score for Crohn’s Disease (SES-CD)), điểm số đánh giá kết hợp qua 5 đoạn hồi tràng-kết tràng về sự hiện diện/kích thước vùng loét, tỷ lệ bề mặt niêm mạc bị bao phủ bởi vùng loét, tỷ lệ bề mặt niêm mạc bị ảnh hưởng bởi bất kỳ tổn thương nào khác và sự hiện diện/loại của hẹp/chít hẹp ruột. Tại tuần thứ 8, sau khi sử dụng một liều đơn theo phác đồ tấn công đường tĩnh mạch, mức độ thay đổi trên thang điểm SES-CD của nhóm dùng ustekinumab (n = 155, thay đổi trung bình = -2,8) lớn hơn nhóm dùng giả dược (n = 97, thay đổi trung bình = -0,7; p = 0,012).
* Đáp ứng trên lỗ rò
Trên một phân nhóm bệnh nhân có lỗ rò thông ở giai đoạn đầu nghiên cứu (8,8%; n = 26), 12/15 (80%) bệnh nhân được điều trị bằng ustekinumab đã ghi nhận hiệu quả trên lỗ rò sau 44 tuần (được định nghĩa là giảm ≥ 50% số lượng lỗ rò thông ở giai đoạn đầu của nghiên cứu tấn công) so với 5/11 (45,5%) trong nhóm bệnh nhân sử dụng giả dược.
* Chất lượng cuộc sống liên quan đến sức khỏe
Chất lượng cuộc sống liên quan đến sức khỏe đã được đánh giá bằng bộ câu hỏi IBDQ và SF-36. Tại tuần 8, các bệnh nhân sử dụng ustekinumab cho thấy mức độ cải thiện lâm sàng lớn hơn có ý nghĩa thống kê và có ý nghĩa lâm sàng về thang điểm tổng thể IBDQ và thang điểm tóm tắt các chỉ tiêu về tinh thần trong bộ câu hỏi SF-36 trong cả hai nghiên cứu UNITI-1 và UNITI-2, và về thang điểm tóm tắt các chỉ tiêu thể chất trong bộ câu hỏi SF-36 trong nghiên cứu UNITI-2, khi so sánh với giả dược. Sự cải thiện này nhìn chung được duy trì tốt hơn trên nhóm bệnh nhân điều trị bằng ustekinumab trong nghiên cứu IM-UNITI cho đến tuần 44 khi so sánh với giả dược.
Quần thể trẻ em
Cơ quan quản lý dược phẩm Châu Âu đã hoãn nghĩa vụ nộp kết quả của các nghiên cứu liên quan đến ustekinumab trên một hoặc nhiều phân nhóm của đối tượng trẻ em trong bệnh Crohn (Xem mục Liều lượng và cách dùng để có thêm thông tin về việc sử dụng thuốc trên trẻ em).
Đặc tính dược động học
Hấp thu
Thời gian trung vị để thuốc đạt được nồng độ tối đa trong huyết tương (tmax) là 8,5 ngày sau khi tiêm dưới da liều đơn 90 mg trên người khỏe mạnh. Giá trị tmax trung vị của ustekinumab sau một liều đơn 45 mg hoặc 90 mg tiêm dưới da ở những bệnh nhân vẩy nến tương đương với tmax trung vị trên người khỏe mạnh.
Ở những bệnh nhân mắc bệnh vẩy nến, sinh khả dụng tuyệt đối của ustekinumab khi tiêm dưới da một liều đơn là khoảng 57,2%.
Phân bố
Trung vị của thể tích phân bố trong giai đoạn cuối (Vz) sau khi tiêm tĩnh mạch một liều đơn trên bệnh nhân vẩy nến nằm trong khoảng 57 đến 83 mL/kg.
Chuyển hóa
Chưa biết rõ con đường chuyển hóa của ustekinumab.
Thải trừ
Ở bệnh nhân mắc bệnh vẩy nến, trung vị của hệ số thanh thải toàn thân (CL) sau khi tiêm tĩnh mạch một liều duy nhất nằm trong khoảng từ 1,99 đến 2,34 mL/ngày/kg cân nặng. Ở bệnh nhân mắc bệnh vẩy nến, viêm khớp vẩy nến hoặc bệnh Crohn, trung vị thời gian bán thải (t1/2) của ustekinumab xấp xỉ 3 tuần, dao động trong khoảng từ 15 đến 32 ngày trong tất cả các nghiên cứu về bệnh vẩy nến và viêm khớp vẩy nến. Trong một phân tích dược động học theo quần thể, hệ số thanh thải biểu kiến (CL/F) và thể tích phân bố biểu kiến (V/F) lần lượt là 0,465 L/ngày và 15,7 L ở bệnh nhân vẩy nến. Hệ số thanh thải biểu kiến CL/F của ustekinumab không bị ảnh hưởng bởi giới tính. Phân tích dược động học theo quần thể cho thấy có xu hướng thải trừ ustekinumab nhiều hơn ở những bệnh nhân có xét nghiệm kháng thể kháng ustekinumab dương tính.
Khoảng tuyến tính của liều dùng
Ở những bệnh nhân mắc bệnh vẩy nến, phơi nhiễm toàn thân của ustekinumab (Cmax và AUC) tăng theo tỷ lệ liều dùng khi tiêm tĩnh mạch một liều đơn nằm trong khoảng từ 0,09 mg/kg đến 4,5 mg/kg hoặc sau khi tiêm dưới da các liều đơn dao động từ 24 mg đến 240 mg.
So sánh giữa đơn liều và đa liều
Đặc tính nồng độ trong huyết thanh theo thời gian của ustekinumab nhìn chung có thể dự đoán được sau khi tiêm thuốc dưới da theo chế độ đơn liều hoặc đa liều. Ở bệnh nhân vẩy nến, nồng độ ustekinumab trong huyết thanh đạt trạng thái ổn định vào tuần 28 sau khi tiêm dưới da các liều ban đầu tại Tuần 0 và Tuần 4, và các liều tiếp theo mỗi 12 tuần. Trung vị nồng độ đáy ở trạng thái ổn định nằm trong khoảng 0,21 mcg/mL đến 0,26 mcg/mL (liều 45 mg) và 0,47 mcg/mL đến 0,49 mcg/mL (liều 90 mg). Khi dùng thuốc tiêm dưới da mỗi 12 tuần, không nhận thấy sự tích lũy rõ rệt về nồng độ ustekinumab trong huyết thanh theo thời gian điều trị.
Ở bệnh nhân mắc bệnh Crohn, sau khi tiêm tĩnh mạch liều ~6 mg/kg, bắt đầu tại tuần 8, tiêm dưới da liều duy trì ustekinumab 90 mg mỗi 8 hoặc 12 tuần. Nồng độ ustekinumab ở trạng thái ổn định đạt được khi bắt đầu liều duy trì lần hai. Trung vị nồng độ đáy ở trạng thái ổn định trong khoảng 1,97 mcg/mL đến 2,24 mcg/mL và từ 0,61 mcg/mL đến 0,76 mcg/mL cho ustekinumab 90 mg mỗi 8 tuần hoặc mỗi 12 tuần tương ứng. Nồng độ đáy ở trạng thái ổn định của liều ustekinumab 90 mg mỗi 8 tuần cho thấy tỷ lệ thuyên giảm lâm sàng cao hơn so với nồng độ đáy ở trạng thái ổn định của liều ustekinumab 90 mg mỗi 12 tuần.
Ảnh hưởng của khối lượng cơ thể đối với dược động học
Trong một phân tích dược động học theo quần thể sử dụng dữ liệu từ các bệnh nhân bị vẩy nến, thể trọng được chứng minh là đồng tham số quan trọng nhất ảnh hưởng đến sự thanh thải ustekinumab. Trung vị hệ số thanh thải CL/F ở những bệnh nhân cân nặng >100kg đã cao hơn khoảng 55% so với những bệnh nhân cân nặng ≤100kg. Trung vị giá trị V/F của những bệnh nhân cân nặng >100kg đã cao hơn khoảng 37% so với những bệnh nhân cân nặng ≤100kg. Trung vị nồng độ đáy của ustekinumab trong huyết thanh ở bệnh nhân nặng cân hơn (>100kg) của nhóm dùng liều 90 mg đã có giá trị tương đương với các trị số của những bệnh nhân nhẹ cân hơn (≤100kg) trong nhóm dùng liều 45 mg. Các kết quả tương tự được lấy từ phân tích xác nhận dữ liệu dược động học theo quần thể bằng cách sử dụng dữ liệu từ các bệnh nhân bị viêm khớp vẩy nến.
Đối tượng đặc biệt
Không có dữ liệu dược động học trên những bệnh nhân suy thận hoặc suy gan. Không có các nghiên cứu chuyên biệt được thực hiện trên bệnh nhân cao tuổi.
Dược động học của ustekinumab nói chung giống nhau giữa bệnh nhân người Châu Á và không phải Châu Á bị bệnh vẩy nến.
Ở bệnh nhân mắc bệnh Crohn, giá trị biến thiên của hệ số thanh thải ustekinumab CL bị ảnh hưởng bởi cân nặng, nồng độ albumin huyết thanh, CRP, tình trạng thất bại đối kháng TNF, giới tính, chủng tộc (Châu Á so với không phải Châu Á), và tình trạng kháng thể kháng ustekinumab trong đó cân nặng là yếu tố đồng biến chính ảnh hưởng tới thể tích phân bố. Dùng đồng thời với các chất điều hòa miễn dịch không gây ảnh hưởng đáng kể đến sự phân bố ustekinumab. Tác động của những tác nhân đồng biến có ý nghĩa thống kê đáng kể trên các thông số dược động học tương ứng trong khoảng ± 20% khi đánh giá trên khoảng đại diện giá trị đồng biến hoặc phân loại dữ liệu trong khoảng giá trị biến thiên tổng thể ghi nhận được trong dược động học của ustekinumab.
Trong phân tích dược động học theo quần thể, không có các dấu hiệu về tác dụng của thuốc lá hoặc rượu lên dược động học của ustekinumab.
Nồng độ ustekinumab trong huyết thanh của bệnh nhi bị vẩy nến tuổi từ 12 đến 17 được điều trị với liều khuyến cáo tính theo cân nặng nhìn chung là tương tự như ở đối tượng người lớn bị bệnh vẩy nến được điều trị với liều cho người lớn, trong khi đó nồng độ ustekinumab trong huyết thanh ở bệnh nhi bị vẩy nến điều trị với nửa liều khuyến cáo tính theo cân nặng nhìn chung là thấp hơn trên bệnh nhân người lớn tương ứng.
Điều hòa các enzyme CYP450
Các tác dụng của IL-12 hoặc IL-23 lên sự điều hòa của các enzyme CYP450 đã được đánh giá trong một nghiên cứu in vitro sử dụng tế bào gan người. Nghiên cứu này cho thấy IL-12 và/hoặc IL-23 ở mức 10 ng/mL không làm thay đổi các hoạt động của enzyme CYP450 ở người (CYP1A2, 2B6, 2C9, 2C19, 2D6, hoặc 3A4, xem phần Tương tác).
Dữ liệu an toàn tiền lâm sàng
Dữ liệu phi lâm sàng cho thấy không có mối nguy hiểm đặc biệt (ví dụ như độc tính trên cơ quan) cho người, dựa vào các nghiên cứu về độc tính dùng liều lặp lại và độc tính trên sự phát triển và khả năng sinh sản, bao gồm các đánh giá về an toàn thuốc. Trong các nghiên cứu độc tính trên sự phát triển và khả năng sinh sản ở khỉ đuôi dài (khỉ cynomolgus), không quan sát thấy tác dụng bất lợi nào lên các chỉ số về khả năng sinh sản của khỉ đực cũng như dị tật bẩm sinh hoặc độc tính trên sự phát triển. Không phát hiện tác dụng bất lợi nào lên các chỉ số về khả năng sinh sản của khỉ cái bằng cách sử dụng một kháng thể tương tự tác động lên IL-12/23 ở chuột nhắt.
Trong các nghiên cứu trên động vật, những mức liều được sử dụng cao hơn đến khoảng 45 lần liều tương đương cao nhất dự định sẽ dùng cho bệnh nhân vẩy nến và dẫn đến nồng độ đỉnh trong huyết thanh ở khỉ cao hơn mức 100 lần so với nồng độ quan sát được ở người.
Không thực hiện các nghiên cứu về tính gây ung thư với ustekinumab do thiếu các mô hình phù hợp đối với một kháng thể không có phản ứng chéo với tiểu đơn vị protein p40 của IL-12/23.
Chỉ định/Công dụng
Bệnh vẩy nến thể mảng: STELARA được chỉ định để điều trị bệnh vẩy nến thể mảng từ mức độ trung bình đến nặng ở người lớn không đáp ứng, hoặc chống chỉ định, hay không dung nạp với các liệu pháp điều trị toàn thân khác bao gồm ciclosporin, methotrexat (MTX) hoặc quang liệu pháp PUVA (uống psoralen và chiếu tia cực tím A) (xem phần Đặc tính dược lực học).
Bệnh viêm khớp vẩy nến: STELARA, dùng đơn độc hoặc phối hợp với MTX, được chỉ định để điều trị viêm khớp vẩy nến thể hoạt động ở bệnh nhân người lớn có đáp ứng không đầy đủ với thuốc chống thấp khớp làm cải thiện bệnh (DMARD) không phải thuốc sinh học đã dùng trước đây (xem phần Đặc tính dược lực học).
Liều lượng & Cách dùng
Sử dụng STELARA dưới sự hướng dẫn và giám sát của các bác sỹ có kinh nghiệm trong việc chẩn đoán và điều trị các bệnh thuộc chỉ định của STELARA.
Liều dùng
Bệnh vẩy nến thể mảng
STELARA được khuyến cáo dùng với liều khởi đầu 45 mg tiêm dưới da, tiếp theo là một liều 45 mg vào 4 tuần sau, và sau đó mỗi 12 tuần.
Cần xem xét ngừng điều trị ở những bệnh nhân không đáp ứng sau 28 tuần điều trị.
Bệnh nhân với thể trọng >100kg: Đối với những bệnh nhân có thể trọng >100kg, liều khởi đầu là 90 mg tiêm dưới da, tiếp theo là một liều 90 mg vào 4 tuần sau, và sau đó mỗi 12 tuần. Ở những bệnh nhân này, liều 45 mg cũng cho thấy hiệu quả. Tuy nhiên, liều 90 mg cho hiệu quả cao hơn (xem phần Đặc tính dược lực học, Bảng 1).
Viêm khớp vẩy nến (PsA)
STELARA được khuyến cáo dùng với liều khởi đầu 45 mg tiêm dưới da, tiếp theo là một liều 45 mg vào 4 tuần sau, và sau đó mỗi 12 tuần. Ngoài ra, có thể dùng liều 90 mg cho bệnh nhân có thể trọng >100kg.
Cần xem xét ngừng điều trị ở những bệnh nhân không đáp ứng sau 28 tuần điều trị.
Bệnh nhân cao tuổi (≥ 65 tuổi): Không cần chỉnh liều ở bệnh nhân cao tuổi (xem phần Cảnh báo).
Suy thận và suy gan: STELARA chưa được nghiên cứu ở các đối tượng bệnh nhân này. Không thể đưa ra khuyến cáo về liều dùng.
Đối tượng trẻ em: Chưa thiết lập được tính an toàn và hiệu quả của STELARA ở trẻ em dưới 12 tuổi bị vẩy nến hoặc trẻ em dưới 18 tuổi bị viêm khớp vẩy nến.
Cách dùng
STELARA trong bơm tiêm chứa sẵn thuốc chỉ được tiêm dưới da. Nếu có thể, nên tránh các vị trí tiêm là những vùng da có sang thương vẩy nến.
Sau khi được huấn luyện thích hợp về kỹ thuật tiêm dưới da, bệnh nhân hoặc những người chăm sóc bệnh nhân có thể tiêm STELARA nếu bác sỹ quyết định điều này là thích đáng. Tuy nhiên, bác sỹ phải đảm bảo theo dõi bệnh nhân cho phù hợp. Cần hướng dẫn bệnh nhân hoặc những người chăm sóc bệnh nhân tiêm lượng thuốc STELARA đã được kê đơn theo các hướng dẫn được cung cấp trong tờ hướng dẫn sử dụng thuốc. Tờ hướng dẫn sử dụng thuốc có ghi chi tiết cách dùng thuốc.
Để biết thêm các hướng dẫn về chuẩn bị thuốc tiêm và thận trọng đặc biệt khi xử lý thuốc, xem Thận trọng.
HƯỚNG DẪN SỬ DỤNG
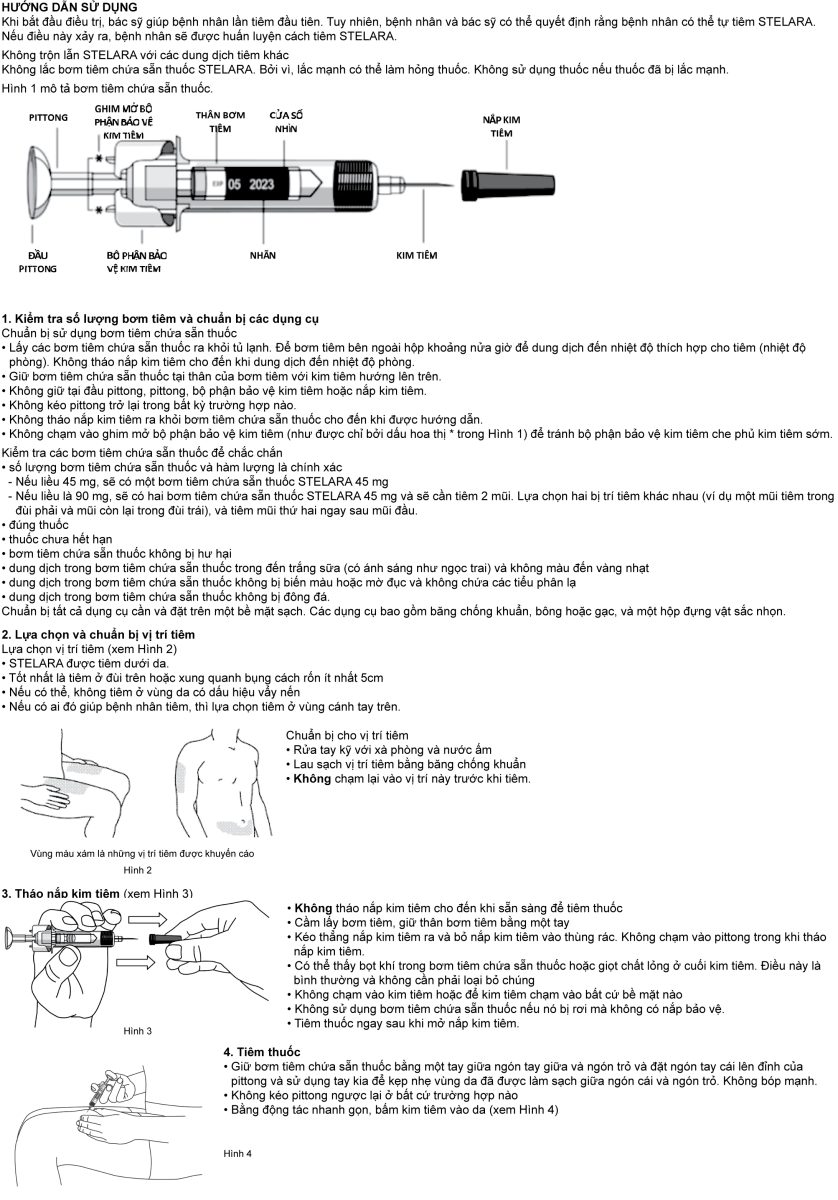

Cảnh báo
Nhiễm khuẩn
Ustekinumab có thể có khả năng làm tăng nguy cơ nhiễm khuẩn và tái kích hoạt các bệnh nhiễm khuẩn tiềm ẩn. Trong các nghiên cứu lâm sàng, đã quan sát thấy các nhiễm khuẩn nghiêm trọng do vi khuẩn, nấm, và virus ở những bệnh nhân đang dùng STELARA (xem phần Tác dụng ngoại ý).
Cần thận trọng khi xem xét sử dụng STELARA ở những bệnh nhân có nhiễm khuẩn mạn tính hoặc có tiền sử nhiễm khuẩn tái phát (xem phần Chống chỉ định).
Trước khi bắt đầu điều trị với STELARA, bệnh nhân nên được đánh giá về tình trạng nhiễm lao. Không được dùng STELARA cho bệnh nhân lao thể hoạt động (xem phần Chống chỉ định). Nên bắt đầu điều trị nhiễm lao thể tiềm ẩn trước khi dùng STELARA. Cũng cần xem xét dùng thuốc chống lao trước khi bắt đầu dùng STELARA ở những bệnh nhân có tiền sử lao tiềm ẩn hoặc lao thể hoạt động khi không thể xác định được liệu trình điều trị đầy đủ ở những bệnh nhân này. Bệnh nhân sử dụng STELARA cần được theo dõi chặt chẽ về các dấu hiệu và triệu chứng của bệnh lao thể hoạt động trong và sau khi điều trị.
Nên hướng dẫn bệnh nhân xin tư vấn bác sỹ nếu có các dấu hiệu hoặc triệu chứng gợi ý của một bệnh nhiễm khuẩn. Nếu bệnh nhân mắc một bệnh nhiễm khuẩn nghiêm trọng, cần theo dõi bệnh nhân chặt chẽ và không được dùng STELARA cho đến khi giải quyết khỏi bệnh lý nhiễm khuẩn này.
Bệnh ác tính
Các chất ức chế miễn dịch như ustekinumab có khả năng làm tăng nguy cơ mắc phải các bệnh ác tính. Một vài bệnh nhân sử dụng STELARA trong các nghiên cứu lâm sàng đã mắc phải những bệnh ác tính ở da và ở các bộ phận khác (xem phần Tác dụng ngoại ý).
Chưa có nghiên cứu nào được tiến hành trên những bệnh nhân có tiền sử mắc bệnh ác tính hoặc tiếp tục điều trị ở những bệnh nhân có dấu hiệu phát triển bệnh ác tính trong khi dùng STELARA. Vì thế, thận trọng khi sử dụng STELARA ở những bệnh nhân này.
Tất cả bệnh nhân, đặc biệt là những bệnh nhân trên 60 tuổi, những bệnh nhân có tiền sử điều trị ức chế miễn dịch kéo dài hoặc những bệnh nhân đã điều trị PUVA, nên được theo dõi dấu hiệu của ung thư da không phải u hắc tố (xem phần Tác dụng ngoại ý).
Phản ứng quá mẫn
Các phản ứng quá mẫn nghiêm trọng đã được báo cáo trong giai đoạn thuốc đã lưu hành trên thị trường, trong đó có một số trường hợp xảy ra vài ngày sau khi điều trị. Đã xuất hiện sốc phản vệ và phù mạch. Nếu như sốc phản vệ hoặc bất kỳ một phản ứng quá mẫn nghiêm trọng nào xảy ra, cần ngừng dùng STELARA và sử dụng các phương pháp điều trị thích hợp (xem phần Tác dụng ngoại ý).
Nhạy cảm với nhựa cao su
Nắp kim tiêm của bơm tiêm trong STELARA bơm tiêm chứa sẵn thuốc được sản xuất từ cao su khô thiên nhiên (một chiết xuất của nhựa cao su) có thể gây phản ứng dị ứng cho những người nhạy cảm với nhựa cao su.
Tiêm chủng
Khuyến cáo không nên dùng vaccine có chứa virus hoặc vi khuẩn còn sống (như trực khuẩn Calmette và Guérin (BCG)) cùng với STELARA. Không có các nghiên cứu chuyên biệt được tiến hành ở những bệnh nhân được chủng ngừa với vaccine virus sống hoặc vi khuẩn sống một thời gian ngắn trước đó. Chưa có dữ liệu khẳng định có nhiễm khuẩn thứ phát ở những bệnh nhân dùng vaccine sống được điều trị bằng STELARA. Trước khi tiêm chủng vaccine virus sống hoặc vi khuẩn sống, nên tạm ngừng việc điều trị với STELARA ít nhất 15 tuần sau khi dùng liều thuốc cuối cùng và có thể bắt đầu dùng lại ít nhất 2 tuần sau khi tiêm chủng. Bác sỹ kê đơn cần tham khảo tài liệu Tóm tắt đặc tính sản phẩm của vaccine cụ thể để biết thêm thông tin và hướng dẫn về sử dụng đồng thời các chất ức chế miễn dịch sau khi tiêm chủng.
Bệnh nhân có thể dùng STELARA cùng với các vaccine đã bất hoạt hoặc không sống.
Điều trị kéo dài với STELARA không cản trở đáp ứng miễn dịch dịch thể đối với polysaccharide phế cầu khuẩn hoặc vaccine uốn ván (xem phần Đặc tính dược lực học).
Liệu pháp ức chế miễn dịch đồng thời
Trong các nghiên cứu vẩy nến, vẫn chưa đánh giá được độ an toàn và tính hiệu quả khi dùng STELARA kết hợp với các chất ức chế miễn dịch bao gồm các sinh phẩm hoặc quang trị liệu. Trong các nghiên cứu viêm khớp vẩy nến, sử dụng đồng thời với MTX không ảnh hưởng đến độ an toàn hoặc hiệu quả của STELARA. Trong các nghiên cứu bệnh Crohn, sử dụng đồng thời với các chất ức chế miễn dịch hoặc corticosteroid không ảnh hưởng tới an toàn hoặc hiệu quả của STELARA. Thận trọng khi dùng kết hợp STELARA với các chất ức chế miễn dịch khác hoặc khi chuyển đổi từ các chế phẩm sinh học ức chế miễn dịch khác (xem phần Tương tác).
Liệu pháp miễn dịch
STELARA vẫn chưa được đánh giá trên những bệnh nhân đang điều trị bằng liệu pháp dị ứng miễn dịch. Chưa biết STELARA có thể ảnh hưởng đến liệu pháp dị ứng miễn dịch hay không.
Các bệnh lý da nghiêm trọng
Đã ghi nhận viêm da tróc vẩy sau khi điều trị ustekinumab ở những bệnh nhân bị bệnh vẩy nến (xem phần Tác dụng ngoại ý). Bệnh nhân bị bệnh vẩy nến thể mảng có thể phát triển thành vẩy nến đỏ da với các triệu chứng không thể phân biệt được trên lâm sàng với bệnh viêm da tróc vẩy, như là một phần của quá trình diễn biến tự nhiên của bệnh. Khi theo dõi điều trị cho bệnh nhân vẩy nến, bác sỹ nên cảnh giác với các triệu chứng của vẩy nến đỏ da hoặc viêm da tróc vẩy. Nếu những triệu chứng này xảy ra, nên tiến hành điều trị thích hợp. Nên ngừng dùng STELARA nếu nghi ngờ có phản ứng thuốc.
Những đối tượng đặc biệt
Bệnh nhân cao tuổi (≥ 65 tuổi): Không có những khác biệt tổng thể về hiệu quả hoặc tính an toàn ở bệnh nhân từ 65 tuổi trở lên đã dùng STELARA so với bệnh nhân trẻ tuổi hơn, tuy nhiên số lượng bệnh nhân từ 65 trở lên không đủ để xác định xem họ đáp ứng khác biệt so với bệnh nhân trẻ tuổi hơn hay không. Nói chung, do tỷ lệ mắc bệnh nhiễm khuẩn cao hơn ở đối tượng người cao tuổi, nên cần thận trọng khi điều trị cho người cao tuổi.
Ảnh hưởng tới việc lái xe và vận hành máy móc
STELARA không gây ảnh hưởng hoặc ảnh hưởng không đáng kể tới việc lái xe và vận hành máy móc.
Quá Liều
Tiêm tĩnh mạch đơn liều tới 6 mg/kg cân nặng đã được nghiên cứu trong các nghiên cứu lâm sàng mà không phát hiện thấy độc tính bị giới hạn bởi liều gây ra. Trong trường hợp quá liều nên theo dõi mọi dấu hiệu hoặc triệu chứng của các phản ứng bất lợi và áp dụng ngay các biện pháp điều trị triệu chứng thích hợp.
Chống chỉ định
Mẫn cảm với hoạt chất hoặc bất kỳ tá dược nào của thuốc được liệt kê trong phần Thành phần.
Các nhiễm khuẩn thể hoạt động quan trọng trên lâm sàng (như bệnh lao thể hoạt động; xem phần Cảnh báo).
Sử dụng ở phụ nữ có thai và cho con bú
Phụ nữ có khả năng sinh con: Phụ nữ có khả năng sinh con nên sử dụng các phương pháp tránh thai hiệu quả trong suốt thời gian điều trị và ít nhất 15 tuần sau khi kết thúc điều trị.
Mang thai: Không có dữ liệu đầy đủ về việc sử dụng ustekinumab ở phụ nữ có thai. Các nghiên cứu trên động vật không cho thấy các tác hại trực tiếp hoặc gián tiếp đối với việc mang thai, sự phát triển của phôi thai/thai, quá trình sinh đẻ hoặc phát triển sau sinh (xem phần Dữ liệu an toàn tiền lâm sàng). Để phòng ngừa, tốt hơn hết nên tránh sử dụng STELARA trong thai kỳ.
Cho con bú: Vẫn chưa biết rõ liệu ustekinumab có được bài tiết trong sữa người mẹ. Các nghiên cứu trên động vật đã cho thấy ustekinumab ít được bài tiết vào sữa. Vẫn chưa biết liệu ustekinumab có được hấp thu toàn thân sau khi uống sữa mẹ. Bởi vì khả năng xảy ra các phản ứng bất lợi do ustekinumab khi cho trẻ sơ sinh bú, phải quyết định ngừng cho con bú trong lúc điều trị và đến 15 tuần sau khi điều trị hoặc ngừng điều trị với STELARA khi cân nhắc lợi ích cho trẻ bú và lợi ích điều trị bằng STELARA cho người mẹ.
Khả năng sinh sản: Chưa đánh giá được tác dụng của ustekinumab lên khả năng sinh sản ở người (xem phần Dữ liệu an toàn tiền lâm sàng).
Tương tác
Không nên dùng đồng thời các vaccine sống với STELARA (xem phần Cảnh báo).
Không có các nghiên cứu tương tác thuốc nào được thực hiện ở người. Trong các phân tích dược động học theo quần thể của các nghiên cứu giai đoạn III, đã khảo sát tác dụng của các thuốc sử dụng đồng thời thường xuyên nhất ở những bệnh nhân mắc bệnh vẩy nến (bao gồm paracetamol, ibuprofen, acid acetylsalicylic, metformin, atorvastatin, levothyroxine) lên dược động học của ustekinumab. Không có dấu hiệu nào cho thấy sự tương tác với các thuốc dùng đồng thời này. Cơ sở cho phân tích này là có ít nhất 100 bệnh nhân (>5% dân số nghiên cứu) được điều trị đồng thời với các thuốc này trong ít nhất 90% thời gian nghiên cứu. Dược động học của ustekinumab không bị ảnh hưởng khi dùng cùng lúc với MTX, các NSAID, 6-mercaptopurine, azathioprine và các corticosteroid đường uống, hoặc trước đó đã sử dụng các chất kháng TNFα, ở những bệnh nhân viêm khớp vẩy nến hoặc bệnh Crohn.
Các kết quả của một nghiên cứu trong phòng thí nghiệm (in vitro) cho thấy không cần thiết phải chỉnh liều thuốc ở những bệnh nhân đang dùng kèm các chất nền của CYP450 (xem phần Đặc tính dược động học).
Trong các nghiên cứu trên bệnh vẩy nến, tính an toàn và hiệu quả của STELARA kết hợp với các chất ức chế miễn dịch, bao gồm các sinh phẩm, hoặc quang trị liệu vẫn chưa được đánh giá. Trong các nghiên cứu về viêm khớp vẩy nến, sử dụng đồng thời MTX không ảnh hưởng đến tính an toàn hoặc hiệu quả của STELARA. Trong các nghiên cứu bệnh Crohn, sử dụng đồng thời với các chất ức chế miễn dịch hoặc corticosteroid không ảnh hưởng đến an toàn hoặc hiệu quả của STELARA (xem phần Cảnh báo).
Tương kỵ
Khi không có nghiên cứu về tính tương hợp, không trộn thuốc này với các thuốc khác.
Tác dụng ngoại ý
Tóm tắt hồ sơ về tính an toàn
Các phản ứng bất lợi thường gặp nhất (>5%) trong giai đoạn có đối chứng của các nghiên cứu lâm sàng trên bệnh nhân vẩy nến người lớn, viêm khớp vẩy nến và bệnh Crohn với ustekinumab là viêm mũi họng và đau đầu. Phần lớn phản ứng đều nhẹ và không đòi hỏi phải ngừng trị liệu nghiên cứu. Các phản ứng bất lợi nghiêm trọng nhất đã được báo cáo đối với STELARA là các phản ứng quá mẫn nghiêm trọng bao gồm sốc phản vệ (xem phần Cảnh báo). Hồ sơ về tính an toàn tổng quát là như nhau trên các bệnh nhân bị vẩy nến, viêm khớp vẩy nến và bệnh Crohn.
Bảng danh sách các phản ứng bất lợi
Các dữ liệu về tính an toàn được mô tả dưới đây phản ánh việc người lớn dùng ustekinumab trong 12 nghiên cứu giai đoạn 2 và 3 trên 5.884 bệnh nhân (4.135 bệnh nhân bị bệnh vẩy nến và/hoặc viêm khớp vẩy nến và 1.749 bệnh nhân bị bệnh Crohn). Trong đó bao gồm việc sử dụng STELARA trong cả giai đoạn có đối chứng và không đối chứng của các thử nghiệm lâm sàng trong ít nhất 6 tháng hoặc 1 năm (4.105 và 2.846 bệnh nhân tương ứng bị bệnh vẩy nến, viêm khớp vẩy nến hoặc bệnh Crohn) và dùng thuốc trong ít nhất 4 hoặc 5 năm (lần lượt là 1.482 và 838 người bị bệnh vẩy nến).
Bảng 7 cung cấp danh sách các phản ứng bất lợi từ các nghiên cứu lâm sàng về bệnh nhân người lớn bị bệnh vẩy nến, viêm khớp vẩy nến và bệnh Crohn cũng như phản ứng bất lợi được báo cáo từ kinh nghiệm sau khi lưu hành. Các phản ứng bất lợi được phân loại theo nhóm hệ thống cơ quan và tần suất, bằng cách sử dụng quy ước sau đây: Rất thường gặp (≥1/10), Thường gặp (≥1/100 đến <1/10), Ít gặp (≥1/1.000 đến <1/100 ), Hiếm gặp (≥1/10.000 đến <1/1.000), Rất hiếm gặp (<1/10.000), không rõ (không thể ước lượng được từ dữ liệu có sẵn). Trong mỗi nhóm tần suất, các phản ứng bất lợi được thể hiện với thứ tự theo mức độ nghiêm trọng giảm dần.
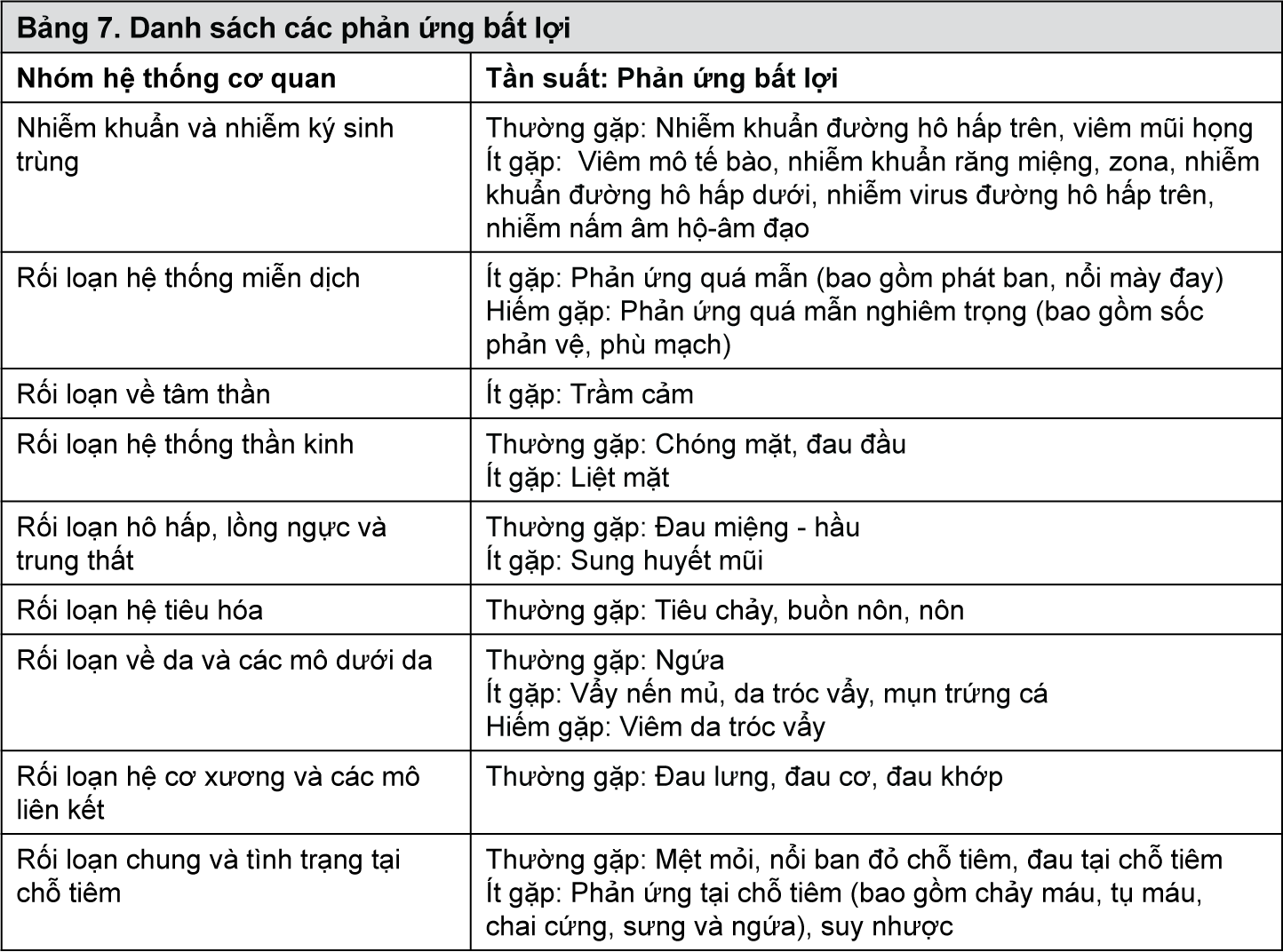
Mô tả các phản ứng bất lợi chọn lọc
Nhiễm khuẩn
Trong những nghiên cứu có đối chứng với giả dược trên bệnh nhân bị bệnh vẩy nến, viêm khớp vẩy nến và bệnh Crohn, tỷ lệ bệnh nhân bị nhiễm khuẩn hoặc nhiễm khuẩn nghiêm trọng giữa nhóm dùng ustekinumab và nhóm dùng giả dược là tương đương nhau. Ở giai đoạn có đối chứng với giả dược của các nghiên cứu lâm sàng trên những bệnh nhân vẩy nến, bệnh nhân viêm khớp vẩy nến và bệnh nhân bị bệnh Crohn, tỷ lệ mắc bệnh nhiễm khuẩn là 1,38 trên bệnh nhân-năm theo dõi ở nhóm dùng ustekinumab, và là 1,35 trên bệnh nhân-năm theo dõi ở nhóm dùng giả dược. Các bệnh nhiễm khuẩn nghiêm trọng đã xảy ra với tỷ lệ 0,03 trên bệnh nhân-năm theo dõi ở nhóm dùng ustekinumab (27 trường hợp nhiễm khuẩn nghiêm trọng trong số 829 bệnh nhân-các năm theo dõi) và tỷ lệ này cũng là 0,03 ở nhóm dùng giả dược (11 trường hợp nhiễm khuẩn nghiêm trọng trong số 385 bệnh nhân-các năm theo dõi) (xem phần Cảnh báo).
Trong các giai đoạn có đối chứng và không có đối chứng của các nghiên cứu lâm sàng trên bệnh vẩy nến, viêm khớp vẩy nến và bệnh Crohn, đã có 10.953 bệnh nhân-các-năm phơi nhiễm ở 5.884 bệnh nhân, trung vị của thời gian theo dõi là 0,99 năm; 3,2 năm cho các nghiên cứu vẩy nến; 1,0 năm cho các nghiên cứu viêm khớp vẩy nến và 0,6 năm cho các nghiên cứu bệnh Crohn. Trong nhóm điều trị với ustekinumab, tỷ lệ mắc bệnh nhiễm khuẩn là 0,91 trên bệnh nhân-năm theo dõi và tỷ lệ mắc các bệnh nhiễm khuẩn nghiêm trọng là 0,02 trên bệnh nhân-năm theo dõi (178 trường hợp nhiễm khuẩn nghiêm trọng trong số 10.953 bệnh nhân-các năm theo dõi) và các nhiễm khuẩn nghiêm trọng đã báo cáo bao gồm áp xe hậu môn, viêm mô tế bào, viêm phổi, viêm túi thừa, viêm dạ dày-ruột và nhiễm virus.
Trong các nghiên cứu lâm sàng, bệnh nhân mắc lao tiềm ẩn được điều trị đồng thời với isoniazid không phát triển thành bệnh lao.
Bệnh ác tính
Ở giai đoạn đối chứng với giả dược trong những nghiên cứu lâm sàng trên bệnh vẩy nến, viêm khớp vẩy nến và bệnh Crohn, tỷ lệ phát sinh các bệnh ác tính ngoại trừ ung thư da không phải u hắc tố là 0,12 trên 100 bệnh nhân-các-năm theo dõi ở nhóm bệnh nhân điều trị với ustekinumab (1 bệnh nhân trong số 829 bệnh nhân-các năm theo dõi) so với tỷ lệ 0,26 ở nhóm bệnh nhân dùng giả dược (1 bệnh nhân trong số 385 bệnh nhân-các-năm theo dõi). Tỷ lệ phát sinh ung thư da không phải u hắc tố là 0,48 trên 100 bệnh nhân-các năm theo dõi đối với nhóm dùng ustekinumab (4 bệnh nhân trong số 829 bệnh nhân-các năm theo dõi) so với 0,52 ở nhóm dùng giả dược (2 bệnh nhân trong số 385 bệnh nhân-các-năm theo dõi).
Trong các giai đoạn có đối chứng và không có đối chứng của các nghiên cứu lâm sàng trên bệnh vẩy nến, viêm khớp vẩy nến và bệnh Crohn, đã có 10.935 bệnh nhân-các năm phơi nhiễm ở 5.884 bệnh nhân, trung vị của thời gian theo dõi là 1,0 năm; 3,2 năm cho những nghiên cứu vẩy nến; 1,0 năm cho các nghiên cứu viêm khớp vẩy nến và 0,6 năm cho các nghiên cứu bệnh Crohn. Các bệnh ác tính ngoại trừ ung thư da không phải u hắc tố đã được báo cáo ở 58 bệnh nhân trong số 10.935 bệnh nhân-các năm theo dõi (tỷ lệ mới mắc là 0,53 trên 100 bệnh nhân-các năm theo dõi đối với nhóm bệnh nhân điều trị với ustekinumab). Tỷ lệ mới mắc những bệnh ác tính được báo cáo ở bệnh nhân dùng ustekinumab có thể so sánh tương đương với tỷ lệ mới mắc đã dự kiến ở nhóm dân số chung (tỷ lệ mới mắc được chuẩn hóa = 0,87 [khoảng tin cậy 95%: 0,66; 1,14], được điều chỉnh theo tuổi, giới tính và chủng tộc). Những bệnh ác tính thường gặp nhất, ngoại trừ ung thư da không phải u hắc tố, là ung thư tuyến tiền liệt, u hắc tố, ung thư đại trực tràng, và ung thư vú. Tỷ lệ mới mắc ung thư da không phải u hắc tố là 0,49 trên 100 bệnh nhân-các năm theo dõi đối với những bệnh nhân dùng trị liệu ustekinumab (53 bệnh nhân trong số 10.919 bệnh nhân-các năm theo dõi). Tỷ số bệnh nhân có ung thư da tế bào đáy so với ung thư tế bào vẩy (4:1) cũng tương đương với tỷ số đã dự kiến ở nhóm dân số chung (xem phần Cảnh báo).
Phản ứng quá mẫn
Trong suốt giai đoạn có đối chứng của các nghiên cứu lâm sàng trên bệnh vẩy nến và viêm khớp vẩy nến của ustekinumab, nổi ban và mày đay xảy ra với tỷ lệ <1% tổng số bệnh nhân (xem phần Cảnh báo).
Tính sinh miễn dịch
Trong các nghiên cứu lâm sàng trên bệnh vẩy nến và viêm khớp vẩy nến, chưa đến 8% bệnh nhân điều trị với ustekinumab đã tạo kháng thể kháng ustekinumab. Trong các nghiên cứu trên bệnh Crohn, chưa đến 3% bệnh nhân điều trị với ustekinumab đã tạo kháng thể kháng ustekinumab. Không thấy sự liên quan rõ ràng giữa việc sinh kháng thể kháng ustekinumab và sự phát triển các phản ứng tại nơi tiêm. Đa số bệnh nhân dương tính với kháng thể kháng ustekinumab đều có kháng thể trung hòa. Hiệu quả điều trị có xu hướng giảm ở những bệnh nhân có kháng thể kháng ustekinumab; tuy nhiên, việc sinh kháng thể đã không gây trở ngại cho đáp ứng lâm sàng.
Đối tượng trẻ em
Tác dụng không mong muốn ở trẻ em từ 12 tuổi trở lên bị vẩy nến thể mảng.
Tính an toàn của ustekinumab đã được nghiên cứu trong nghiên cứu giai đoạn 3 trên 110 bệnh nhân từ 12 đến 17 tuổi trong 60 tuần. Các tác dụng không mong muốn được báo cáo trong nghiên cứu này tương đương với các tác dụng không mong muốn ghi nhận được trong các nghiên cứu trước đây trên bệnh nhân người lớn bị vẩy nến thể mảng.
Báo cáo các phản ứng bất lợi nghi ngờ
Báo cáo các phản ứng bất lợi nghi ngờ sau khi cấp phép của một thuốc là rất quan trọng. Điều này cho phép tiếp tục kiểm soát cân bằng lợi ích/nguy cơ của thuốc. Nhân viên y tế cần báo cáo tất cả các phản ứng bất lợi nghi ngờ thông qua hệ thống báo cáo của quốc gia.
Thận trọng
Không được lắc dung dịch trong bơm tiêm chứa sẵn thuốc STELARA. Kiểm tra các vật thể lạ trong dung dịch hoặc sự biến màu của dung dịch bằng mắt thường trước khi tiêm dưới da. Dung dịch dạng trong đến vẩn sữa, từ không màu đến màu vàng nhạt và có thể chứa một vài tiểu phân protein trắng hoặc trong mờ nhỏ. Sự xuất hiện này không phải là điều bất thường đối với các dung dịch có protein. Không nên sử dụng sản phẩm nếu dung dịch bị biến màu hoặc đục, hoặc nếu có sự xuất hiện của vật thể lạ. Trước khi sử dụng, cần bảo quản STELARA trong nhiệt độ phòng (xấp xỉ nửa giờ). Hướng dẫn chi tiết được ghi trong hướng dẫn sử dụng.
STELARA không chứa chất bảo quản; vì thế lượng thuốc còn dư trong bơm tiêm không được sử dụng lại. STELARA được đóng gói trong một bơm tiêm sử dụng một lần, vô khuẩn. Không được phép tái sử dụng bơm tiêm và kim tiêm. Bất kỳ lượng thuốc không sử dụng hoặc vật liệu thải loại cần được tiêu hủy theo đúng quy định.
Bảo quản
Bảo quản trong tủ lạnh: 2ºC đến 8ºC.
Bảo quản trong hộp carton nguyên bản cho đến khi sử dụng.
Tránh ánh sáng.
Không để bị đông lạnh.
Không lắc.
Phân loại ATC
L04AC05 - ustekinumab
Trình bày/Đóng gói
Dung dịch tiêm: hộp 1 bơm tiêm chứa sẵn 0,5 mL thuốc.
- Abacavir
- Abernil
- Abiiogran
- Acarbose
- ACC
- Acebutolol
- Acenocoumarol
- Acetate Ringer's
- Acetazolamide
- Acetylcystein
- Acetylsalicylic acid
- Aciclovir
- Acid acetylsalicylic
- Acid aminocaproic
- Acid ascorbic
- Acid boric
- Acid chenodeoxycholic
- Acid ethacrynic
- Acid folic
- Acid fusidic
- Acid iopanoic
- Acid ioxaglic
- Acid nalidixic
- Acid pantothenic
- Acid para-aminobenzoic
- Acid salicylic
- Acid tranexamic
- Acid valproic
- Acid zoledronic
- Acitretin
- Aclasta
- Aclon
- Actapulgite
- Actelsar
- Actelsar HCT
- Actemra
- Actilyse
- Acular
- Acupan
- Acuvail
- Acyclovir STADA
- Acyclovir STADA Cream
- Adalat
- Adenosin
- Adenosin Ebewe
- Adipiodon
- Advagraf
- Aerius
- Afinitor
- Agicarvir
- Agifovir-E
- Agilosart
- Agilosart-H
- Agimepzol
- Agimosarid
- Agimstan
- Agimstan-H
- Agiremid
- Agivastar
- Aibezym
- Air-X
- Alaxan
- Albendazol
- Albiomin
- Albumin
- Albumin người Grifols 20%
- Albuminar
- AlbuRx
- Albutein
- Alcuronium chloride
- Aldesleukin
- Alendronat
- Alertin
- Alfa-Lipogamma 600 Oral
- Alfuzosin hydrochlorid
- Algotra
- Alimemazin
- Alimta
- Allipem
- Allopurinol
- Allopurinol STADA
- Aloxi
- Alprazolam
- Alpha Chymotrypsin
- Alpha tocopherol
- Alphachymotrypsin Glomed
- Alphagan-P
- Aluvia
- Alzental
- Amaryl
- Ambroco
- Ambroxol
- Amcinol-Paste
- Amigold
- Amikacin
- Aminocaproic acid
- Aminoleban
- Aminoleban Oral
- Aminosteril N-Hepa
- Amiparen
- Amitriptyline
- Amiyu
- Amlodipine
- Amlor
- Amoxicillin
- Amoxicillin & clavulanate
- Ampicillin
- Amquitaz
- Anaferon for children
- Anargil
- Anaropin
- Andriol Testocaps
- Anepzil
- Anyfen
- Apaisac
- Apidra SoloStar
- Apitim 5
- Aprovel
- Aquaphil
- Arcalion
- Arcoxia
- Aricept Evess
- Arimidex
- Arnetine
- Artrodar
- A-Scabs
- Ascorbic acid
- Asperlican/Candinazol
- Aspilets EC
- Aspirin
- Asthmatin
- Atelec
- Atocib 120
- Atocib 90
- Atosiban PharmIdea
- Atozet
- Attapulgite
- Atussin
- Atropin
- Augbactam
- Augmentin Sachet
- Augmentin SR
- Augmentin Tablets
- Augmex
- Avamys
- Avastin
- Avelox Dịch truyền
- Avelox Viên nén
- Avodart
- Axcel Cefaclor-125 Suspension
- Axcel Cetirizine Syrup
- Axcel Chlorpheniramine
- Axcel Dexchlorpheniramine
- Axcel Dicyclomine-S Syrup
- Axcel Diphenhydramine Paediatric Syrup
- Axcel Erythromycin ES
- Axcel Eviline
- Axcel Fungicort Cream
- Axcel Fusidic acid Cream
- Axcel Fusidic acid-B Cream
- Axcel Hydrocortisone Cream
- Axcel Lignocaine 2% Sterile Gel
- Axcel Loratadine
- Axcel Miconazole Cream
- Axcel Paracetamol
- Axcel Urea Cream
- Axitan
- Azenmarol
- Azicine
- Aziphar
- Azithromycin