Nhà sản xuất
Astellas
Thành phần
Mỗi viên: Tacrolimus 0.5mg, 1mg hoặc 5mg.
Mỗi mL: Tacrolimus 5mg.
Cơ chế tác dụng
Tacrolimus kéo dài sự sống còn của ký chủ và mảnh ghép trên mô hình động vật ghép gan, thận, tim, tủy xương, ruột non, tụy, phổi và phế quản, da, giác mạc và chi.
Ở động vật, tacrolimus đã được khẳng định làm suy giảm sự miễn dịch và, đối với các phản ứng qua trung gian tế bào như đào thải mảnh ghép, thuốc gây trì hoãn sự tăng nhạy cảm theo từng loại, viêm khớp do collagen, viêm não dị ứng trên mô hình thử nghiệm và mảnh ghép so với bệnh của người được ghép.
Tacrolimus ức chế sự hoạt hóa tế bào lympho-T mặc dù cơ chế tác động chính xác chưa được biết. Bằng chứng các thí nghiệm cho rằng tacrolimus gắn kết với protein nội bào, FKBP-12. Sau đó tạo thành phức hợp tacrolimus FKBP-12 calcium, calmodulin và calcineurin và hoạt tính men phosphatase của calcineurin bị ức chế. Tác động này ngăn chặn sự dephosphoryl hóa và sự di chuyển nhân tố thuộc nhân tế bào T được hoạt hóa (NF-AT); cấu thành nhân thông qua khởi xướng sự sao chép gen cho việc hình thành lymphokines (như là interleukin-2, gamma-interferon). Kết quả cuối cùng là ức chế sự hoạt hóa tế bào lympho-T (ức chế miễn dịch).
Dược động học
Hoạt tính của tacrolimus chủ yếu do phân tử mẹ. Dược động học của tacrolimus được xác định sau khi chỉ định tiêm tĩnh mạch và đường uống ở người tình nguyện khoẻ mạnh, bệnh nhân ghép gan và ghép thận (xem bảng bên dưới).
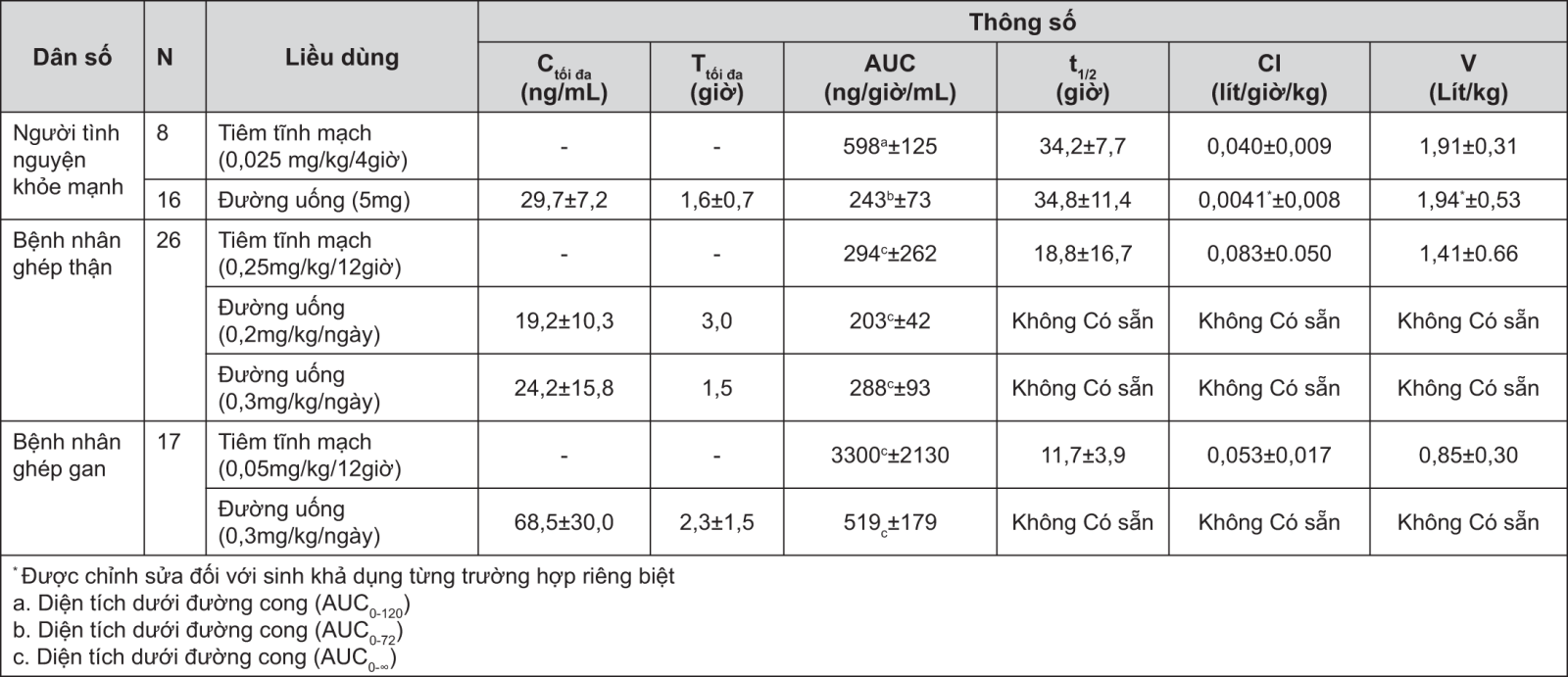
Do sự đa dạng của các đối tượng đang nghiên cứu về dược động học của tacrolimus, nên rất cần thiết xác định rõ phác đồ liều cho điều trị tối ưu. Dữ liệu về dược động học chỉ ra rằng toàn bộ nồng độ trong máu được xem như mẫu thích hợp hơn nồng độ trong huyết thanh để mô tả dược động học của tacrolimus.
Hấp thu:
Sau khi chỉ định uống, sự hấp thụ tacrolimus ở đường tiêu hóa không hoàn toàn và biến thiên. Sinh khả dụng tuyệt đối của tacrolimus là 17±10% ở bệnh nhân ghép thận trưởng thành (N=25); là 22±6% ở bệnh nhân ghép gan trưởng thành (N=17) và là 18±5% ở người khỏe mạnh (N=15).
Nghiên cứu liều đơn được dẫn dắt trên 32 người tình nguyện khỏe mạnh đánh giá độ tương đồng của viên nang 1mg và 5mg. Nồng độ đỉnh trong máu của tacrolimus và diện tích dưới đường cong (AUC) dường như gia tăng theo kiểu tỉ lệ với liều dùng trên 18 người tình nguyện khỏe mạnh nhận liều uống đơn 3,7 và 10mg.
Trên 18 bệnh nhân ghép thận, nồng độ tacrolimus thấp nhất từ 3 đến 30ng/ml được tính lúc 10-12 giờ sau khi uống tương quan với diện tích dưới đường cong (hệ số tương liên: 0,93). Trên 24 bệnh nhân ghép gan, toàn bộ dãy nồng độ là 10-60ng/ml, hệ số tương liên là 0,94.
Ảnh hưởng của thức ăn: tốc độ và phạm vi của sự hấp thu tacrolimus cao nhất trong điều kiện lúc bụng đói. Sự hiện diện của thức ăn và thành phần thức ăn làm giảm tốc độ và phạm vi của sự hấp thu tacrolimus được quan sát đối với 15 người tình nguyện khỏe mạnh.
Ảnh hưởng này được nhìn thấy rõ rệt ở bữa ăn nhiều chất béo (848 kcal, 46% chất béo): diện tích trung bình dưới đường cong giảm 37% và nồng độ đỉnh giảm 77%; thời gian đạt nồng độ đỉnh kéo dài gấp 5 lần. Bữa ăn có nhiều hydrate carbon (668 kcal, 85% hydrate carbon) làm giảm diện tích dưới đường cong 28% và giảm nồng độ đỉnh trung bình 65%.
Trên người tình nguyện khỏe mạnh (N=16), thời gian dùng bữa ăn cũng ảnh hưởng sinh khả dụng của tacrolimus. Khi cho dùng thuốc ngay sau bữa ăn, nồng độ thuốc tối đa giảm 71% và diện tích trung bình dưới đường cong giảm 39% so với điều kiện lúc bụng đói. Khi dùng thuốc 1,5 giờ sau bữa ăn, nồng độ thuốc tối đa trung bình giảm 63% và diện tích trung bình dưới đường cong giảm 39% so với điều kiện lúc bụng đói.
Trên 11 bệnh nhân ghép gan, Prograf được chỉ định 15 phút sau bữa sáng có nhiều chất béo (40 kcal, 34% chất béo), kết quả diện tích dưới đường cong giảm 27±18% và nồng độ thuốc tối đa giảm (50±19%), được so với điều kiện lúc bụng đói.
Phân bố:
Sự gắn kết protein huyết thanh là khoảng 99% và độc lập với nồng độ trên khoảng 5-50 ng/ml.
Tacrolimus gắn kết chủ yếu với albumin và alpha-1 acid glycoprotein và có mức liên kết cao với hồng cầu. Sự phân bố tacrolimus giữa trong máu toàn phần và huyết thanh phụ thuộc vào nhiều yếu tố như là hematocrit, nhiệt độ ở thời gian phân tách huyết thanh, nồng độ thuốc và nồng độ protein huyết thanh. Trong 1 nghiên cứu ở Mỹ, tỉ lệ nồng độ thuốc trong máu toàn phần và trong huyết thanh khoảng trung bình 35 (12-67).
Chuyển hóa:
Tacrolimus được chuyển hóa hoàn toàn bởi hệ thống oxy hóa chức năng hỗn hợp, chủ yếu hệ thống cytochrome P-450 (CYP3A). Con đường chuyển hóa dẫn đến có thể hình thành 8 chất chuyển hóa. Quá trình demethyl hóa và hydroxyl hóa được nhận định là cơ chế chủ yếu của sự chuyển giao sinh học in vitro. Chất chuyển hóa chủ yếu được nhận định trong môi trường ủ với men microsome gan người là 13-demethyl tacrolimus. Trong nghiên cứu in vitro, chất chuyển hóa 31-demethyl đã được báo cáo có cùng hoạt tính như tacrolimus.
Bài tiết:
Độ thanh thải trung bình của tacrolimus sau khi dùng đường tĩnh mạch là 0,04 lít/giờ/kg trên người khỏe mạnh, 0,083 lít/giờ/kg trên bệnh nhân ghép thận trưởng thành và 0,053 lít/giờ/kg trên bệnh nhân ghép gan trưởng thành. Ở người, < 1% liều uống được bài tiết ở dạng không thay đổi qua nước tiểu.
Trong một nghiên cứu rộng rãi về tacrolimus được đánh dấu phóng xạ dùng đường tĩnh mạch trên 6 người tình nguyện khỏe mạnh, chất đánh dấu phóng xạ được tìm thấy lại là 77,8%±12,7%. Sự thải trừ qua phân khoảng 92,4±1% và thời gian bán hủy thải trừ dựa vào hoạt tính phóng xạ là 48,1±15,9 giờ trong khi dựa vào nồng độ tacrolimus là 43,5±11,6 giờ. Độ thanh thải trung bình của chất đánh dấu phóng xạ là 0,029±0,015 lít/giờ/kg và của tacrolimus là 0,029±0,009 lít/giờ/kg. Khi chỉ định đường uống, nồng độ chất đánh dấu phóng xạ trung bình được tìm thấy lại là 94,9±30,7%. Sự đào thải qua phân khoảng 92,6±30,7%, qua nước tiểu là 2,3±1,1% và thời gian bán hủy thải trừ dựa vào hoạt tính phóng xạ là 31,9±10,5 giờ trong khi dựa vào nồng độ tacrolimus là 48,4±12,3 giờ. Độ thanh thải trung bình của chất đánh dấu phóng xạ là 0,226±0,116 lít/giờ/kg và của tacrolimus là 0,172±0,088 lít/giờ/kg.
Dân số đặc biệt
Trẻ em:
Dược động học của tacrolimus đã được nghiên cứu trên bệnh nhân ghép gan ở độ tuổi 0,7 đến 13,2 tuổi. Sau khi dùng liều 0,037 mg/kg/ngày bằng đường tĩnh mạch trên 12 bệnh nhi, thời gian bán hủy tận cùng trung bình là 11,5±3,8 giờ, thể tích phân bố là 2,6±2,1 lít/kg và độ thanh thải là 0,138±0,071 lít/giờ/kg.
Sau khi chỉ định đường uống trên 9 bệnh nhi, diện tích đưới đường cong trung bình là 337±167ng.giờ/ml và nồng độ thuốc tối đa là 43,4±27,9ng/ml. Sinh khả dụng tuyệt đối là 31±21%.
Nồng độ trong máu toàn phần tối thiểu trong 31 bệnh nhi < 12 tuổi cho thấy bệnh nhi cần liều cao hơn người lớn để đạt nồng độ thuốc tối thiểu tương đương (xem Liều và chỉ định).
Suy thận và suy gan:
Thông số dược động học trung bình của tacrolimus sau khi dùng liều đơn trên bệnh nhân suy thận và suy gan được mô tả trong bảng bên dưới:
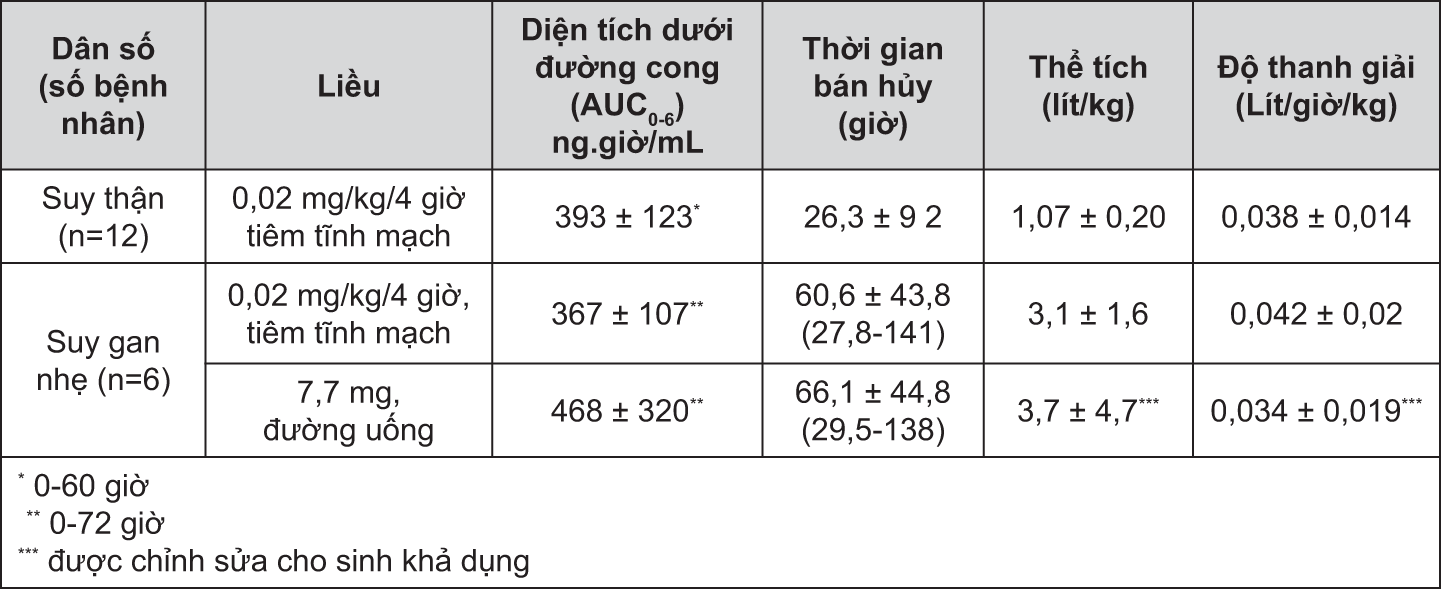
Suy thận:
Dược động học tacrolimus sau khi dùng đường tĩnh mạch liều đơn được xác định trên 12 bệnh nhân (7 bệnh nhân không lọc máu, creatinin huyết thanh: 3,9± 1,6 và 5 bệnh nhân lọc máu creatinin huyết thanh 12,0±2,4mg/dl) trước khi ghép thận. Thông số dược động học đạt được tương tự ở cả 2 nhóm.
Độ thanh thải trung bình của tacrolimus trên bệnh nhân rối loạn chức năng thận thì tương tự như trên người tình nguyện khoẻ mạnh (xem bảng ở trên).
Suy gan:
Dược động học tacrolimus đã được xác định trên 6 bệnh nhân rối loạn chức năng gan nhẹ (điểm Pugh trung bình: 6,2) sau khi dùng liều đơn đường tĩnh mạch và đường uống. Độ thanh thải trung bình ở bệnh nhân rối loạn chức năng gan nhẹ không khác biệt đáng kể so với người tình nguyện khoẻ mạnh (xem bảng trên).
Chủng tộc:
Một nghiên cứu chính thức đánh giá sự phân bố dược động học của tacrolimus trên bệnh nhân da đen đòi hỏi liều cao tacrolimus để đạt được nồng độ tối thiểu tương đương.
Giới:
Ảnh hưởng giới tính trên dược động học chưa được đánh giá, tuy nhiên không có sự khác biệt về liều bởi giới tính trong các nghiên cứu ghép thận.
NGHIÊN CỨU LÂM SÀNG
Trường hợp ghép gan
Tính an toàn và hiệu quả ức chế miễn dịch của Prograf sau khi ghép gan được đánh giá trong hai nghiên cứu viễn cảnh, đa trung tâm, không mù, ngẫu nhiên. Nhóm đối chứng tích cực được điều trị bằng chất ức chế miễn dịch cyclosporin. Cả hai nghiên cứu đều sử dụng đồng thời corticoid thượng thận như một phần của phác đồ thuốc ức chế miễn dịch. Những nghiên cứu này được hoạch định để đánh giá xem cả hai chế độ điều trị có tương đương về mặt trị liệu hay không, về sự sống sót của bệnh nhân và mô ghép tại thời điểm 12 tháng sau khi ghép, được xem là điểm giới hạn đánh giá đầu tiên. Phác đồ sử dụng thuốc ức chế miễn dịch Prograf được tìm thấy là có giá trị tương đương với phác đồ dùng thuốc ức chế miễn dịch cyclosporin.
Trong một thử nghiệm, 529 bệnh nhân được tuyển chọn tại 12 cơ sở lâm sàng ở Hoa Kỳ; trước khi phẫu thuật 263 bệnh nhân được chọn ngẫu nhiên vào phác đồ điều trị sử dụng chất ức chế miễn dịch Prograf và 266 bệnh nhân vào nhóm có phác đồ điều trị ức chế miễn dịch với cyclosporin (CBIR). 10 trong 12 cơ sở lâm sàng này sử dụng cùng một protocol CBIR, trong khi 2 cơ sở còn lại dùng các protocol kiểm chứng khác nhau. Thử nghiệm này không bao gồm những bệnh nhân rối loạn chức năng thận, suy gan bạo phát với bệnh não giai đoạn IV, và ung thư; những bệnh nhân nhi (<12 tuổi) được phép tham gia.
Trong thử nghiệm thứ hai, 545 bệnh nhân được tuyển chọn tại 8 cơ sở lâm sàng ở Châu Âu; trước khi phẫu thuật 270 bệnh nhân được chọn ngẫu nhiên vào phác đồ điều trị sử dụng chất ức chế miễn dịch Prograf và 275 bệnh nhân vào nhóm CBIR. Trong nghiên cứu này, mỗi trung tâm sử dụng phác đồ CBIR tiêu chuẩn cơ sở trong kiểm chứng tích cực. Thử nghiệm này không bao gồm bệnh nhân nhi, nhưng cho phép tuyển chọn những bệnh nhân rối loạn chức năng thận, suy gan bạo phát với bệnh não giai đoạn IV, và ung thư ngoại trừ ung thư gan di căn.
Trong cả hai nghiên cứu, sự sống còn của mô ghép và của bệnh nhân một năm trong nhóm điều trị bằng Prograf thì tương đương với nhóm điều trị CBIR. Số bệnh nhân sống sót sau một năm tổng cộng (của nhóm điều trị bằng Prograf và nhóm CBIR) là 88% trong nghiên cứu ở Hoa Kỳ và 78% trong nghiên cứu ở châu Âu. Số cơ quan ghép tồn tại sau một năm (của nhóm điều trị bằng Prograf và nhóm CBIR) là 81% trong nghiên cứu ở Hoa Kỳ và 73% trong nghiên cứu ở Châu Âu. Trong cả hai nghiên cứu thời gian trung bình để chuyển từ đường tiêm tĩnh mạch sang Prograf uống là 2 ngày. Do bản chất của hoạch định nghiên cứu, việc so sánh sự khác nhau ở điểm giới hạn đánh giá thứ hai, như tỉ lệ thải ghép cấp tính, sự thải ghép chống kháng hay việc sử dụng OKT*3 cho trường hợp thải ghép đề kháng steroid không thể thực hiện với kết quả đáng tin cậy.
Trường hợp ghép thận
Sự ức chế miễn dịch bằng Prograf sau khi ghép thận được đánh giá trong nghiên cứu viễn cảnh, không mù, đa trung tâm, ngẫu nhiên. Có 412 bệnh nhân ghép thận được tuyển chọn tại 19 cơ sở lâm sàng ở Hoa Kỳ. Việc điều trị nghiên cứu được khởi đầu khi chức năng thận ổn định, chỉ thị bằng trị số creatinin huyết thanh dưới hoặc bằng 4mg/dL (trung bình của 4 ngày sau khi ghép, trong khoảng từ 1 đến 14 ngày). Không bao gồm những bệnh nhân dưới 6 tuổi.
Có 205 bệnh nhân được điều trị ngẫu nhiên với chất ức chế miễn dịch Prograf và 207 bệnh nhân được điều trị ngẫu nhiên với cyclosporin. Tất cả bệnh nhân đều được điều trị cảm ứng phòng ngừa bao gồm chế phẩm kháng thể kháng lymphocyte, corticoid và azathioprine. Số bệnh nhân và cơ quan ghép sống sót sau một năm thì tương đương nhau và lần lượt là 96,1% và 89,6% ở cả hai cách điều trị.
Do bản chất của hoạch định nghiên cứu, việc so sánh sự khác nhau ở điểm giới hạn đánh giá thứ hai, như là tỉ lệ thải ghép cấp tính, sự thải ghép chống kháng hay việc sử dụng OKT*3 cho trường hợp thải ghép đề kháng steroid không thể được thực hiện với kết quả đáng tin cậy.
Chỉ định/Công dụng
Prograf được chỉ định phòng ngừa sự đào thải cơ quan ghép ở bệnh nhân ghép thận hoặc gan dị sinh.
Người ta đề nghị nên sử dụng Prograf đồng thời với corticosteroid thượng thận. Do nguy cơ quá mẫn, việc tiêm Prograf nên dành cho trường hợp bệnh nhân không thể sử dụng bằng đường uống viên nang Prograf.
Liều lượng & Cách dùng
Prograf tiêm (Tacrolimus tiêm)
Chỉ đối với dung dịch tiêm truyền tĩnh mạch
Chú ý: Phản ứng quá mẫn xảy ra với thuốc tiêm sử dụng dẫn xuất của dầu thầu dầu. Xem phần Khuyến cáo.
Những bệnh nhân không dùng được viên nang Prograf có thề khởi đầu điều trị bằng Prograf tiêm. Liều Prograf đầu tiên nên dùng ngay trong 6 giờ đầu sau khi ghép tạng. Prograf tiêm nên được dùng với liều khởi đầu là 0,03-0,05mg/kg/ngày theo đường truyền tĩnh mạch. Người trưởng thành nên dùng liều ở mức thấp nhất ở khoảng liều trên. Nên sử dụng liệu pháp corticoide đồng thời ngay sau khi ghép tạng. Tiếp tục truyền tĩnh mạch Prograf tiêm đến khi bệnh nhân có thể uống được Prograf dạng viên nang.
Chế phẩm/Độ ổn định
Prograf tiêm phải được pha loãng bằng dịch truyền NaCl 0,9% hoặc dextrose 5% để được nồng độ 0,004 mg/ml và 0,02 mg/ml trước khi sử dụng. Dịch truyền đã pha loãng được đựng trong chai thủy tinh hoặc polyethylene và nên được hủy sau 24 giờ. Dịch truyền đã pha loãng không nên bảo quản trong lọ chứa PVC vì làm giảm độ ổn định và có khả năng thôi Phthalate. Trong trường hợp dịch truyền được pha loãng nhiều hơn (như trong trường hợp dùng cho bệnh nhân nhi…), những vật liệu không chứa PVC dạng ống nên hạn chế sử dụng để giảm thiểu khả năng thuốc bị thấm một cách đáng kể vào thành ống. Các chế phẩm không dùng theo đường uống nên được kiểm tra bằng mắt về độ đục hoặc sự mất màu trước khi sử dụng, kể cả dung dịch và dụng cụ chứa. Do Tacrolimus không ổn định về mặt hóa học trong môi trường kiềm trung tính, Prograf tiêm không nên hoà lẫn hoặc pha cùng với dung dịch có pH bằng 9 hoặc lớn hơn (VD: ganciclovir, acyclovir).
Viên nang Prograf (viên nang tacrolimus)
Tóm tắt liều khởi đầu và nồng độ tối thiểu trong máu toàn phần đặc trưng:
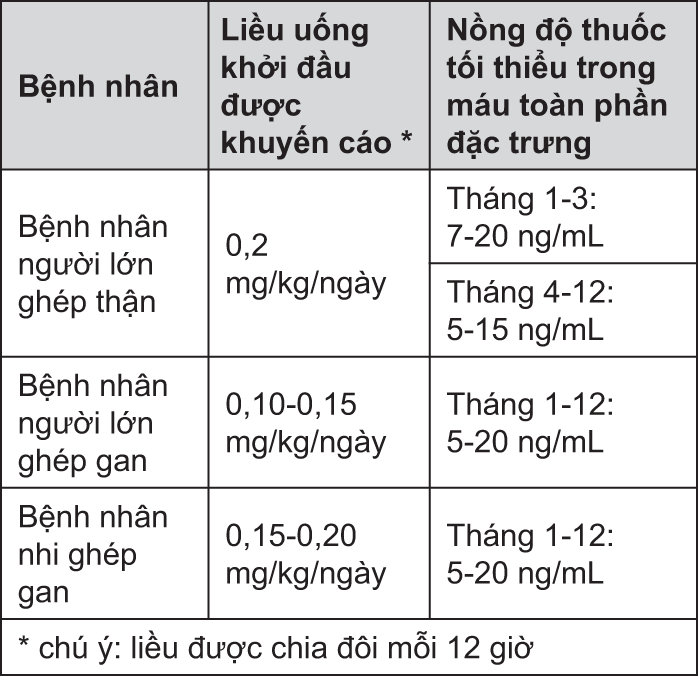
Bệnh nhân ghép gan
Bệnh nhân được khuyến cáo trị liệu khởi đầu bằng đường uống với viên nang Prograf nếu có thể. Nếu cần thiết trị liệu tiêm tĩnh mạch, nên chuyển đổi từ tiêm tĩnh mạch sang uống ngay khi trị liệu đường uống có thể dung nạp. Điều này xảy ra trong vòng 2-3 ngày. Liều khởi đầu của Prograf nên được chỉ định không sớm hơn 6 giờ sau khi ghép. Ở bệnh nhân truyền tĩnh mạch, liều uống đầu tiên nên cho lúc 8-12 giờ sau khi ngưng truyền tĩnh mạch. Liều uống khởi đầu của viên nang Prograf là 0,10-0,15 mg/kg/ngày được chia thành 2 lần cách nhau 12 giờ mỗi ngày. Uống cùng lúc với nước bưởi có thể làm gia tăng nồng độ tối thiểu của tacrolimus trong máu toàn phần đặc trưng ở bệnh nhân ghép gan (xem phần các thuốc có thể làm thay đổi nồng độ Tacrolimus).
Chuẩn liều nên dựa vào đánh giá lâm sàng sự đào thải hay dung nạp cơ quan ghép. Liều thấp của Prograf có lẽ thích hợp cho điều trị duy trì. Điều trị hỗ trợ với corticosteroide thượng thận nên sử dụng sớm sau khi ghép cơ quan. Liều và nồng độ tacrolimus tối thiểu trong máu toàn phần đặc trưng được chỉ ra bảng trên. Các chi tiết về nồng độ trong máu được mô tả trong bảng kiểm tra nồng độ máu ở bệnh nhân ghép gan bên dưới.
Bệnh nhân ghép thận
Liều uống khởi đầu được khuyến cáo dùng là 0,2 mg/kg/ngày, chia thành 2 lần cách nhau 12 giờ. Liều khởi đầu của Prograf nên được dùng trong vòng 24 giờ sau khi ghép, nhưng nên được trì hoãn cho đến khi chức năng thận hồi phục (như được chỉ ra trong ví dụ là nồng độ creatinine trong huyết thanh là ≤ 4mg/dl). Bệnh nhân da đen đòi hỏi liều cao hơn để đạt được nồng độ trong máu tương đương. Liều và nồng độ tacrolimus tối thiểu trong máu toàn phần đặc trưng được chỉ ra ở bảng trên. Các chi tiết về nồng độ trong máu được mô tả trong bảng kiểm tra nồng độ máu ở bệnh nhân ghép thận bên dưới.
Dữ liệu về bệnh nhân ghép thận cho thấy bệnh nhân da đen đòi hỏi liều cao hơn để đạt được nồng độ tối thiểu tương đương so với bệnh nhân da trắng.
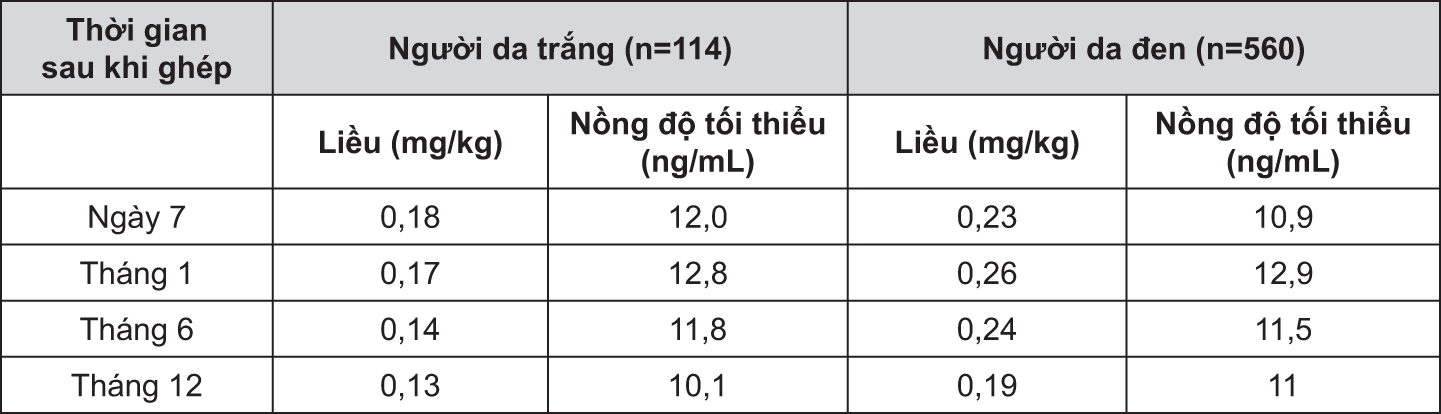
Bệnh nhân nhi
Bệnh nhân nhi ghép gan không bị rối loạn gan hay thận trước đó có nhu cầu và khả năng uống liều cao hơn người lớn để đạt được nồng độ trong máu tương đương. Vì vậy, ở bệnh nhân nhi được khuyến cáo nên khởi đầu ở liều bắt đầu tiêm tĩnh mạch là 0,03-0,05 mg/kg/ngày và liều bắt đầu đường uống là 0,15-0,20mg/kg/ngày. Nên điều chỉnh liều. Kinh nghiệm sử dụng ở bệnh nhân nhi ghép thận còn hạn chế.
Bệnh nhân rối loạn chức năng gan và thận
Do có khả năng gây độc tính thận, bệnh nhân suy thận hoặc gan nên nhận liều điều trị ở mức thấp nhất của khoảng liều đề nghị cho phép đường uống hay đường tiêm tĩnh mạch. Đôi lúc đòi hỏi giảm liều thấp hơn khoảng liều đề nghị. Điều trị Prograf thường nên trì hoãn đến 48 giờ hoặc lâu hơn ở bệnh nhân bị tiểu ít sau phẫu thuật.
Chuyển đổi từ một phác đồ thuốc suy giảm miễn dịch này sang thuốc khác
Prograf không nên được dùng cùng lúc với cyclosporine. Prograf hoặc cyclosporine nên được ngưng ít nhất 2 giờ trước khi bắt đầu thuốc khác. Khi sự hiện diện nồng độ Prograf hoặc cyclosporine tăng cao, nên trì hoãn thêm liều của các thuốc khác.
Giám sát nồng độ máu:
Giám sát nồng độ tacrolimus trong máu kết hợp với các thông số xét nghiệm về lâm sàng khác được xem xét như là công cụ chủ yếu để quản lý bệnh nhân nhằm đánh giá sự thải ghép, độc tính, điều chỉnh liều và sự tương thích. Các yếu tố ảnh hưởng tần xuất giám sát bao gồm không bị giới hạn đối với rối loạn chức năng gan hoặc thận, thêm hoặc ngưng các thuốc có khả năng tương tác và thời gian hậu ghép. Giám sát nồng độ máu không phải là cách thay thế cho giám sát chức năng gan và thận và sinh thiết mô.
Hai phương pháp được sử dụng để định lượng tacrolimus, miễn dịch định lượng enzyme vi tiểu phân (MEIA) và test ELISA. Cả 2 phương pháp có cùng kháng thể đơn dòng đối với tacrolimus. So sánh nồng độ dựa trên các tài liệu đã được công bố và nồng độ của bệnh nhân dùng các phép định lượng hiện tại phải được làm bởi những người có kiến thức chi tiết về phương pháp định lượng và thiết bị sinh học. Máu toàn phần là chất nền lựa chọn và mẫu máu nên được thu thập vào ống nghiệm đang chứa chất kháng đông ethylene diamine tetraacetic acid (EDTA). Chất kháng đông heparin không được khuyến cáo sử dụng vì có khuynh hướng hình thành các cục máu khi lưu trữ. Mẫu máu chưa được phân tích ngay lập tức nên được lưu trữ ở nhiệt độ phòng hoặc trong tủ lạnh và nên định lượng trong vòng 7 ngày. Nếu mẫu máu được giữ lâu hơn thì phải được làm đông ở nhiệt độ 20oC lên đến 12 tháng.
Ghép gan
Mặc dầu còn thiếu mối liên quan trực tiếp giữa nồng độ tacrolimus và hiệu quả của thuốc, dữ liệu từ nghiên cứu pha III và pha IV trên bệnh nhân ghép gan đã chứng tỏ có sự gia tăng tần suất tác động ngoại ý với nồng độ tối thiểu của thuốc trong máu. Hầu hết bệnh nhân ổn định khi nồng độ tối thiểu trong máu toàn phần được duy trì khoảng 5-20ng/ml. Bệnh nhân hậu ghép lâu dài thường duy trì ở liều thấp của khoảng liều đề nghị.
Dữ liệu từ nghiên cứu lâm sàng ở Mỹ chứng tỏ cho thấy nồng độ tacrolimus trong máu toàn phần, được đo bằng test ELISA, thì biến thiên trong suốt tuần đầu hậu ghép. Sau giai đoạn sớm này, nồng độ thuốc tối thiểu trung bình, đo ở khởi điểm từ tuần thứ 2 đến 1 năm hậu ghép, trong khoảng 9,8ng/ml đến 19,4 ng/ml.
Trong tài liệu “Giám sát thuốc điều trị, 1995, Vol 17, số 6 có 1 phần tham khảo và nhiều trang đề cập đến giám sát điều trị tacrolimus từ hội thảo thế giới về thống nhất cách điều trị thuốc ức chế miễn dịch. Tham khảo bản thảo này cho thảo luận thêm về giám sát tacrolimus.
Ghép thận
Dữ liệu từ nghiên cứu ở Mỹ chỉ ra rằng nồng độ tối thiểu của tacrolimus trong máu toàn phần, được đo lường bằng máy IMX, hầu như rất biến thiên trong suốt tuần đầu dùng thuốc. Trong suốt 3 tháng đầu tiên, 80% bệnh nhân duy trì nồng độ tối thiểu khoảng 7-20 ng/ml và khoảng 1 năm sau đó là 5-15ng/ml.
Nguy cơ tương đối về độc tính gia tăng theo nồng độ thuốc tối thiểu nhất. Do đó, giám sát nồng độ thuốc tối thiểu trong máu toàn phần được đề nghị để trợ giúp cho việc đánh giá lâm sàng về độc tính.
Thận trọng lúc dùng
Gia tăng sự nhạy cảm đối với việc nhiễm và có thể phát triển u lympho xảy ra từ sự suy giảm miễn dịch. Chỉ duy nhất bác sĩ có kinh nghiệm trong điều trị suy giảm miễn dịch và quản lý bệnh nhân ghép tạng được kê toa Prograf. Bệnh nhân dùng Prograf nên được quản lý bởi cơ sở được trang bị và bố trí phòng xét nghiệm và các hỗ trợ y khoa đầy đủ. Bác sĩ chịu trách nhiệm cho việc điều trị duy trì nên có thông tin đầy đủ cần thiết để theo dõi bệnh nhân.
Chung
Cao huyết áp là tác dụng phụ phổ biến khi dùng Prograf (xem TÁC DỤNG NGOẠI Ý).
Cao huyết áp nhẹ đến trung bình thường gặp hơn cao huyết áp nặng. Nên điều trị cao huyết áp. Huyết áp có thể được kiểm soát bởi các thuốc điều trị cao huyết áp thông thường. Vì tacrolimus có thể gây tăng kali huyết, do đó nên tránh dùng thuốc lợi tiểu tiết kiệm kali. Các thuốc chẹn kênh canxi điều trị hiệu quả việc tăng huyết áp do Prograf, nhưng nên thận trọng bởi vì cần giảm liều do sự tương tác với chuyển hóa tacrolimus (xem TƯƠNG TÁC THUỐC).
Bệnh nhân suy thận và suy gan
Đối với bệnh nhân suy thận, một vài bằng chứng cho thấy nên sử dụng liều thấp hơn (xem LIỀU LƯỢNG VÀ CÁCH DÙNG và CHỈ ĐỊNH). Việc sử dụng Prograf ở bệnh nhân ghép gan bị suy gan hậu ghép có thể liên kết với nguy cơ phát triển suy thận gia tăng liên quan đến nồng độ tarcolimus trong máu toàn phần cao. Những bệnh nhân này nên được giám sát chặt chẽ và nên xem xét việc chỉnh liều. Vài chứng cứ đề nghị rằng nên sử dụng liều thấp hơn trên những bệnh nhân này (xem LIỀU LƯỢNG VÀ CÁCH DÙNG và CHỈ ĐỊNH).
Phì đại cơ tim
Phì đại cơ tim đã được báo cáo có liên quan đến chỉ định Prograf và thường được biểu hiện bởi chụp vang siêu âm tim chứng tỏ có sự gia tăng thành tâm thất trái sau theo kiểu đồng tâm và dày vách ngăn nội tâm thất. Phù đã được quan sát trên trẻ sơ sinh, trẻ em và người trưởng thành. Hiện tượng này có thể được hoán đổi trong hầu hết trường hợp sau khi giảm liều hoặc ngưng điều trị. Trong một nhóm 20 bệnh nhân với chụp vang siêu âm tim trước và sau điều trị chứng tỏ có phì đại cơ tim, nồng độ trung bình tacrolimus trong máu toàn phần trong suốt thời gian trước khi chẩn đoán là phì đại cơ tim trong khoảng từ 11-53ng/ml ở trẻ sơ sinh (n=10, tuổi: 0,4-2năm), từ 4-46ng/ml ở trẻ em (n=7, tuổi: 2-15) và 11-24ng/ml ở người lớn (n=3, tuổi: 37-53).
Ở bệnh nhân phát triển suy thận hoặc biểu lộ trên lâm sàng rối loạn tâm thất trong lúc nhận điều trị Prograf, nên xem xét đánh giá chụp vang siêu âm tim. Nếu đã chẩn đoán là phì đại cơ tim, nên giảm liều hoặc ngưng điều trị Prograf.
Thông tin cho bệnh nhân
Bệnh nhân nên được thông báo về sự cần thiết phải làm lặp lại các xét nghiệm thích hợp trong khi dùng Prograf. Bệnh nhân nên được chỉ dẫn kỹ về liều dùng, tham vấn về nguy cơ rủi ro trong suốt thai kỳ, và được thông báo về nguy cơ gia tăng u tân sinh. Bệnh nhân nên được thông báo là không được thay đổi liều trước khi tham vấn bác sĩ.
Bệnh nhân nên được thông báo rằng Prograf có thể gây tiểu đường và nên được khuyên là cần gặp bác sĩ nếu như thấy tăng tần suất đi tiểu, gia tăng thèm khát hoặc đói.
Các xét nghiệm
Creatinine, kali, glucose huyết lúc đói nên được đánh giá thường xuyên, nên thực hiện việc giám sát thường qui sự chuyển hóa và hệ huyết học để bảo đảm về mặt lâm sàng.
Bệnh nhân nhi
Kinh nghiệm về Prograf ở bệnh nhân nhi ghép thận còn hạn chế. Sự ghép gan thành công đã được thực hiện ở những bệnh nhân nhi (đến 16 tuổi) sử dụng Prograf. Hai thử nghiệm đối chứng tích cực ngẫu nhiên của Prograf trong ghép gan bao gồm 56 bệnh nhân nhi. 31 bệnh nhân được điều trị ngẫu nhiên bằng Prograf so với 25 bệnh nhân điều trị ngẫu nhiên bằng cyclosporin. Ngoài ra một lượng tối thiểu trong 122 bệnh nhân nhi được nghiên cứu trong một thử nghiệm không đối chứng của tacrolimus về sự sống liên quan đến người cho gan ghép.
Những bệnh nhân nhi nói chung cần các liều cao hơn của Prograf để duy trì nồng độ tối thiểu của tacrolimus trong máu tương tự như ở bệnh nhân người lớn (xem LIỀU LƯỢNG VÀ CÁCH DÙNG).
Tác động của thuốc khi lái xe và vận hành máy móc:
Prograf có liên quan đến rối loạn thị giác và thần kinh. Những bệnh nhân đang điều trị bằng Prograf nếu có các rối loạn trên không nên lái xe hoặc vận hành các máy móc nguy hiểm. Những tác động này có thể tăng lên nếu Prograf được uống cùng với rượu.
Khả năng sinh ung thư, đột biến gen và suy giảm khả năng thụ tinh
Khả năng gia tăng bệnh ác tính là một biến chứng được thừa nhận của sự ức chế miễn dịch ở người nhận cơ quan ghép. Dạng ung thư phổ biến nhất là bệnh u lympho non-Hodgkin và ung thư da. Như với các liệu pháp ức chế miễn dịch khác, nguy cơ ác tính ở người nhận ghép sử dụng Prograf có thể cao hơn so với trong dân số bình thường, khỏe mạnh. Các rối loạn tăng sản lympho đi kèm với nhiễm virus Epstein-Barr đã được quan sát thấy. Có báo cáo cho rằng sự giảm hoặc ngưng điều trị ức chế miễn dịch có thể làm giảm thương tổn.
Không có bằng chứng về độc tính trên gen được tìm thấy ở vi khuẩn (Salmonella và E coli) hoặc ở loài hữu nhũ (tế bào phổi chuột túi Trung Quốc) trong thử nghiệm khả năng gây đột biến in vitro, trong thử nghiệm khả năng gây đột biến CHO/HGPRT in vitro, hoặc trong thử nghiệm khả năng biến đổi gen invivo thực hiện ở chuột; tacrolimus không gây ra sự tổng hợp ADN lạ ở tế bào gan loài gặm nhấm.
Những nghiên cứu về khả năng sinh ung thư được thực hiện ở chuột cống và chuột nhắt đực và cái. Trong nghiên cứu trên chuột nhắt 80 tuần và nghiên cứu trên chuột cống 104 tuần, không tìm thấy mối quan hệ của nguy cơ bị khối u đối với liều lượng tacrolimus. Các liều cao nhất dùng trong nghiên cứu ở chuột nhắt và chuột cống là 0,8-2,5 lần (chuột nhắt) và 3,5-7,1 lần (chuột cống) khoảng liều lâm sàng đề nghị 0,1-0,2 mg/kg/ngày được hiệu chỉnh theo diện tích bề mặt cơ thể.
Không thấy có sự suy giảm khả năng thụ tinh trong các nghiên cứu ở chuột cống đực và cái. Khi cho dùng đường uống 1mg/kg (0,7-1,4 lần khoảng liều lâm sàng đề nghị 0,1-0,2mg/kg/ngày được hiệu chỉnh theo diện tích bề mặt cơ thể) ở chuột cống đực và cái trước và trong khi giao phối, cũng như ở con mẹ trong suốt kỳ thai nghén và cho con bú, tacrolimus đi kèm với khả năng gây chết bào thai và những tác dụng phụ có hại trên sự sinh sản của chuột cái. Tác động trên sự sinh sản của chuột cái (quá trình sinh đẻ) và tác động gây chết bào thai được dẫn chứng bởi một tỉ lệ cao hơn về tổn thất trước khi thụ thai và số lượng chuột con không sống được cũng như không được sinh ra bị gia tăng. Khi cho dùng liều 3,2mg/kg (2,3-4,6 lần khoảng liều đề nghị được hiệu chỉnh theo diện tích bề mặt cơ thể, tacrolimus kèm theo độc tính ở cha và mẹ cũng như độc tính trên sự sinh sản bao gồm những tác dụng phụ có hại ghi nhận trên chu kỳ động dục, quá trình sinh đẻ, khả năng sống của chuột con và sự dị dạng chuột con.
Cảnh báo
Chứng tiểu đường mellitus sau khi ghép phụ thuộc insulin (PTDM) được báo cáo với tỉ lệ 20% ở những bệnh nhân ghép thận điều trị bằng Prograf (xem bảng). Thời gian trung bình xuất hiện PTDM là 68 ngày. Sự phụ thuộc insulin có thể đảo ngược ở 15% trong số bệnh nhân này 1 năm và ở 50% 2 năm sau khi ghép. Những bệnh nhân ghép thận người Tây Ban Nha, Bồ Đào Nha và da đen có nguy cơ gia tăng việc phát triển PTDM.
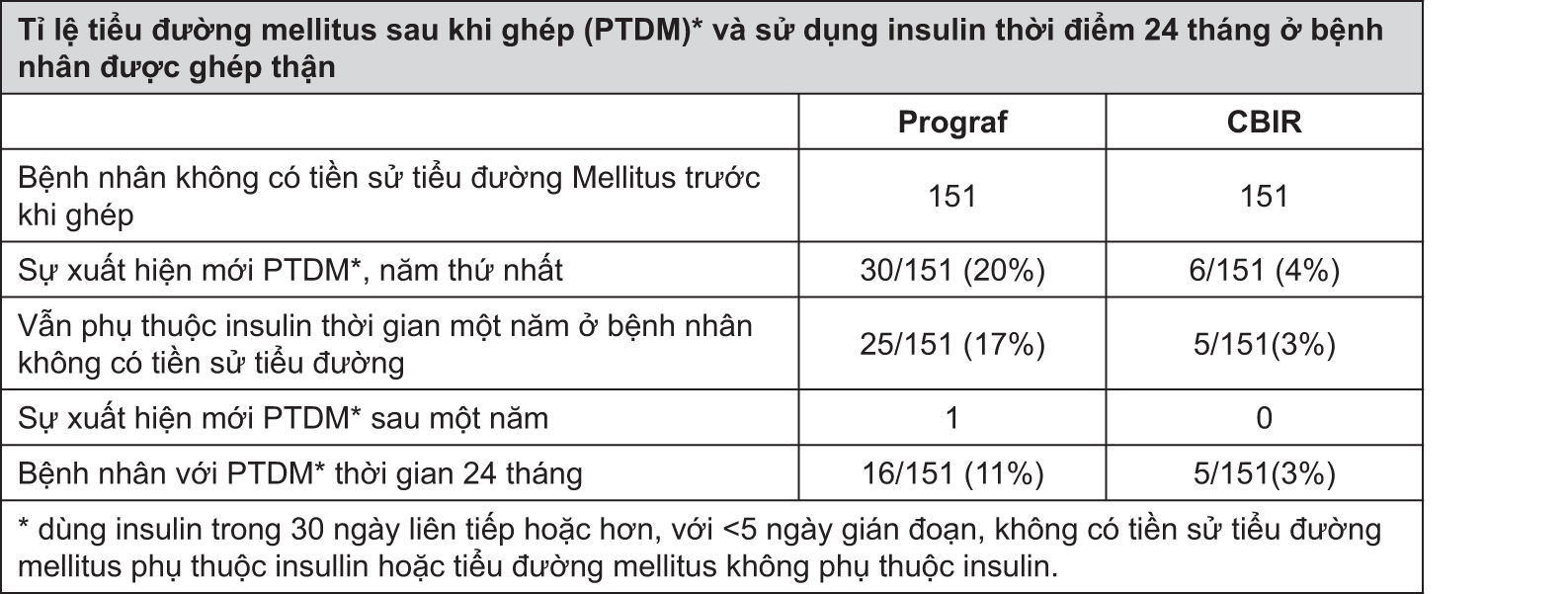

Tiểu đường mellitus sau khi ghép phụ thuộc insulin được báo cáo ở 18% và 11% bệnh nhân ghép gan điều trị bằng Prograf và đảo nghịch ở 45% và 31% trong số những bệnh nhân này trong thời gian một năm sau khi ghép lần lượt trong nghiên cứu ngẫu nhiên ở Hoa Kỳ và Châu Âu (xem bảng bên dưới). Sự tăng đường huyết đi kèm với việc sử dụng Prograf ở 47% và 33% người nhận gan ghép lần lượt trong các nghiên cứu ngẫu nhiên ở Hoa Kỳ và châu Âu và có thể cần phải điều trị (xem phần TÁC DỤNG NGOẠI Ý).
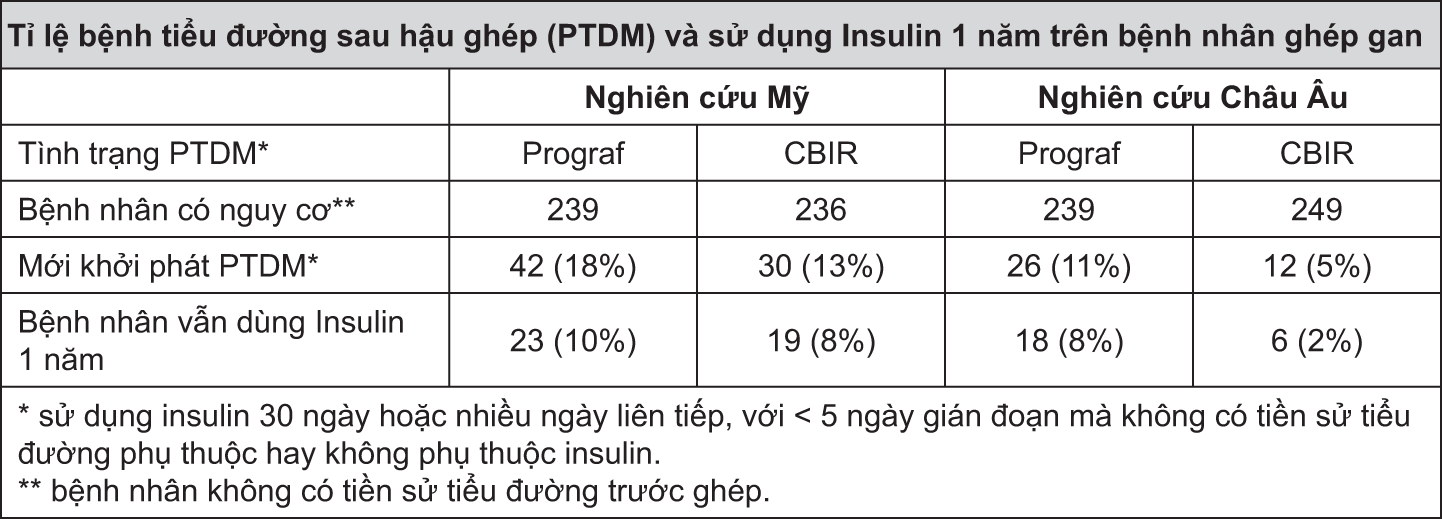
Prograf có thể gây độc tính thần kinh và thận, đặc biệt khi sử dụng ở liều cao. Độc tính thận được báo cáo xấp xỉ khoảng 52% ở bệnh nhân ghép thận, 40% và 36% ở bệnh nhân ghép gan dùng Prograf trong một nghiên cứu ngẫu nhiên ở Mỹ, Châu Âu theo thứ tự (xem TÁC DỤNG NGOẠI Ý).
Thêm độc tính thận đã được ghi nhận sớm sau ghép, đặc điểm bởi gia tăng creatinin huyết thanh và giảm lượng nước tiểu thải ra. Bệnh nhân thương tổn chức năng thận nên được giám sát cẩn thận bởi vì liều Prograf có thể cần được giảm. Ở bệnh nhân có sự gia tăng creatinin huyết thanh liên tục mà không đáp ứng với sự điều chỉnh liều, nên xem xét lại để thay đổi liệu pháp thuốc suy giảm miễn dịch khác. Nên thận trọng dùng tacrolimus với các thuốc khác có độc tính trên thận. Đặc biệt, tránh gây độc tính thận quá mức, không nên sử dụng Prograf cùng lúc với cyclosporine. Nên ngưng Prograf hoặc cyclosporine ít nhất 24 giờ trước khi bắt đầu thuốc khác. Nên trì hoãn thêm các thuốc khác nếu sự hiện diện của nồng độ Prograf hoặc cyclosporine cao.
Tăng kali huyết nhẹ đến nặng được báo cáo trên 31% bệnh nhân ghép thận, 45% và 13% bệnh nhân ghép gan được điều trị bằng Prograf theo thứ tự ngẫu nhiên ở nghiên cứu ở Mỹ và Châu Âu (xem TÁC DỤNG NGOẠI Ý). Nên giám sát nồng độ Kali huyết và không được sử dụng thuốc lợi tiểu tiết kiệm kali trong khi dùng Prograf (xem THẬN TRỌNG LÚC DÙNG). Độc tính thần kinh, bao gồm run, nhức đầu và các thay đổi khác về tình trạng tâm thần chức năng vận động và chức năng cảm nhận được báo cáo trên khoảng 55% bệnh nhân ghép gan trong 2 nghiên cứu ngẫu nhiên. Run thường xảy ra ở bệnh nhân ghép thận điều trị bằng Prograf (54%) hơn là bệnh nhân dùng cyclosporin. Tần suất các biến cố thần kinh khác trên bệnh nhân ghép thận thì tương tự ở 2 nhóm điều trị (xem TÁC DỤNG NGOẠI Ý). Run và nhức đầu có liên quan đến nồng độ tacrolimus trong máu toàn phần cao và có thể được chỉnh liều. Cơn động kinh có thể xảy ra trên bệnh nhân người lớn và trẻ em dùng Prograf (xem TÁC DỤNG NGOẠI Ý). Hôn mê và sảng cũng liên quan đến nồng độ tacrolimus trong huyết thanh cao.
Như ở những bệnh nhân dùng các thuốc suy giảm miễn dịch, bệnh nhân dùng Prograf tăng nguy cơ phát triển u lympho và các bệnh ác tính khác, đặc biệt trên da. Nguy cơ này xuất hiện dường như liên quan đến mức độ và khoảng thời gian dùng thuốc suy giảm miễn dịch hơn là việc dùng bất kỳ 1 thuốc đặc hiệu nào.
Rối loạn sự sinh sản lympho (LPD) liên quan đến nhiễm virus Epstein-Barr (EBV) đã được báo cáo ở bệnh nhân ghép tạng suy giảm miễn dịch. Nguy cơ LPD dường như cao hơn ở trẻ nhỏ có nguy cơ nhiễm EBV nguyên phát trong lúc bị suy giảm miễn dịch hoặc bệnh nhân được chuyển sang Prograf sau khi điều trị thuốc suy giảm miễn dịch lâu dài. Vì sự nguy hiểm về việc ức chế quá mức hệ miễn dịch mà có thể gia tăng sự nhạy cảm đối sự nhiễm trùng, do đó nên thận trọng việc điều trị kết hợp các thuốc suy giảm miễn dịch.
Ở 1 vài bệnh nhân tiêm Prograf bị phản ứng sốc phản vệ. Mặc dù nguyên nhân chính xác của phản ứng này chưa được biết, nhưng cho thấy có liên kết giữa các thuốc có dẫn xuất dầu thầu dầu trong công thức với phản ứng phản vệ ở tỷ lệ nhỏ bệnh nhân. Vì nguy cơ tiềm tàng gây sốc phản vệ, nên dè dặt sử dụng Prograf chích cho bệnh nhân không thể dùng Prograf viên. Bệnh nhân dùng Prograf chích nên được giám sát liên tục ít nhất 30 phút sau khi bắt đầu truyền và sau đó nên giám sát định kỳ thường xuyên. Nếu xảy ra dấu hiệu hoặc triệu chứng sốc phản vệ, nên ngừng ngay truyền Prograf. Nên có sẵn dung dịch epinephrine có nước tại giường bệnh nhân cũng như nguồn oxygen.
Quá Liều
Đã có rất ít trường hợp quá liều. Quá liều cấp gấp 30 lần liều dự định đã được báo cáo. Hầu hết các trường hợp không có triệu chứng và tất cả bệnh nhân được hồi phục mà không bị di chứng. Đôi khi quá liều cấp xảy ra theo sau bởi các tác dụng phụ dai dẳng được liệt kê trong phần tác dụng ngoại ý, ngoại trừ 1 trường hợp thấy có mề đay và hôn mê thoáng qua. Do tính hòa tan trong nước kém và sự gắn kết nhiều với hồng cầu và protein huyết tương, nên tacrolimus được biết trước là không thể thẩm tách thành lượng đáng kể nào. Chưa có trường hợp nào cần thẩm phân máu qua thận. Có trường hợp dùng than hoạt đường uống trong điều trị quá liều cấp, nhưng chưa có kinh nghiệm đầy đủ để khuyến cáo sử dụng. Các phương pháp hỗ trợ chung và điều trị triệu chứng đặc hiệu nên được áp dụng trong tất cả các trường hợp quá liều.
Trong các nghiên cứu độc tính cấp đường uống và tiêm tĩnh mạch, trường hợp tử vong được thấy bằng hoặc lớn hơn các liều sau: ở chuột cống trưởng thành, liều gấp 52 lần liều uống được khuyến cáo sử dụng ở người, ở chuột cống con, liều gấp 16 lần liều uống ở người và ở chuột cống trưởng thành, liều gấp 16 lần liều được khuyến cáo tiêm tĩnh mạch ở người (tất cả dựa trên diện tích bề mặt cơ thể).
Chống chỉ định
Prograf chống chỉ định ở những bệnh nhân mẫn cảm với tacrolimus. Thuốc tiêm Prograf chống chỉ định ở những bệnh nhân nhạy cảm với HCO-60 (dầu thầu dầu polyoxyl 60 hydrogen hóa).
Sử dụng ở phụ nữ có thai và cho con bú
Phụ nữ mang thai
Trong các nghiên cứu về sự sinh sản ở thỏ và chuột cống, các tác dụng phụ có hại trên bào thai được quan sát thấy chủ yếu ở những liều độc đối với thú mẹ. Tacrolimus ở các liều uống 0,32 và 1mg/kg trong suốt quá trình tạo cơ quan ở thỏ đi kèm với độc tính ở mẹ cũng như gia tăng tỉ lệ sẩy thai; những liều này tương đương với 0,5-1 lần và 1,6-3,3 lần khoảng liều lâm sàng đề nghị (0,1-0,2mg/kg) được hiệu chỉnh theo diện tích bề mặt cơ thể. Ở liều cao duy nhất này, tỉ lệ gia tăng về dị dạng và những thay đổi về sự phát triển tâm thần cũng được quan sát thấy. Tacrolimus ở liều uống 3,2mg/kg trong quá trình tạo cơ quan ở chuột đi kèm với độc tính ở mẹ và gây ra sự gia tăng sự tiêu thai muộn, giảm số thú con sống sinh ra, giảm cân nặng và khả năng sống của thú con. Tacrolimus, dùng uống ở liều 1 và 3,2mg/kg (tương đương với 0,7-1,4 lần và 2,3-4,6 lần khoảng liều lâm sàng đề nghị được hiệu chỉnh theo diện tích bề mặt cơ thể) ở chuột mang thai sau quá trình tạo cơ quan và trong lúc cho con bú, đi kèm với sự giảm cân nặng thú con.
Không có chứng cứ về sự giảm khả năng thụ tinh ở thú đực và cái.
Không có những nghiên cứu có đối chứng tốt và đầy đủ ở phụ nữ mang thai. Tacrolimus di chuyển qua nhau thai. Việc sử dụng tacrolimus trong thời gian mang thai đi kèm với chứng cao kali huyết sơ sinh và rối loạn chức năng thận. Prograf sử dụng trong thời gian mang thai chỉ khi cân nhắc thấy lợi ích có thể có được ở người mẹ thuyết phục hơn là nguy cơ tiềm ẩn đối với bào thai.
Phụ nữ đang nuôi con bằng sữa mẹ
Vì tacrolimus tiết qua sữa mẹ, nên tránh sử dụng ở phụ nữ đang cho con bú.
Tương tác
Nghiên cứu tương tác thuốc với tacrolimus chưa được thực hiện. Do tiềm năng cộng hưởng thêm suy giảm hiệp lực chức năng thận, nên thận trọng khi sử dụng Prograf cùng với những thuốc có thể liên quan đến chức năng thận. Điều này kể cả không giới hạn đối với các aminoglycoside, amphotericin B, và cisplatin. Kinh nghiệm lâm sàng ban đầu khi sử dụng đồng thời Prograf và cyclosporine đã gây nên độc tính cộng hưởng/hiệp lực trên thận. Các bệnh nhân chuyển từ cyclosporine sang Prograf nên sử dụng liều Prograf đầu tiên không sớm hơn 24 giờ sau khi dùng liều cyclosporine cuối. Liều dùng nên được trì hoãn lâu hơn trong trường hợp nồng độ cyclosporine tăng cao.
Những thuốc có thể làm thay đổi nồng độ tacrolimus
Do tacrolimus chủ yếu được chuyển hóa bởi hệ thống men CYP3A, các chất được biết làm ức chế men này có thể làm giảm chuyển hóa của tacrolimus với kết quả là làm gia tăng nồng độ tacrolimus trong máu toàn phần hoặc huyết tương. Các thuốc được biết kích thích hệ thống men này có thể dẫn đến sự gia tăng chuyển hóa của tacrolimus và làm giảm nồng độ tacrolimus trong máu toàn phần hoặc huyết tương. Giám sát nồng độ trong máu và điều chỉnh liều thích hợp là cần thiết khi các thuốc trên được sử dụng đồng thời.
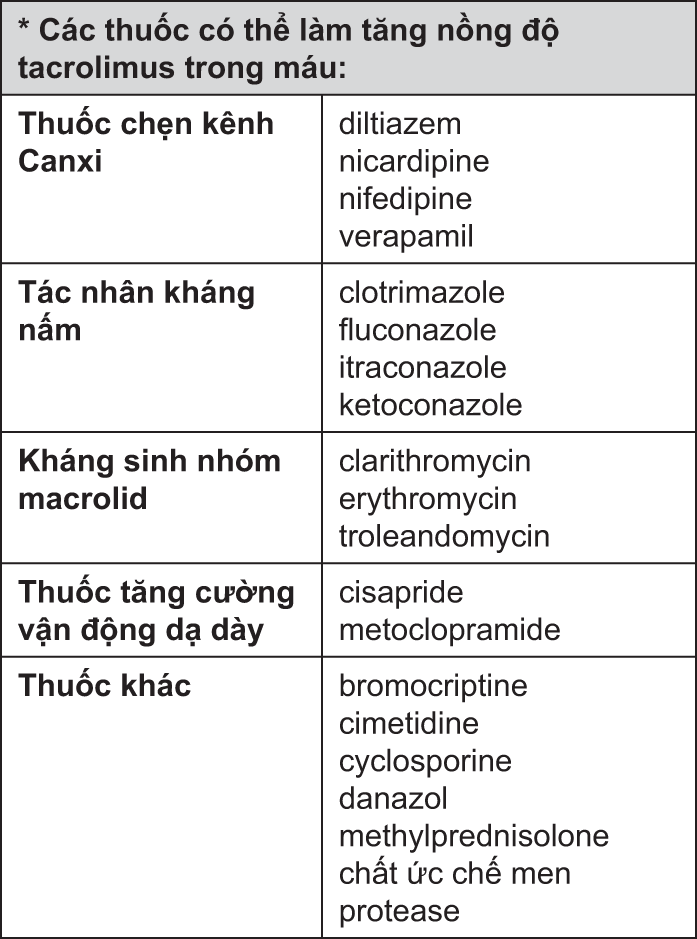

* Bảng này không bao gồm tất cả.
Các nghiên cứu về sự tương tác với các thuốc dùng trong điều trị HIV chưa thực hiện. Tuy nhiên, nên thận trọng theo dõi khi những thuốc có độc tính trên thận (ví dụ như ganciclovir) hoặc các thuốc được chuyển hóa bởi CYP3A (ví dụ như ritonavir) được dùng đồng thời với tacrolimus. Nước bưởi ảnh hưởng lên sự chuyển hóa trung gian của CYP3A và nên được tránh dùng (xem phần LIỀU LƯỢNG VÀ CÁCH DÙNG).
Tương tác với các thuốc khác
Các chất ức chế miễn dịch có thể ảnh hưởng đến sự chủng ngừa. Vì vậy trong suốt thời gian điều trị với Prograf, sự chủng ngừa có thể kém công hiệu. Việc sử dụng vacxin sống nên tránh; bao gồm hầu hết các vacxin sống, nhưng không giới hạn đối với trường hợp sởi, quai bị, rubella, bại liệt đường uống, BCG, sốt vàng và thương hàn TY21a.1
1CDC: Đề nghị của Ủy ban tư vấn về miễn dịch thực hành: Sử dụng vacxin và globulin miễn dịch ở bệnh nhân có khả năng miễn dịch bị thay đổi. MMWR 1993; 42(rr-4): 1-18.
Tác dụng ngoại ý
Trường hợp ghép gan
Các phản ứng ngoại ý chủ yếu của Prograf là run, nhức đầu, tiêu chảy, cao huyết áp, nôn mửa và loạn chức năng thận. Điều này xảy ra với Prograf tiêm tĩnh mạch và uống và có thể đáp ứng đối với sự giảm liều. Tiêu chảy đôi khi đi kèm với các biến chứng khác ở dạ dày ruột như buồn nôn và nôn mửa.
Sự tăng kali máu và sự giảm magie máu xảy ra ở những bệnh nhân nhận liệu pháp Prograf. Sự tăng đường huyết được ghi nhận ở nhiều bệnh nhân; vài trường hợp đòi hỏi phải điều trị bằng insulin (xem CHÚ Ý ĐỀ PHÒNG)
Tỉ lệ các phản ứng ngoại ý được xác định ở hai thử nghiệm ghép gan so sánh ngẫu nhiên trong số 514 bệnh nhân điều trị với tacrolimus và steroid; và 515 bệnh nhân nhận phác đồ điều trị với cyclosporin (CBIR). Tỉ lệ bệnh nhân báo cáo nhiều hơn một phản ứng ngoại ý muốn là 99,8% ở nhóm tacrolimus và 99,6% ở nhóm CBIR.
Phải thận trọng khi so sánh tỉ lệ các trường hợp phản ứng ngoại ý trong nghiên cứu ở Hoa Kỳ so với trong nghiên cứu ở Châu Âu. Thông tin 12 tháng hậu ghép từ nghiên cứu ở Hoa Kỳ và từ nghiên cứu ở Châu Âu được trình bày bên dưới. Hai nghiên cứu này cũng bao gồm những dân số khác nhau và các bệnh nhân được điều trị với các phác đồ ức chế miễn dịch cường độ khác nhau. Các trường hợp phản ứng ngoại ý muốn được báo cáo ở ≥15% bệnh nhân trong số những bệnh nhân sử dụng tacrolimus (kết hợp các kết quả nghiên cứu) được trình bày bên dưới về hai thử nghiệm có đối chứng trong ghép gan.
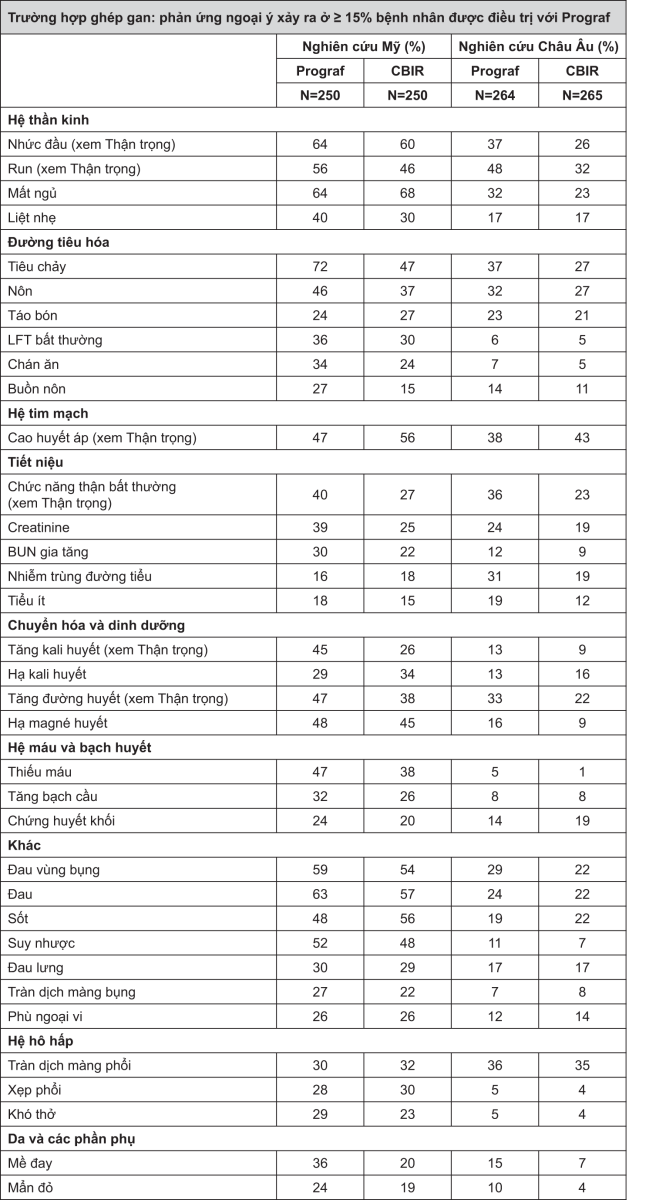
Các phản ứng phụ có hại xảy ra ít thường xuyên ở bệnh nhân ghép gan và ghép thận được mô tả ở phần Các phản ứng ngoại ý được báo cáo ít thường xuyên bên dưới.
Trường hợp ghép thận
Các phản ứng ngoại ý muốn được báo cáo thông thường nhất là nhiễm trùng, run, cao huyết áp, suy giảm chức năng thận, táo bón, tiêu chảy, nhức đầu, đau bụng và mất ngủ.
Các phản ứng ngoại ý muốn xảy ra ở ≥ 15% bệnh nhân ghép thận được điều trị với Prograf được trình bày bên dưới.
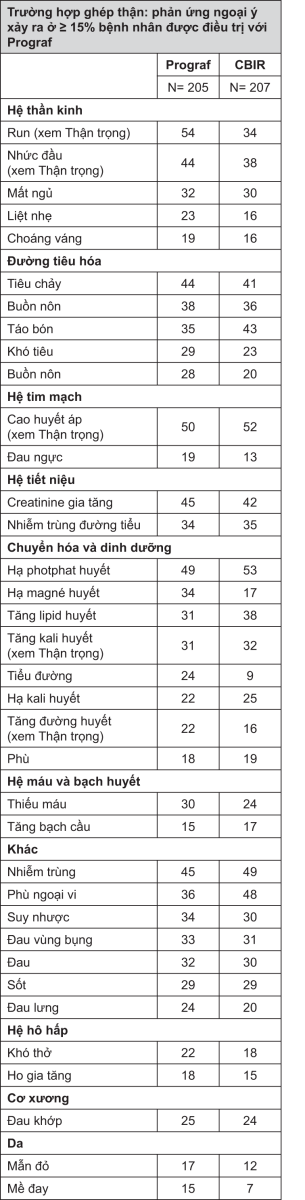
Các phản ứng ngoại ý xảy ra ít thường xuyên ở bệnh nhân ghép gan và ghép thận được mô tả ở phần Các phản ứng ngoại ý được báo cáo ít thường xuyên bên dưới.
Các phản ứng ngoại ý được báo cáo ít thường xuyên
Các phản ứng ngoại ý dưới đây được báo cáo trong khoảng từ 3% đến dưới 15% những người nhận gan ghép hoặc thận ghép được điều trị với tacrolimus trong những thử nghiệm so sánh pha 3.
Hệ thần kinh (xem Chú ý đề phòng): ác mộng, kích động, chứng quên, lo âu, lú lẫn, co giật, trầm cảm, choáng váng, dễ xúc động, bệnh não, ảo giác, tăng trương lực cơ, mất phối hợp, giật rung cơ, bồn chồn, bệnh thần kinh, rối loạn tâm thần, buồn ngủ, suy nghĩ bất thường.
Các giác quan đặc biệt: sự nhìn không bình thường, giảm thị lực, đau tai, viêm tai giữa, ù tai.
Dạ dày ruột: chán ăn, viêm tiểu quản mật, vàng da tắc mật, khó tiêu, viêm thực quản, đầy hơi, viêm dạ dày, xuất huyết dạ dày ruột, tăng GGT, thủng dạ dày ruột, viêm gan, tắc ruột, tăng cảm giác thèm ăn, vàng da, tổn thương gan, thử nghiệm chức năng gan bất thường, nhiễm nấm Candida, rối loạn trực tràng, viêm miệng.
Tim mạch: đau thắt ngực, đau ngực, viêm tĩnh mạch huyết khối sâu, điện tâm đồ bất thường, xuất huyết, hạ huyết áp, hạ huyết áp tư thế, rối loạn mạch ngoại biên, viêm tĩnh mạch, huyết khối, dãn mạch.
Niệu sinh dục (xem Chú ý đề phòng): albumin niệu, viêm bọng đái, huyết niệu, thủy thũng thận, suy thận, hoại tử ống thận, tiểu đêm, tiểu ra mủ, tiểu ít, tiểu thường xuyên, tiểu dầm, viêm âm đạo.
Chuyển hóa/dinh dưỡng: nhiễm acid, phosphatase kiềm gia tăng, nhiễm kiềm, tăng SGPT, tăng SGOT, giảm bicarbonat, bilirubin niệu, BUN gia tăng, mất nước, GGT tăng, liền da bất thường, tăng calci huyết, tăng cholesterol huyết, tăng lipid huyết, tăng phosphat huyết, tăng acid uric huyết, tăng dung lượng máu, giảm canxi huyết, giảm đường huyết, giảm natri huyết, giảm phosphat huyết, giảm protein huyết, tăng dehydrogenase lactic, tăng cân.
Nội tiết (xem Thận trọng): hội chứng Cushing, tiểu đường mellitus.
Huyết/bạch huyết: rối loạn đông máu, vết bầm máu, thiếu máu nhược sắc, chứng tăng bạch cầu, giảm bạch cầu, tăng hồng cầu, giảm prothrombin, tiểu cầu, sắt huyết thanh giảm.
Các cơ quan khác: bụng to, áp xe, thương tổn tình cờ, phản ứng dị ứng, viêm tế bào, ớn lạnh, hội chứng cúm, phù, thoát vị, viêm phúc mạc, phản ứng nhạy cảm với ánh sáng, nhiễm trùng.
Cơ xương: đau khớp, vọp bẻ, co thắt, rối loạn khớp, vọp bẻ chân, đau cơ, nhược cơ, loãng xương.
Hô hấp: hen suyễn, viêm phế quản, ho gia tăng, khó chịu ở phổi, tràn khí ngực, phù phổi, viêm hầu, viêm phổi, rối loạn hô hấp, viêm mũi, viêm xoang, đổi tiếng.
Da: mụn trứng cá, rụng tóc, viêm tróc da, viêm da do nấm, Herpes, rậm lông, đổi màu da, rối loạn da, viêm da, đổ mồ hôi.
Hiếm có những báo cáo tự phát về sự phì đại cơ tim kèm với loạn chức năng tâm thất biểu hiện lâm sàng ở những bệnh nhân nhận phác đồ điều trị với Prograf (xem Thận trọng– Sự phì đại cơ tim).
Bảo quản
* Viên nang: bảo quản ở nhiệt độ phòng, 15-30°C.
* Ống tiêm: bảo quản ở nhiệt độ từ 5oC đến 30oC.
Phân loại ATC
L04AD02
Trình bày/Đóng gói
Viên nang: vỉ 10 viên, hộp 5 vỉ.
Ống tiêm: hộp 10 ống 1mL.
- Abacavir
- Abernil
- Abiiogran
- Acarbose
- ACC
- Acebutolol
- Acenocoumarol
- Acetate Ringer's
- Acetazolamide
- Acetylcystein
- Acetylsalicylic acid
- Aciclovir
- Acid acetylsalicylic
- Acid aminocaproic
- Acid ascorbic
- Acid boric
- Acid chenodeoxycholic
- Acid ethacrynic
- Acid folic
- Acid fusidic
- Acid iopanoic
- Acid ioxaglic
- Acid nalidixic
- Acid pantothenic
- Acid para-aminobenzoic
- Acid salicylic
- Acid tranexamic
- Acid valproic
- Acid zoledronic
- Acitretin
- Aclasta
- Aclon
- Actapulgite
- Actelsar
- Actelsar HCT
- Actemra
- Actilyse
- Acular
- Acupan
- Acuvail
- Acyclovir STADA
- Acyclovir STADA Cream
- Adalat
- Adenosin
- Adenosin Ebewe
- Adipiodon
- Advagraf
- Aerius
- Afinitor
- Agicarvir
- Agifovir-E
- Agilosart
- Agilosart-H
- Agimepzol
- Agimosarid
- Agimstan
- Agimstan-H
- Agiremid
- Agivastar
- Aibezym
- Air-X
- Alaxan
- Albendazol
- Albiomin
- Albumin
- Albumin người Grifols 20%
- Albuminar
- AlbuRx
- Albutein
- Alcuronium chloride
- Aldesleukin
- Alendronat
- Alertin
- Alfa-Lipogamma 600 Oral
- Alfuzosin hydrochlorid
- Algotra
- Alimemazin
- Alimta
- Allipem
- Allopurinol
- Allopurinol STADA
- Aloxi
- Alprazolam
- Alpha Chymotrypsin
- Alpha tocopherol
- Alphachymotrypsin Glomed
- Alphagan-P
- Aluvia
- Alzental
- Amaryl
- Ambroco
- Ambroxol
- Amcinol-Paste
- Amigold
- Amikacin
- Aminocaproic acid
- Aminoleban
- Aminoleban Oral
- Aminosteril N-Hepa
- Amiparen
- Amitriptyline
- Amiyu
- Amlodipine
- Amlor
- Amoxicillin
- Amoxicillin & clavulanate
- Ampicillin
- Amquitaz
- Anaferon for children
- Anargil
- Anaropin
- Andriol Testocaps
- Anepzil
- Anyfen
- Apaisac
- Apidra SoloStar
- Apitim 5
- Aprovel
- Aquaphil
- Arcalion
- Arcoxia
- Aricept Evess
- Arimidex
- Arnetine
- Artrodar
- A-Scabs
- Ascorbic acid
- Asperlican/Candinazol
- Aspilets EC
- Aspirin
- Asthmatin
- Atelec
- Atocib 120
- Atocib 90
- Atosiban PharmIdea
- Atozet
- Attapulgite
- Atussin
- Atropin
- Augbactam
- Augmentin Sachet
- Augmentin SR
- Augmentin Tablets
- Augmex
- Avamys
- Avastin
- Avelox Dịch truyền
- Avelox Viên nén
- Avodart
- Axcel Cefaclor-125 Suspension
- Axcel Cetirizine Syrup
- Axcel Chlorpheniramine
- Axcel Dexchlorpheniramine
- Axcel Dicyclomine-S Syrup
- Axcel Diphenhydramine Paediatric Syrup
- Axcel Erythromycin ES
- Axcel Eviline
- Axcel Fungicort Cream
- Axcel Fusidic acid Cream
- Axcel Fusidic acid-B Cream
- Axcel Hydrocortisone Cream
- Axcel Lignocaine 2% Sterile Gel
- Axcel Loratadine
- Axcel Miconazole Cream
- Axcel Paracetamol
- Axcel Urea Cream
- Axitan
- Azenmarol
- Azicine
- Aziphar
- Azithromycin