Nhà sản xuất
Novartis Pharma
Nhà phân phối
Zuellig Pharma
Thành phần
Mỗi viên: Acid mycophenolic (MPA) 180mg hoặc 360mg (tương đương với 192,4mg hoặc 384,4mg natri mycophenolate).
Trình bày/Đóng gói
Viên nén bao tan trong ruột: hộp 12 vỉ x 10 viên.
Cơ chế tác dụng
MPA ức chế sự tăng sinh của các tế bào lympho T và lympho B mạnh hơn so với các tế bào khác, vì khác với các loại tế bào khác có thể sử dụng quá trình tận dụng purin, sự tăng sinh tế bào lympho phụ thuộc chủ yếu vào sự tổng hợp mới. Như vậy, cơ chế tác dụng là bổ trợ cho các chất ức chế calcineurin, những chất can thiệp vào sự phiên mã cytokin và giữ ở trạng thái nghỉ các tế bào lympho T.
Dược động học
• Hấp thu: Sau khi uống, natri mycophenolat hấp thu rất mạnh. Phù hợp theo thiết kế viên bao tan trong ruột, thời gian để nồng độ MPA đạt mức tối đa khoảng 1,5 đến 2 giờ. Những nghiên cứu in vitro chứng minh rằng dạng thuốc bao tan trong ruột của Myfortic ngăn chặn được sự giải phóng MPA trong điều kiện acid như ở trong dạ dày.
Những bệnh nhân ghép thận ổn định nhờ tác dụng ức chế miễn dịch của ciclosporin dạng vi nhũ tương, sự hấp thu qua đường tiêu hoá của MPA là 93% và sinh khả dụng tuyệt đối là 72%. Dược động học của Myfortic thì tỷ lệ thuận với liều dùng và tuyến tính trong phạm vi liều đã nghiên cứu từ 180 đến 2.160 mg. So với trạng thái đói, dùng Myfortic 720 mg với một bữa ăn nhiều chất béo (55 g mỡ, 1.000 calo) không có ảnh hưởng đến sự tiếp xúc toàn thân của MPA (AUC); đó là thông số pk có liên quan nhất tới hiệu quả. Tuy nhiên, nồng độ tối đa của MPA (Cmax) giảm 33%.
• Phân bố: Thể tích phân bố của MPA ở trạng thái ổn định là 50 lít. Cả hai acid mycophenolic và dạng glucuronid của acid mycophenolic đều gắn kết cao với protein, theo thứ tự là 97% và 82%. Nồng độ MPA tự do có thể tăng trong điều kiện các nơi gắn kết với protein giảm (urê huyết, suy gan, giảm albumin huyết, dùng đồng thời các thuốc cũng gắn kết cao với protein). Điều này có thể làm cho bệnh nhân có nguy cơ cao với tác dụng bất lợi có liên quan đến MPA.
• Biến đổi sinh học/Chuyển hóa: Thời gian bán thải của MPA là 11,7 giờ và độ thanh thải là 8,6 lít/giờ. MPA bị chuyển hoá chủ yếu bởi glucuronyl transferase để tạo thành glucuronid phenolic của MPA, glucuronid của acid mycophenolic (MPAG). MPAG là chất chuyển hoá chủ yếu của MPA và không thấy có hoạt tính sinh học. Ở bệnh nhân ghép thận ổn định về trạng thái ức chế miễn dịch do ciclosporin dạng vi nhũ tương, khoảng 28% liều uống Myfortic được chuyển thành MPAG do sự chuyển hoá trước hệ tuần hoàn. Thời gian bán thải của MPAG dài hơn của MPA, khoảng 15,7 giờ và độ thanh thải là 0,45 lít/giờ.
• Thải trừ: Mặc dù chỉ có một lượng không đáng kể của MPA có mặt trong nước tiểu (< 1,0%), đa số MPA được thải trừ trong nước tiểu dưới dạng MPAG. MPAG tiết vào mật, rồi được khử liên hợp bởi hệ vi khuẩn đường ruột. MPA sinh ra do sự khử liên hợp này lại có thể được hấp thu trở lại. Khoảng 6 đến 8 giờ sau khi dùng Myfortic, có thể đo được đỉnh thứ hai của MPA, đó là do sự tái hấp thu MPA đã được khử liên hợp.
• Dược động học ở bệnh nhân ghép thận được ức chế miễn dịch do ciclosporin dạng vi nhũ tương: Được biểu thị trong bảng 1 là các thông số dược động học trung bình của MPA sau khi dùng Myfortic. Dược động học Myfortic dùng liều một lần dự đoán được dược động học dùng nhiều lần và dùng lâu dài. Trong giai đoạn sớm sau khi ghép, AUC trung bình của MPA và Cmax trung bình của MPA xấp xỉ bằng một nửa các trị số đo được lúc 6 tháng sau khi ghép.
- xem Bảng 1.

• Đối tượng đặc biệt
+ Người suy thận: Dược động học của MPA không thay đổi trong phạm vi chức năng thận từ bình thường đến không có. Ngược lại, sự tiếp xúc MPAG tăng khi chức năng thận giảm; sự tiếp xúc MPAG cao hơn xấp xỉ 8 lần khi vô niệu. Độ thanh thải của cả MPA cả MPAG đều không bị ảnh hưởng khi thẩm tách máu. MPA tự do cũng tăng có ý nghĩa khi suy thận. Đó có thể là do sự gắn kết MPA với protein trong huyết tương giảm khi nồng độ urê trong máu tăng cao.
+ Người suy gan: Ở người tình nguyện bị xơ gan do rượu, quá trình glucuronid hoá MPA ở gan tương đối không bị ảnh hưởng bởi bệnh nhu mô gan. Các ảnh hưởng của bệnh gan lên quá trình này có thể phụ thuộc vào từng bệnh riêng. Tuy nhiên, bệnh gan có tổn thương chủ yếu ở mật, như xơ gan mật nguyên phát, có thể biểu hiện một tác động khác.
+ Trẻ em: Chưa có tài liệu về độ an toàn và hiệu quả ở trẻ em. Tài liệu dược động học hiện có về sử dụng Myfortic cho trẻ em còn hạn chế. Trong bảng trên có biểu thị trị số trung bình (SD) của các thông số dược động học MPA đối với bệnh nhi ghép thận ổn định được ức chế miễn dịch bằng ciclosporin dạng vi nhũ tương. Tính biến thiên tăng Cmax và AUC của MPA được ghi nhận ở các bệnh nhi này so với bệnh nhân người lớn được ghép thận. AUC trung bình của MPA ở liều này cao hơn khi đo ở người lớn dùng liều 720 mg Myfortic. Độ thanh thải biểu kiến trung bình của MPA khoảng 7,7 lít/giờ. Một liều Myfortic 200-300 mg/m2 có thể đạt được AUC của MPA 30-50 microgam.giờ/mL.
+ Giới tính: Không có sự khác nhau có ý nghĩa lâm sàng theo giới tính về dược động học của Myfortic.
+ Người cao tuổi: Dựa trên những tài liệu sơ bộ, sự tiếp xúc MPA không thay đổi đến mức có ý nghĩa lâm sàng theo tuổi.
+ Dân tộc/Chủng tộc: Dùng liều đơn 720 mg Myfortic cho 18 người Nhật Bản và người da trắng khỏe mạnh, người Nhật Bản thấp hơn người da trắng về nồng độ (AUCinf) MPA là 15% và MPAG là 22%. Nồng độ đỉnh (Cmax) của MPAG tương tự giữa 2 nhóm đối tượng, tuy nhiên, người Nhật Bản có Cmax MPA cao hơn 9.6%. Những kết quả này không cho thấy bất kỳ sự khác biệt lâm sàng có liên quan.
CÁC NGHIÊN CỨU LÂM SÀNG
Hai thử nghiệm quan trọng đa trung tâm ngẫu nhiên, mù đôi sử dụng Myfortic (MPA) cho người lớn. Cả hai nghiên cứu là các nghiên cứu lâm sàng đối chứng có kiểm soát điều trị sử dụng Cellcept bán thương mại (MMF) như chất so sánh. Cả hai nghiên cứu chỉ ra hiệu quả và độ an toàn tương đương với MMF. Nghiên cứu đầu tiên bao gồm 423 người lớn mới được ghép thận (ERLB301) và chỉ ra rằng MPA hiệu quả tương đương với MMF và có độ an toàn có thể so sánh được. Nghiên cứu thứ hai tiến hành trên 322 người đã ghép thận (ERLB302) và chứng minh rằng các bệnh nhân ghép thận dùng MMF để duy trì điều trị ức chế miễn dịch có thể được chuyển sang MPA một cách an toàn mà không ảnh hưởng đến hiệu quả.
Các bệnh nhân người lớn mới ghép thận (Nghiên cứu ERL B301): Nghiên cứu ngẫu nhiên mù đôi, hai lần giả (double-dummy) (ERLB301) dùng thuốc lúc mới ghép tiến hành trên 423 bệnh nhân ghép thận (MPA=213, MMF=210), tuổi từ 18-75, và được thiết kế tiến cứu để thử nghiệm tương đương điều trị của MPA với MMF được đo bằng tỷ lệ thất bại hiệu quả (ví dụ như thải trừ cấp tính được chứng minh sinh thiết (BPAR), thải ghép, tử vong hoặc mất theo dõi) trong 6 tháng đầu điều trị (kết luận chính) và bằng tỷ lệ tử vong, thải ghép hoặc mất theo dõi tại 12 tháng (đồng kết luận chính).
Bệnh nhân được dùng hoặc 1,44 g MPA/ngày hoặc 2 g MMF/ngày trong 48 giờ sau ghép đến 12 tháng, dùng kết hợp với cyclosporin và các corticosteroid. Có 39,4% bệnh nhân trong nhóm dùng MPA và 42,9% bệnh nhân trong nhóm dùng MMF sử dụng điều trị kháng thể như một điều trị dẫn nhập.
Dựa trên tỷ lệ thất bại hiệu quả tại thời điểm 6 tháng (25,8% MPA so với 26,2% MMF; %; 95% CI: [-8,7, +8,0]) sự tương đương điều trị đã được chứng minh. Tại 12 tháng, tỷ lệ của BPAR, thải ghép hoặc tử vong là 26,3% và 28,1%, và của riêng BPAR là 22,5% đối với MPA và 24,3% đối với MMF. Trong số những trường hợp BPAR, tỉ lệ thải trừ cấp tính nghiêm trọng là 2,1% với MPA và 9,8% với MMF (p=ns).
- xem Bảng 2.
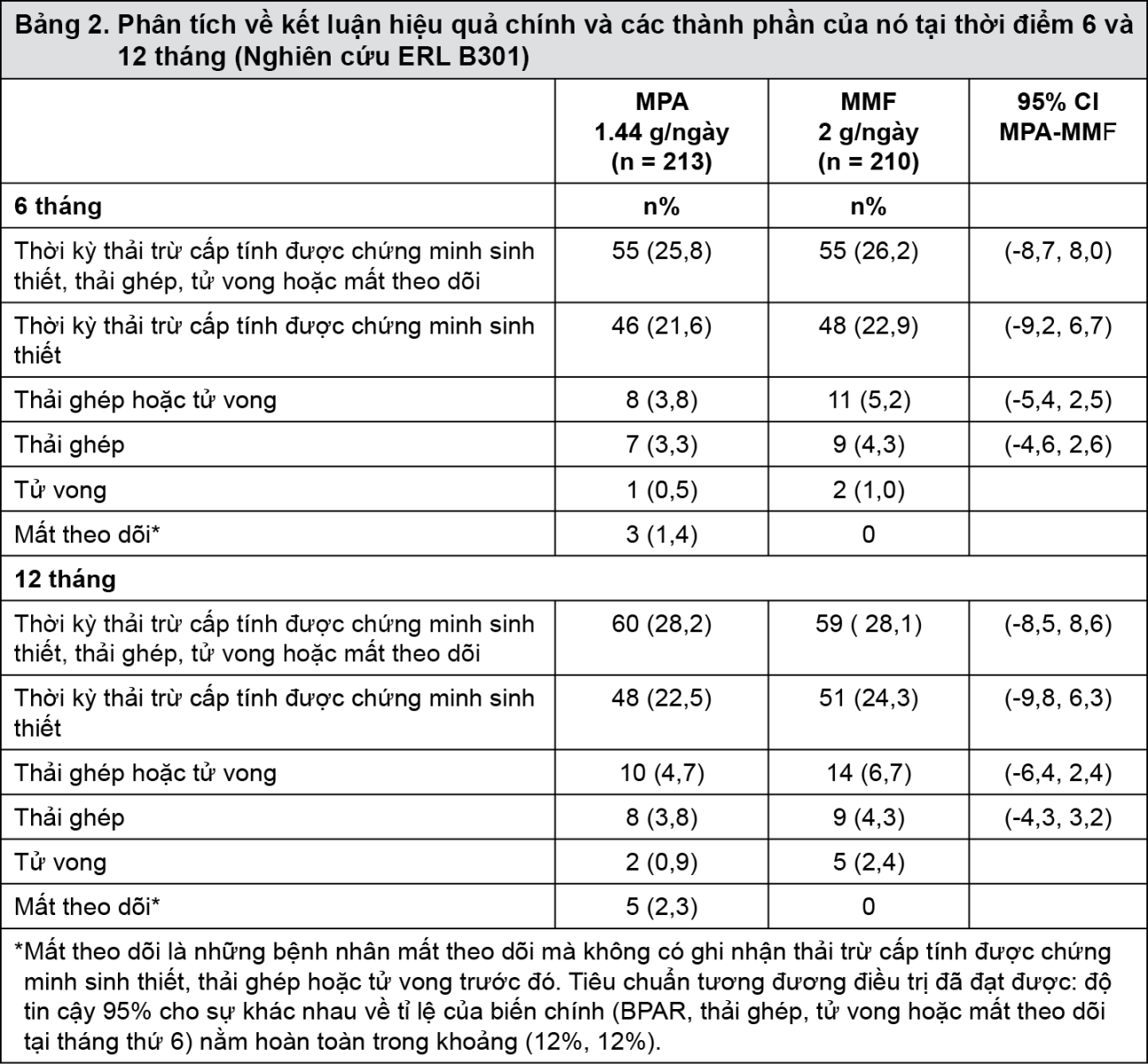
Dữ liệu an toàn và huyết học nói chung tương tự nhau giữa 2 nhóm điều trị. Những phản ứng bất lợi nghi ngờ do thuốc là 51,1% ở nhóm MPA so với 60,5% ở nhóm MMF. Không quan sát thấy có sự khác nhau về tỉ lệ nhiễm khuẩn chung. Tỉ lệ chung về nhiễm khuẩn nặng là 22,1% ở nhóm MPA và 27,1% ở nhóm MMF. Tỉ lệ viêm phổi nặng ở nhóm MPA thấp hơn (0,5% so với 4,3%, p= 0,01). Không quan sát thấy có sự khác biệt về tỉ lệ chung các phản ứng bất lợi đường tiêu hóa (80,8% ở nhóm MPA so với 80% ở nhóm MMF, p=ns).
Bệnh nhân người lớn ghép thận giai đoạn duy trì (Nghiên cứu ERL B302): Nghiên cứu duy trì được tiến hành ở 322 bệnh nhân ghép thận (MPA=159, MMF=163), tuổi từ 18-75, đã ghép thận ít nhất 6 tháng dùng 2 g MMF/ngày kết hợp với cyclosporin, có hoặc không có kết hợp với corticosteroid trong ít nhất 4 tuần trước khi bắt đầu tham gia nghiên cứu. Bệnh nhân được xếp ngẫu nhiên 1:1 dùng 1,44 g MPA/ngày hoặc 2 g MMF/ngày trong 12 tháng. Kết luận về hiệu quả là tỉ lệ thất bại hiệu quả (tức là BPAR, thải ghép hoặc tử vong) lúc 6 và 12 tháng.
Lúc 12 tháng, tỉ lệ tương tự về thất bại hiệu quả (MPA 2,5%; MMF 6,1%; p=ns), thải trừ cấp tính được chứng minh bằng sinh thiết (MPA 1,3%; MMF 3,1%; p=ns) và thải trừ mạn tính đã được chứng minh sinh thiết (MPA 3,8%; MMF 4,9%; p=ns) đã được quan sát ở cả 2 nhóm.
- xem Bảng 3.
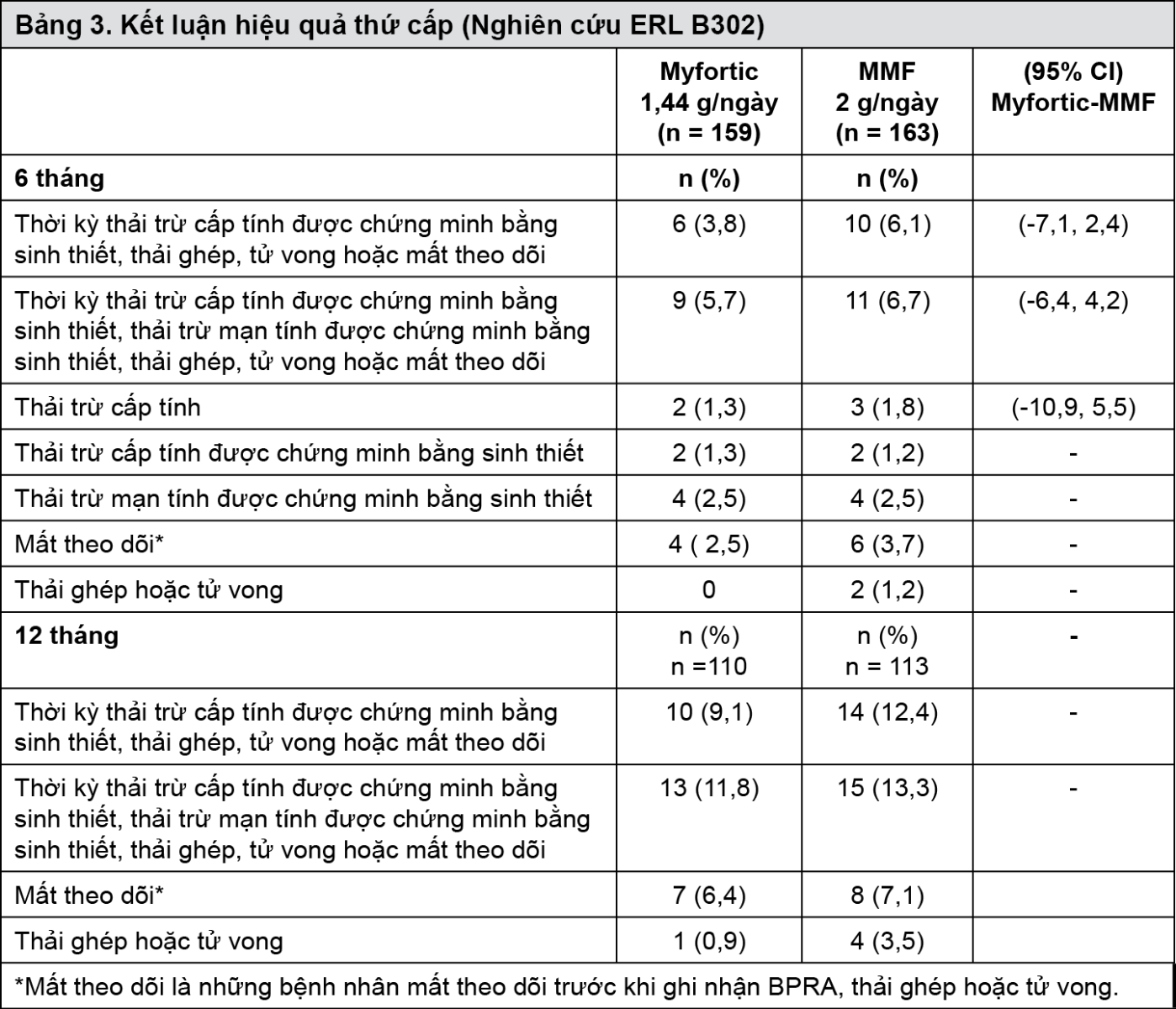
Nghiên cứu duy trì cũng chứng minh độ an toàn nói chung tương tự, ngoại trừ tỉ lệ nhiễm khuẩn nặng (8,8% ở nhóm MPA so với 16% ở nhóm MMF, p < 0,05). Tỉ lệ nhiễm khuẩn nói chung là 59% ở mỗi nhóm. Quan sát thấy ít trường hợp viêm phổi ở nhóm MPA (1,9%) hơn so với nhóm MMF (4,9%), nhưng nó không có ý nghĩa thống kê. Cũng quan sát thấy tỉ lệ tương tự về các phản ứng bất lợi về tiêu hóa nói chung (69,2% ở nhóm MPA so với 61,8% ở nhóm MMF), mặc dù “bất kỳ phản ứng bất lợi về tiêu hóa” đều cao hơn về số lượng ở các bệnh nhân điều trị bằng MPA tới 12 tháng (29,6% so với 24,5% ở tháng 12), và sự tăng mức độ nặng ở đường tiêu hóa có xu hướng thấp hơn ở các bệnh nhân dùng MPA.
DỮ LIỆU AN TOÀN PHI LÂM SÀNG
Ung thư, Đột biến gen, Suy giảm khả năng sinh sản: Trong một nghiên cứu sinh ung thư cho chuột cống uống 104 tuần natri mycophenolat với liều hàng ngày 9 mg/kg không sinh ra u. Liều cao nhất đã thử bằng khoảng 0,6-1,2 lần sự tiếp xúc toàn thân quan sát thấy ở bệnh nhân ghép thận ở liều khuyến cáo 1,44 g/ngày. Những kết quả tương tự cũng đã thu được trong một nghiên cứu song song ở chuột cống dùng mycophenolate mofetil. Trong một thử nghiệm sinh ung thư dùng mô hình chuột nhắt chuyển gen P53± (dị hợp tử) uống thuốc 26 tuần, natri mycophenolat ở liều hàng ngày tới 200 mg/kg cũng không sinh khối u. Liều thử cao nhất 200 mg/kg gây ra sự tiếp xúc toàn thân gấp khoảng 5 lần sự tiếp xúc quan sát được ở bệnh nhân ghép thận (dùng liều 1,44 g/ngày).
Khả năng độc gen của natri mycophenolat đã được xác định bằng 5 thử nghiệm. MPA độc gen trong thử nghiệm u lympho/thymidin kinase ở chuột nhắt, thử nghiệm vi nhân trong tế bào chuột Hamster V79 và thử nghiệm vi nhân in vivo ở chuột nhắt. Natri mycophenolat không gây độc gen trong thử nghiệm biến chủng vi khuẩn hoặc thử nghiệm sai lạc nhiễm sắc thể tế bào lympho người. Liều thấp nhất biểu hiện tác dụng độc gen trong thử nghiệm vi nhân tuỷ xương chuột nhắt trắng xấp xỉ 3 lần sự tiếp xúc toàn thân (AUC hoặc Cmax) quan sát được ở bệnh nhân ghép thận ở liều thử lâm sàng Myfortic 1,44 g mỗi ngày. Có thể tác dụng sinh biến chủng quan sát thấy là do sự dịch chuyển tương đối phong phú của các nucleotid trong khoang tế bào được dùng để tổng hợp DNA.
Natri mycophenolat không có tác dụng trên sinh sản của chuột cống đực ở liều tới 40 mg/kg/ngày. Sự phơi nhiễm toàn thân ở liều này xấp xỉ 9 lần sự tiếp xúc lâm sàng ở liều thử lâm sàng 1,44 g Myfortic mỗi ngày. Không có tác dụng trên sinh sản của chuột cống cái khi dùng liều đến 20 mg/kg, là liều đã thấy rõ gây ra độc cho mẹ và độc cho phôi.
Độc tính trên động vật và dược lý: Hệ tạo máu và hệ lympho là những cơ quan bị ảnh hưởng chủ yếu khi nghiên cứu độc tính được tiến hành với natri mycophenolat ở chuột cống và chuột nhắt. Thiếu máu bất sản, thiếu máu tái tạo đã được xác định như là độc tính liều giới hạn ở các loài gặm nhấm dùng MPA. Đánh giá về tủy đồ chỉ ra sự giảm đáng kể trong các tế bào hồng cầu (nguyên hồng cầu đa sắc và nguyên hồng cầu có nhân kết đặc) và lách to phụ thuộc liều và tăng tạo máu ngoài tủy xương. Các tác dụng này xảy ra ở mức độ tiếp xúc toàn thân tương đương hoặc thấp hơn mức tiếp xúc lâm sàng với liều khuyến cáo Myfortic 1,44 g/ngày ở bệnh nhân ghép thận.
Dữ liệu độc tính phi lâm sàng của natri mycophenolat cũng nhất quán với các tác dụng bất lợi quan sát được ở người tiếp xúc với MPA, điều này cung cấp tài liệu an toàn có liên quan nhiều hơn đến nhóm bệnh nhân (xem mục Tác dụng ngoại ý).
Những liều uống một lần của MPA dung nạp khá tốt ở chuột cống (LD50 từ 350 đến 700 mg/kg), dung nạp tốt ở chuột nhắt hoặc khỉ (LD50 lớn hơn 1.000 mg/kg), và dung nạp cực kỳ tốt ở thỏ (LD50 lớn hơn 6.000 mg/kg).
Trong một nghiên cứu khả năng gây quái thai tiến hành với natri mycophenolat ở chuột cống, một liều thấp 1 mg/kg đã gây ra dị dạng cho các con chuột con, như tật không nhãn cầu, não ngoài hộp sọ và thoát vị rốn. Sự tiếp xúc toàn thân ở liều này chỉ bằng 0,05 lần sự tiếp xúc lâm sàng ở liều Myfortic 1,44 g/ngày (xem mục Sử dụng ở phụ nữ có thai và cho con bú). Trong một nghiên cứu trước và sau khi sinh ở chuột cống, acid mycophenolic (dạng muối natri) đã gây ra chậm phát triển (phản xạ đồng tử bất thường ở chuột cái và tách bao quy đầu ở chuột đực) tại liều cao nhất 3 mg/kg.
Chỉ định/Công dụng
Myfortic được chỉ định dùng phối hợp với ciclosporin dạng vi nhũ tương và corticosteroid để dự phòng sự thải loại mảnh ghép cấp tính ở bệnh nhân ghép thận dị gen.
Liều lượng & Cách dùng
Liều lượng: Liều được khuyến cáo là 720 mg (4 viên Myfortic không tan trong dạ dày loại 180 mg hoặc 2 viên loại 360 mg), ngày 2 lần (liều mỗi ngày 1.440 mg). Ở bệnh nhân đang dùng mycophenolate mofetil (MMF) 2 g, việc điều trị có thể được thay bằng 720 mg Myfortic ngày 2 lần (liều mỗi ngày 1.440 mg).
Đối tượng mục tiêu chung: Việc điều trị với Myfortic cần được bắt đầu và duy trì bởi các chuyên gia về cấy ghép có trình độ thích hợp.
Việc điều trị với Myfortic cần được bắt đầu điều trị ở bệnh nhân mới ghép trong vòng 48 giờ sau khi cấy ghép.
Myfortic có thể được uống cùng với thức ăn hoặc không.
Đối tượng đặc biệt
+ Suy thận: Không cần phải điều chỉnh liều ở bệnh nhân đang trải qua thời kỳ chức năng thận ghép chậm hoạt động sau phẫu thuật (xem mục Dược động học). Bệnh nhân bị suy thận mạn tính nặng (tốc độ lọc cầu thận < 25mL/phút/1,73m2) cần được theo dõi cẩn thận.
+ Suy gan: Không cần phải điều chỉnh liều đối với bệnh nhân ghép thận bị bệnh nhu mô gan nặng.
+ Trẻ em: Tính an toàn và hiệu quả ở bệnh nhi còn chưa được xác định. Các tài liệu dược động học hiện có đối với các bệnh nhi ghép thận còn hạn chế (xem mục Cơ chế tác dụng, Dược động học).
+ Người cao tuổi: Không cần phải điều chỉnh liều trong nhóm các bệnh nhân này.
Điều trị trong các đợt thải loại: Việc thải loại thận ghép không làm thay đổi dược động học của acid mycophenolic (MPA) nên không cần giảm liều hoặc ngừng dùng Myfortic.
Cách dùng: Không nên nghiền nát viên thuốc Myfortic để duy trì tính nguyên vẹn của màng bao tan trong ruột (xem phần Cơ chế tác dụng, Dược động học).
Cảnh báo
Thuốc này chỉ dùng theo sự kê đơn của bác sĩ.
Bệnh nhân bị thiếu hụt hypoxanthin-guanin-phosphoribosyl-transferase (HGPRT) di truyền hiếm gặp: Myfortic là một chất ức chế IMPDH (inosin monophosphat dehydrogenase). Do đó, về mặt lý thuyết, cần tránh dùng cho bệnh nhân bị thiếu hụt hypoxanthin-guanin-phosphoribosyl-transferase (HGPRT) do di truyền hiếm gặp như hội chứng Lesch-Nyhan và Kelly-Seegmiller.
Phụ nữ có khả năng mang thai (WOCBP), có thai và nuôi con bú: Dùng Myfortic trong khi có thai thường làm tăng nguy cơ sẩy thai bao gồm sẩy thai tự nhiên và dị dạng bẩm sinh. Việc điều trị Myfortic không nên bắt đầu ở phụ nữ có khả năng mang thai cho đến khi có kết quả xét nghiệm thai âm tính. Thông tin về dùng thuốc trong khi có thai và cần phải ngừa thai, xem mục Sử dụng ở phụ nữ có thai và cho con bú.
Không nên dùng Myfortic trong quá trình nuôi con bú (xem mục Sử dụng ở phụ nữ có thai và cho con bú).
Các bệnh ác tính: Bệnh nhân điều trị các thuốc ức chế miễn dịch phối hợp bao gồm cả Myfortic làm tăng nguy cơ phát triển các u lympho và các bệnh ác tính khác, đặc biệt là ở da (xem mục Tác dụng ngoại ý). Nguy cơ xuất hiện có liên quan đến cường độ và thời gian dùng thuốc ức chế miễn dịch hơn là do dùng một chất đặc trưng nào. Lời khuyên chung để làm giảm nguy cơ ung thư da là nên hạn chế tiếp xúc với ánh nắng mặt trời, đèn tử ngoại bằng cách mặc quần áo bảo hộ và dùng chất chống nắng có chỉ số bảo vệ cao.
Nhiễm khuẩn: Bệnh nhân dùng Myfortic cần được hướng dẫn là phải thông báo ngay lập tức khi có bất cứ biểu hiện nhiễm khuẩn nào, vết thâm tím bất thường, xuất huyết hoặc bất cứ biểu hiện nào của suy tuỷ xương.
Ức chế quá mức hệ miễn dịch làm tăng sự nhạy cảm với nhiễm trùng, kể cả nhiễm trùng cơ hội, nhiễm trùng gây tử vong và nhiễm trùng huyết (xem phần Tác dụng ngoại ý).
Tái hoạt bệnh viêm gan B (HBV) hoặc viêm gan C (HCV) đã được báo cáo ở những bệnh nhân được điều trị ức chế miễn dịch, bao gồm cả acid Mycophenolic (MPA) dẫn chất của Myfortic và MMF. Khuyến cáo theo dõi bệnh nhân bị nhiễm về các dấu hiệu lâm sàng và xét nghiệm của nhiễm HBV hoặc HCV hoạt động.
Những trường hợp bệnh lý chất trắng não đa ổ tiến triển (PML), đôi khi gây tử vong, đã được báo cáo ở bệnh nhân được điều trị bằng các dẫn chất MPA trong đó bao gồm cả mycophenolate mofetil và natri mycophenolate (xem phần Tác dụng ngoại ý). Những trường hợp đã báo cáo thường có các yếu tố nguy cơ bị PML gồm điều trị các thuốc ức chế miễn dịch và tổn thương chức năng miễn dịch. Ở bệnh nhân bị ức chế miễn dịch, thầy thuốc cần lưu ý đến PML trong chẩn đoán phân biệt cho bệnh nhân có các triệu chứng thần kinh và nên xem xét việc hội chẩn với bác sĩ chuyên khoa thần kinh khi có chỉ định trên lâm sàng. Bệnh thận do virut Polyoma (PVAN), đặc biệt là do nhiễm virut BK, phải được tính đến trong chẩn đoán phân biệt ở những bệnh nhân bị suy giảm miễn dịch kèm theo chức năng thận bị suy (xem Tác dụng ngoại ý). Cần xem xét giảm tổng lượng thuốc ức chế miễn dịch ở bệnh nhân phát triển PML hoặc PVAN. Tuy nhiên ở những bệnh nhân cấy ghép, giảm ức chế miễn dịch có thể gây nguy cơ cho mô ghép.
Các bệnh về máu: Bệnh nhân dùng Myfortic nên được theo dõi kiểm tra các rối loạn về tạo máu (ví dụ như giảm bạch cầu trung tính hoặc thiếu máu - xem Tác dụng ngoại ý), điều này có thể liên quan đến chính MPA, dùng các thuốc phối hợp, nhiễm trùng do vi khuẩn hoặc do một số kết hợp của những nguyên nhân này. Bệnh nhân dùng Myfortic phải kiểm tra công thức máu toàn phần hàng tuần trong tháng đầu điều trị, 2 lần/tháng trong tháng thứ hai và tháng thứ ba điều trị, sau đó mỗi tháng 1 lần trong năm đầu tiên. Nếu có các rối loạn về máu (ví dụ như giảm bạch cầu trung tính với tổng số bạch cầu trung tính < 1,5x103/microL hoặc thiếu máu) nên tạm ngừng hoặc ngừng hẳn việc điều trị bằng Myfortic.
Các trường hợp bị bất sản hồng cầu đơn thuần (PRCA) đã được báo cáo ở những bệnh nhân điều trị bằng các dẫn chất MPA kết hợp với các thuốc ức chế miễn dịch khác (xem phần Tác dụng ngoại ý). Cơ chế của các dẫn chất MPA gây ra PRCA chưa được biết đến; mối liên quan của các thuốc ức chế miễn dịch khác và sự kết hợp của các thuốc này trong một phác đồ điều trị ức chế miễn dịch cũng chưa được biết đến. Tuy nhiên, các dẫn chất MPA có thể gây ra các rối loạn về máu (xem phía trên). Trong một số trường hợp bị PRCA nhận thấy có sự phục hồi khi giảm liều hoặc tạm dừng trị liệu với các dẫn chất MPA. Tuy nhiên ở những bệnh nhân cấy ghép, giảm ức chế miễn dịch có thể gây nguy cơ cho mô ghép. Những thay đổi với trị liệu Myfortic trên người nhận ghép chỉ nên được tiến hành dưới sự giám sát thích hợp nhằm giảm đến mức tối thiểu nguy cơ thải mảnh ghép.
Tiêm chủng: Bệnh nhân cần được khuyên rằng trong thời gian điều trị bằng MPA thì việc tiêm chủng có thể ít hiệu quả và nên tránh tiêm vắc xin sống giảm độc lực (xem mục Tương tác thuốc). Việc tiêm chủng vắc xin cúm có thể đạt được hiệu quả. Thầy thuốc nên tham khảo hướng dẫn quốc gia về tiêm chủng vắc xin cúm.
Rối loạn dạ dày ruột: Do các dẫn chất của MPA có liên quan đến tăng tỉ lệ các tác dụng có hại trên hệ tiêu hoá, bao gồm các ca hiếm gặp loét và xuất huyết và thủng đường tiêu hoá; nên phải cẩn thận khi dùng Myfortic cho bệnh nhân đang mắc bệnh hệ tiêu hóa nặng tiến triển.
Phối hợp với các thuốc khác: Trong các thử nghiệm lâm sàng Myfortic đã được dùng phối hợp với các thuốc sau đây: globulin kháng tế bào tuyến giáp, basiliximab, ciclosporin dạng vi nhũ tương và corticosteroid. Hiệu quả và tính an toàn của Myfortic khi phối hợp với các thuốc ức chế miễn dịch khác chưa được nghiên cứu.
Quá Liều
Đã có các báo cáo ngẫu nhiên về quá liều vô tình hoặc cố ý với Myfortic, trong khi không phải tất cả các bệnh nhân có liên quan đến tác dụng bất lợi.
Trong những trường hợp quá liều mà có tác dụng bất lợi đã được báo cáo, các tác dụng bất lợi này rơi vào nhóm đặc tính an toàn đã biết. Quá liều Myfortic có thể gây nên sự quá ức chế hệ miễn dịch và có thể làm tăng nhạy cảm với nhiễm khuẩn bao gồm nhiễm khuẩn cơ hội, nhiễm khuẩn gây tử vong và nhiểm khuẩn huyết. Nếu xảy ra các rối loạn về máu (ví dụ như giảm bạch cầu trung tính với số lượng bạch cầu trung tính tuyệt đối < 1,5x103/microL hay thiếu máu), có thể tạm ngừng hoặc dừng điều trị bằng Myfortic (xem phần Cảnh báo và phần Tác dụng ngoại ý).
Mặc dù thẩm tách có thể được dùng để loại bỏ chất chuyển hoá không có hoạt tính MPAG, nhưng không chắc rằng có thể loại bỏ được những lượng có ý nghĩa về lâm sàng của một nửa số MPA có hoạt tính. Chất này chiếm một lượng lớn do sự gắn kết với protein huyết tương rất cao của MPA, 97%. Bằng cách can thiệp vào tuần hoàn ruột-gan của MPA, dùng chất liên kết với acid mật như cholestyramin có thể làm giảm sự tiếp xúc toàn thân MPA.
Chống chỉ định
Myfortic chống chỉ định ở bệnh nhân mẫn cảm với natri mycophenolat, acid mycophenolic hoặc mycophenolate mofetil hoặc với bất cứ tá dược nào.
Sử dụng ở phụ nữ có thai và cho con bú
Việc điều trị Myfortic không nên bắt đầu ở phụ nữ có khả năng mang thai cho đến khi có kết quả xét nghiệm thai âm tính.
Phụ nữ có khả năng mang thai phải sử dụng biện pháp tránh thai hiệu quả cao trước khi bắt đầu, trong quá trình điều trị Myfortic và sau 6 tuần sau khi dùng liều Myfortic cuối cùng (xem phần Tương tác thuốc).
• Phụ nữ có thai: Dùng Myfortic trong thời kỳ có thai làm tăng nguy cơ dị dạng bẩm sinh. Mặc dù còn chưa có những nghiên cứu đầy đủ và có kiểm soát tốt ở phụ nữ có thai dùng Myfortic, nhưng dựa trên tài liệu của chương trình Đăng ký Quốc gia về ghép cơ quan cho người mang thai của Mỹ (NTPR), dùng mycophenolate mofetil phối hợp với thuốc ức chế miễn dịch trong thời kỳ có thai có liên quan với tăng tỷ lệ dị dạng bẩm sinh lên 22% (4 trường hợp trong số 18 trẻ sinh ra có phơi nhiễm), so với tỷ lệ 4-5% dị dạng trong số những bệnh nhân cấy ghép quan sát được ở NTPR. Các dị dạng bẩm sinh đã được báo cáo với mycophenolate mofetil gồm có bất thường tai ngoài và các bất thường khác ở mặt bao gồm khe hở môi và vòm miệng, thoát vị hoành bẩm sinh, dị thường chi dưới, tim, thực quản và thận. Việc sử dụng mycophenolate mofetil trong quá trình mang thai cũng đã được báo cáo là có liên quan đến tăng nguy cơ sẩy thai tự nhiên. Do MMF chuyển thành MPA sau khi uống hoặc tiêm tĩnh mạch, các nguy cơ nói trên cũng phải được lưu ý với Myfortic. Khả năng sinh quái thai của MPA đã được ghi nhận trong các nghiên cứu ở động vật (xem mục Dữ liệu an toàn phi lâm sàng).
Myfortic chỉ được dùng cho phụ nữ có thai nếu cân nhắc thấy lợi ích cho mẹ hơn hẳn nguy cơ cho thai. Cần hướng dẫn bệnh nhân đến khám thầy thuốc ngay nếu xảy ra có thai.
• Phụ nữ nuôi con bú: Còn chưa biết liệu MPA có bài tiết được vào sữa mẹ hay không.
Không nên dùng Myfortic trong thời kỳ nuôi con bú (xem phần Cảnh báo).
Vì nhiều thuốc được bài tiết vào sữa mẹ, và vì khả năng bị các tác dụng bất lợi nghiêm trọng ở trẻ sơ sinh bú mẹ/trẻ nhỏ, cần phải quyết định xem nên tránh cho con bú trong khi điều trị và trong 6 tuần sau khi ngừng điều trị hay tránh sử dụng thuốc, lưu ý tới tầm quan trọng của thuốc đối với người mẹ.
• Bệnh nhân nam: Nam giới có khả năng hoạt động tình dục nên sử dụng bao cao su trong thời gian điều trị, và trong trọn 13 tuần sau liều Myfortic cuối cùng. Ngoài ra, bạn tình của những người đàn ông này nên sử dụng biện pháp tránh thai có hiệu quả cao trong quá trình điều trị và trong trọn 13 tuần sau liều Myfortic cuối.
Tương tác
Các tương tác quan sát được từ việc sử dụng đồng thời không khuyến cáo
+ Azathioprin: Không khuyến cáo dùng Myfortic đồng thời với azathioprin vì việc dùng đồng thời như vậy còn chưa được nghiên cứu (xem mục Cảnh báo).
+ Vắc xin sống: Vắc xin sống không được dùng cho bệnh nhân đáp ứng miễn dịch bị tổn thương. Đáp ứng kháng thể đối với các vắc xin khác có thể bị giảm (xem mục Cảnh báo).
Các tương tác đã quan sát thấy cần được xem xét
+ Aciclovir: Các nồng độ cao hơn trong huyết tương của cả MPAG (glucuronid của acid mycophenolic) và aciclovir có thể xảy ra khi có suy thận. Do đó, hai thuốc này có khả năng cạnh tranh bài tiết ở ống thận, làm tăng thêm nồng độ của cả MPAG và aciclovir. Trong tình huống này, bệnh nhân cần được theo dõi cẩn thận.
+ Các thuốc bảo vệ dạ dày:
· Các thuốc kháng acid chứa magie và nhôm hydroxide: Sự hấp thu natri mycophenolat bị giảm khi dùng với thuốc kháng acid. Dùng đồng thời Myfortic và thuốc kháng acid có magie và nhôm hydroxyd làm giảm 37% sự tiếp xúc của cơ thể với MPA và giảm 25% nồng độ tối đa của MPA. Cần dùng thận trọng khi phối hợp với thuốc kháng acid (chứa magie và nhôm hydroxyd) với Myfortic.
· Các thuốc ức chế bơm proton: Ở những người tình nguyện khỏe mạnh, dùng đồng thời MMF 1.000 mg và pantoprazole 40 mg 2 lần/ngày dẫn đến giảm 27% AUC của MPA và giảm 57% Cmax của MPA. Tuy nhiên, trong cùng một nghiên cứu, không quan sát thấy những thay đổi về dược động học của MPA khi dùng đồng thời Myfortic và pantoprazole.
+ Ganciclovir: Dược động học của MPA và MPAG không bị ảnh hưởng khi dùng thêm ganciclovir. Độ thanh thải của ganciclovir không thay đổi trong tình huống có tiếp xúc MPA trong điều trị. Tuy nhiên, ở bệnh nhân bị suy thận, dùng phối hợp Myfortic và ganciclovir, những khuyến cáo về liều ganciclovir là nên kiểm soát và theo dõi bệnh nhân cẩn thận.
+ Tacrolimus: Trong một nghiên cứu chuyển nhóm chéo dùng calcineurin ở bệnh nhân ghép thận đã ổn định, dược động học Myfortic ở trạng thái ổn định đã được đo trong điều trị với cả Neoral và tacrolimus. AUC trung bình của MPA cao hơn 19% và Cmax thấp hơn khoảng 20%. Ngược lại, AUC trung bình của MPAG và Cmax thấp hơn khoảng 30% khi điều trị với tacrolimus so với khi điều trị Neoral.
+ Ciclosporin A: Nghiên cứu ở bệnh nhân ghép thận đã ổn định, dược động học của ciclosporin A không bị ảnh hưởng bởi liều dùng ở trạng thái ổn định của Myfortic.
Các tương tác dự kiến được xem xét
+ Cholestyramin và thuốc gây ảnh hưởng tuần hoàn ruột-gan: Do khả năng phong bế vòng tuần hoàn ruột-gan của thuốc, cholestyramin có thể làm giảm sự tiếp xúc toàn thân của MPA. Cần dùng thận trọng khi phối hợp cholestyramin hoặc các thuốc gây cản trở tuần hoàn ruột-gan vì có thể làm giảm hiệu lực của Myfortic.
+ Thuốc tránh thai dạng uống: Các thuốc tránh thai dùng đường uống bị chuyển hoá theo con đường oxy hoá trong khi Myfortic lại chuyển hoá theo con đường glucuronid hoá. Tác dụng có ý nghĩa lâm sàng của thuốc tránh thai dạng uống trên dược động học của Myfortic không được tiên liệu trước. Tuy nhiên, vẫn chưa biết ảnh hưởng của việc dùng Myfortic lâu dài trên dược động học của các thuốc tránh thai dạng uống, có thể là hiệu quả của thuốc tránh thai dạng uống có lẽ bị ảnh hưởng theo hướng bất lợi (xem mục Sử dụng ở phụ nữ có thai và cho con bú).
Tương kỵ
Chưa thấy.
Tác dụng ngoại ý
Tóm tắt về tính an toàn: Các tác dụng không mong muốn sau bao gồm các phản ứng có hại của thuốc từ 2 thử nghiệm lâm sàng có đối chứng. Thử nghiệm đánh giá tính an toàn của Myfortic và mycophenolate mofetil ở 423 trường hợp ghép mới và 322 bệnh nhân ghép thận trong giai đoạn duy trì (ngẫu nhiên 1:1); tỷ lệ các tác dụng bất lợi là tương tự nhau giữa các trị liệu trong mỗi nhóm.
Các phản ứng bất lợi của thuốc rất thường gặp (≥ 10%) khi dùng Myfortic phối hợp với ciclosporin dạng vi nhũ tương và với corticosteroid là giảm bạch cầu và tiêu chảy.
Bệnh ác tính: Bệnh nhân điều trị các thuốc ức chế miễn dịch phối hợp, bao gồm cả MPA thì làm tăng nguy cơ phát triển các u lympho và các bệnh ác tính khác, đặc biệt hay gặp trên da (xem mục Cảnh báo). Tỷ lệ chung các bệnh ác tính quan sát được trong các thử nghiệm lâm sàng với Myfortic là như sau: bệnh tăng sinh lympho hoặc u lympho xuất hiện ở 2 bệnh nhân mới (0,9%) và 2 bệnh nhân trong giai đoạn duy trì (1,3%) dùng Myfortic được trên 1 năm; carcinom da không thuộc u hắc bào là 0,9% bệnh nhân mới và 1,8% bệnh nhân đang dùng duy trì Myfortic được trên 1 năm; các loại bệnh ác tính khác gặp ở 0,5% bệnh nhân mới và 0,6% bệnh nhân trong giai đoạn duy trì.
Các bệnh nhiễm trùng cơ hội: Tất cả bệnh nhân ghép đều bị tăng nguy cơ mắc bệnh nhiễm trùng cơ hội; nguy cơ tăng cao cùng với tổng liều thuốc ức chế miễn dịch (xem mục Cảnh báo). Các bệnh nhiễm trùng cơ hội thường gặp nhất ở bệnh nhân ghép thận mới dùng Myfortic phối hợp với các thuốc ức chế miễn dịch khác trong thử nghiệm lâm sàng có đối chứng của các bệnh nhân ghép thận được theo dõi trong 1 năm là CMV, bệnh nấm Candida và bệnh Herpes. Tỷ lệ chung của nhiễm CMV (trong huyết thanh, nhiễm vi rút huyết hoặc bệnh CMV) quan sát thấy trong thử nghiệm lâm sàng với Myfortic được báo cáo ở 21,6% bệnh nhân ghép thận mới và 1,9% trong giai đoạn duy trì.
Bảng tóm tắt các phản ứng bất lợi của thuốc từ các nghiên cứu lâm sàng: Các phản ứng bất lợi (Bảng 4) được xếp loại dưới tiêu đề của tần suất, đầu tiên là tần suất thường gặp nhất, sử dụng quy ước sau: rất thường gặp (≥ 1/10); thường gặp (≥ 1/100, < 1/10); ít gặp (≥ 1/1.000, < 1/100); hiếm gặp (≥ 1/10.000, < 1/1.000) rất hiếm gặp (< 1/10.000), bao gồm các báo cáo riêng lẻ. Trong mỗi nhóm tần suất, các phản ứng bất lợi được xếp loại theo thứ tự mức độ nghiêm trọng giảm dần.
Bảng 4 dưới đây bao gồm các phản ứng có hại do thuốc có thể hoặc hầu như chắc chắn có liên quan đến Myfortic được báo cáo trong 2 thử nghiệm lâm sàng đa trung tâm có đối chứng, mù đôi, ngẫu nhiên giai đoạn III: 1 là ở các bệnh nhân mới ghép thận và 1 là ở các bệnh nhân ghép thận trong giai đoạn duy trì, trong đó Myfortic được dùng liều 1.440 mg/ngày trong 12 tháng, cùng với ciclosporin dạng vi nhũ tương và corticosteroid. Bảng này được biên soạn theo phân loại cơ quan theo hệ thống Med DRA.
- xem Bảng 4.
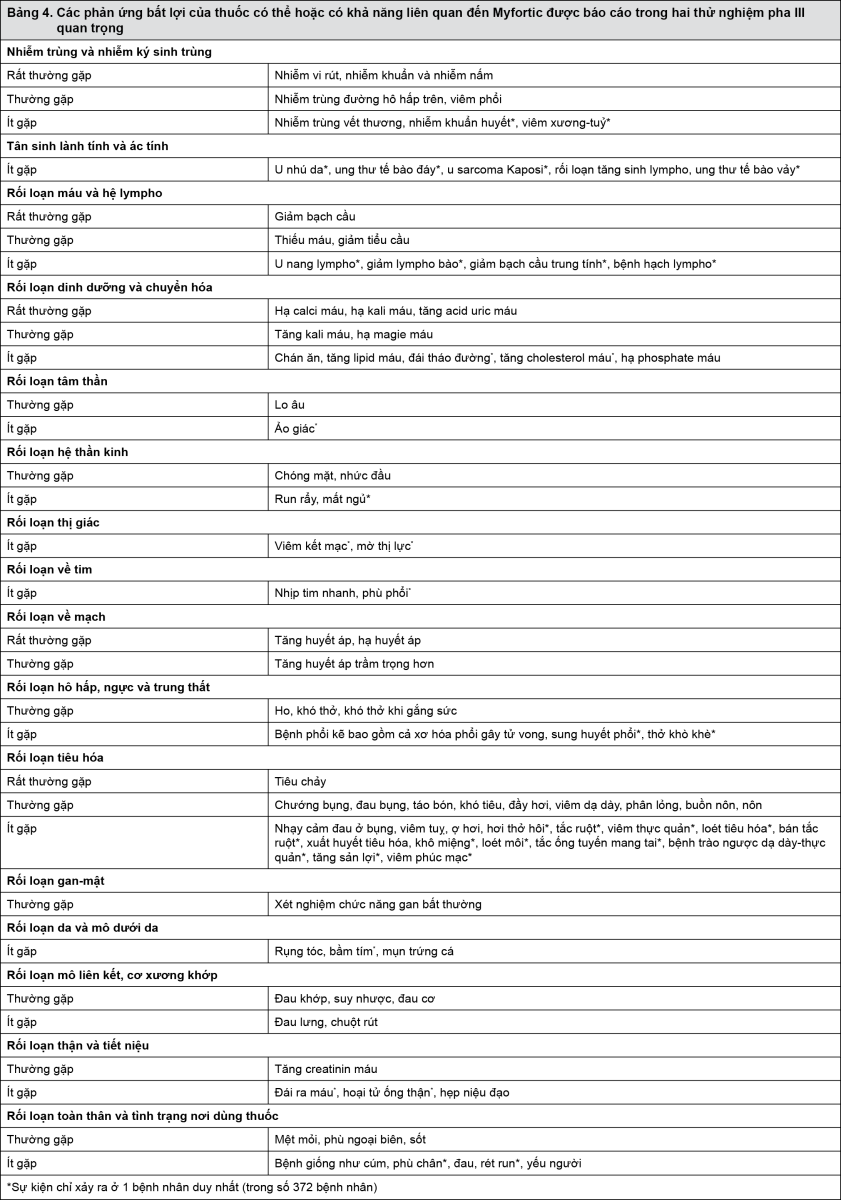
Ghi chú: Bệnh nhân ghép thận được điều trị 1.440 mg Myfortic mỗi ngày cho đến 1 năm. Kết quả thu được tương tự nhau ở nhóm dùng thuốc ngay lúc mới ghép (de novo) và nhóm dùng trong giai đoạn duy trì sau ghép, mặc dù tỷ lệ có khuynh hướng thấp hơn ở các bệnh nhân trong giai đoạn duy trì.
Danh sách các phản ứng bất lợi sau khi lưu hành: Các phản ứng bất lợi của thuốc sau đây từ nguồn kinh nghiệm hậu tiếp thị Myfortic thông qua các báo cáo tự phát và các trường hợp y văn. Vì các phản ứng này được báo cáo tự nguyện từ một nhóm dân số có quy mô không biết rõ nên không thể ước tính tần suất của nó một cách đáng tin cậy, vì thế phân loại là không rõ. Các phản ứng bất lợi của thuốc được liệt kê dựa vào hệ phân loại cơ quan trong MedDRA. Trong mỗi lớp hệ cơ quan, các phản ứng bất lợi của thuốc được trình bày theo thứ tự mức độ nghiêm trọng giảm dần.
- Rối loạn về da và mô dưới da: Phát ban đã được nhận biết như là một phản ứng bất lợi từ các thử nghiệm lâm sàng sau khi được duyệt, khảo sát sau khi lưu hành và các báo cáo tự phát.
- Các tác dụng bất lợi sau đây được quy cho các dẫn chất MPA như là tác dụng của nhóm:
+ Nhiễm trùng và nhiễm ký sinh trùng: Các bệnh nhiễm trùng nặng, đôi khi đe dọa đến tính mạng, bao gồm viêm màng não, viêm nội tâm mạc do nhiễm trùng, bệnh lao và nhiễm Mycobacterium không điển hình. Bệnh thận do virut Polyma (PVAN), đặc biệt là do nhiễm virut BK. Những trường hợp bệnh lý chất não trắng đa ổ tiến triển (PML) đôi khi gây tử vong đã được báo cáo (xem mục Cảnh báo).
+ Các rối loạn về máu và hệ bạch huyết: Mất bạch cầu hạt, giảm bạch cầu trung tính, giảm toàn bộ các loại huyết cầu. Các trường hợp bị bất sản hồng cầu đơn thuần (PRCA) đã được báo cáo ở những bệnh nhân điều trị bằng các dẫn chất MPA kết hợp với các thuốc ức chế miễn dịch khác (xem phần Cảnh báo).
+ Các rối loạn về dạ dày ruột: Viêm kết tràng, viêm thực quản (kể cả viêm kết tràng và viêm thực quản do CMV), viêm dạ dày do CMV, viêm tụy, thủng ruột, xuất huyết tiêu hóa, loét dạ dày, loét tá tràng, tắc ruột.
Bệnh nhân cao tuổi: Nói chung, các bệnh nhân cao tuổi có thể bị tăng nguy cơ các phản ứng có hại do thuốc ức chế miễn dịch. Các bệnh nhân cao tuổi dùng Myfortic như là một phần trong phác đồ ức chế miễn dịch phối hợp không biểu hiện tăng nguy cơ các tác dụng bất lợi so với người trẻ trong thử nghiệm lâm sàng với Myfortic.
Bảo quản
Bảo quản ở điều kiện không quá 30oC, trong bao bì kín, tránh ẩm.
Phân loại ATC
L04AA06
- Abacavir
- Abernil
- Abiiogran
- Acarbose
- ACC
- Acebutolol
- Acenocoumarol
- Acetate Ringer's
- Acetazolamide
- Acetylcystein
- Acetylsalicylic acid
- Aciclovir
- Acid acetylsalicylic
- Acid aminocaproic
- Acid ascorbic
- Acid boric
- Acid chenodeoxycholic
- Acid ethacrynic
- Acid folic
- Acid fusidic
- Acid iopanoic
- Acid ioxaglic
- Acid nalidixic
- Acid pantothenic
- Acid para-aminobenzoic
- Acid salicylic
- Acid tranexamic
- Acid valproic
- Acid zoledronic
- Acitretin
- Aclasta
- Aclon
- Actapulgite
- Actelsar
- Actelsar HCT
- Actemra
- Actilyse
- Acular
- Acupan
- Acuvail
- Acyclovir STADA
- Acyclovir STADA Cream
- Adalat
- Adenosin
- Adenosin Ebewe
- Adipiodon
- Advagraf
- Aerius
- Afinitor
- Agicarvir
- Agifovir-E
- Agilosart
- Agilosart-H
- Agimepzol
- Agimosarid
- Agimstan
- Agimstan-H
- Agiremid
- Agivastar
- Aibezym
- Air-X
- Alaxan
- Albendazol
- Albiomin
- Albumin
- Albumin người Grifols 20%
- Albuminar
- AlbuRx
- Albutein
- Alcuronium chloride
- Aldesleukin
- Alendronat
- Alertin
- Alfa-Lipogamma 600 Oral
- Alfuzosin hydrochlorid
- Algotra
- Alimemazin
- Alimta
- Allipem
- Allopurinol
- Allopurinol STADA
- Aloxi
- Alprazolam
- Alpha Chymotrypsin
- Alpha tocopherol
- Alphachymotrypsin Glomed
- Alphagan-P
- Aluvia
- Alzental
- Amaryl
- Ambroco
- Ambroxol
- Amcinol-Paste
- Amigold
- Amikacin
- Aminocaproic acid
- Aminoleban
- Aminoleban Oral
- Aminosteril N-Hepa
- Amiparen
- Amitriptyline
- Amiyu
- Amlodipine
- Amlor
- Amoxicillin
- Amoxicillin & clavulanate
- Ampicillin
- Amquitaz
- Anaferon for children
- Anargil
- Anaropin
- Andriol Testocaps
- Anepzil
- Anyfen
- Apaisac
- Apidra SoloStar
- Apitim 5
- Aprovel
- Aquaphil
- Arcalion
- Arcoxia
- Aricept Evess
- Arimidex
- Arnetine
- Artrodar
- A-Scabs
- Ascorbic acid
- Asperlican/Candinazol
- Aspilets EC
- Aspirin
- Asthmatin
- Atelec
- Atocib 120
- Atocib 90
- Atosiban PharmIdea
- Atozet
- Attapulgite
- Atussin
- Atropin
- Augbactam
- Augmentin Sachet
- Augmentin SR
- Augmentin Tablets
- Augmex
- Avamys
- Avastin
- Avelox Dịch truyền
- Avelox Viên nén
- Avodart
- Axcel Cefaclor-125 Suspension
- Axcel Cetirizine Syrup
- Axcel Chlorpheniramine
- Axcel Dexchlorpheniramine
- Axcel Dicyclomine-S Syrup
- Axcel Diphenhydramine Paediatric Syrup
- Axcel Erythromycin ES
- Axcel Eviline
- Axcel Fungicort Cream
- Axcel Fusidic acid Cream
- Axcel Fusidic acid-B Cream
- Axcel Hydrocortisone Cream
- Axcel Lignocaine 2% Sterile Gel
- Axcel Loratadine
- Axcel Miconazole Cream
- Axcel Paracetamol
- Axcel Urea Cream
- Axitan
- Azenmarol
- Azicine
- Aziphar
- Azithromycin





