Nhà sản xuất
Merck Sharp & Dohme
Thành phần
Mỗi liều 0.5mL: Protein L1 HPV týp 6 20mcg, protein L1 týp 11 40mcg, protein L1 HPV týp 16 40mcg, protein L1 týp 18 20mcg.
Cơ chế tác dụng
GARDASIL chứa protein L1 VLP (virus like particles, mẫu giống vi-rút), là những protein tương tự như những vi-rút gây nhiễm tự nhiên. Do những mẫu giống vi-rút không chứa DNA của vi-rút, chúng không thể gây nhiễm tế bào hay sinh sản.
Trong nghiên cứu tiền lâm sàng, kháng thể kháng vi-rút do cảm ứng vắc-xin L1 VLP có kết quả bảo vệ ngừa nhiễm bệnh. Tiêm huyết thanh của động vật đã chủng ngừa vào động vật chưa được chủng ngừa dẫn đến sự bảo vệ kháng HPV được truyền sang động vật chưa được chủng ngừa. Những dữ liệu này gợi ý hiệu lực của vắc-xin chứa L1 VLP có được thông qua trung gian của đáp ứng miễn dịch dịch thể.
Dược lực học
* Gánh nặng bệnh lý:
Trên toàn cầu, hơn 490.000 trường hợp ung thư cổ tử cung được chẩn đoán hàng năm. Chiến lược ngừa ung thư cổ tử cung tập trung vào việc tầm soát lặp lại (như làm xét nghiệm Papanicolaou [Pap] và/hoặc xét nghiệm tìm vi-rút sinh u nhú ở người [HPV]) và can thiệp sớm. Chiến lược này đã làm giảm tỷ lệ ung thư gần 75% tại các nước đã phát triển nhưng đã chuyển gánh nặng từ quản lý ung thư cổ tử cung sang giám sát và điều trị một số lớn các tổn thương tiền ác tính.
Nguyên nhân ung thư cổ tử cung là do nhiễm vi-rút sinh u nhú ở người (HPV) kéo dài. Nhiễm HPV kéo dài là yếu tố thiết yếu để phát triển thành ung thư biểu mô tế bào gai cổ tử cung (và những tổn thương tiền ung thư như là tân sinh nội biểu mô cổ tử cung [CIN] 1 và CIN 2/3) và ung thư biểu mô tuyến cổ tử cung (và tiền tổn thương là ung thư biểu mô tuyến cổ tử cung tại chỗ [AIS]). HPV cũng gây ung thư âm hộ và âm đạo và tổn thương tiền ung thư như tân sinh trong biểu mô âm hộ (VIN) và tân sinh trong biểu mô âm đạo (VaIN).
Nhiễm HPV rất phổ biến. Trong trường hợp không tiêm ngừa, trên 50% người trưởng thành có sinh hoạt tình dục sẽ nhiễm HPV trong đời. Đa số trường hợp nhiễm HPV sẽ được loại trừ mà không để lại di chứng nào tuy nhiên một vài trường hợp sẽ tiến triển đến ung thư cổ tử cung. Nhiễm HPV týp 6, 11, 16, và 18 có thể sẽ đưa đến kết quả bất thường khi xét nghiệm Pap và sang thương loạn sản mức độ thấp (CIN 1, VIN 1, và VaIN 1). Sang thương liên quan đến HPV 6 và HPV 11 chưa hẳn tiến triển đến ung thư nhưng không thể phân biệt được trên lâm sàng sang thương tiền ung thư gây ra do HPV 16 và HPV 18.
Nhiễm HPV 16 và HPV 18 là nguyên nhân gây ra 70% các trường hợp ung thư hậu môn và dương vật và tiền sang thương của chúng.
Nhiễm HPV 6 và HPV 11 cũng gây mụn cóc sinh dục (mào gà sinh dục), đó là các khối u sùi hiếm khi tiến triển đến ung thư của niêm mạc cổ tử cung âm đạo, âm hộ và vùng chung quanh hậu môn và bộ phận sinh dục ngoài. Nguy cơ nhiễm mụn cóc sinh dục trong cuộc đời ước chừng hơn 10%. Tỷ lệ mới mắc tổn thương này thường tương đương nhau ở cả nam và nữ.
Đa bướu gai hô hấp tái diễn (Recurrent Respiratory Papillomatosis: RRP), một bệnh lý ở trẻ em và người lớn cũng do nhiễm HPV 6 và HPV 11. Đặc điểm của RRP là các bướu gai phát triển tái phát ở đường hô hấp. Tại Hoa Kỳ, mỗi năm có khoảng 5900 trường hợp được chẩn đoán. Để điều trị cần phải lặp lại phẫu thuật nhiều lần.
GARDASIL là vắc-xin tái tổ hợp chứa các protein L1 giống HPV týp 6, 11, 16, và 18.
HPV týp 16 và 18 gây ra gần:
- 70% trường hợp ung thư cổ tử cung, AIS, CIN 3;
- 50% trường hợp CIN 2; và
- 70% trường hợp ung thư âm hộ và âm đạo liên quan đến HPV, VIN 2/3, và VaIN 2/3
HPV týp 6, 11 và 18 gây ra gần:
- 35-50% tất cả trường hợp CIN 1, VIN 1, và VaIN 1
HPV týp 6 và 11 gây ra gần:
- 90% trường hợp mào gà (mụn cóc) sinh dục và RRP (đa bướu gai hô hấp tái diễn); và
- 9-12% trường hợp CIN 1
* Nghiên cứu lâm sàng:
Ở phụ nữ, CIN 2/3 và ung thư biểu mô tuyến tại chỗ (Adenocarcinoma in situ: AIS) theo thứ tự, là thể tiền ung thư trực tiếp của ung thư biểu mô tế bào gai xâm lấn và ung thư biểu mô tuyến xâm lấn cổ tử cung. Việc phát hiện và phẫu thuật cắt bỏ khối u được chứng minh có tác dụng phòng ngừa ung thư xâm lấn (phòng ngừa thứ yếu); vì vậy, việc phòng ngừa chủ yếu qua tiêm ngừa sẽ ngăn ngừa được ung thư xâm lấn.
Không thể sử dụng ung thư cổ tử cung xâm lấn là tiêu chí đánh giá về hiệu quả trong các nghiên cứu vắc-xin HPV vì tầm quan trọng của việc áp dụng các phương pháp phòng ngừa thứ yếu. Vì vậy, các thể tiền ung thư trực tiếp, CIN 2 (loạn sản cổ tử cung mức độ trung bình), CIN 3 (loạn sản cổ tử cung mức độ cao bao gồm ung thư biểu mô tại chỗ - carcinoma in situ), và AIS là tiêu chí đánh giá thích hợp nhất để chứng minh hiệu quả ngừa ung thư cổ tử cung khi tiêm ngừa HPV.
CIN 3 và AIS được xếp loại là những ung thư cổ tử cung Giai đoạn 0 theo FIGO (Liên đoàn Quốc tế Sản và Phụ khoa - International Federation of Obstetrics and Gynaecology). VIN 2/3 và VaIN 2/3, theo thứ tự là thể tiền ung thư trực tiếp của ung thư âm hộ và ung thư âm đạo liên quan đến HPV.
Hiệu quả của GARDASIL đã được đánh giá trong 4 thử nghiệm lâm sàng giai đoạn II và giai đoạn III theo phương pháp ngẫu nhiên, mù đôi, có đối chứng placebo. Nghiên cứu thứ nhất giai đoạn II đánh giá thành phần HPV 16 của GARDASIL (Protocol 005, N = 2391 thiếu nữ và phụ nữ) và nghiên cứu thứ hai đánh giá tất cả thành phần của GARDASIL (Protocol 007, N = 551 thiếu nữ và phụ nữ). Nghiên cứu giai đoạn III, có tên FUTURE (Females United To Unilaterally Reduce Endo/Ectocervical Disease: Phụ nữ cùng hành động để làm giảm bệnh cổ trong/cổ ngoài cổ tử cung trên toàn cầu), đã đánh giá GARDASIL trên 5442 (FUTURE I) và 12.157 (FUTURE II) thiếu nữ và phụ nữ. Tổng cộng, những nghiên cứu này đã đánh giá 20.541 thiếu nữ và phụ nữ có độ tuổi từ 16-26 tuổi khi vào nghiên cứu. Trung vị thời gian theo dõi là 4,0; 3,0; 3,0 và 3,0 năm đối với Protocol 005, Protocol 007, FUTURE I, và FUTURE II, theo thứ tự. Đối tượng đã được tiêm vắc-xin hay placebo vào ngày bắt đầu tham gia và 2 tháng và 6 tháng sau. Hiệu quả của vắc-xin đã được phân tích riêng biệt cho từng nghiên cứu và phân tích tổng hợp từ tất cả các nghiên cứu trên thiếu nữ và phụ nữ.
Những nghiên cứu này không có giai đoạn sàng lọc. Do vậy, những đối tượng đã phơi nhiễm với một loại HPV có trong vắc-xin trước khi nghiên cứu cũng được thu nhận vào những nghiên cứu này. Nói chung, 73% đối tượng từ 16-26 tuổi không nhiễm với cả 4 týp HPV của vắc-xin tại thời điểm thu nhận. Những đối tượng này có nguy cơ nhiễm bệnh và mắc bệnh do nhiễm cả 4 týp HPV có trong vắc-xin.
* Hiệu quả dự phòng HPV týp 6, 11 và 18 ở thiếu nữ và phụ nữ tuổi từ 16-26:
GARDASIL có hiệu quả cao trong giảm tỷ lệ ung thư cổ tử cung, ung thư âm hộ, ung thư âm đạo, CIN (bất kỳ mức độ nào); AIS; ung thư cổ tử cung không xâm lấn (CIN 3 và AIS); và các tổn thương bộ phận sinh dục ngoài, bao gồm sùi mào gà, VIN (bất kỳ mức độ nào) và VaIN (bất kỳ mức độ nào) gây bởi HPV týp 6, 11, 16, 18. Căn cứ trên một phân tích đã định trước đối với các tổn thương bắt đầu biểu hiện rõ rệt vào 30 ngày sau liều 1, vắc-xin được chứng minh có hiệu quả trong suốt lịch tiêm 3 liều.
Những phân tích chủ yếu về hiệu quả đã được thực hiện trên dân số hiệu quả theo đề cương nghiên cứu (per-protocol efficacy, PPE), bao gồm những cá nhân đã tiêm đủ 3 liều trong một năm tham gia nghiên cứu, không có thay đổi quan trọng khác so với đề cương nghiên cứu, và chưa nhiễm các týp HPV liên quan trước khi tiêm liều 1 và suốt 1 tháng sau liều 3 (Tháng thứ 7). Hiệu quả được bắt đầu đánh giá sau lần khám vào tháng thứ 7.
Hiệu quả của GARDASIL trên CIN 2/3 hay AIS liên quan đến HPV týp 16 hay 18 là 98.2% (95% CI: 93.5%; 99.8%) trong các nghiên cứu tổng hợp. Phân tích từng nghiên cứu cho thấy các kết quả sau đây: 100% (95% CI: 65.1%; 100,0%) trong Protocol 005; 100% (95% CI: 0.0%; 100%) trong Protocol 007; 100% (95% CI: 89.2%; 100,0%) trong FUTURE I; 96.9% (95% CI: 88.2%; 99.6%) trong FUTURE II. Có 2 trường hợp CIN 3 xảy ra ở nhóm nhận GARDASIL. HPV 16 và 52 được tìm thấy ở trường hợp thứ nhất. Người này nhiễm mãn tính HPV 52 (nhiễm vào ngày 1, vào tháng thứ 32.5 và 32.6) trong 8 trên 11 mẫu thử, bao gồm mẫu mô cắt bỏ từ phẫu thuật cắt đốt từ vòng điện (LEEP). HPV 16 được tìm thấy trong 1 trên 11 mẫu xét nghiệm vào tháng thứ 32.5. Không tìm thấy HPV 16 trong mô bị cắt đốt khi làm phẫu thuật LEEP. Trường hợp thứ 2 tìm thấy HPV 51 và 56. Người này nhiễm HPV 51 (phát hiện nhiễm qua PCR vào ngày 1) trong 2 trên 9 mẫu thử. HPV 56 được phát hiện (trong các mô cắt bỏ từ phẫu thuật LEEP) trong 3 trên 9 mẫu thử vào tháng 52. HPV 16 được phát hiện trong 1 trên 9 mẫu sinh thiết vào tháng 51. Vì hai trường hợp này xảy ra trong tình huống nhiễm trùng hỗn hợp, với týp ưu thế không phải là týp có trong vắc-xin nên chắc chắn týp HPV liên quan trong vắc-xin không phải là týp HPV gây bệnh.
Dựa trên đánh giá này, có thể suy luận rằng hiệu quả của vắc-xin ngừa CIN 2/3 hoặc AIS liên quan HPV 16/18 là 100%.
Hiệu quả của GARDASIL trên CIN 2/3 hoặc AIS liên quan HPV 16 là 97.9% (95% CI: 92.3%; 99.8%) trong tổng hợp các nghiên cứu. Hiệu quả của GARDASIL trên CIN 2/3 hoặc AIS liên quan HPV 18 là 100% (95% CI: 86.6%, 100%) trong tổng hợp các nghiên cứu.
Hiệu quả của GARDASIL trên VIN 2/3 liên quan HPV 16 hoặc 18 là 100% (95% CI: 55.5%; 100%) trong tổng hợp các nghiên cứu. Phân tích từng nghiên cứu cho thấy các kết quả như sau: 100% (95% CI: 14.4%; 100.0%) trong FUTURE I và 100% (95% CI; 100.0%) trong FUTURE II.
Hiệu quả của GARDASIL trên VaIN 2/3 liên quan HPV 16 hoặc 18 là 100% (95% CI: 49.5%; 100%) trong tổng hợp các nghiên cứu. Phân tích từng nghiên cứu cho thấy các kết quả như sau: 100% (95% CI: 0.0%; 100.0%) trong FUTURE I và 100% (95% CI: 0.0%; 100.0%) trong FUTURE II.
Hiệu quả của GARDASIL trên CIN (CIN 1, CIN 2/3) hay AIS liên quan đến HPV týp 6, 11, 16 hay 18 là 96.0% (95% CI: 92.3%; 98.2%) trong tổng hợp các nghiên cứu. Phân tích từng nghiên cứu cho thấy các kết quả như sau: 100% (95% CI: 0.0%; 100,0%) trong Protocol 007; 100% (95% CI: 95.1%; 100.0%) trong FUTURE I và 93.8% (95% CI: 88.0%; 97,2%) trong FUTURE II.
Hiệu quả của GARDASIL trên những tổn thương sinh dục liên quan đến HPV týp 6, 11, 16 hay 18 (mụn cóc sinh dục, VIN, VaIN, ung thư âm hộ, và ung thư âm đạo) là 99.1% (95% CI: 96.8%; 99.9%) trong tổng hợp các nghiên cứu. Phân tích từng nghiên cứu cho thấy các kết quả như sau: 100% (95% CI: 0.0%; 100.0%) trong Protocol 007; 100% (95% CI: 94.9%; 100.0%) trong FUTURE I và 98.7% (95% CI: 95.2%; 99.8%) trong FUTURE II.
Hiệu quả của GARDASIL trên mụn cóc sinh dục liên quan đến HPV týp 6 hoặc 11 là 99.0% (95% CI: 96.2%; 99.9%) trong tổng hợp các nghiên cứu.
* Phân tích bổ sung về hiệu quả trên những tiêu chí đánh giá ung thư ở thiếu nữ và phụ nữ từ 16-26 tuổi:
Trong một phân tích bổ sung, hiệu quả của GARDASIL trên ung thư cổ tử cung giai đoạn không theo phân loại FIGO (CIN 3 hay AIS) và trên các tổn thương tiền ung thư trực tiếp đối với ung thư âm hộ và âm đạo (VIN 2/3 hay VaIN 2/3) liên quan HPV 16/18 ở dân số hiệu quả theo đề cương nghiên cứu (PPE) và dân số dự định điều trị đã thay đổi nhóm 2 (MITT-2). Dân số MITT-2 bao gồm cá thể chưa nhiễm các týp HPV liên quan (týp 6, 11, 16 và 18) trước khi tiêm liều vắc-xin đầu tiên, nhận ít nhất 1 liều vắc-xin hoặc placebo, và có ít nhất 1 lần khám theo dõi sau ngày 30 sau khi tiêm vắc-xin. Dân số MITT-2 khác với dân số PPE ở chỗ trong nghiên cứu này có các cá thể vi phạm đề cương nghiên cứu đáng kể và có người đã nhiễm 1 týp HPV trong quá trình chủng ngừa. Hiệu quả được bắt đầu đánh giá từ 30 ngày sau liều 1 đối với dân số MITT-2.
Hiệu quả của GARDASIL ngừa bệnh liên quan đến HPV týp 16/18 là 96.9% (95% CI: 88.4%; 99.9%), 100% (95% CI: 30.6%; 100.0%) và 100% (95% CI: 78.6%; 100%), lần lượt đối với CIN 3, AIS và VIN 2/3 ở dân số tuân theo đề cương. Hiệu quả của GARDASIL ngừa bệnh liên quan đến HPV týp 16/18 là 96.7% (95% CI: 90.2%; 99.3%); 100% (95% CI: 60.0%; 100.0%) và 97.0% (95% CI: 82.4%; 99.9%), lần lượt đối với CIN 3, AIS và VIN 2/3 hoặc VaIN 2/3 ở dân số MITT-2.
Hiệu quả bảo vệ ngừa nhiễm trùng nói chung hoặc bệnh lý trong giai đoạn mở rộng của protocol 007, bao gồm dữ liệu đến tháng 60, là 95.8% (95% CI: 83.8%; 99.5%). Ở nhóm nhận GARDASIL, không có trường hợp nào ghi nhận miễn dịch suy giảm.
GARDASIL có hiệu quả như nhau trong phòng ngừa bệnh do nhiễm các týp HPV 6, 11, 16 và 18.
* Hiệu quả ở thiếu nữ và phụ nữ từ 16 đến 26 tuổi đang hoặc đã bị nhiễm HPV týp 6, 11, 16 hoặc 18:
Những đối tượng nhiễm một hoặc nhiều týp HPV của vắc-xin trước khi chủng ngừa đã được bảo vệ khỏi các bệnh do các týp HPV còn lại của vắc-xin.
Những đối tượng có bằng chứng bị nhiễm trước đó nhưng đã sạch nhiễm trước khi chủng ngừa đã được bảo vệ không bị tái nhiễm vi-rút hoặc không bị viêm tái phát dẫn đến bệnh lâm sàng.
Những đối tượng dùng GARDASIL, nhưng đang nhiễm HPV tại thời điểm chủng ngừa sẽ giảm 21.6% (95% CI: 0.0%; 42.1%) nguy cơ bị CIN (CIN 1 hay CIN 2/3) hoặc AIS do nhiễm vi-rút này khi so với placebo. Đang bị nhiễm được xác định là bị nhiễm 1 týp HPV của vắc-xin khi bắt đầu tham gia nghiên cứu, nhưng không có bằng chứng đáp ứng miễn dịch.
* Bảo vệ ngừa gánh nặng chung về các bệnh lý cổ tử cung, âm hộ và âm đạo do nhiễm HPV ở thiếu nữ 16-26 tuổi:
Một phân tích định trước đã đánh giá tác động của GARDASILlên nguy cơ chung về bệnh lý cổ tử cung, âm hộ và âm đạo do nhiễm HPV (nghĩa là bệnh do nhiễm bất kỳ týp HPV) trên 17599 đối tương tham gia vào nghiên cứu FUTURE I và FUTURE II. Trong số các đối tượng chưa nhiễm ít nhất đối với 1 trong 14 týp HPV phổ biến và/hoặc đã có xét nghiệm Pap âm tính về tổn thương trong biểu mô tế bào gai [SIL] vào ngày 1 (dân số MITT-2), tỷ lệ mới mắc CIN 2/3 hoặc AIS do nhiễm các týp HPV có hoặc không có trong vắc-xin đã giảm đến 33.8% (95% CI: 20.7%, 44.8%) khi chủng ngừa với GARDASIL.
Đã có những phân tích hiệu quả khác tiến hành trong 2 dân số liên quan lâm sàng: (1) dân số chưa nhiễm HPV (âm tính đối với 14 týp HPV phổ biến và có xét nghiệm Pap âm tính về tổn thương trong biểu mô tế bào gai [SIL] vào ngày 1), tương tự dân số gồm các đối tượng chưa có hoạt động tình dục cùng với các đối tượng vừa mới bắt đầu hoạt động tình dục: và (2) dân số nghiên cứu chung là các đối tượng không kể tình trạng HPV ban đầu, trong số đó có vài người đã có bệnh liên quan HPV lúc bắt đầu chủng ngừa.
Trong số các đối tượng chưa nhiễm HPV và trong dân số nghiên cứu chung (bao gồm các đối tượng nhiễm HPV lúc bắt đầu chủng ngừa), tỷ lệ mới mắc chung của CIN 2/3 hoặc AIS; của VIN 2/3 hoặc VaIN 2/3; của CIN (bất kỳ mức độ) hoặc AIS; và của mụn cóc sinh dục đã giảm khi dùng GARDASIL. Giảm các tỷ lệ này chủ yếu do giảm các tổn thương do nhiễm HPV týp 6, 11, 16 và 18. Trong số các đối tượng chưa nhiễm HPV và trong dân số nghiên cứu chung, lợi ích của vắc-xin liên quan đến tỷ lệ mới mắc chung của CIN 2/3 hoặc AIS (do nhiễm bất kỳ týp HPV) trở nên rõ ràng hơn theo thời gian. Điều này bởi vì GARDASIL không ảnh hưởng đến diễn biến của bệnh nhiễm trùng hiện diện lúc bắt đầu chủng ngừa. Các đối tượng như thế có thể đã có tổn thương CIN hoặc AIS lúc bắt đầu chủng ngừa và vài người sẽ phát triển CIN 2/3 hoặc AIS trong thời gian theo dõi. GARDASIL làm giảm tỷ lệ mới mắc CIN 2/3 hoặc AIS do nhiễm các týp HPV 6, 11, 16 và 18 xảy ra sau khi bắt đầu tiêm vắc-xin.
GARDASIL đã được chứng minh không đem lại sự bảo vệ ngừa các bệnh lý do tất cả các týp HPV gây ra và sẽ không bảo vệ chống lại bệnh đã có sẵn. Hiệu quả chung của GARDASIL sẽ thay đổi tùy theo tần suất nhiễm HPV và bệnh lý lúc ban đầu, tỷ lệ mới mắc các bệnh nhiễm trùng mà GARDASIL có hiệu quả bảo vệ, và những bệnh nhiễm trùng mà GARDASIL được chứng minh không có hiệu quả bảo vệ.
* Tác động lên tỷ lệ xét nghiệm Pap bất thường và các phẫu thuật ở cổ tử cung, âm hộ và âm đạo ở thiếu nữ và phụ nữ 16-26 tuổi:
Tác động của GARDASIL lên tỷ lệ xét nghiệm Pap bất thường và các phẫu thuật ở cổ tử cung (sinh thiết qua nội soi điều trị triệt để) không kể týp HPV gây bệnh đã được đánh giá ở 18150 đối tượng tham gia vào Protocol 007, FUTURE I và FUTURE II. Tác động của GARDASIL lên tỷ lệ phẫu thuật cắt bỏ cơ quan sinh dục để điều trị những tổn thương do bất kỳ týp HPV gây ra đã được đánh giá ở 5442 đối tượng tham gia vào nghiên cứu FUTURE I. Hai nhóm dân số được xem xét: (1) dân số chưa nhiễm HPV (âm tính đối với 14 týp HPV phổ biến và có xét nghiệm Pap âm tính về tổn thương trong biểu mô tế bào gai [SIL] vào ngày 1), tương tự dân số gồm các đối tượng chưa có hoạt động tình dục cùng với các đối tượng vừa mới bắt đầu hoạt động tình dục; và (2) dân số nghiên cứu chung là các đối tượng không kể tình trạng HPV ban đầu, trong số đó có vài người đã có bệnh liên quan HPV lúc bắt đầu chủng ngừa.
Ở cả hai nhóm dân số này, GARDASIL làm giảm tỷ lệ các đối tượng có xét nghiệm Pap bất thường gợi ý CIN, giảm thủ tục soi cổ tử cung sinh thiết, phẫu thuật điều trị cổ tử cung triệt để (thủ thuật cắt đốt vòng điện LEEP hoặc khoét chóp bằng dao lạnh), sinh thiết âm hộ hoặc âm đạo hoặc phẫu thuật cắt bỏ triệt để âm đạo và âm hộ.
Ngoài ra, khi dùng GARDASIL cho dân số chung 16-26 tuổi chưa nhiễm HPV, tỷ lệ mới mắc các xét nghiệm Pap bất thường liên quan HPV 16 và HPV 18 (ASC-US HR dương tính, LSIL, hoặc tổn thương trở nên xấu hơn) đến 92.4% (95% CI: 83.7%, 97.0%) và 96.9% (95% CI: 81.6%, 99.9%) trong nghiên cứu FUTURE I.
* Tính sinh miễn dịch:
+ Xét nghiệm đánh giá đáp ứng miễn dịch:
Các xét nghiệm đặc hiệu theo týp vi-rút với các tiêu chí đặc hiệu theo týp đã được dùng để đánh giá tính sinh miễn dịch đối với từng týp HPV chứa trong vắc-xin. Các xét nghiệm này đo kháng thể chống lại các epitope trung hòa đối với từng týp HPV, hơn là đo toàn bộ kháng thể nhằm vào các VLP có trong vắc-xin. Hệ thống phân độ đối với các xét nghiệm này là chuyên biệt cho từng týp HPV; như vậy, việc so sánh giữa các týp và với các xét nghiệm thì hoàn toàn không có ý nghĩa. Các xét nghiệm dùng để đánh giá đáp ứng miễn dịch đối với GARDASIL đã chứng minh có tương quan với khả năng trung hòa các phân tử HPV còn sống, đang hoạt động.
Vì GARDASIL có hiệu quả rất cao trong các thử nghiệm lâm sàng, nên không thể xác định được nồng độ tối thiểu của kháng thể kháng HPV 6, kháng HPV 11, kháng HPV 16, và kháng HPV 18 có tác dụng bảo vệ ngừa bệnh lâm sàng do nhiễm HPV.
Tính sinh miễn dịch của GARDASIL đã được đánh giá trên 8915 phụ nữ (GARDASIL N=4666; placebo N=4249), tuổi từ 18 đến 26, 1346 bé trai từ 9 đến 15 tuổi (GARDASIL N=1071; placebo N=275), và 2054 thiếu nữ từ 9 đến 17 tuổi (GARDASIL N=1474; placebo N=583).
+ Đáp ứng miễn dịch với GARDASIL:
Những phân tích chủ yếu về đáp ứng miễn dịch đã được thực hiện trên dân số sinh miễn dịch tuân thủ triệt để đề cương nghiên cứu (per-protocol immunogenicity, PPI). Dân số này gồm những cá nhân có huyết thanh âm tính và phản ứng chuỗi trùng hợp (Polymerase Chain Reation: PCR) âm tính đối với týp HPV tương ứng có trong vắc-xin khi vào nghiên cứu, và vẫn duy trì HPV PCR âm tính với một trong các týp HPV tương ứng có trong vắc-xin qua 1 tháng sau liều 3 (tháng thứ 7), đều được tiêm cả 3 liều, và không có bất kỳ khác biệt lớn nào so với đề cương nghiên cứu để không ảnh hưởng đến việc đánh giá tác dụng của vắc-xin.
Tính sinh miễn dịch được đánh giá qua (1) tỷ lệ % đối tượng có huyết thanh dương tính đối với những kháng thể chống các týp HPV liên quan trong vắc-xin, và (2) hiệu quả kháng thể (Geometric Mean Titer-GMT).
Trong các nghiên cứu lâm sàng, 99.9%; 99.8%; 99.8% và 99.6% các đối tượng đã được tiêm GARDASIL, theo thứ tự có huyết thanh dương tính kháng HPV 6, kháng HPV 11, kháng HPV 16, và kháng HPV 18 vào khoảng 1 tháng sau liều 3 ở tất cả các nhóm tuổi thử nghiệm. Sau khi tiêm GARDASIL, trị số Geometric Mean Titers (GMTs) kháng HPV tăng cao vào khoảng 1 tháng sau liều 3 ở tất cả các nhóm tuổi thử nghiệm.
Nồng độ kháng HPV do đáp ứng với tiêm vắc-xin, cao hơn đáng kể so với trị số đo được ở những phụ nữ có bằng chứng đã có nhiễm sau đó có đáp ứng miễn dịch và dẫn đến loại bỏ khỏi nhiễm trước khi thu nhận.
Trong một nghiên cứu đo lường đáp ứng miễn dịch đối với GARDASIL, chế độ tiêm 3 liều trong thời gian của liệu trình tiêm phòng ngừa, nồng độ kháng HPV sau liều 2 cao hơn nồng độ quan sát được trong theo dõi lâu dài trong những nghiên cứu Pha III. Nói chung, 97.6% đến 100% có nồng độ kháng thể dương tính kháng HPV 6, kháng HPV 11, và kháng HPV 18 theo thứ tự, vào khoảng tháng thứ 1 sau liều 2. Những kết quả này hỗ trợ cho quan sát rằng hiệu quả phòng ngừa của GARDASIL đã có trong suốt thời gian liệu trình tiêm 3 liều.
Hiệu quả bắc cầu của GARDASIL từ nhóm người trẻ tuổi qua nhóm thanh thiếu niên.
Một nghiên cứu lâm sàng đã so sánh đáp ứng kháng HPV 6, HPV 11, HPV 16, và HPV 18 ở trẻ em nam và nữ 10-15 tuổi với đáp ứng ở thanh thiếu niên và phụ nữ trẻ 16-23 tuổi. Trong số đối tượng nhận GARDASIL, 99.1%-100% người có huyết thanh dương tính với kháng thể kháng HPV 6, HPV 11, HPV 16, và HPV 18, theo thứ tự, vào thời điểm 1 tháng sau liều 3. Đáp ứng kháng HPV trong cả hai nhóm nữ 10-15 tuổi và nam 10-15 tuổi đều cao hơn đáng kể so với nhóm 16-23 tuổi.
Kết quả tương tự cũng được ghi nhận khi so sánh đáp ứng kháng HPV một tháng sau liều 3 ở nhóm trẻ em nữ 9-15 tuổi với đáp ứng kháng HPV ở nhóm thanh thiếu nữ và phụ nữ trẻ 16-26 tuổi trong các dữ liệu tổng hợp từ các thử nghiệm lâm sàng của GARDASIL về tính sinh miễn dịch.
Trên cơ sở bắc cầu tính sinh miễn dịch, hiệu quả của GARDASIL ở các bé gái 9-15 tuổi tương đương với hiệu quả của GARDASIL ghi nhận trong những thử nghiệm giai đoạn III trên thanh thiếu nữ và phụ nữ trẻ 16-26 tuổi. Ngoài ra, hiệu quả của GARDASIL ở nhóm bé trai 9-15 tuổi so sánh tương đương với hiệu quả của GARDASIL trong các nghiên cứu ở nhóm thanh niên, nam trưởng thành 16-26 tuổi.
Đáp ứng miễn dịch tồn tại lâu dài đối với GARDASIL.
Chưa xác lập được thời gian kéo dài miễn dịch sau khi hoàn tất lịch chủng ngừa với GARDASIL. Sau khi đạt mức tối đa vào tháng 7, GMT đối với tất cả các týp HPV đã giảm cho đến tháng 24, sau đó ổn định ở mức cao hơn mức ban đầu.
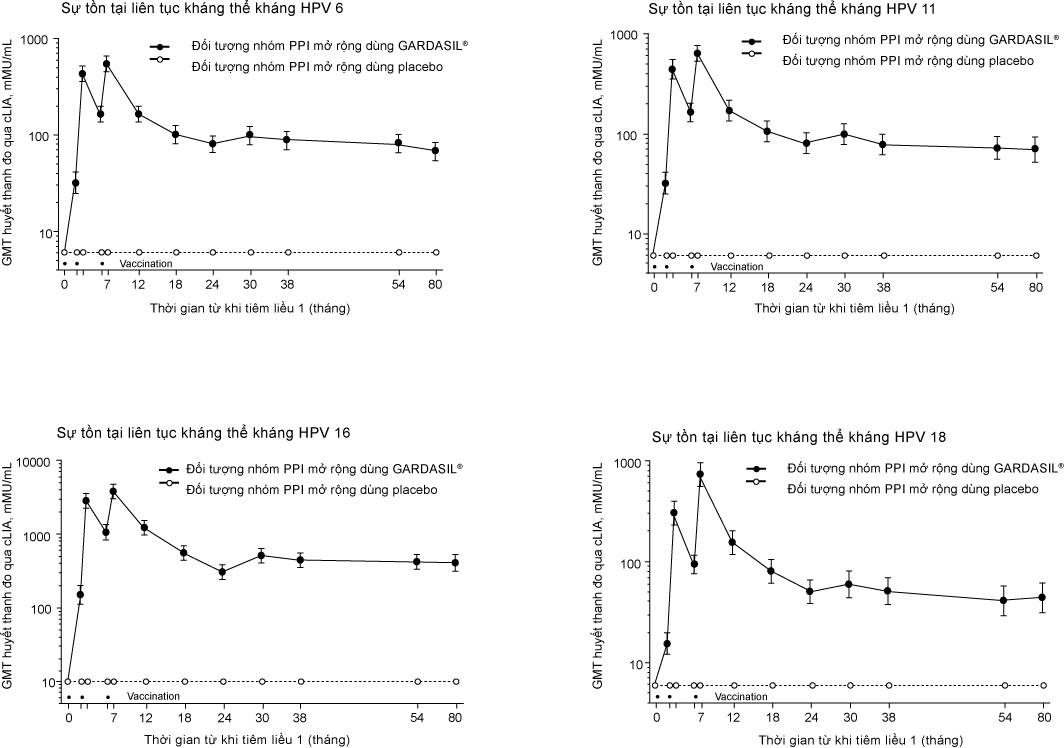
Trong protocol 007, GMT tối đa kháng HPV 6, 11, 16 và 18 được ghi nhận vào tháng 7. GMT giảm cho đến tháng 24 và sau đó ổn định cho đến ít nhất vào tháng 60 (xem Hình 1).
Hinh 1: Đáp ứng kháng thể kháng HPV tồn tại lâu dài sau khi tiêm 3 liều GARDASIL
+ Bằng chứng về đáp ứng trí nhớ (trí nhớ miễn dịch):
Bằng chứng về đáp ứng trí nhớ được nhận biết ở những người đã chủng ngừa có huyết thanh dương tính đối với các týp HPV trước khi tiêm vắc-xin.
Trong một nghiên cứu đámh giá khả năng tạo trí nhớ miễn dịch, người đã nhận đợt chủng ngừa cơ bản 3 mũi được tiêm 1 liều GARDASIL kích thích (thách thức) vào 5 năm sau khi bắt đầu chủng ngừa. Những người này đã biểu hiện đáp ứng trí nhớ nhanh và mạnh, vượt quá mức GMT kháng HPV quan sát được 1 tháng sau liều 3 (tháng 7). GMT đo được vào 1 tuần sau liều vắc-xin kích thích, lần lượt cao gấp 0.9, 2.2, 1.2 và 1.4 lần GMT sau liều 3 đối với các týp 6, 11, 16 và 18. GMT đo được vào 1 tháng sau liều vắc-xin kích thích, lần lượt cao gấp 1.3, 4.2, 1.5 và 1.7 lần GMT sau liều 3 đối với các týp 6, 11, 16 và 18. Một tuần sau liều vắc-xin kích thích, 87.2%, 94.9%, 86.4% và 95.2% đối tượng đã có GMT kháng HPV 6, 11,16 và 18 cao hơn GMT phát hiện ở tháng 60.
Hơn nữa, một phân nhóm đối tượng nhận 3 liều vắc-xin cơ bản trên danh nghĩa đã có huyết thanh âm tính kháng HPV 18 vào tháng 60. Mặc dù các cá thể này trên danh nghĩa có huyết thanh âm tính kháng HPV 18 nhưng không tìm thấy trường hợp bệnh lý nào liên quan HPV 18. Các cá thể này cũng biểu hiện trí nhớ miễn dịch: khi cho các đối tượng này tiếp xúc 1 liều GARDASIL kích thích (vào tháng 60), có 93% và 97% đối tượng đã có huyết thanh dương tính kháng HPV 18 sau khi dùng liều vắc-xin kích thích, lần lượt 1 tuần và 1 tháng; 73% đối tượng này có kháng thể kháng HPV 18 vào 1 tháng sau khi kích thích ở mức cao hơn nồng độ kháng thể kháng HPV 18 đạt vào tháng 7 (1 tháng sau liều 3).
+ Lịch tiêm linh hoạt:
Tất cả các đối tượng được đánh giá trong dân số hiệu quả tuân thủ đề cương nghiên cứu (PPE) từ những nghiên cứu giai đoạn II và III đã nhận GARDASIL 3 liều trong thời gian 1 năm, không kể đến khoảng thời gian giữa các liều. Một phân tích về dữ liệu đáp ứng miễn dịch gợi ý cho thấy một lịch tiêm linh hoạt ± 1 tháng đối với liều 2 (nghĩa là tháng 1 cho đến tháng 3 của lịch tiêm) và ± 2 tháng đối với liều 3 (nghĩa là tháng 4 cho đến tháng 8 của lịch tiêm) không ảnh hưởng đáng kể đến đáp ứng miễn dịch đối với GARDASIL (xem Liều lượng và Cách dùng).
+ Nghiên cứu với những vắc-xin khác:
- H-B-VAX II [vắc-xin viêm gan B (tái tổ hợp)]: Tính an toàn và sinh miễn dịch khi tiêm đồng thời GARDASIL và H-B-VAX II [vắc-xin viêm gan B (tái tổ hợp)] (cùng ngày tiêm, khác vị trí tiêm) đã được đánh giá trong một nghiên cứu phân nhóm ngẫu nhiên trên 1871 phụ nữ 16-24 tuổi lúc vào nghiên cứu. Đáp ứng miễn dịch và tính an toàn của hai vắc-xin H-B-VAX II [vắc-xin viêm gan B (tái tổ hợp)] và GARDASIL khi tiêm cùng ngày hoặc khác ngày đều như nhau.
- Repevax [Vắc-xin hấp phụ, chứa hàm lượng thấp các kháng nguyên vi-rút bại liệt bất hoạt, bạch hầu, uốn ván, ho gà (thành phần vô bào)]: Tính an toàn và sinh miễn dịch khi tiêm đồng thời GARDASIL và Repevax [Vắc-xin hấp phụ, chứa hàm lượng thấp các kháng nguyên vi-rút bại liệt bất hoạt, bạch hầu, uốn ván, ho gà (thành phần vô bào)] (cùng ngày tiêm, khác vị trí tiêm) đã được đánh giá trong một nghiên cứu phân nhóm ngẫu nhiên trên 843 bé gái và bé trai 11-17 tuổi lúc vào nghiên cứu. Tiêm GARDASIL đồng thời với Repevax [Vắc-xin hấp phụ, chứa hàm lượng thấp các kháng nguyên vi-rút bại liệt bất hoạt, bạch hầu, uốn ván, ho gà (thành phần vô bào)] không ảnh hưởng tới đáp ứng tạo kháng thể đối với các thành phần của cả 2 vắc-xin. Hơn nữa, tính an toàn của vắc-xin tương tự nhau (xem Tác dụng ngoại ý, Sử dụng cùng với các vắc-xin khác).
- Menactra [Vắc-xin liên hợp não mô cầu (nhóm A,C,Y và W-135) với polysaccharide biến độc tố bạch hầu] và Adacel [Vắc-xin hấp phụ biến độc tố bạch hầu, biến độc tố uốn ván và vi-rút ho gà vô bào hàm lượng thấp (Tdap)]: Tính an toàn và sinh miễn dịch khi tiêm đồng thời GARDASIL và Menactra [Vắc-xin liên hợp não mô cầu (nhóm A,C,Y và W-135) với polysaccharide biến độc tố bạch hầu] và Adacel [Vắc-xin hấp phụ biến độc tố bạch hầu, biến độc tố uốn ván và vi-rút ho gà vô bào hàm lượng thấp (Tdap)] (cùng ngày tiêm, khác vị trí tiêm) đã được đánh giá trong một nghiên cứu phân nhóm ngẫu nhiên trên 1040 bé gái và bé trai 11-17 tuổi lúc vào nghiên cứu. Tiêm GARDASIL đồng thời với Menactra [Vắc-xin liên hợp não mô cầu (nhóm A,C,Y và W-135) với polysaccharide biến độc tố bạch hầu] và Adacel [Vắc-xin hấp phụ biến độc tố bạch hầu, biến độc tố uốn ván và vi-rút ho gà vô bào hàm lượng thấp (Tdap)] không ảnh hưởng tới đáp ứng tạo kháng thể đối với các thành phần của cả 2 vắc-xin. Hơn nữa, tính an toàn của các vắc-xin tương tự nhau (xem Tác dụng ngoại ý, Sử dụng cùng với các vắc-xin khác).
Dược động học
Không yêu cầu đánh giá các nghiên cứu dược động học đối với vắc-xin.
Chỉ định/Công dụng
GARDASIL là vắc-xin được chỉ định cho bé gái và phụ nữ từ 9 đến 26 tuổi để phòng ngừa ung thư cổ tử cung, âm hộ, âm đạo, các tổn thương tiền ung thư hoặc loạn sản, mụn cóc sinh dục và bệnh lý do nhiễm HPV.
• GARDASIL được dùng để ngăn ngừa các bệnh sau đây:
- Ung thư cổ tử cung, âm hộ và âm đạo gây ra bởi HPV týp 16 và 18.
- Mụn cóc sinh dục (mào gà sinh dục) gây ra bởi HPV týp 6 và 11.
• Nhiễm và bị các tổn thương tiền ung thư hoặc loạn sản gây ra bởi HPV týp 6, 11, 16 và 18:
- Tân sinh trong biểu mô cổ tử cung (CIN) độ 2/3 và ung thư biểu mô tuyến cổ tử cung tại chỗ (AIS).
- Tân sinh trong biểu mô cổ tử cung (CIN) độ 1.
- Tân sinh trong biểu mô âm hộ (VIN) độ 2 và 3.
- Tân sinh trong biểu mô âm đạo (VaIN) độ 2 và 3.
- Tân sinh trong biểu mô âm hộ (VIN) và tân sinh trong biểu mô âm đạo (VaIN) độ 1.
Liều lượng & Cách dùng
GARDASIL dùng tiêm bắp với 3 liều 0,5 ml cách nhau theo lịch tiêm như sau:
Liều tiêm đầu tiên: vào ngày đã chọn.
Liều thứ hai: 2 tháng sau liều đầu tiên.
Liều thứ ba: 6 tháng sau liều đầu tiên.
Nên tuân thủ lịch tiêm chủng 0, 2 và 6 tháng như trên. Tuy nhiên các nghiên cứu lâm sàng đã chứng minh hiệu quả của vắc-xin ở các đối tượng nhận tất cả 3 liều trong thời gian 1 năm. Khi cần điều chỉnh lịch tiêm, liều thứ hai nên dùng ít nhất 1 tháng sau liều đầu tiên, và liều thứ ba nên dùng ít nhất 3 tháng sau liều thứ hai.
Cách dùng:
Nên tiêm bắp GARDASIL vào vùng cơ delta của phần trên cánh tay hoặc vào vùng trước-bên của phía trên đùi.
Không được tiêm GARDASIL vào mạch máu. Cả đường tiêm dưới da và trong da đều được nghiên cứu, vì vậy không khuyến cáo các đường dùng này.
Khi sử dụng loại lọ đơn liều, cần dùng ống tiêm và kim tiêm vô khuẩn riêng biệt cho từng người được tiêm.
Vắc-xin chỉ được dùng nguyên dạng, không cần phải hoàn nguyên hoặc pha loãng. Nên dùng đầy đủ liều đã khuyến cáo của vắc-xin.
Lắc kỹ lọ/bơm tiêm trước khi sử dụng:
Cần lắc kỹ ngay trước khi tiêm để giữ được dạng dịch treo của vắc-xin.
Sau khi lắc kỹ, GARDASIL sẽ là dịch đục màu trắng. Trước khi dùng, cần kiểm tra các sản phẩm dạng tiêm bằng mắt thường để phát hiện tiểu phân lạ hoặc sự đổi màu. Hủy bỏ sản phẩm có các tiểu phân lạ hoặc đổi màu.
Cách sử dụng lọ thuốc tiêm đơn liều:
Lấy 0,5 ml liều vắc-xin từ lọ vắc-xin đơn liều, bằng cách dùng bơm tiêm và kim tiêm vô khuẩn không chứa chất bảo quản, thuốc sát khuẩn và chất tẩy rửa. Khi đã mở lọ vắc-xin đơn liều, nên tiêm vắc-xin ngay, và hủy bỏ lọ vắc-xin.
Quá Liều
Đã có những báo cáo về dùng GARDASIL quá liều khuyến cáo. Nói chung các tác dụng bất lợi được báo cáo khi dùng quá liều cũng tương tự như khi dùng các liều đơn của GARDASIL theo khuyến cáo.
Chống chỉ định
Mẫn cảm với hoạt chất hoặc với bất kỳ thành phần của vắc-xin. Không được sử dụng các liều GARDASIL tiếp theo nếu gặp các triệu chứng mẫn cảm sau khi tiêm 1 liều GARDASIL.
Sử dụng ở phụ nữ có thai và cho con bú
MANG THAI
Các nghiên cứu trên chuột cống cái
Nghiên cứu trên động vật không cho thấy không có gây hại trực tiếp hoặc gián tiếp đến tình trạng mang thai, hoặc sự phát triển của phôi/thai, quá trình sinh đẻ hoặc động vật con sau sinh. GARDASIL cảm ứng đáp ứng kháng thể đặc hiệu chống HPV týp 6, 11, 16 và 18 ở chuột cống mang thai sau một hoặc nhiều lần tiêm bắp. Các kháng thể chống tất cả 4 týp HPV đều được truyền sang chuột con trong thời gian mang thai và có thể trong thời gian tiết sữa.
Các nghiên cứu lâm sàng trên người
Tuy nhiên, chưa có các nghiên cứu đầy đủ và có đối chứng ở phụ nữ mang thai. Vì những nghiên cứu về sự sinh sản trên động vật không phải lúc nào cũng tiên đoán được đáp ứng ở người, nên cần tránh có thai trong thời gian chủng ngừa GARDASIL.
Trong nghiên cứu lâm sàng, phụ nữ được làm xét nghiệm nước tiểu thử thai trước khi dùng mỗi liều GARDASIL. Phụ nữ nào được phát hiện có thai trước khi tiêm xong 3 liều GARDASIL đều được hướng dẫn hoãn lịch tiêm cho tới khi giải quyết xong thai nghén. Sau khi tiêm liều 3, những liệu trình không chuẩn như vậy vẫn cho kết quả đáp ứng kháng thể chống HPV 6, HPV 11, HPV 16 và HPV 18 tương đương với đáp ứng quan sát được ở phụ nữ dùng lịch tiêm chuẩn 0, 2 và 6 tháng (xem Liều lượng và Cách dùng).
Trong các thử nghiệm lâm sàng có 3315 phụ nữ (1657 người dùng vắc-xin và 1658 người dùng placebo) mang thai ít nhất một lần. Tỷ lệ chung khi mang thai có kèm theo kết quả bất lợi, được xác định bởi số lượng tổng hợp các trường hợp sẩy thai tự phát, thai chết lưu muộn và dị tật bẩm sinh trong tổng số trường hợp phụ nữ mang thai có kết quả thai nghén được biết rõ ràng (và không bao gồm các trường hợp bỏ thai theo dự tính), là 23.2% (393/1693) trong số những người dùng GARDASIL và 23.8% (403/1692) trong số những người dùng placebo.
Đã tiến hành những phân tích sâu hơn để đánh giá các trường hợp ước chừng bắt đầu mang thai trong vòng 30 ngày hoặc sau 30 ngày từ khi dùng một liều GARDASIL hoặc placebo. Trong số các trường hợp bắt đầu có thai ước chừng trong vòng 30 ngày tính từ ngày tiêm chủng, có gặp 5 trường hợp bất thường bẩm sinh ở nhóm dùng GARDASIL so với không có trường hợp nào bất thường bẩm sinh ở nhóm dùng placebo. Ngược lại, trong số những người bắt đầu có thai từ 30 ngày trở lên sau khi tiêm chủng, có 32 trường hợp bất thường bẩm sinh ở nhóm dùng GARDASIL so với 27 trường hợp ở nhóm dùng placebo. Những loại bất thường được quan sát thấy này phù hợp với những bất thường hay nhận thấy ở phụ nữ mang thai trong độ tuổi 16-26 (bất kể thời điểm mang thai so với lúc tiêm chủng).
Như vậy chưa có bằng chứng gợi ý sử dụng GARDASIL ảnh hưởng có hại đến khả năng sinh sản, tình trạng mang thai hoặc gây hậu quả cho trẻ sơ sinh.
CHO CON BÚ
Vẫn chưa rõ các kháng nguyên của vắc-xin và các kháng thể được tạo thành do cảm ứng vắc-xin có bài tiết qua sữa mẹ hay không.
Có thể dùng GARDASIL cho phụ nữ trong thời kỳ cho con bú.
Tổng cộng 995 bà mẹ đang cho con bú dùng GARDASIL hoặc placebo trong suốt giai đoạn chủng ngừa trong những nghiên cứu lâm sàng. Trong các nghiên cứu đó, tỷ lệ các phản ứng có hại ở mẹ và ở trẻ bú mẹ là tương đương giữa các nhóm tiêm chủng. Thêm vào đó, tính sinh miễn dịch của vắc-xin là tương đương giữa các bà mẹ cho con bú với các phụ nữ không nuôi con bú trong thời kỳ tiêm chủng.
Tương tác
Sử dụng với các vắc-xin khác:
Kết quả từ nghiên cứu lâm sàng cho thấy có thể dùng GARDASIL cùng lúc với H-B-VAX IITM [Vắc-xin viêm gan B (tái tổ hợp)], Menactra [Vắc-xin liên hợp não mô cầu (nhóm A,C,Y và W-135) với polysaccharide biến độc tố bạch hầu], Adacel [Vắc-xin hấp phụ biến độc tố bạch hầu, biến độc tố uốn ván và vi-rút ho gà vô bào hàm lượng thấp (Tdap)], và Repevax [Vắc-xin hấp phụ chứa hàm lượng thấp các kháng nguyên vi-rút bại liệt bất hoạt, bạch hầu, uốn ván, ho gà (thành phần vô bào)].
Sử dụng với các thuốc thông thường khác:
Trong nghiên cứu lâm sàng ở thiếu nữ và phụ nữ (từ 16-26 tuổi), có 11,9% người dùng thuốc giảm đau; 9,5% dùng thuốc kháng viêm; 6,9% dùng kháng sinh và 4,3% dùng chế phẩm vitamin. Hiệu quả, tính sinh miễn dịch và tính an toàn của vắc-xin không bị ảnh hưởng bởi các thuốc trên.
Sử dụng với các thuốc nội tiết ngừa thai:
Trong các nghiên cứu lâm sàng, 57,5% phụ nữ (từ 16 đến 26 tuổi) dùng GARDASIL đã dùng các thuốc nội tiết ngừa thai. Sử dụng các thuốc nội tiết ngừa thai không ảnh hưởng đến đáp ứng miễn dịch đối với GARDASIL.
Sử dụng với steroid:
Trong các nghiên cứu lâm sàng ở thiếu nữ và phụ nữ (từ 16-26 tuổi), có 1,7% (n=158) đối tượng dùng thuốc ức chế miễn dịch dạng hít; 0,6% (n=56) dùng dạng tại chỗ; và 1,0% (n=89) dùng dạng tiêm. Tất cả các đối tượng dùng corticosteroid đều gần thời điểm tiêm 1 liều GARDASIL. Những thuốc này xem ra không ảnh hưởng đến đáp ứng miễn dịch đối với GARDASIL. Rất ít đối tượng trong các nghiên cứu lâm sàng này dùng steroid và lượng thuốc ức chế miễn dịch được cho là thấp.
Sử dụng với các thuốc ức chế miễn dịch dùng toàn thân:
Chưa có dữ liệu về sử dụng các thuốc ức chế miễn dịch mạnh cùng lúc với GARDASIL. Đối tượng dùng các thuốc ức chế miễn dịch (liều dùng toàn thân của corticosteroid, thuốc chống chuyển hóa, thuốc alkyl, thuốc gây độc tế bào) có thể không có đáp ứng tối ưu đối với miễn dịch chủ động (xem Thận trọng, Thận trọng chung).
Tác dụng ngoại ý
Trong 5 thử nghiệm lâm sàng (4 thử nghiệm có đối chứng với placebo), các đối tượng được tiêm GARDASIL hoặc placebo vào ngày bắt đầu thử nghiệm, và khoảng 2 và 6 tháng sau. GARDASIL biểu hiện tính an toàn thuận lợi khi so sánh với placebo (có hoặc không chứa nhôm). Một số ít người (0,2%) đã phải ngừng thuốc do tác dụng bất lợi. Trong mọi thử nghiệm lâm sàng (trừ 1 thử nghiệm), tính an toàn được đánh giá qua phiếu báo cáo tiêm chủng theo dõi trong vòng 14 ngày sau mỗi lần tiêm GARDASIL hoặc placebo. Có 6160 người (5088 phụ nữ 9-26 tuổi và 1072 nam 9-16 tuổi lúc bắt đầu tham gia thử nghiệm) dùng GARDASILvà 4064 người dùng placebo được theo dõi và sử dụng phiếu báo cáo tiêm chủng.
Những tác dụng bất lợi liên quan tới vắc-xin sau đây gặp ở những người dùng GARDASIL với tần số ít nhất là 1,0% và cũng có tần số cao hơn so với nhóm placebo, được liệt kê theo tần số và hệ thống phân loại các cơ quan.
Phân loại tần suất như sau:
Rất phổ biến (≥ 1/10); phổ biến (≥ 1/100, < 1/10); ít gặp (≥ 1/1000, < 1/100); hiếm gặp (≥ 1/10000, < 1/1000); rất hiếm (< 1/10000).
Rối loạn toàn thân và phản ứng tại chỗ tiêm: Rất phổ biến: sốt.
Những phản ứng sau đây tại chỗ tiêm ở nhóm dùng GARDASIL có tần số cao hơn so với ở nhóm dùng nước muối sinh lý làm giả dược: Rất hay gặp: ban đỏ, đau, sưng. Hay gặp: bầm tím và ngứa.
Những phản ứng sau đây tại chỗ tiêm là rất hay gặp và có tần số cao hơn ở nhóm dùng GARDASIL so với ở nhóm dùng giả dược có chứa nhôm: ban đỏ, đau, sưng.
Phần lớn các phản ứng tại nơi tiêm có mức độ nhẹ tới trung bình.
Ngoài ra, rất hiếm gặp phản ứng bất lợi nghiêm trọng là co thắt phế quản.
Sử dụng đồng thời vắc-xin khác
Tính an toàn của GARDASIL khi dùng đồng thời với các vắc-xin khác đã được đánh giá qua các thử nghiệm lâm sàng.
Khi tiêm GARDASIL cùng lúc với vắc-xin viêm gan B (tái tổ hợp), tần số các tác dụng bất lợi tương tự như khi tiêm riêng GARDASIL.
Tần số nhức đầu và sưng tại chỗ tiêm tăng khi tiêm GARDASIL cùng lúc với vắc-xin hấp phụ chứa hàm lượng thấp các kháng nguyên bạch hầu, uốn ván, ho gà (vô bào) và bại liệt bất hoạt.
Tấn số sưng tại nơi tiêm tăng khi tiêm GARDASIL cùng lúc với vắc-xin liên hợp não mô cầu (nhóm A,C,Y và W-135) với polysaccharide biến độc tố bạch hầu và vắc-xin hấp phụ biến độc tố bạch hầu, biến độc tố uốn ván và vi-rút ho gà vô bào hàm lượng thấp (Tdap).
Phần lớn các phản ứng bất lợi khi tiêm cùng lúc với các vắc-xin khác có mức độ từ nhẹ đến trung bình.
Báo cáo hậu mãi
Những tác dụng bất lợi sau đây được báo cáo tự phát trong quá trình sử dụng GARDASIL trên thị trường vì các tác dụng bất lợi này được báo cáo tự phát từ một dân số chưa rõ cỡ mẫu, nên không thể ước tính chính xác tần số của chúng hoặc xác lập mối liên quan về nguyên nhân đối với việc sử dụng vắc-xin.
Rối loạn máu và hệ bạch huyết: ban xuất huyết giảm tiểu cầu tự phát, bệnh lý hạch.
Rối loạn hệ thần kinh: viêm não tủy lan tỏa cấp, choáng váng, hội chứng Guillain-Barré, nhức đầu đôi khi ngất kèm theo các hoạt động co cứng-rung giật.
Rối loạn tiêu hóa: buồn nôn, nôn.
Rối loạn cơ xương và mô liên kết: đau khớp, đau cơ.
Rối loạn toàn thân và tình trạng tại chỗ tiêm: suy nhược, ớn lạnh, mệt mỏi, khó ở.
Rối loạn hệ miễn dịch: phản ứng quá mẫn bao gồm phản ứng phản vệ/giả phản vệ, co thắt phế quản và nổi mề đay.
Thận trọng
Thận trọng chung:
Như bất kỳ vắc-xin, tiêm chủng GARDASIL không bảo vệ hết tất cả những người được tiêm.
Vắc-xin này không dùng để điều trị các tổn thương sinh dục ngoài đang tiến triển, ung thư cổ tử cung, âm hộ hoặc âm đạo; tân sinh trong biểu mô cổ tử cung, âm hộ hoặc âm đạo (CIN, VIN hoặc VaIN).
Vắc-xin này không ngừa các bệnh không phải do HPV gây ra.
Như bất kỳ vắc-xin dạng tiêm, cần chuẩn bị sẵn các phương tiện điều trị thích hợp phòng trường hợp có các phản ứng phản vệ (tuy hiếm) xảy ra sau khi dùng vắc-xin.
Ngất (choáng) có thể xảy ra khi chủng ngừa bất kỳ vắc-xin nào, đặc biệt ở thanh thiếu niên và người lớn trẻ tuổi. Đã có báo cáo về ngất, đôi khi kết hợp với ngã quỵ, xảy ra sau khi tiêm vắc-xin GARDASIL. Do đó, nên theo dõi kỹ đối tượng trong khoảng 15 phút sau khi tiêm GARDASIL (xem Tác dụng ngoại ý, Các báo cáo hậu mãi).
Quyết định tiêm hoặc hoãn tiêm do đang sốt hoặc vừa bị sốt chủ yếu tùy thuộc vào độ nghiêm trọng của các triệu chứng và nguyên nhân của các triệu chứng đó. Thường không chống chỉ định chủng ngừa khi chỉ có sốt nhẹ và nhiễm khuẩn nhẹ đường hô hấp trên.
Đáp ứng kháng thể có thể giảm đối với sự tạo miễn dịch chủ động ở những người giảm đáp ứng miễn dịch do hoặc sử dụng liệu pháp ức chế miễn dịch, có khiếm khuyết di truyền, nhiễm HIV hoặc do các nguyên nhân khác (xem Tương tác).
Cần thận trọng khi dùng vắc-xin này cho người giảm tiểu cầu hoặc có bất kỳ rối loạn đông máu vì có thể xuất huyết sau khi tiêm bắp.
Sử dụng ở trẻ em: Chưa đánh giá tính an toàn và hiệu lực của GARDASIL ở trẻ em dưới 9 tuổi.
Sử dụng ở người cao tuổi: Chưa đánh giá tính an toàn và hiệu lực của GARDASIL ở người lớn trên 26 tuổi.
Sử dụng ở các đối tượng đặc biệt khác: Chưa đánh giá đầy đủ về tính an toàn, tính sinh miễn dịch và hiệu quả của GARDASIL ở người nhiễm HIV.
Tác động lên khả năng lái xe và vận hành máy móc: Không có dữ liệu nào cho thấy GARDASIL có tác động lên khả năng lái xe hoặc vận hành máy móc.
Bảo quản
* Bảo quản lạnh ở 2-8°C (36-46°F). Không được đông lạnh. Tránh ánh sáng.
* Nên sử dụng GARDASIL càng sớm càng tốt sau khi lấy khỏi tủ lạnh. Có thể lấy GARDASIL khỏi tủ lạnh (để nhiệt độ bằng hoặc dưới 25°C) trong khoảng thời gian không qua 72 giờ.
Phân loại ATC
J07BM01 - papillomavirus (human types 6, 11, 16, 18)
Trình bày/Đóng gói
Dung dịch tiêm: hộp 1 lọ đơn liều 0.5mL.
- Abacavir
- Abernil
- Abiiogran
- Acarbose
- ACC
- Acebutolol
- Acenocoumarol
- Acetate Ringer's
- Acetazolamide
- Acetylcystein
- Acetylsalicylic acid
- Aciclovir
- Acid acetylsalicylic
- Acid aminocaproic
- Acid ascorbic
- Acid boric
- Acid chenodeoxycholic
- Acid ethacrynic
- Acid folic
- Acid fusidic
- Acid iopanoic
- Acid ioxaglic
- Acid nalidixic
- Acid pantothenic
- Acid para-aminobenzoic
- Acid salicylic
- Acid tranexamic
- Acid valproic
- Acid zoledronic
- Acitretin
- Aclasta
- Aclon
- Actapulgite
- Actelsar
- Actelsar HCT
- Actemra
- Actilyse
- Acular
- Acupan
- Acuvail
- Acyclovir STADA
- Acyclovir STADA Cream
- Adalat
- Adenosin
- Adenosin Ebewe
- Adipiodon
- Advagraf
- Aerius
- Afinitor
- Agicarvir
- Agifovir-E
- Agilosart
- Agilosart-H
- Agimepzol
- Agimosarid
- Agimstan
- Agimstan-H
- Agiremid
- Agivastar
- Aibezym
- Air-X
- Alaxan
- Albendazol
- Albiomin
- Albumin
- Albumin người Grifols 20%
- Albuminar
- AlbuRx
- Albutein
- Alcuronium chloride
- Aldesleukin
- Alendronat
- Alertin
- Alfa-Lipogamma 600 Oral
- Alfuzosin hydrochlorid
- Algotra
- Alimemazin
- Alimta
- Allipem
- Allopurinol
- Allopurinol STADA
- Aloxi
- Alprazolam
- Alpha Chymotrypsin
- Alpha tocopherol
- Alphachymotrypsin Glomed
- Alphagan-P
- Aluvia
- Alzental
- Amaryl
- Ambroco
- Ambroxol
- Amcinol-Paste
- Amigold
- Amikacin
- Aminocaproic acid
- Aminoleban
- Aminoleban Oral
- Aminosteril N-Hepa
- Amiparen
- Amitriptyline
- Amiyu
- Amlodipine
- Amlor
- Amoxicillin
- Amoxicillin & clavulanate
- Ampicillin
- Amquitaz
- Anaferon for children
- Anargil
- Anaropin
- Andriol Testocaps
- Anepzil
- Anyfen
- Apaisac
- Apidra SoloStar
- Apitim 5
- Aprovel
- Aquaphil
- Arcalion
- Arcoxia
- Aricept Evess
- Arimidex
- Arnetine
- Artrodar
- A-Scabs
- Ascorbic acid
- Asperlican/Candinazol
- Aspilets EC
- Aspirin
- Asthmatin
- Atelec
- Atocib 120
- Atocib 90
- Atosiban PharmIdea
- Atozet
- Attapulgite
- Atussin
- Atropin
- Augbactam
- Augmentin Sachet
- Augmentin SR
- Augmentin Tablets
- Augmex
- Avamys
- Avastin
- Avelox Dịch truyền
- Avelox Viên nén
- Avodart
- Axcel Cefaclor-125 Suspension
- Axcel Cetirizine Syrup
- Axcel Chlorpheniramine
- Axcel Dexchlorpheniramine
- Axcel Dicyclomine-S Syrup
- Axcel Diphenhydramine Paediatric Syrup
- Axcel Erythromycin ES
- Axcel Eviline
- Axcel Fungicort Cream
- Axcel Fusidic acid Cream
- Axcel Fusidic acid-B Cream
- Axcel Hydrocortisone Cream
- Axcel Lignocaine 2% Sterile Gel
- Axcel Loratadine
- Axcel Miconazole Cream
- Axcel Paracetamol
- Axcel Urea Cream
- Axitan
- Azenmarol
- Azicine
- Aziphar
- Azithromycin