Nhà sản xuất
Korea United Pharm
Thành phần
Mỗi viên: Capecitabin 500mg.
Mô tả
Viên nén bao phim màu quả đào, hình thuôn dài, hai mặt lồi.
Dược lực học
Capecitabin là dẫn xuất fluoropyrimidin carbamat có hoạt tính chống ung thư. Chất này là một tiền chất và có rất ít tác động dược lý cho đến khi nó được chuyển đổi thành Fluorouracil, một chất chống chuyển hóa. Vì Capecitabin được biến đổi thành Fluorouracil bởi các enzym có nồng độ cao hơn trong các khối u so với các mô bình thường và huyết tương, dẫn tới nồng độ của dạng thuốc có hoạt tính trong khối u đạt được cao hơn và độc tính toàn thân thấp hơn. Trong các tế bào bình thường và các tế bào khối u, Fluorouracil được chuyển hóa thành 5-fluoro-2'-deoxyuridin monophosphat-5' (FdUMP) và 5-fluorouridin triphosphat (FUTP). Những chất chuyển hóa này sẽ làm tổn thương tế bào bằng hai cơ chế. Đầu tiên, Deoxyribonucleotid của FdUMP và đồng yếu tố folat (N5-10-methylenetetrahydrofolate) gắn với thymidylat synthase (TS) tạo thành một phức hợp gồm ba yếu tố đồng hóa trị, sự gắn kết này sẽ ức chế sự hình thành thymidylat từ 2'-deoxyuridylat. Thymidylat là một tiền chất cần thiết của thymidin triphosphat, một chất cần thiết cho sự tổng hợp tổng hợp DNA, vì vậy sự thiếu hụt hợp chất này có thể ức chế sự phân chia tế bào. Thứ hai, các men sao chép nhân có thể kết hợp một cách nhầm lẫn FUTP thay vì uridin triphosphat (UTP) trong quá trình tổng hợp RNA. Lỗi chuyển hóa này có thể ảnh hưởng tới sự tổng hợp RNA và protein.
Dược động học
Capecitabin được hấp thu nhanh chóng qua đường tiêu hóa, nồng độ tối đa trong huyết tương đạt được sau 1,5 giờ. Thức ăn làm giảm tỉ lệ và mức độ hấp thu của thuốc. Capecitabin liên kết với protein huyết tương dưới 60%. Capecitabin bị thủy phân ở gan thành 5’-deoxy-5-fluorocytidin (5’-DFCR), sau đó được chuyển hóa thành 5’-deoxy-5-fluorouridin và tiếp theo thành 5-fluorouracil trong tế bào cơ thể. 5-fluorouracil lại tiếp tục được chuyển hóa. Khoảng 3% liều dùng của Capecitabin được đào thải qua nước tiểu dưới dạng chưa chuyển hóa.
Chỉ định/Công dụng
Ung thư đại trực tràng
Xeltabine được chỉ định điều trị bước 1 ở bệnh nhân ung thư đại trực tràng di căn.
Xeltabine được chỉ định điều trị hỗ trợ cho những bệnh nhân ung thư đại tràng giai đoạn III sau phẫu thuật (Duke C).
· Xeltabine được chỉ định đơn trị liệu ở bệnh nhân đã cắt bỏ hoàn toàn khối u nguyên phát khi chế độ đơn trị liệu với Fluoropyrimidin được ưu tiên lựa chọn.
· Xeltabine được chỉ định phối hợp với Oxaliplatin ở bệnh nhân đã cắt bỏ hoàn toàn khối u nguyên phát.
Ung thư vú
Xeltabine được chỉ định đơn trị liệu trong điều trị những bệnh nhân ung thư vú tiến triển tại chỗ hoặc di căn sau khi thất bại với chế độ hóa trị liệu với thuốc nhóm taxan (Paclitaxel hoặc Docetaxel) và cả nhóm anthracyclin và hoặc cho những ung thư khác mà không có chỉ định dùng anthracyclin (ví dụ bệnh nhân điều trị liều tích lũy Doxorubicin 400 mg/m2 hoặc tương đương).
Xeltabine phối hợp với Docetaxel được chỉ định để điều trị những bệnh nhân ung thư vú tiến triển tại chỗ hoặc di căn sau khi thất bại với hóa trị liệu độc tế bào.
Ung thư dạ dày: Xeltabine phối hợp với hợp chất platin được chỉ định điều trị bước một cho những bệnh nhân ung thư dạ dày tiến triển.
Liều lượng & Cách dùng
Nên uống Xeltabine với nước trong vòng 30 phút sau khi ăn.
Đơn trị liệu
Ung thư đại trực tràng và ung thư vú: Liều đơn trị liệu được khuyến cáo của Xeltabine là 1250 mg/m2, uống 2 lần mỗi ngày (sáng và tối, tương đương với tổng liều 2500 mg/m2 mỗi ngày) trong 2 tuần, sau đó ngưng thuốc 1 tuần trong chu kỳ điều trị 3 tuần.
Điều trị phối hợp
Ung thư vú: Trong trường hợp điều trị phối hợp với Docetaxel, liều khuyến cáo của Xeltabine là 1250 mg/m2, uống 2 lần mỗi ngày trong 2 tuần sau đó ngưng thuốc 1 tuần, phối hợp với Docetaxel 75 mg/m2 truyền tĩnh mạch trong vòng 1 giờ mỗi 3 tuần. Theo hướng dẫn sử dụng của Docetaxel, nên chuẩn bị trước thuốc nhóm corticosteroid đường uống như Dexamethason trước khi dùng Docetaxel ở những bệnh nhân điều trị kết hợp Xeltabine với Docetaxel.
Ung thư đại trực tràng: Trong trường hợp điều trị phối hợp với Oxaliplatin, liều khuyến cáo của Xeltabine là 1000 mg/m2, uống 2 lần mỗi ngày trong 2 tuần sau đó ngưng thuốc 1 tuần, phối hợp với Oxaliplatin 130 mg/m2 truyền tĩnh mạch trong vòng 2 giờ vào ngày đầu tiên mỗi 3 tuần, trong vòng 24 tuần. Theo hướng dẫn sử dụng của Oxaliplatin, nên chuẩn bị trước thuốc chống nôn trước khi dùng Oxaliplatin ở những bệnh nhân điều trị kết hợp Xeltabine với Oxaliplatin.
Ung thư dạ dày
Liều khuyến cáo của Xeltabine là 1000 mg/m2 uống 2 lần mỗi ngày trong 14 ngày sau đó ngưng thuốc 7 ngày, hoặc 625 mg/m2 uống 2 lần mỗi ngày nếu điều trị liên tục. Theo hướng dẫn sử dụng của Cisplatin, nên chuẩn bị trước để đảm bảo nước và thuốc chống nôn trước khi dùng Cisplatin ở những bệnh nhân điều trị kết hợp Xeltabine với Cisplatin.
· Phối hợp với Cisplatin: Liều khuyến cáo của Xeltabine là 1000 mg/m2, uống 2 lần mỗi ngày trong 2 tuần sau đó ngưng thuốc 1 tuần, phối hợp với Cisplatin 80 mg/m2 truyền tĩnh mạch trong 2 giờ mỗi 3 tuần.
· Phối hợp với Cisplatin hoặc Epirubicin: Liều khuyến cáo của Xeltabine là 625 mg/m2, uống 2 lần mỗi ngày liên tục trong 3 tuần, phối hợp với Cisplatin 60 mg/m2 truyền tĩnh mạch trong 2 giờ và Epirubicin 50 mg/m2 tiêm tĩnh mạch nhanh mỗi 3 tuần.
Cách tính liều chuẩn và giảm liều theo diện tích bề mặt cơ thể
- xem Bảng 1 & Bảng 2.
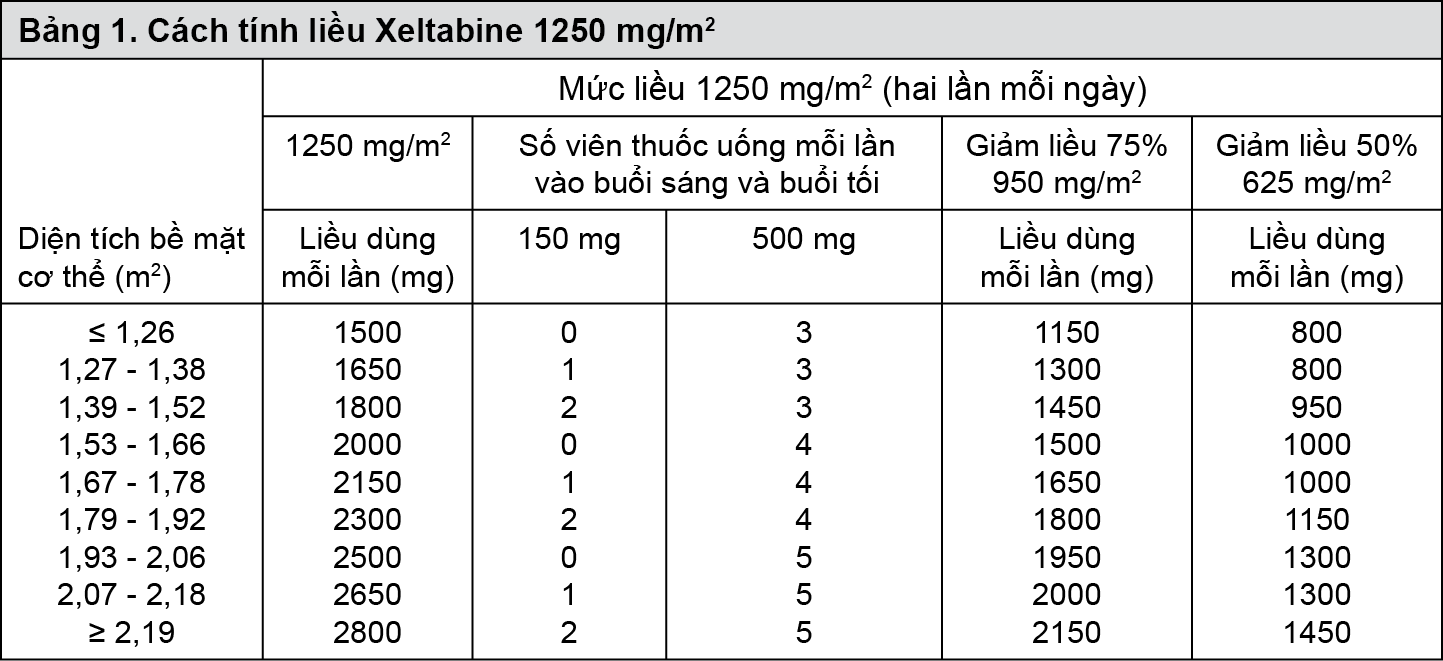
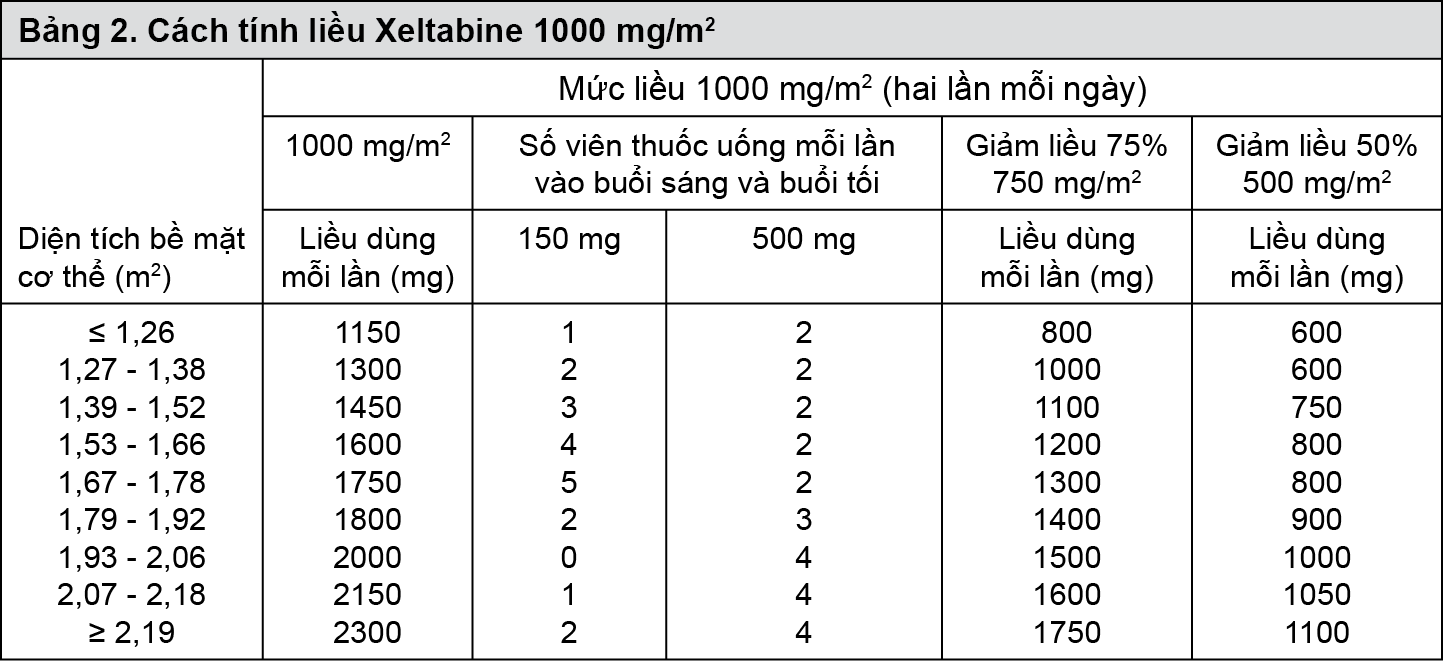
Điều chỉnh liều trong điều trị
Độc tính do dùng Xeltabine có thể kiểm soát bằng việc điều trị triệu chứng và/hoặc thay đổi liều dùng Xeltabine (ngừng điều trị hoặc giảm liều). Khi đã giảm liều thì không nên tăng ở những lần sau đó.
Những độc tính được bác sĩ điều trị cân nhắc là gần như không nghiêm trọng hoặc không đe dọa mạng sống thì điều trị có thể tiếp tục với liều ban đầu mà không cần giảm liều hoặc ngưng liều như rụng tóc, thay đổi vị giác, thay đổi về móng... Bệnh nhân dùng Xeltabine nên được thông báo về việc ngưng điều trị ngay lập tức nếu xuất hiện độc tính mức độ trung bình hoặc nặng hơn.
Kế hoạch giảm liều Xeltabine
- xem Bảng 3.
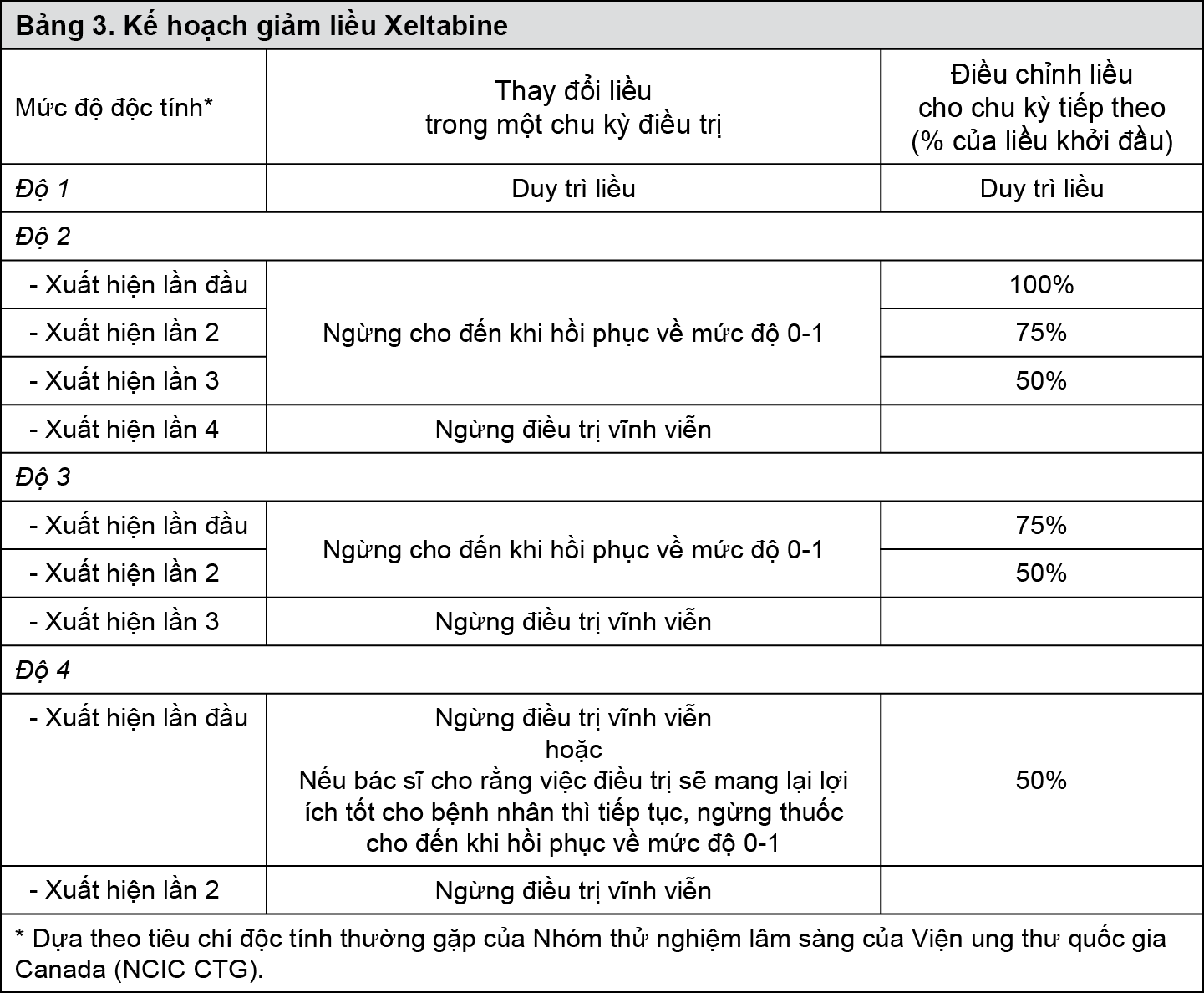
Lưu ý về huyết học: Không nên điều trị Xeltabine ở những bệnh nhân có lượng bạch cầu trung tính ban đầu < 1,5x109/l và/hoặc tiểu cầu < 100x109/l. Nếu những đánh giá xét nghiệm đột xuất trong suốt chu kỳ điều trị cho thấy lượng bạch cầu trung tính < 1,0x109/l hoặc tiểu cầu < 75x109/l thì nên ngưng điều trị Xeltabine.
Điều chỉnh liều do độc tính khi điều trị kết hợp Xeltabine với thuốc khác: Dựa trên bảng kế hoạch giảm liều Xeltabine và theo hướng dẫn sử dụng của các thuốc khác một cách thích hợp nhất.
· Khi bắt đầu một chu kỳ điều trị, nếu hoãn điều trị được chỉ định cho Xeltabine hoặc các thuốc khác, thì sau đó nên hoãn tất cả các thuốc cho đến khi có những yêu cầu được dùng tất cả các thuốc trở lại.
· Trong suốt chu kỳ điều trị những độc tính được cân nhắc bởi bác sĩ điều trị mà không liên quan đến Xeltabine thì việc điều trị với Xeltabine nên được tiếp tục và tiến hành điều chỉnh liều của những thuốc khác dựa vào thông tin của tờ hướng dẫn sử dụng.
· Nếu các thuốc khác phải ngừng điều trị vĩnh viễn thì điều trị bằng Xeltabine có thể được bắt đầu lại nếu có các yêu cầu được dùng Xeltabine trở lại.
Quá Liều
Biểu hiện của quá liều cấp tính bao gồm buồn nôn, nôn, tiêu chảy, viêm niêm mạc, kích thích và chảy máu đường tiêu hóa, và suy tủy.
Việc điều trị quá liều nên bao gồm điều trị thông thường và các can thiệp về y khoa hỗ trợ nhằm chữa trị những triệu chứng lâm sàng đang hiện diện và đề phòng những biến chứng có thể xảy ra.
Chống chỉ định
Không sử dụng thuốc ở những bệnh nhân sau:
- Quá mẫn với Capecitabin hoặc với bất kỳ thành phần nào của thuốc.
- Có tiền sử xảy ra các phản ứng không mong muốn và nghiêm trọng khi điều trị với Fluoropyrimidin.
- Phụ nữ có thai và cho con bú.
- Bệnh nhân suy thận nặng (độ thanh thải Creatinin < 30ml/phút).
- Bệnh nhân đang điều trị với Sorivudin hoặc các chất tương tự có liên quan về mặt hóa học như Brivudin.
- Bệnh nhân được biết là có thiếu hụt men dihydropyrimidin dehydrogenase (DPD) (do đã ghi nhận các độc tính nghiêm trọng không dự đoán trước liên quan tới Fluorouracil như như viêm miệng, tiêu chảy, giảm bạch cầu trung tính và nhiễm độc thần kinh).
- Bệnh nhân giảm bạch cầu, giảm bạch cầu trung tính, giảm tiểu cầu nặng.
- Bênh nhân suy gan nặng.
- Bệnh nhân đang uống dạng phức hợp Tegafur, Gimeracil, Oteracil kali hoặc trong vòng 7 ngày sau khi ngưng thuốc.
- Thuốc có chứa tá dược Lactose khan, do đó không nên sử dụng thuốc này ở những bệnh nhân có vấn đề về di truyền hiếm gặp như không dung nạp galactose, thiếu hụt Lapp lactase hoặc kém hấp thu glucose-galactose.
Sử dụng ở phụ nữ có thai và cho con bú
Chưa có các nghiên cứu trên phụ nữ có thai dùng Xeltabine. Trong các nghiên cứu độc tính sinh sản trên động vật, dùng Capecitabin có thể gây chết phôi thai và quái thai. Những bằng chứng này được dự đoán ở những dẫn xuất của Fluoropyrimidin. Sử dụng Capacitabin trong khi mang thai có thể gây hại cho thai nhi, Capecitabin được cho rằng có khả năng gây quái thai ở người. Vì vậy chống chỉ định Capecitabin trong khi mang thai. Nếu dùng Xeltabine trong khi mang thai hoặc nếu bệnh nhân có thai trong khi đang dùng thuốc này phải thông báo cho bệnh nhân biết nguy cơ tiềm ẩn cho thai nhi. Nên sử dụng biện pháp tránh thai trong khi sử dụng Xeltabine.
Chưa biết thuốc có được bài tiết qua sữa mẹ hay không. Trong một nghiên cứu ở chuột đang cho con bú, một lượng đáng kể Capecitabin và các chất chuyển hóa được tìm thấy trong sữa. Nên ngừng cho con bú trong khi điều trị với Xeltabine.
Tương tác
Thuốc chống đông máu Coumarin: Bệnh nhân dùng các thuốc chống đông dẫn xuất của coumarin cùng với Xeltabine nên được theo dõi cẩn thận về những thay đổi các thông số đông máu (PT hoặc INR) và phải điều chỉnh liều thuốc chống đông cho phù hợp. Đã ghi nhận các thông số đông máu thay đổi và/hoặc chảy máu ở những bệnh nhân dùng Xeltabine cùng với các thuốc chống đông dẫn xuất coumarin như Warfarin và Phenprocoumon. Những tác dụng không mong muốn này xảy ra trong vài ngày và kéo dài tới vài tháng sau khi bắt đầu điều trị Xeltabine, và một số ít trường hợp xảy ra trong một tháng sau khi ngừng Xeltabine. Trong một nghiên cứu tương tác lâm sàng, sau khi dùng Warfarin liều đơn 20mg, việc điều trị Xeltabine làm tăng AUC của S-Warfarin khoảng 57% và giá trị INR tăng 91%. Vì chất chuyển hóa R-Warfarin không thay đổi, điều này chứng tỏ Capecitabin ức chế isozym 2C9 nhưng không ảnh hưởng trên các isozym 1A2 và 3A4.
Thuốc kháng acid: Tác động của nhôm hydroxyd và thuốc kháng acid có chứa magnesi hydroxyd lên dược động học của Capecitabin đã được nghiên cứu. Nồng độ huyết tương của Capecitabin và một chất chuyển hóa (5'DFCR) tăng ít; không thấy tác động lên ba chất chuyển hóa chính (5'DFUR, 5-FU và FBAL).
Allopurinol: Tương tác với Allopurinol đã được ghi nhận ở 5-FU, thuốc có thể làm giảm hiệu quả của 5-FU. Do đó nên tránh sử dụng đồng thời Allopurinol và Xeltabine.
Sorivudin và các thuốc tương tự: Tương tác thuốc-thuốc có ý nghĩa lâm sàng giữa Sorivudin và 5-FU, là do Sorivudin ức chế dihydropyrimidin dehydrogenase, đã được mô tả trong tài liệu nghiên cứu. Tương tác này, dẫn tới tăng độc tính của dihydropyrimidin dehydrogenase, có thể nguy hiểm đến tính mạng. Vì vậy, không nên dùng Xeltabine với Sorivudin hoặc các thuốc tương tự có liên quan về mặt hóa học như Brivudin (xem phần Chống chỉ định). Cần đợi ít nhất 4 tuần sau khi kết thúc điều trị với Sorivudin hoặc các thuốc tương tự có liên quan về mặt hóa học như Brivudin trước khi bắt đầu trị liệu với Xeltabine.
Phenytoin: Nồng độ huyết tương của Phenytoin tăng dẫn đến triệu chứng của ngộ độc Phenytoin trong 1 trường hợp được ghi nhận trong khi dùng đồng thời Xeltabine và Phenytoin. Những bệnh nhân dùng đồng thời Phenytoin và Xeltabine nên được theo dõi cẩn thận vì nồng độ huyết tương của Phenytoin tăng.
Protein huyết tương: Capecitabin có tỉ lệ gắn kết với protein huyết tương thấp (54%). Do đó tương tác do cạnh tranh vị trí với các thuốc có tỉ lệ gắn kết với protein huyết tương cao không đáng kể.
Cytochrom P-450 2C9: Xem phần các dẫn chất của thuốc chống đông Coumarin về sự tương tác với các isozym 1A2, 2C9, 3A4.
Interferon alpha: Liều dung nạp tối đa của Xeltabine là 2000 mg/m2/ngày khi kết hợp Interferon alpha-2a (3 MIU/m2/ngày), trong khi liều dung nạp tối đa của Xeltabine khi sử dụng riêng lẻ là 3000 mg/m2/ngày.
Xạ trị: Liều dung nạp tối đa của Xeltabine khi sử dụng riêng lẻ là 3000 mg/m2/ngày, tuy nhiên khi kết hợp với xạ trị trong điều trị ung thư trực tràng liều dung nạp tối đa của Xeltabine là 2000 mg/m2/ngày (sử dụng chế độ điều trị liên tục hoặc mỗi ngày từ thứ hai đến thứ sáu trong đợt xạ trị 6 tuần).
Acid folinic: Một nghiên cứu kết hợp Xeltabine và acid folinic cho thấy acid folinic không ảnh hưởng nhiều đến dược động học của Xeltabine và các chất chuyển hóa. Tuy nhiên, acid folinic có ảnh hưởng trên dược lực học của Xeltabine và làm gia tăng độc tính của Xeltabine: Liều dung nạp tối đa của Xeltabine khi sử dụng riêng lẻ với chế độ điều trị liên tục là 3000 mg/m2/ngày trong khi đó chỉ là 2000 mg/m2/ngày khi kết hợp với acid folinic (30mg uống 2 lần mỗi ngày).
Phức hợp Tegafur, Gimeracil và Oteracil kali: Chống chỉ định khi sử dụng đồng thời với Xetabine hoặc trong vòng 7 ngày sau khi ngưng uống Xeltabine. Hàm lượng Fluorouracil trong máu tăng đáng kể do Gimeracil ức chế sự chuyển hóa của Fluorouracil gây rối loạn đường tiêu hóa như rối loạn máu nặng, tiêu chảy, viêm miệng…
Oxaliplatin: Không có sự khác biệt đáng kể khi tiếp xúc với Capecitabin và các chất chuyển hóa, platin tự do hay platin toàn phần khi Capecitabin phối hợp với Oxaliplatin hoặc Oxaliplatin và Bevacizumab.
Bevacizumab: Không có sự ảnh hưởng có ý nghĩa lâm sàng của Bevacizumab lên các thông số dược động học của Capecitabin hoặc các chất chuyển hóa của nó khi điều trị phối hợp với Oxaliplatin.
Tác dụng ngoại ý
Tương tự như Fluorouracil, tiêu chảy (có thể xảy ra trầm trọng), buồn nôn và nôn, đau bụng, viêm miệng, hội chứng bàn tay-bàn chân (rối loạn cảm giác đỏ da lòng bàn tay-bàn chân) thường xảy ra với Capecitabin và có thể giới hạn liều dùng. Các tác dụng không mong muốn khác thường xảy ra bao gồm: mệt mỏi, suy nhược, chán ăn. Phát ban, rụng tóc, ban đỏ, khô da, ngứa, rối loạn sắc tố da và rối loạn móng có thể xảy ra. Một số tác dụng không mong muốn khác như: sốt, đau, đau cơ, táo bón, khó tiêu, dị cảm, nhức đầu, chóng mặt, mất ngủ, tăng hoặc giảm calci huyết và mất nước. Viêm da, ngộ độc tim và suy tủy xương cũng đã được ghi nhận. Tăng biliribin máu cũng đã xảy ra.
Ảnh hưởng đến lipid máu: Đã ghi nhận trường hợp tăng triglycerid máu trên những bệnh nhân uống Capecitabin ở giai đoạn đầu điều trị. Mặc dù đã sử dụng liệu pháp hạ lipid máu, nhưng nồng độ triglycerid vẫn cao hơn mức bình thường và nồng độ này chỉ giảm sau vài tuần ngưng dùng Capecitabin.
Ảnh hưởng trên mắt: Đã ghi nhận trường hợp kích ứng mắt nặng với lắng đọng giác mạc và suy giảm thị lực ở 2 bệnh nhân sử dụng Capecitabin. Triệu chứng phục hồi sau vài tuần ngưng dùng thuốc.
Ảnh hưởng trên tim: Đau ngực do thiếu máu cục bộ cấp tính đã được báo cáo, thường xảy ra vài ngày sau khi bắt đầu sử dụng Capecitabin. Triệu chứng từ các ca báo cáo và tỷ lệ trường hợp mắc phải trong các nghiên cứu pha III tương tự ở những bệnh nhân sử dụng Fluorouracil. Các triệu chứng được báo cáo có thể phục hồi, tuy nhiên đã ghi nhận trường hợp chết do nhồi máu cơ tim. Một bệnh nhân đã xảy ra ngộ độc tim khi điều trị Fluorouracil, nhưng những trường hợp khác các yếu tố nguy cơ không rõ ràng.
Ảnh hưởng trên hệ thần kinh: Bệnh thần kinh ngoại biên và bệnh não đã được báo cáo liên quan đến việc sử dụng Capecitabin.
Ảnh hưởng trên da và móng: Hội chứng tay-chân thường gặp ở bệnh nhân điều trị bằng Capecitabin, các tổn thương da khác hiếm khi gặp. Đã ghi nhận trường hợp mất móng và bong móng. U hạt có mủ cũng đã được ghi nhận khi sử dụng Capecitabin, có sự tái tạo sắc tố da trong rối loạn sắc tố da do hóa trị liệu.
Phản ứng quá mẫn: Một bệnh nhân đã thực hiện truyền tĩnh mạch liên tục thành công với Fluorouracil mặc dù trước đó đã xảy ra quá mẫn với Capecitabin. Có thể cho rằng phản ứng quá mẫn có thể gây ra do Capecitabin và các chất chuyển hóa trung gian, và không có sự nhạy cảm chéo giữa Capecitabin và Fluorouracil.
Hội chứng bàn tay-bàn chân (rối loạn cảm giác đỏ da lòng bàn tay-bàn chân): Hay gặp khi sử dụng Capecitabin đơn trị liệu hoặc như một phần tác dụng không mong muốn của phác đồ hóa trị liệu kết hợp. Hội chứng xảy ra trong vòng 2 chu kỳ đầu của chế độ đơn trị liệu và trong 3 chu kỳ đầu của chế độ điều trị kết hợp do sự thay đổi của liều của Capecitabin trong điều trị kết hợp. Sử dụng phối hợp với Docetaxel và viêm miệng do hóa trị liệu trước đó được cho là các yếu tố nguy cơ đáng kể cho sự xuất hiện hội chứng này. Phương pháp kiểm soát duy nhất có hiệu quả là điều trị gián đoạn và điều chỉnh liều. Cần sử dụng các biện pháp hỗ trợ để giảm đau, khó chịu và ngăn ngừa nhiễm trùng thứ phát. Điều trị đồng thời với Celecoxib được cho là giảm tỷ lệ mắc hội chứng bàn tay-bàn chân gây ra do Capecitabin.
Hội chứng phân giải khối u: Một trường hợp tử vong đã được ghi nhận do hội chứng phân giải khối u sau khi sử dụng Capecitabin.
Thận trọng
Tiêu chảy: Xeltabine có thể gây tiêu chảy, đôi khi nặng. Bệnh nhân bị tiêu chảy nặng nên được theo dõi cẩn thận và nếu bị mất nước, nên bù nước và chất điện giải. Nên bắt đầu liệu pháp chuẩn điều trị tiêu chảy (như dùng Loperamid) và tiến hành giảm liều khi cần thiết.
Mất nước: Mất nước nên được ngăn chặn hoặc điều trị kịp thời. Những bệnh nhân chán ăn, suy nhược, buồn nôn, nôn hoặc tiêu chảy có thể bị mất nước nhanh chóng. Nếu xuất hiện mất nước độ 2 (hoặc cao hơn), nên ngừng điều trị Xeltabine ngay lập tức và tiến hành bù nước. Không nên điều trị lại khi bệnh nhân vẫn còn mất nước và bất kỳ nguyên nhân sớm nào gây ra phải được điều chỉnh hoặc kiểm soát. Khi cần thiết nên điều chỉnh liều đối với những tác dụng không mong muốn xuất hiện sớm.
Hội chứng bàn tay-bàn chân (rối loạn cảm giác đỏ da lòng bàn tay-bàn chân)
· Độ 1 của hội chứng được xác định bởi tê, rối loạn cảm giác/dị cảm, cảm giác kiến bò, sưng hoặc ban đỏ không gây đau ở tay và/hoặc chân và/hoặc cảm giác khó chịu nhưng không ảnh hưởng đến sinh hoạt bình thường của bệnh nhân.
· Độ 2 được xác định là ban đỏ và sưng tay và/hoặc chân gây đau và/hoặc khó chịu ảnh hưởng đến sinh hoạt hàng ngày của bệnh nhân.
· Độ 3 được xác định là sự tróc vẩy da, loét, rộp gia và đau nhiều ở tay và/hoặc chân và/hoặc cảm giác rất khó chịu khiến bệnh nhân không thể làm việc hoặc thực hiện các sinh hoạt bình thường hàng ngày.
Nếu xảy ra hội chứng bàn tay-bàn chân độ 2 hoặc 3, nên ngưng dùng Xeltabine cho đến khi các triệu chứng hồi phục hoặc giảm xuống độ 1.
Sau khi xuất hiện hội chứng bàn tay-bàn chân độ 3, nên giảm liều tiếp theo của Xeltabine. Khi sử dụng kết hợp Xeltabine và Cisplatin, không nên sử dụng vitamin B6 (Pyridoxin) để điều trị triệu chứng hoặc điều trị dự phòng thứ phát của hội chứng bàn tay-bàn chân vì theo các báo cáo đã công bố, điều này có thể làm giảm hiệu quả của Cisplatin.
Độc tính tim mạch: Độc tính trên tim mạch đđược ghi nhận ở Xeltabine cũng tương tự độc tính ghi nhận được ở Fluoropyrimidin khác. Những độc tính này bao gồm nhồi máu cơ tim, đau thắt ngực… Những tác dụng không mong muốn này thường gặp hơn ở những bệnh nhân có tiền sử bệnh mạch vành. Do đó cần thận trong khi sử dụng thuốc ở những bệnh nhân có tiền sử bị bệnh tim mạch.
Bệnh nhân được điều trị bằng Xeltabine nên được theo dõi cẩn thận về độc tính. Phần lớn các tác dụng không mong muốn có thể hồi phục và không yêu cầu phải ngừng thuốc vĩnh viễn, mặc dù cần phải ngừng thuốc tạm thời và giảm liều.
Thận trọng chung
Nên sử dụng thuốc thận trọng ở những bệnh nhân sau:
- Bệnh nhân suy thận nặng.
- Bệnh nhân suy gan.
- Bệnh nhân có tiền sử tăng hoặc giảm calci huyết.
- Bệnh nhân có tiền sử bệnh thần kinh trung ương hoặc thần kinh ngoại biên, như u não di căn, bệnh thần kinh.
- Bệnh nhân có tiền sử đái tháo đường hoặc rối loạn điện giải.
- Người già.
- Bệnh nhân có tiền sử bệnh mạch vành (nhồi máu cơ tim có thể xảy ra).
- Bệnh nhân suy tủy (suy tủy có thể trầm trọng hơn).
- Bệnh nhân bị loét hoặc xuất huyết đường tiêu hóa.
Sử dụng ở người già
Không cần điều chỉnh liều khởi đầu khi dùng Xeltabine đơn trị liệu. Tuy nhiên các tác dụng không mong muốn liên quan đến điều trị độ 3 hoặc độ 4 xuất hiện thường xuyên hơn ở bệnh nhân trên 60 tuổi so với những bệnh nhân trẻ tuổi.
Khi điều trị Xeltabine kết hợp với các thuốc khác ở người già ≥65 tuổi, thường xảy ra các tác dụng không mong muốn độ 3 và độ 4 có thể dẫn đến tạm ngừng điều trị. Nên theo dõi cẩn thận khi dùng thuốc ở bệnh nhân ≥65 tuổi.
· Khi điều trị kết hợp với Docetaxel: Tỷ lệ tăng các tác dụng không mong muốn nghiêm trọng liên quan đến điều trị và các tác dụng không mong muốn liên quan đến điều trị độ 3 hoặc độ 4 tăng ở bệnh nhân ≥60 tuổi. Với những bệnh nhân ≥60 tuổi nên giảm liều khởi đầu của Xeltabine xuống còn 75% (950 mg/m2 hai lần mỗi ngày). Nếu không xuất hiện độc tính ở liều đã giảm trên bệnh nhân ≥60 tuổi được điều trị phối hợp Xeltabine và Docetaxel, liều Xeltabine có thể tăng dần một cách thận trọng đến liều 1250 mg/m2 hai lần mỗi ngày.
Sử dụng ở trẻ em: Chưa có kinh nghiệm sử dụng thuốc ở trẻ em dưới 18 tuổi.
Sử dụng ở bệnh nhân suy gan: Chưa có dữ liệu về tính an toàn và hiệu quả của thuốc ở bệnh nhân suy gan để đưa ra liều khuyến cáo phù hợp. Xeltabine nên được sử dụng một cách thận trọng ở bệnh nhân suy gan di căn hoặc không di căn từ nhẹ đến trung bình. Xeltabine có thể làm tăng bilirubin máu. Nên ngưng dùng thuốc nếu bilirubin tăng > 3,0xULN (trên giới hạn bình thường) có liên quan đến điều trị hoặc men gan aminotransferase (ALT, AST) tăng > 2,5xULN có liên quan đến điều trị. Có thể bắt đầu điều trị lại khi bilirubin giảm xuống còn ≤ 3,0xULN hoặc men gan aminotransferase giảm xuống còn ≤ 2,5xULN.
Sử dụng ở bệnh nhân suy thận: Xeltabine chống chỉ định ở bệnh nhân suy thận nặng (độ thanh thải Creatinin dưới 30ml/phút). Các phản ứng không mong muốn ở mức độ 3 hoặc 4 xảy ra ở bệnh nhân suy thận trung bình (độ thanh thải Creatinin 30-50ml/phút) nhiều hơn so với người bình thường. Bệnh nhân suy thận trung bình, khuyến cáo giảm liều xuống 75% với liều khởi đầu là 1250 mg/m2, không cần giảm liều với liều khởi đầu là 1000 mg/m2. Bệnh nhân suy thận nhẹ (độ thanh thải Creatinin dưới 51-80ml/phút) không cần điều chỉnh liều khởi đầu.
Nên theo dõi cẩn thận và ngừng điều trị ngay lập tức nếu bệnh nhân có các tác dụng ngoại ý độ 2, 3, hoặc 4 và sau đó điều chỉnh liều như bảng chỉ dẫn. Nên tạm ngừng điều trị Xeltabine, nếu độ thanh thải Creatinin giảm dưới 30ml/phút.
Điều chỉnh liều cho những bệnh nhân bị suy thận áp dụng cho cả việc điều trị đơn liều và điều trị phối hợp.
Ảnh hưởng đến khả năng lái xe và vận hành máy móc: Xeltabine ảnh hưởng nhẹ hoặc trung bình đến khả năng lái xe và vận hành máy móc do Xeltabine có thể gây buồn ngủ, mệt mỏi và nôn mửa.
Bảo quản
Bảo quản ở nhiệt độ phòng không quá 30ºC.
Phân loại ATC
L01BC06 - capecitabine
Trình bày/Đóng gói
Viên nén bao phim: hộp 12 vỉ x 10 viên.
- Abacavir
- Abernil
- Abiiogran
- Acarbose
- ACC
- Acebutolol
- Acenocoumarol
- Acetate Ringer's
- Acetazolamide
- Acetylcystein
- Acetylsalicylic acid
- Aciclovir
- Acid acetylsalicylic
- Acid aminocaproic
- Acid ascorbic
- Acid boric
- Acid chenodeoxycholic
- Acid ethacrynic
- Acid folic
- Acid fusidic
- Acid iopanoic
- Acid ioxaglic
- Acid nalidixic
- Acid pantothenic
- Acid para-aminobenzoic
- Acid salicylic
- Acid tranexamic
- Acid valproic
- Acid zoledronic
- Acitretin
- Aclasta
- Aclon
- Actapulgite
- Actelsar
- Actelsar HCT
- Actemra
- Actilyse
- Acular
- Acupan
- Acuvail
- Acyclovir STADA
- Acyclovir STADA Cream
- Adalat
- Adenosin
- Adenosin Ebewe
- Adipiodon
- Advagraf
- Aerius
- Afinitor
- Agicarvir
- Agifovir-E
- Agilosart
- Agilosart-H
- Agimepzol
- Agimosarid
- Agimstan
- Agimstan-H
- Agiremid
- Agivastar
- Aibezym
- Air-X
- Alaxan
- Albendazol
- Albiomin
- Albumin
- Albumin người Grifols 20%
- Albuminar
- AlbuRx
- Albutein
- Alcuronium chloride
- Aldesleukin
- Alendronat
- Alertin
- Alfa-Lipogamma 600 Oral
- Alfuzosin hydrochlorid
- Algotra
- Alimemazin
- Alimta
- Allipem
- Allopurinol
- Allopurinol STADA
- Aloxi
- Alprazolam
- Alpha Chymotrypsin
- Alpha tocopherol
- Alphachymotrypsin Glomed
- Alphagan-P
- Aluvia
- Alzental
- Amaryl
- Ambroco
- Ambroxol
- Amcinol-Paste
- Amigold
- Amikacin
- Aminocaproic acid
- Aminoleban
- Aminoleban Oral
- Aminosteril N-Hepa
- Amiparen
- Amitriptyline
- Amiyu
- Amlodipine
- Amlor
- Amoxicillin
- Amoxicillin & clavulanate
- Ampicillin
- Amquitaz
- Anaferon for children
- Anargil
- Anaropin
- Andriol Testocaps
- Anepzil
- Anyfen
- Apaisac
- Apidra SoloStar
- Apitim 5
- Aprovel
- Aquaphil
- Arcalion
- Arcoxia
- Aricept Evess
- Arimidex
- Arnetine
- Artrodar
- A-Scabs
- Ascorbic acid
- Asperlican/Candinazol
- Aspilets EC
- Aspirin
- Asthmatin
- Atelec
- Atocib 120
- Atocib 90
- Atosiban PharmIdea
- Atozet
- Attapulgite
- Atussin
- Atropin
- Augbactam
- Augmentin Sachet
- Augmentin SR
- Augmentin Tablets
- Augmex
- Avamys
- Avastin
- Avelox Dịch truyền
- Avelox Viên nén
- Avodart
- Axcel Cefaclor-125 Suspension
- Axcel Cetirizine Syrup
- Axcel Chlorpheniramine
- Axcel Dexchlorpheniramine
- Axcel Dicyclomine-S Syrup
- Axcel Diphenhydramine Paediatric Syrup
- Axcel Erythromycin ES
- Axcel Eviline
- Axcel Fungicort Cream
- Axcel Fusidic acid Cream
- Axcel Fusidic acid-B Cream
- Axcel Hydrocortisone Cream
- Axcel Lignocaine 2% Sterile Gel
- Axcel Loratadine
- Axcel Miconazole Cream
- Axcel Paracetamol
- Axcel Urea Cream
- Axitan
- Azenmarol
- Azicine
- Aziphar
- Azithromycin






