Nhà sản xuất
AstraZeneca
Thành phần
Symbicort Rapihaler 80/4.5 Mỗi liều: Budesonid 80μg, formoterol 4.5μg.
Symbicort Rapihaler 160/4.5 Mỗi liều: Budesonid 160μg, formoterol 4.5μg.
Dược lý
Đặc tính dược lực
Symbicort Rapihaler chứa budesonid và formoterol, các chất này có cơ chế tác động khác nhau và có tác động cộng hợp làm giảm các đợt kịch phát hen và COPD. Các đặc tính chuyên biệt của budesonid và formoterol cho thấy sản phẩm kết hợp có thể dùng như liệu pháp duy trì thường xuyên và giảm triệu chứng hen và điều trị triệu chứng cho bệnh nhân COPD từ trung bình đến nặng.
Budesonid
Budesonid là một glucocorticosteroid với tác động kháng viêm tại chỗ mạnh. Budesonid cho thấy tác dụng chống phản vệ và kháng viêm trong các nghiên cứu kích thích trên động vật và người, biểu hiện bằng việc giảm tắc nghẽn phế quản tức thì cũng như giai đoạn muộn của phản ứng dị ứng. Budesonid cũng cho thấy làm giảm phản ứng đường thở đối với tác nhân kích thích trực tiếp (histamin, methacholin) và gián tiếp (tập thể dục) trên bệnh nhân quá mẫn. Budesonid sử dụng đường hít có tác dụng kháng viêm nhanh chóng (trong vài giờ) và phụ thuộc liều, làm giảm triệu chứng và ít xảy ra các đợt kịch phát. Budesonid đường hít có ít tác dụng ngoại ý nặng so với khi sử dụng corticosteroid toàn thân. Cơ chế chính xác đối với tác động kháng viêm của glucocoticorsteroid vẫn chưa được biết.
Formoterol
Formoterol là chất chủ vận beta-2 adrenegic chọn lọc mạnh, có tác dụng làm giãn cơ trơn phế quản. Do đó thuốc có tác dụng giãn phế quản ở các bệnh nhân tắc nghẽn đường hô hấp có thể phục hồi và ở các bệnh nhân co thắt phế quản do tác nhân kích thích trực tiếp (methacholin) và gián tiếp (tập thể dục). Tác dụng làm giãn phế quản phụ thuộc vào liều với thời gian khởi phát tác dụng trong vòng 1-3 phút sau khi hít. Thời gian tác động kéo dài tối thiểu 12 giờ sau khi dùng liều đơn.
Đặc tính dược động
Sinh khả dụng của budesonid và formoterol của Symbicort Rapihaler và Symbicort Turbuhaler là tương tự nhau sau khi sử dụng liều đơn chứa 1280 μg budesonid và 36 μg formoterol (8 lần hít) ở người lớn tình nguyện khỏe mạnh. Sinh khả dụng của budesonid và formoterol của Symbicort Rapihaler cũng được so sánh với liều tương tự của sản phẩm chứa đơn thành phần, Pulmicort (budesonid) Turbuhaler, Oxis (formoterol) Turbuhaler và hỗn dịch dùng để hít có chứabudesonid và HFA được nén lại.
Không có bằng chứng về tương tác dược động học giữa budesonid và formoterol.
Budesonid
Budesonid dạng hít được hấp thu nhanh chóng và nồng độ tối đa trong huyết tương đạt được trong vòng 30 phút sau khi hít. Độ gắn kết protein huyết tương của budesonid xấp xỉ 90% và thể tích phân bố là 3 L/kg. Budesonid được sinh chuyển hóa mạnh (khoảng 90%) khi lần đầu qua gan để tạo thành chất chuyển hóa có hoạt tính glucocorticosteroid thấp. Hoạt tính glucocorticosteroid của các chất chuyển hóa chính, 6β-hydroxy-budesonid và 16α-hydroxy-prednisolon, ít hơn 1% so với hoạt tính của budesonid.
Budesonid được thải trừ bằng cách chuyển hóa chủ yếu qua CYP3A4. Các chất chuyển hóa của budesonid được bài tiết trong nước tiểu ở dạng tự do hoặc kết hợp. Chỉ có một lượng không đáng kể budesonid không đổi được tìm thấy trong nước tiểu. Budesonid có độ thanh thải toàn thân cao (xấp xỉ 1,2 L/phút) và thời gian bán thải trong huyết tương sau khi tiêm tĩnh mạch trung bình là 4 giờ.
Formoterol
Formoterol dạng hít được hấp thu nhanh chóng và nồng độ tối đa trong huyết tương đạt được trong vòng 10 phút sau khi hít. Độ gắn kết protein huyết tương khoảng 50% đối với formoterol và thể tích phân bố là khoảng 4 L/kg.
Formoterol bị bất hoạt qua các phản ứng liên hợp (các chất chuyển hóa khử O-metyl và khử formyl có hoạt tính được hình thành, nhưng chúng chủ yếu được tìm thấy ở dạng liên hợp không hoạt tính).
Phần lớn liều của formoterol được thải trừ bằng chuyển hóa qua gan sau đó bài tiết qua thận. Sau khi hít formoterol qua dụng cụ Turbuhaler 8%-13% liều phóng thích của formoterol được bài tiết dưới dạng không chuyển hóa vào nước tiểu. Formoterol có độ thanh thải toàn thân cao (xấp xỉ 1,4 L/phút) và thời gian bán thải pha cuối trung bình là 17 giờ.
Đặc tính dược động học của budesonid hoặc formoterol ở trẻ em, người lớn tuổi và bệnh nhân suy thận chưa được nghiên cứu. Khả dụng toàn thân của budesonid và formoterol có thể tăng lên ở các bệnh nhân có bệnh gan.
THỬ NGHIỆM LÂM SÀNG
Hen (suyễn)
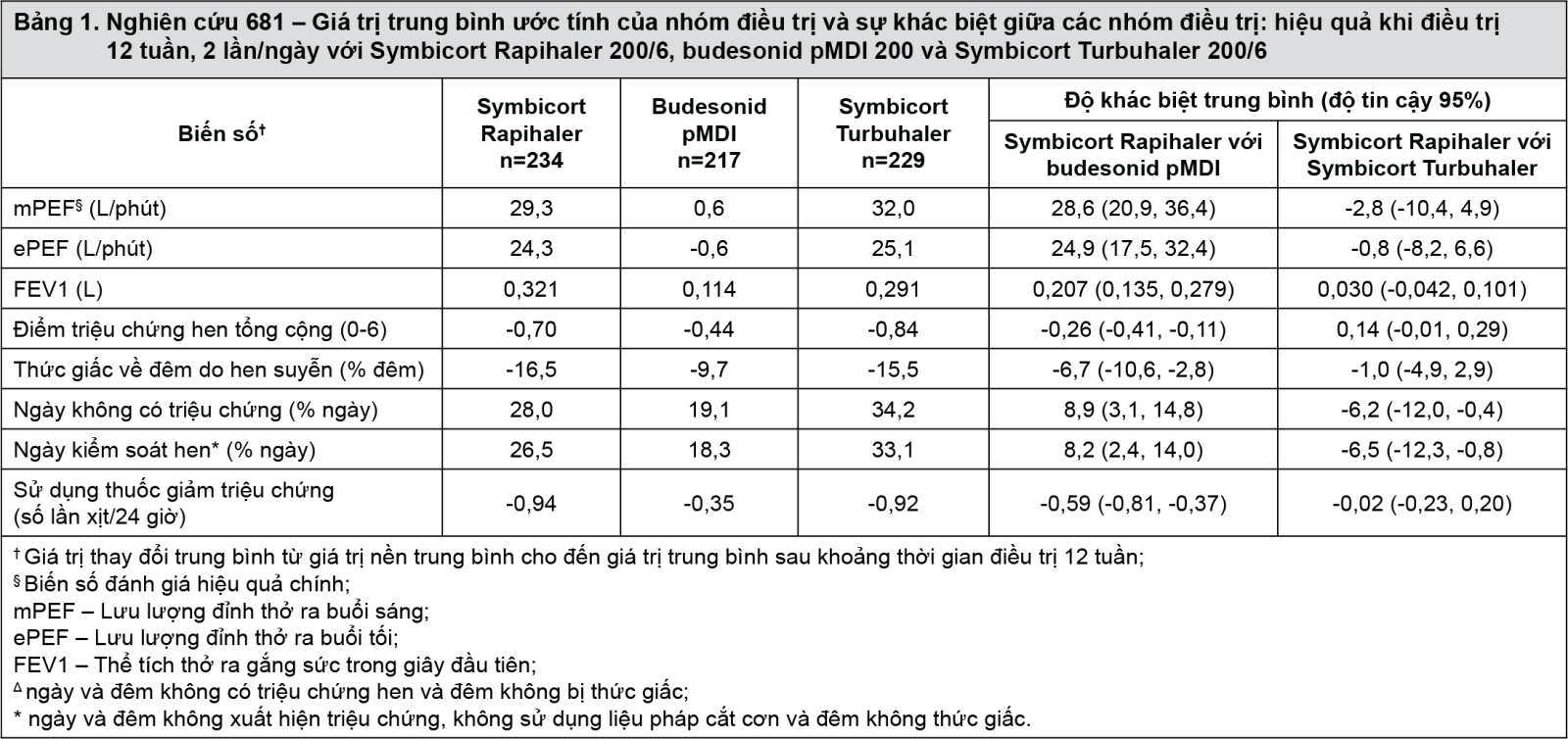
Trong nghiên cứu 681, Symbicort Rapihaler 160/4.5 (2 hít, 2 lần/ngày) được so sánh với liều tương ứng của budesonid bình xịt định liều áp lực cao (pMDI) (200 μg; 2 hít, 2 lần/ngày), hoặc Symbicort Turbuhaler (160/4.5; 2 hít, 2 lần/ngày) ở người lớn và thanh thiếu niên (≥12 tuổi) mắc hen (suyễn) từ trung bình đến nặng [trung bình của thể tích thở ra gắng sức trong giây đầu tiên (FEV1) ≥50% và ≤90% so với chỉ số dự đoán bình thường (PN) và khả năng phục hồi FEV1 ≥12%]. Symbicort Rapihaler cho thấy có thể cải thiện đáng kể lưu lượng đỉnh thở ra buổi sáng (biến số đánh giá hiệu quả chính), các thông số chức năng phổi khác, các điểm triệu chứng và thuốc giảm triệu chứng được sử dụng so với budesonid và tương đương với Symbicort Turbuhaler.
- xem Bảng 1.
Nghiên cứu 715 chủ yếu đánh giá tính an toàn của Symbicort Rapihaler 160/4.5 (2 hít, 2 lần/ngày) trong 12 tháng. Nhóm điều trị đối chứng là nhóm sử dụng tương ứng Symbicort Turbuhaler 160/4.5 và trên đối tượng dân số người lớn và trẻ vị thành niên (≥12 tuổi) với hen vừa đến nặng (trị số FEV1 trung bình ≥50% của giá trị dự đoán bình thường (PN) và khả năng phục hồi FEV1 ≥12%). Nghiên cứu là thiết kế nhãn mở.
Không có sự khác biệt có ý nghĩa thống kê giữa Symbicort Rapihaler và Symbicort Turbuhaler liên quan đến FEV1 và FVC (Dung tích sống gắng sức). Tỷ lệ bệnh nhân trải qua một hoặc nhiều đợt hen kịch phát nặng là không khác nhau giữa hai nhóm Symbicort: 11% ở nhóm Symbicort Rapihaler và 13% ở nhóm Symbicort Turbuhaler. Số lượng đợt kịch phát nặng tối đa ở mỗi bệnh nhân là 6 ở nhóm Symbicort Rapihaler là 4 ở nhóm Symbicort Turbuhaler. Không có sự khác biệt có ý nghĩa thống kê về thời gian xuất hiện đợt hen kịch phát nặng đầu tiên giữa hai nhóm điều trị.
COPD
Hiệu quả và an toàn của Symbicort trong điều trị bệnh nhân COPD từ vừa đến nặng (FEV1 (trước khi dùng thuốc giãn phế quản) ≤50% giá trị dự đoán bình thường) đã được đánh giá qua bốn thử nghiệm lâm sàng ngẫu nhiên, mù đôi, giả dược và hoạt chất, nhóm đối chứng, đa trung tâm. Hai nghiên cứu 12 tháng được thực hiện với ống hít thuốc bột khô Symbicort Turbuhaler (nghiên cứu 629 và 670), và một nghiên cứu 12 tháng và một nghiên cứu 6 tháng được thực hiện với bình xịt định liều áp lực cao (pMDI) Symbicort Rapihaler (tương ứng với nghiên cứu 001 và 002).
Nghiên cứu 001 và 002
Kế hoạch nghiên cứu là giống nhau. Cả hai nghiên cứu đều sử dụng Symbicort Rapihaler. Đối với nghiên cứu 001, sau khi thăm khám sàng lọc (lần thăm khám thứ 1), các đối tượng được đưa vào giai đoạn dẫn nhập hai tuần trước khi họ được phân ngẫu nhiên (lần thăm khám thứ 2) vào một trong bốn nhóm điều trị sau:
1/ Symbicort Rapihaler 160/4.5, kết hợp cố định 200 μg budesonid và 6 μg formoterol trong mỗi lần xịt, sử dụng 2 xịt, 2 lần/ngày.
2/ Symbicort Rapihaler 80/4.5, kết hợp cố định 100 μg budesonid và 6 μg formoterol trong mỗi lần xịt, sử dụng 2 xịt, 2 lần/ngày.
3/ Formoterol Turbuhaler, 6 μg mỗi hít, sử dụng 2 hít mỗi ngày.
4/ Giả dược
Nghiên cứu 002 có thêm 2 nhóm điều trị:
5/ Budesonid pMDI 200 μg mỗi lần xịt, sử dụng 2 xịt, 2 lần/ngày.
6/ Dạng kết hợp riêng lẻ của budesonid pMDI 200 μg mỗi lần xịt cộng với formoterol Turbuhaler 6 μg mỗi lần xịt, sử dụng 2 xịt mỗi loại, 2 lần/ngày.
Tổng số bệnh nhân tham gia nghiên cứu 001 là 1964 bệnh nhân và nghiên cứu 002 là 1704 bệnh nhân bị COPD từ trung bình đến nặng được phân ngẫu nhiên, trong đó có 494 bệnh nhân (ở nghiên cứu 001) và 277 bệnh nhân (ở nghiên cứu 002) được điều trị với Symbicort Rapihaler 160/4.5. Dân số nghiên cứu có tuổi trung bình từ 63 tuổi và FEV1 trung bình là 1,04-1,05 L hoặc 34% giá trị dự đoán bình thường ở mức nền.
Nghiên cứu 001
Ở nghiên cứu 001, hiệu quả được đánh giá trong vòng 12 tháng sử dụng biến số đánh giá hiệu quả chính của sự thay đổi từ mức nền ở giá trị trung bình FEV1 trước khi dùng thuốc và 1 giờ sau khi dùng thuốc trong suốt quá trình điều trị.
Kết quả chính:
- Symbicort Rapihaler 80/4.5 có sự thay đổi lớn hơn đáng kể trong chỉ số FEV1 sau khi xịt thuốc so với giả dược (trung bình bình phương tối thiểu (LS) = 0,16 L; p<0,001); tuy nhiên thay đổi của FEV1 trước khi xịt thuốc không khác biệt đáng kể so với formoterol 6 μg (trung bình bình phương tối thiểu (LS) = 0,02 L; p=0,161).
- Symbicort Rapihaler 160/4.5 cải thiện đáng kể FEV1 trước khi xịt thuốc 1 giờ so với formoterol và giả dược tương ứng là 0,04 L (p=0,008) và 0,09 L (p<0,001).
- Symbicort Rapihaler 160/4.5 cải thiệt đáng kể FEV1 sau khi xịt thuốc trong suốt quá trình điều trị so với formoterol và giả dược tương ứng là 0,03 L (p=0,023) và 0,18 L (p<0,001).
Các giá trị FEV1 được đo trong suốt 12 giờ ở một nhóm bệnh nhân (N=491). Trung vị của thời gian khởi phát giãn phế quản (chỉ số FEV1 cải thiện >15%) được nhận thấy là trong khoảng 5 phút tại thời điểm cuối của đợt điều trị trên bệnh nhân sử dụng Symbicort Rapihaler 160/4.5 (N=121). Chỉ số FEV1 cải thiện tối đa sau 2 giờ xịt thuốc và hiệu quả giãn phế quản sau khi xịt thuốc được duy trì trong suốt 12 giờ.
Các đợt kịch phát (biến số phụ):
Symbicort Rapihaler làm giảm có ý nghĩa thống kê số đợt kịch phát COPD nặng (được định nghĩa là tình trạng COPD xấu đi đòi hỏi phải sử dụng steroid đường uống hoặc/và nhập viện). Nhìn chung, trong 34,1% số bệnh nhân trải qua 1159 đợt kịch phát: trong đó Symbicort Rapihaler 160/4.5, 30,8%; Symbicort Rapihaler 80/4.5, 32,6%; giả dược 37,2%. Hầu hết các đợt kịch phát được điều trị với các glucocorticosteroid dạng uống: Symbicort Rapihaler 160/4.5, 96,5% các đợt kịch phát; Symbicort Rapihaler 80/4.5, 94,1%; giả dược 97,4%. Các nhóm điều trị được so sánh bởi giá trị trung bình của tỉ suất (RR) ước tính, Cls và giá trị p tính từ hồi quy Poisson điều chỉnh cho điều trị, quốc gia, mức độ điều trị khác nhau.
Symbicort Rapihaler 160/4.5 chứng tỏ làm giảm tỷ lệ đợt kịch phát/bệnh nhân-năm có ý nghĩa thống kê 37% (p<0,001) và 25% (p=0,004) so với bệnh nhân sử dụng giả dược và formoterol. Symbicort Rapihaler 80/4.5 giảm tỷ lệ đợt kịch phát 41% so với giả dược (p<0,001). Symbicort Rapihaler 160/4.5 kéo dài đáng kể thời gian xuất hiện đợt kịch phát COPD nặng đầu tiên so với giả dược, giảm nguy cơ của đợt kịch phát COPD nặng khoảng 26% (p=0,009). Số bệnh nhân cần điều trị (NNT) để phòng ngừa một đợt kịch phát COPD nặng trong 1 năm của Symbicort Rapihaler so với formoterol là 5,4.
Nghiên cứu 002
Trong nghiên cứu 002, hiệu quả được đánh giá trong 6 tháng sử dụng biến số đánh giá hiệu quả kết hợp chính của thay đổi từ mức nền của giá trị FEV1 trung bình trước và 1 giờ sau khi xịt thuốc trong suốt khoảng thời gian điều trị.
- Symbicort Rapihaler 80/4.5: FEV1 sau khi xịt thuốc tăng đáng kể từ mức nền đến mức trung bình của đợt điều trị (trung bình LS [95%CI] = 0,19 [0,17, 0,22]). Symbicort Rapihaler 80/4.5 thay đổi đáng kể từ mức nền so với sử dụng budesonid (trung bình bình phương tối thiểu (LS) = 0,16; p<0,001). FEV1 trước khi xịt thuốc tăng đáng kể từ mức nền đến mức trung bình của đợt điều trị, trung bình bình phương tối thiểu (LS) = 0,06 [0,03, 0,08]. Tuy nhiên, thay đổi từ mức nền trên chỉ số FEV1 trước khi sử dụng thuốc so với sử dụng formoterol là không có ý nghĩa thống kê, trung bình bình phương tối thiểu (LS) = 0,02 [-0,02, 0,05; p=0,335].
- Symbicort Rapihaler 160/4.5 cải thiện đáng kể FEV1 trước khi xịt thuốc so với formoterol khoảng 0,04 L (p=0,026) và so với giả dược và budesonid khoảng 0,08 L (p<0,001) trong cả hai nhóm so sánh.
- Symbicort Rapihaler 160/4.5 cải thiện đáng kể FEV1 sau khi xịt thuốc 1 giờ so với formoterol khoảng 0,04 L (p=0,039) và so với giả dược và budesonid khoảng 0,17 L (p<0,001) trong cả hai nhóm so sánh.
Nghiên cứu 002 không cho thấy hiệu quả trên các đợt kịch phát COPD nặng.
Các giá trị FEV1 được đo trong suốt 12 giờ ở một nhóm bệnh nhân (N=681). Trung vị thời gian khởi phát giãn phế quản (chỉ số FEV1 cải thiện >15%) được nhận thấy là trong khoảng 5 phút tại thời điểm cuối của đợt điều trị ở bệnh nhân sử dụng Symbicort Rapihaler 160/4.5 (N=101). Chỉ số FEV1 cải thiện tối đa sau 2 giờ xịt thuốc và hiệu quả giãn phế quản sau khi xịt thuốc được duy trì trong suốt 12 giờ.
Chỉ định/Công dụng
Hen (suyễn)
Symbicort Rapihaler được chỉ định điều trị hen (suyễn) khi liệu pháp kết hợp (corticosteroid hít và chất chủ vận beta-2 tác dụng kéo dài) thích hợp ở người lớn và trẻ vị thành niên. Bao gồm:
- Bệnh nhân vẫn còn triệu chứng khi sử dụng liệu pháp corticosteroid dạng hít
- Bệnh nhân được điều trị thường xuyên bởi chất chủ vận beta-2 kéo dài và liệu pháp corticosteroid dạng hít.
Symbicort Rapihaler không được dùng cho liệu pháp điều trị duy trì và giảm triệu chứng hen (SMART: Symbicort maintenance and reliever therapy).
Bệnh phổi tắc nghẽn mạn tính (COPD)
Symbicort Rapihaler 160/4.5 được chỉ định điều trị triệu chứng bệnh phổi tắc nghẽn mạn tính (COPD) (FEV1sau khi dùng thuốc giãn phế quản <70% so với chỉ số dự đoán bình thường) ở người lớn trên 18 tuổi có tiền sử các đợt kịch phát mặc dù thường xuyên sử dụng thuốc giãn phế quản.
Liều lượng & Cách dùng
Hen (suyễn)
Symbicort Rapihaler được sử dụng như liệu pháp duy trì thường xuyên, cùng với thuốc giãn phế quản tác dụng nhanh để giảm triệu chứng. Bệnh nhân được khuyên luôn có sẵn thuốc giãn phế quản tác dụng nhanh để giảm triệu chứng.
Việc tăng sử dụng thuốc giãn phế quản để giảm triệu chứng cho thấy bệnh hen đang diễn tiến nặng hơn và cần phải đánh giá lại liệu pháp điều trị hen. Liều lượng của Symbicort Rapihaler nên được cá thể hóa theo mức độ nghiêm trọng của bệnh. Khi việc kiểm soát hen đã đạt được, liều dùng nên được chỉnh xuống liều thấp nhất mà hiệu quả kiểm soát hen vẫn được duy trì.
Người lớn và trẻ vị thành niên (≥12 tuổi)
2 hít Symbicort Rapihaler (80/4.5 hoặc 160/4.5), 2 lần/ ngày. Liều duy trì hàng ngày được khuyến cáo tối đa là 4 hít (2 hít, 2 lần/ngày tương đương 800 μg budesonid/24 μg formoterol).
Đối với người lớn (≥18 tuổi) liều duy trì mỗi ngày cần cao hơn, liều duy trì hàng ngày được khuyến cáo tối đa có thể tăng thêm 4 hít Symbicort Rapihaler 160/4.5 2 lần/ngày (tương đương với 1600 μg budesonid/48 μg formoterol).
Bệnh phổi tắc nghẽn mạn tính (COPD) - Người lớn
Liều khuyến cáo: 2 hít Symbicort Rapihaler 160/4.5, 2 lần/ngày.
Thông tin tổng quát
Để có hiệu quả tốt nhất bệnh nhân nên sử dụng Symbicort Rapihaler ngay cả khi không có triệu chứng.
Người lớn tuổi
Không cần chỉnh liều ở bệnh nhân lớn tuổi.
Trẻ em
Symbicort Rapihaler không được khuyến cáo dùng cho trẻ em dưới 12 tuổi vì không có đủ dữ liệu về hiệu quả và an toàn.
Bệnh nhân suy gan/thận
Không có dữ liệu về sử dụng Symbicort Rapihaler ở các bệnh nhân suy gan hoặc suy thận. Tuy nhiên vì budesonid và formoterol chủ yếu đào thải qua chuyển hóa gan nên khả dụng toàn thân có thể tăng lên ở các bệnh nhân suy gan nặng.
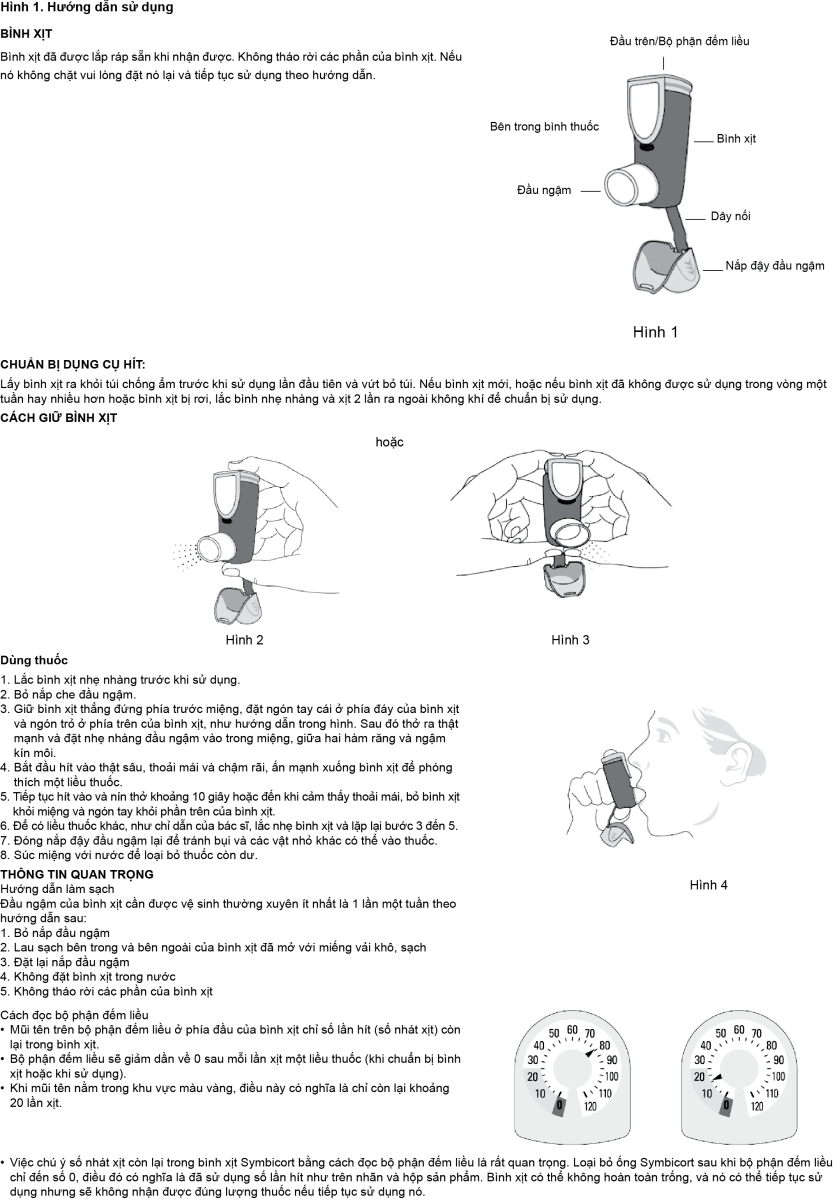
Hướng dẫn để dùng Rapihaler đúng cách
Ở mỗi lần xịt Symbicort Rapihaler, một lượng hỗn dịch thuốc được phóng ra từ bình xịt với tốc độ cao. Khi bệnh nhân hít qua đầu ngậm cùng lúc với ấn bình xịt, thuốc sẽ theo luồng khí hít vào phế quản.
Chú ý: Các hướng dẫn quan trọng cho bệnh nhân:
- Đọc kỹ hướng dẫn sử dụng trong tờ Thông tin kê toa được cung cấp trong mỗi hộp Symbicort Rapihaler.
- Lắc kỹ bình xịt trước mỗi lần sử dụng để hỗn hợp được pha trộn đúng cách.
- Khởi động bình xịt bằng cách xịt 2 lần vào trong không khí đối với bình xịt mới, hoặc bình xịt không được sử dụng nhiều hơn một tuần hoặc nếu bình xịt bị rơi.
- Cho đầu ngậm vào trong miệng. Hít vào chậm và sâu đồng thời ấn bình xịt để giải phóng thuốc. Tiếp tục hít vào và nín thở trong khoảng 10 giây hoặc đến khi cảm thấy thoải mái. Lắc lại bình xịt lần nữa và lặp lại bước này cho lần hít thứ hai.
- Súc miệng với nước sau khi sử dụng liều duy trì để giảm thiểu nguy cơ nhiễm nấm hầu-họng.
Thường xuyên vệ sinh đầu ngậm của bình xịt, ít nhất mỗi tuần một lần với vải sạch khô. Không đặt bình xịt vào trong nước.
Hướng dẫn sử dụng đúng Symbicort Rapihaler với buồng đệm
Sử dụng Symbicort Rapihaler với buồng đệm được khuyến cáo cho các bệnh nhân gặp khó khăn trong việc kết hợp hít với xịt, như trẻ em hay người lớn tuổi, để mang lại hiệu quả điều trị tốt hơn.
Chú ý: Điều này đặc biệt quan trọng cần hướng dẫn cho bệnh nhân:
Đọc kỹ hướng dẫn sử dụng trong tờ hướng dẫn sử dụng được để trong buồng đệm.
Sau mỗi nhát xịt, liều thuốc được giải phóng vào buồng hít. Buồng hít được làm trống sau hai hơi thở chậm và sâu. Trẻ nhỏ có thể cần thở 5 đến 10 lần qua đầu ngậm. Với các nhát xịt tiếp theo, quá trình được lặp lại. Với trẻ nhỏ không thể thở qua đầu ngậm, có thể sử dụng mặt nạ. Mặt nạ phù hợp có sẵn cho mỗi đối tượng bệnh nhân và cần chú ý để đảm bảo sự thích hợp.
- xem Hình 1.
Cảnh báo
Thận trọng
Điều trị hen hoặc COPD nên tuân theo các hướng dẫn điều trị quốc gia hiện hành.
Bệnh nhân bị hen nên có một kế hoạch điều trị bệnh hen cá nhân được tư vấn bởi bác sĩ. Kế hoạch này nên kết hợp chế độ điều trị từng bước được thiết lập nếu tình trạng hen suyễn của bệnh nhân được cải thiện hoặc giảm bớt. Khi ngưng thuốc sau quá trình điều trị lâu dài, liều lượng thuốc nên được giảm dần và không nên ngưng thuốc đột ngột.
Tình trạng xấu đi đột ngột hay liên tục trong kiểm soát hen hoặc COPD tiềm ẩn nguy cơ đe dọa tính mạng và bệnh nhân nên được thực hiện các đánh giá y khoa khẩn cấp. Ở tình huống này, nên xem xét tới việc tăng cường điều trị với corticosteroid (như dùng một đợt corticosteroid uống) hoặc điều trị bằng kháng sinh nếu như có nhiễm khuẩn. Bệnh nhân nên tham khảo ý kiến bác sĩ nếu cảm thấy việc điều trị không hiệu quả hay đã sử dụng vượt quá liều kê toa Symbicort Rapihaler.
Bệnh nhân nên luôn luôn có sẵn thuốc hít để giảm triệu chứng. Không nên sử dụng Symbicort Rapihaler như liệu pháp khởi đầu để điều trị một đợt hen kịch phát nặng.
Cũng như các trị liệu đường hít khác, co thắt phế quản nghịch thường có thể xảy ra với triệu chứng thở khò khè tăng lên đột ngột và khó thở sau khi hít thuốc. Nếu bệnh nhân gặp phải tình trạng co thắt phế quản nghịch thường nên ngừng Symbicort ngay lập tức, bệnh nhân cần được đánh giá và thay thế bằng một liệu pháp khác, nếu cần. Co thắt phế quản nghịch thường đáp ứng với thuốc giãn phế quản dạng hít tác dụng nhanh và nên được điều trị ngay.
Sử dụng corticosteroid đường uống
Symbicort Rapihaler không nên được sử dụng để khởi đầu điều trị bằng steroid dạng hít ở những bệnh nhân được chuyển từ steroid dạng uống. Nên thận trọng khi bắt đầu điều trị bằng Symbicort Rapihaler, đặc biệt nếu có bất kỳ lý do nào để nghi ngờ suy giảm chức năng thượng thận do liệu pháp steroid toàn thân trước đó.
Các tác động toàn thân có thể xảy ra khi dùng corticosteroid dạng hít
Các steroid dạng hít được thiết kế để đưa glucocorticoid trực tiếp vào phổi để giảm nồng độ tiếp xúc glucocorticoid toàn thân và các tác dụng phụ. Tuy nhiên, ở liều cao hơn liều khuyến cáo, các steroid dạng hít có thể có các tác dụng ngoại ý, các tác động toàn thân có thể xảy ra khi dùng steroid dạng hít bao gồm ức chế trục HPA, giảm mật độ xương, đục thủy tinh thể và tăng nhãn áp, chậm tăng trưởng ở trẻ em. Ở những bệnh nhân phụ thuộc steroid, việc sử dụng steroid toàn thân trước đó có thể là một nhân tố đóng góp nhưng các tác dụng này cũng có thể xảy ra ở các bệnh nhân sử dụng steroid dạng hít thường xuyên.
Ức chế trục HPA và suy thượng thận
Sự ức chế trục HPA phụ thuộc vào liều (biểu hiện bởi nước tiểu 24 giờ và/hoặc AUC của cortisol trong huyết tương) đã được ghi nhận với budesonid dạng hít, mặc dù nhịp sinh lý của cortisol huyết tương vẫn được duy trì. Điều này cho thấy sự ức chế trục HPA là biểu hiện của tình trạng đáp ứng về mặt sinh lý đối với budesonid dạng hít, không nhất thiết có suy tuyến thượng thận. Vẫn chưa thiết lập được liều thuốc thấp nhất dẫn đến suy tuyến thượng thận có biểu hiện lâm sàng. Rất hiếm trường hợp rối loạn chức năng thượng thận có biểu hiện lâm sàng đã được ghi nhận trên bệnh nhân dùng budesonid dạng hít ở liều khuyến cáo.
Các rối loạn trên lâm sàng nghiêm trọng của trục HPA và/hoặc suy thượng thận gây ra bởi stress nặng (như chấn thương, phẫu thuật, nhiễm khuẩn đặc biệt là viêm dạ dày-ruột hoặc các tình trạng do mất điện giải trầm trọng) có thể liên quan đến budesonid dạng hít ở đối tượng bệnh nhân đặc biệt. Đó là các bệnh nhân chuyển từ corticosteroid đường uống (xem Sử dụng corticosteroid đường uống) và các bệnh nhân đang dùng đồng thời các thuốc chuyển hóa bởi enzym CYP3A4 (xem Tương tác). Nên theo dõi dấu hiệu rối loạn chức năng tuyến thượng thận ở các bệnh nhân này. Đối với các bệnh nhân này, cũng nên xem xét dùng thêm glucocorticoid toàn thân trong giai đoạn stress, cơn hen nặng hoặc có phẫu thuật không cấp thiết.
Mật độ xương
Mặc dù corticosteroid liều cao có thể ảnh hưởng đến khối lượng xương, nhưng các nghiên cứu theo dõi dài hạn (3-6 năm) về điều trị budesonid trên người trưởng thành ở các liều khuyến cáo,cũng như một nghiên cứu thực hiện trên bệnh nhân có nguy cơ loãng xương cao đều không chứng tỏ tác động bất lợi trên mật độ xương so với giả dược. Vẫn chưa thiết lập liều thấp nhất ảnh hưởng đến mật độ xương.
Các chỉ số mật độ khoáng xương ở trẻ em nên được phân tích thận trọng vì sự tăng trưởng vùng xương ở trẻ em đang phát triển có thể phản ánh sự gia tăng thể tích xương. Trong 3 nghiên cứu lớn ở trẻ em (5-16 tuổi) có thời gian dùng thuốc từ trung bình đến dài hạn (12 tháng - 6 năm), không ghi nhận có tác động nào trên mật độ khoáng xương sau khi dùng budesonid (liều 189-1322 µg/ngày) so với khi dùng nedocromil, giả dược hoặc có các nhóm chứng theo tuổi. Tuy nhiên, trong một nghiên cứu ngẫu nhiên trong 18 tháng ở trẻ em (n=176; 5-10 tuổi), mật độ khoáng xương giảm đáng kể khoảng 0,11g/cm2 (p=0,023) ở nhóm dùng budesonid hít qua Turbuhaler so với nhóm dùng disodium cromoglycate dạng hít. Liều budesonid là 400 µg x 2 lần/ngày trong 1 tháng, 200 µg x 2 lần/ngày trong 5 tháng và 100 µg x 2 lần/ngày trong 12 tháng. Liều dinatri cromoglycat là 10 mg x 3 lần/ngày. Vẫn chưa chắc chắn về ý nghĩa lâm sàng của kết quả nghiên cứu này.
Sự tăng trưởng
Các nghiên cứu dài hạn cho thấy trẻ em điều trị bằng budesonid dạng hít cuối cùng cũng đạt đến chiều cao mục tiêu khi trưởng thành. Tuy nhiên, sự giảm tốc độ tăng trưởng lúc đầu (khoảng 1cm) đã được ghi nhận và thường xảy ra trong năm điều trị đầu tiên. Nhân viên y tế nên theo dõi chặt chẽ sự tăng trưởng ở trẻ em và trẻ vị thành niên có sử dụng corticosteroid dài hạn.
Hiếm gặp các bệnh nhân nhạy cảm khác thường với corticosteroid đường hít. Nên thực hiện các phép đo chiều cao để nhận biết các bệnh nhân quá nhạy cảm. Cần cân nhắc giữa ảnh hưởng lên sự tăng trưởng khi dùng thuốc dài hạn với hiệu quả lâm sàng. Để giảm thiểu tác động toàn thân của corticosteroid dạng hít, nên xác định liều thuốc thấp nhất có hiệu quả cho từng bệnh nhân (xem Liều lượng và Cách dùng).
Không nên ngưng thuốc đột ngột khi điều trị bổ sung bằng steroid toàn thân.
Trong quá trình chuyển từ dạng uống sang Symbicort, sẽ có một tác động steroid toàn thân thấp hơn thông thường có thể dẫn đến xuất hiện các triệu chứng dị ứng hoặc viêm khớp như viêm mũi, chàm và đau cơ và khớp. Cần bắt đầu điều trị đặc hiệu cho những triệu chứng này. Trong một số hiếm trường hợp có thể nghi ngờ hiệu quả glucocorticosteroid không đủ nếu xuất hiện các triệu chứng như mệt mỏi, nhức đầu, buồn nôn và nôn. Trong những trường hợp này, đôi khi cần tăng liều tạm thời glucocorticosteroid đường uống.
Để giảm thiểu nguy cơ nhiễm Candida hầu họng, bệnh nhân nên được chỉ dẫn súc miệng bằng nước sau mỗi lần hít. Nên tránh điều trị đồng thời với itraconazol, ritonavir hoặc các chất ức chế CYP3A4 mạnh. Nếu không thể tránh được, nên kéo dài khoảng cách giữa các lần dùng các thuốc có tương tác với nhau càng lâu càng tốt.
Symbicort nên được dùng thận trọng đối với bệnh nhân nhiễm độc giáp, u tế bào ưa crôm, đái tháo đường, giảm kali máu chưa điều trị, bệnh cơ tim phì đại tắc nghẽn, hẹp động mạch chủ dưới van vô căn, tăng huyết áp nặng, phình mạch hay các rối loạn tim mạch trầm trọng khác như là bệnh tim thiếu máu cục bộ, nhịp tim nhanh hoặc suy tim nặng.
Thận trọng khi điều trị ở bệnh nhân có khoảng thời gian QTc kéo dài. Bản thân formoterol có thể kéo dài thời gian QTc.
Bệnh nhân nhiễm khuẩn và bệnh lao
Liều cao glucocorticosteroid có thể che lấp dấu hiệu nhiễm khuẩn và tình trạng nhiễm khuẩn mới có thể xảy ra trong khi dùng thuốc. Cần đặc biệt lưu ý ở bệnh nhân lao phổi hoặc nhiễm nấm, vi khuẩn hoặc virút đường hô hấp thể tiến triển hoặc tiềm ẩn.
Nhạy cảm với các amin cường giao cảm
Ở các bệnh nhân tăng nhạy cảm với các amin cường giao cảm (như cường giáp không kiểm soát hoàn toàn), formoterol nên được sử dụng một cách thận trọng.
Các rối loạn tim mạch
Các chất chủ vận beta-2 có nguy cơ gây loạn sản thất phải nên cần cân nhắc trước khi bắt đầu điều trị co thắt phế quản.
Các nghiên cứu về độc tính cấp cũng như độc tính mạn cho thấy tác động của formoterol lên hệ tim mạch là chính bao gồm sung huyết, nhịp tim nhanh, loạn nhịp tim và các tổn thương cơ tim. Các biểu hiện dược lý được quan sát thấy sau khi sử dụng liều cao của chất chủ vận beta-2 adrenegic.
Bệnh nhân có vấn đề về tim mạch trước đó có thể tăng nguy cơ gặp các tác động ngoại ý trên tim mạch khi sử dụng các chất chủ vận beta-2 adrenegic. Cần thận trọng khi chỉ định formoterol cho các bệnh nhân có các vấn đề tim mạch nghiêm trọng như bệnh thiếu máu tim cục bộ, loạn nhịp tim nhanh hay suy tim nặng.
Giảm kali máu
Liều cao của chất chủ vận beta-2 có thể làm giảm kali huyết thanh do tái phân phối kali từ khoang ngoại bào vào khoang nội bào thông qua kích thích Na+/K+-ATPase ở các tế bào cơ.
Khả năng hạ kali máu nghiêm trọng có thể xảy ra. Cần đặc biệt thận trọng trong các đợt kịch phát bởi các nguy cơ khác có thể bị tăng lên do thiếu oxy máu. Tác động giảm kali huyết có thể tiềm ẩn do các điều trị kết hợp (xem Tương tác). Các bệnh nhân sử dụng digoxin đặc biệt nhạy cảm với giảm kali máu. Nồng độ kali huyết thanh nên được theo dõi trong trường hợp này.
Đái tháo đường
Do tác dụng làm tăng đường huyết của các chất kích thích beta-2, nên việc tăng cường kiểm soát đường máu được khuyến cáo ngay khi bệnh nhân đái tháo đường bắt đầu điều trị với formoterol.
Rối loạn thị giác
Rối loạn thị giác có thể được báo cáo đối với sử dụng corticosteroid toàn thân hay tại chỗ. Nếu bệnh nhân xuất hiện các triệu chứng như nhìn mờ hoặc các rối loạn thị giác khác, bệnh nhân nên được xem xét chuyển đến bác sĩ nhãn khoa để đánh giá các nguyên nhân có thể bao gồm đục thủy tinh thể, tăng nhãn áp hoặc các bệnh hiếm gặp như bệnh hắc võng mạc trung tâm thanh dịch (CSCR), loại bệnh đã được báo cáo sau khi sử dụng corticosteroid toàn thân hoặc tại chỗ.
Suy gan và suy thận
Tác động của việc giảm chức năng gan và chức năng thận trên dược động học của formoterol và budesonid chưa được biết đến. Tuy nhiên do budesonid và formoterol chủ yếu được đào thải qua chuyển hóa gan, nên tăng nồng độ thuốc có thể xảy ra ở các bệnh nhân bệnh gan nặng.
Viêm phổi
Các nghiên cứu lâm sàng và phân tích gộp đã chỉ ra rằng điều trị COPD với corticosteroid dạng hít có thể làm tăng nguy cơ viêm phổi. Tuy nhiên, nguy cơ tuyệt đối của budesonid là thấp. Một phân tích gộp từ 11 thử nghiệm mù đôi COPD gồm 10570 bệnh nhân không chứng minh được việc tăng nguy cơ viêm phổi có ý nghĩa thống kê trên các bệnh nhân điều trị với budesonid (có kết hợp với formoterol hoặc không) so với liệu pháp điều trị không chứa budesonid (giả dược hoặc formoterol). Tỷ lệ mới mắc viêm phổi được báo cáo như là biến cố ngoại ý nghiêm trọng là 1,9%/năm ở các liệu pháp điều trị chứa budesonid và 1,5%/năm ở các liệu pháp điều trị không chứa budesonid. Tỷ số nguy cơ gộp so sánh giữa toàn bộ các liệu pháp điều trị chứa budesonid và liệu pháp điều trị không chứa budesonid là 1,15 (95% CI: 0,83, 1,57). Tỷ số nguy cơ gộp so sánh giữa budesonid/formoterol so với formoterol hoặc giả dược là 1,00 (95% CI: 0,69, 1,44). Mối liên hệ nhân quả giữa các sản phẩm chứa budesonid chưa được thiết lập.
Khả năng gây ung thư
Nguy cơ gây ung thư của dạng kết hợp budesonid/formoterol chưa được thấy ở các nghiên cứu trên động vật.
Trong các nghiên cứu về khả năng gây ung thư của formoterol được thực hiện bởi AstraZeneca, có sự tăng phụ thuộc liều của tỷ lệ mới mắc u cơ tử cung lành tính ở chuột bạch sử dụng liều uống 0,1, 0,5, và 2,5 mg/kg/ngày trong hai năm, và u màng treo buồng trứng lành tính được quan sát thấy ở chuột cái sử dụng liều hít 0,13 mg/kg/ngày trong hai năm. Các tác động được quan sát thấy khi sử dụng liều cao chất chủ vận beta-2.
Các nghiên cứu về khả năng gây ung thư của formoterol được thực hiện bởi các công ty khác sử dụng liều toàn thân cao gấp 800-4800 lần so với liều dự kiến khi sử dụng trên lâm sàng của formoterol (dựa trên liều 18 μg/ngày).
Một số hoạt tính gây ung thư được quan sát thấy chuột bạch và chuột. Tuy nhiên, ở liều mà những tác động đó được quan sát thấy và thực tế là formoterol không gây đột biến (ngoại trừ hoạt tính rất yếu ở nồng độ cao trong một hệ thống thử nghiệm), có thể kết luận rằng nguy cơ gây ung thư ở bệnh nhân điều trị bởi formoterol furmarat là không cao hơn so với chất chủ vận beta-2 adrenegic khác.
Khả năng gây ung thư của budesonid đã được đánh giá ở chuột bạch với liều uống lên đến 200 μg và chuột ở liều uống 50 μg/kg/ngày. Ở chuột đực sử dụng liều 10, 25, và 50 μg budesonid/kg/ngày, những con chuột sử dụng liều 25, và 50 μg kg/ngày cho thấy tăng tỷ lệ các khối u tế bào gan nguyên phát. Trong một nghiên cứu lặp lại, tác động này được quan sát thấy ở một số nhóm steroid (budesonid, prednisolon, triamcinolon acetonid), vì vậy cho thấy đây là tác động nhóm của corticosteroid.
Độc tính trên gen
Một cách riêng lẻ, budesonid và formoterol gây độc trên gen trong một loạt các thử nghiệm về đột biến gen (ngoại trừ sự tăng nhẹ tần số đột biến đảo ngược của Salmonella typhimurium ở nồng độ cao của formoterol), tổn thương nhiễm sắc thể và sửa chữa ADN. Sự kết hợp của budesonid và formoterol chưa được kiểm chứng trong các thử nghiệm về độc tính trên gen.
Ảnh hưởng trên khả năng sinh sản
Chưa có nghiên cứu trên động vật về tác động của kết hợp budesonid/formoterol trên khả năng sinh sản.
Điều trị dài hạn trên chuột bạch cái và chuột cái với formoterol fumarat gây kích thích buồng trứng, sự phát triển u nang buồng trứng và sự tăng sản tế bào hạt/vỏ nang do đặc tính chủ vận beta-2 của hợp chất. Một nghiên cứu của một công ty khác chỉ ra rằng không có ảnh hưởng trên khả năng sinh sản của chuột cái ở liều formoterol fumarat uống 60 mg/kg/ngày trong 2 tuần. Kết quả này được lặp lại trên một nghiên cứu của AstraZeneca, không tác động nào được thấy trên khả năng sinh sản của chuột cái ở liều formoterol fumaratuống 15 mg/kg/ngày trong vòng 2 tuần.
Teo tinh hoàn đã được quan sát thấy ở chuột sử dụng formoterol fumarat trong chế độ ăn ở mức liều 0,2-50 mg/kg/ngày trong hai năm, nhưng trong một nghiên cứu được thực hiện bởi một công ty khác lại cho thấy không tác động nào trên khả năng sinh sản của chuột đực ở liều uống 60 mg/kg/ngày trong 9 tuần.
Ảnh hưởng trên khả năng lái xe và vận hành máy móc
Người lái xe và vận hành máy móc cần thận trọng khi sử dụng Symbicort Rapihaler cho đến khi tác động của Symbicort Rapihaler lên cá thể được xác định. Symbicort Rapihaler gần như không ảnh hưởng đến khả năng lái xe và vận hành máy móc.
Quá Liều
Quá liều formoterol có thể sẽ dẫn đến tác động điển hình của các chủ vận beta-2 adrenegic: run rẩy, nhức đầu, đánh trống ngực và nhịp tim nhanh. Kiểm soát nồng độ kali huyết thanh có thể được khuyến cáo. Hạ huyết áp, nhiễm toan chuyển hóa, hạ kali máu, tăng đường huyết có thể xảy ra. Điều trị hỗ trợ và điều trị triệu chứng có thể được chỉ định. Các thuốc chẹn beta cần thận trọng khi sử dụng vì có khả năng gây co thắt phế quản ở bệnh nhân nhạy cảm. Liều định chuẩn 120 μg dùng trong 3 giờ ở bệnh nhân tắc nghẽn phế quản cấp không gây quan ngại về mặt an toàn.
Quá liều cấp budesonid, thậm chí ngay cả khi dùng các liều quá mức, không là một vấn đề lâm sàng. Tuy nhiên, nồng độ cortisol huyết tương sẽ giảm và số lượng, tỷ lệ bạch cầu trung tính sẽ tăng lên. Số lượng và tỷ lệ của các tế bào lympho và bạch cầu ái toan sẽ đồng thời giảm. Khi sử dụng lâu dài các liều quá mức, có thể xảy ra các tác động glucocorticosteroid toàn thân như là cường năng vỏ thượng thận và ức chế tủy thượng thận.
Ngưng dùng Symbicort Rapihaler hoặc giảm liều budesonid sẽ loại bỏ tác dụng này, mặc dù cơ chế tác dụng ức chế trục HPA có thể diễn ra chậm hơn.
Chống chỉ định
Mẫn cảm với budesonid, formoterol hay bất kỳ thành phần nào của thuốc.
Sử dụng ở phụ nữ có thai và cho con bú
Sử dụng cho phụ nữ có thai - Nhóm C
Không có dữ liệu lâm sàng về việc dùng phối hợp budesonid và formoterol ở phụ nữ có thai.
Dị tật thai nhi (thoát vị rốn và hở hàm ếch), triệu chứng điển hình của ngộ độc corticoid ở động vật xảy ra với chuột dùng Symbicort Rapihaler ở liều hít budesonid 12 μg/kg/ngày và formoterol 0,66 μg/kg/ngày, với giá trị AUC huyết tương cả hai thuốc thấp hơn so với dự đoán ở bệnh nhân sử dụng liều lâm sàng tối đa. Không có tác dụng gây quái thai được phát hiện ở liều budesonid 2,5 μg/kg/ngày và liều formoterol 0,14 μg/kg/ngày.
Symbicort Rapihaler chỉ nên sử dụng trong thai kỳ khi lợi ích mang lại hơn hẳn so với nguy cơ đối với thai nhi. Symbicort Rapihaler chỉ được sử dụng trong ba tháng đầu của thai kỳ và thời gian ngắn trước khi sinh sau khi đã cân nhắc thật kỹ lưỡng.
Bởi vì các chất chủ vận beta, bao gồm formoterol, có khả năng gây cản trở co thắt tử cung do tác dụng làm giãn cơ trơn tử cung, nên Symbicort Rapihaler chỉ được sử dụng trong thời gian sinh chỉ khi lợi ích mang lại hơn hẳn so với nguy cơ.
Budesonid
Kết quả từ một nghiên cứu tiến cứu lớn về dịch tễ học và các kinh nghiệm trong quá trình lưu hành thuốc trên toàn thế giới cho thấy dùng budesonid dạng hít trong thời gian mang thai không gây các tác dụng ngoại ý đối với bào thai hoặc trẻ sơ sinh.
Nếu việc điều trị bởi glucocorticosteroid trong thời kỳ mang thai là không thể tránh khỏi, các corticosteroid dạng hít như budesonid có thể được xem xét bởi vì tác động toàn thân thấp. Liều thấp nhất có tác dụng của budesonid để duy trì kiểm soát hen nên được sử dụng.
Formoterol
Không có tác động gây quái thai được tìm thấy trong chuột dùng formoterol fumarat ở liều uống 60 mg/kg/ngày hoặc liều hít 1,2 mg/kg/ngày. Dị tật tim mạch ở thai nhi được tìm thấy ở một nghiên cứu trong đó thỏ mang thai được sử dụng liều uống 125 mg hoặc 500 mg/kg/ngày trong giai đoạn hình thành hệ cơ quan, nhưng kết quả tương tự không được ghi nhận ở một nghiên cứu khác với mức liều tương đương. Trong một nghiên cứu thứ ba, sự tăng tỷ lệ các nang dưới bao gan được quan sát thấy trong bào thai thỏ sử dụng liều uống 60 mg/kg/ngày. Giảm cân nặng khi sinh và tăng tử suất chu sinh/sau sinh được quan sát thấy khi chuột được sử dụng formoterol fumarat ở liều uống 0,2 mg/kg/ngày hoặc cao hơn trong giai đoạn cuối thai kỳ.
Sử dụng cho phụ nữ cho con bú
Budesonid được bài tiết qua sữa mẹ. Tuy nhiên, do liều dùng tương đối thấp khi sử dụng qua đường hít nên nếu thuốc có hiện diện trong sữa mẹ thì cũng với một lượng thấp.
Người ta vẫn chưa biết formoterol có bài tiết vào trong sữa mẹ hay không. Trên chuột, formoterol bài tiết vào sữa mẹ. Không có nghiên cứu nào trên động vật đang cho con bú sử dụng dạng kết hợp budesonid/formoterol. Tăng tỷ lệ tử vong sau sinh ở liều uống formoterol sử dụng cho mẹ là 0,2 mg/kg/ngày hoặc nhiều hơn, và chậm tăng trưởng ở các con ở mức liều uống 15 mg/kg/ngày đã được quan sát thấy ở một nghiên cứu trên chuột. Không có nghiên cứu nào được kiểm soát tốt trên phụ nữ cho con bú sử dụng Symbicort Rapihaler. Bởi vì nhiều thuốc được bài tiết qua sữa mẹ, cân nhắc sử dụng Symbicort Rapihaler cho phụ nữ đang cho con bú nếu lợi ích mang lại cho mẹ lớn hơn so với nguy cơ đối với trẻ.
Tương tác
Tương tác dược động học
Chuyển hóa của budesonid chủ yếu qua trung gian bởi enzym CYP3A4. Các chất ức chế mạnh CYP3A4 (như ketoconazol, itraconazol, voriconazol, posaconazol, clarithromycin, telithromycin, nefazodon và thuốc ức chế protease HIV) có thể làm tăng đáng kể nồng độ budesonid huyết tương và nên tránh dùng đồng thời các thuốc này. Nếu không thể thì khoảng thời gian giữa việc dùng chất ức chế và budesonid nên càng cách xa càng tốt.
Điều này ít có ý nghĩa lâm sàng khi điều trị ngắn hạn (1-2 tuần) với ketoconazol, nhưng cần xem xét khi điều trị lâu dài với ketoconazol hoặc các chất ức chế mạnh CYP3A4 khác.
Tương tác dược lực học
Cả budesonid và formoterol đều không tương tác với bất kỳ thuốc nào khác trong điều trị hen suyễn và COPD.
Các thuốc chẹn thụ thể beta
Các thuốc chẹn thụ thể beta, đặc biệt là loại không chọn lọc có thể ức chế một phần hoặc hoàn toàn tác dụng của các chất chủ vận beta-2. Các thuốc này cũng có thể làm tăng sức cản đường thở, vì vậy không khuyến cáo sử dụng các thuốc này cho bệnh nhân hen suyễn.
Các thuốc cường giao cảm khác
Các chất kích thích β-adrenergic hoặc amin cường giao cảm như ephedrin không nên được dùng đồng thời với formoterol, vì hiệu lực cộng dồn. Các bệnh nhân đã sử dụng liều cao amin cường giao cảm không nên sử dụng formoterol.
Các dẫn xuất xanthin, mineralocorticosteroid và các thuốc lợi tiểu
Giảm kali máu có thể xảy ra do liệu pháp sử dụng các chất chủ vận beta-2 và có thể tăng lên nếu điều trị kết hợp với các dẫn xuất xanthin, mineralocorticosteroid và các thuốc lợi tiểu (xem Cảnh báo - Giảm kali máu).
Các chất ức chế monoamin oxida, các thuốc chống trầm cảm ba vòng, quinidin, disopyramid, procainamid, phenothiazin và kháng histamin
Các tác động bất lợi trên tim mạch của formoterol có thể trầm trọng hơn do dùng đồng thời với các thuốc có tác dụng kéo dài khoảng QT và làm tăng nguy cơ rối loạn nhịp thất. Vì những lý do này cần thận trọng khi sử dụng formoterol cho những bệnh nhân đang dùng các chất ức chế monoamin oxida, các thuốc chống trầm cảm ba vòng, quinidin, disopyramid, procainamid, phenothiazin hoặc kháng histamin liên quan đến kéo dài khoảng QT (terfenadin, astemizol).
Hơn nữa, L-Dopa, L-thyroxin, oxytocin và rượu có thể ảnh hưởng tính dung nạp của tim đối với thuốc cường giao cảm beta-2.
Dùng đồng thời với các chất ức chế monoamin oxida kể cả những tác nhân có đặc tính tương tự như furazolidon và procarbazin có thể thúc đẩy phản ứng tăng huyết áp.
Tăng nguy cơ loạn nhịp tim ở bệnh nhân đang gây mê với hydrocarbon halogen hóa.
Dùng đồng thời với các thuốc cường giao cảm beta khác hoặc các thuốc kháng cholinergic có thể có tác động giãn phế quản cộng hợp mạnh.
Giảm kali máu có thể làm tăng khuynh hướng loạn nhịp tim ở bệnh nhân điều trị bằng digitalis glycosid.
Tác dụng ngoại ý
Bởi vì Symbicort Rapihaler chứa cả hai hoạt chất budesonid và formoterol, có thể xảy ra các tác động ngoại ý tương tự như đã được báo cáo với các chất này. Người ta không thấy sự tăng tỉ lệ mới phát sinh tác dụng ngoại ý khi dùng đồng thời cả hai chất trên. Phản ứng ngoại ý liên quan đến thuốc thường gặp nhất là những phản ứng phụ có thể dự báo trước về mặt dược lý học của chất chủ vận beta-2, như run rẩy và đánh trống ngực. Các phản ứng này nhẹ và thường biến mất sau vài ngày điều trị.
Trong chương trình thử nghiệm lâm sàng so sánh Symbicort Rapihaler và Symbicort Turbuhaler ở 679 người trưởng thành và trẻ vị thành niên (nghiên cứu 681 và nghiên cứu 715) được sử dụng Symbicort Rapihaler 800/24 μg mỗi ngày với thời gian trung bình là 359 ngày đối với nghiên cứu 681 và từ 1 đến 427 ngày với nghiên cứu 715.
Không có sự khác biệt rõ ràng trong mô hình tổng thể của biến cố ngoại ý giữa nhóm Symbicort Rapihaler và nhóm Symbicort Turbuhaler trong chương trình thử nghiệm lâm sàng. Các biến cố ngoại ý thường ở mức độ từ nhẹ đến vừa và kiểu thường thấy ở đối tượng bệnh nhân hen dai dẳng và bị ảnh hưởng bởi các triệu chứng của biến cố đường hô hấp trên.
Nhìn chung biến cố ngoại ý là tương tự ở bệnh nhân sử dụng Symbicort Rapihaler và Symbicort Turbuhaler với cùng tổng liều hàng ngày, tuổi, giới tính, nhóm chủng tộc và không có bất kỳ quan ngại nào mới về vấn đề an toàn được xác định với Symbicort Rapihaler.
Nếu nấm Candida hầu họng phát triển, có thể điều trị bằng thuốc kháng nấm thích hợp trong khi vẫn tiếp tục điều trị bằng thuốc Symbicort. Tỷ lệ nhiễm Candida nhìn chung có thể được giữ ở mức tối thiểu bằng cách bệnh nhân súc miệng bằng nước sau khi hít liều duy trì.
Các tác dụng ngoại ý có liên quan đến budesonid, formoterol và Symbicort Rapihaler được liệt kê trong bảng 2.
- xem Bảng 2.

Nhiễm nấm Candida hầu họng là do sự lắng đọng của thuốc. Bệnh nhân nên súc miệng bằng nước sau mỗi lần dùng thuốc sẽ giảm thiểu nguy cơ. Nhiễm nấm Candida hầu họng thường đáp ứng với điều trị chống nấm tại chỗ mà không cần phải ngưng dùng corticosteroid dạng hít.
Tác dụng toàn thân của corticosteroid đường hít có thể xảy ra khi dùng liều cao trong một thời gian dài. Những tác động này ít có khả năng xảy ra hơn so với corticosteroid uống. Các tác động toàn thân có thể bao gồm hội chứng Cushing, các đặc điểm Cushing, ức chế thượng thận, chậm phát triển ở trẻ em và trẻ vị thành niên, giảm mật độ khoáng trong xương, đục thủy tinh thể và tăng nhãn áp. Tăng tính nhạy cảm đối với nhiễm trùng và suy giảm khả năng thích nghi với stress cũng có thể xảy ra. Tác dụng có thể phụ thuộc vào liều, thời gian tiếp xúc với steroid, dùng steroid đồng thời và trước đó và độ nhạy cảm cá nhân.
Cũng như các dạng thuốc hít khác, co thắt phế quản nghịch thường có thể xảy ở rất hiếm các trường hợp.
Việc điều trị bằng các chất cường giao cảm beta có thể làm tăng nồng độ insulin máu, acid béo tự do, glycerol và ceton máu.
Bảo quản
Không bảo quản trên 30°C. Bảo quản bình xịt với đầu ngậm quay xuống. Đậy nắp đầu ngậm sau khi sử dụng Symbicort Rapihaler.
Phân loại ATC
R03AK07 - formoterol and budesonide
Trình bày/Đóng gói
Thuốc hít: hộp 1 bình xịt 120 liều.
- Abacavir
- Abernil
- Abiiogran
- Acarbose
- ACC
- Acebutolol
- Acenocoumarol
- Acetate Ringer's
- Acetazolamide
- Acetylcystein
- Acetylsalicylic acid
- Aciclovir
- Acid acetylsalicylic
- Acid aminocaproic
- Acid ascorbic
- Acid boric
- Acid chenodeoxycholic
- Acid ethacrynic
- Acid folic
- Acid fusidic
- Acid iopanoic
- Acid ioxaglic
- Acid nalidixic
- Acid pantothenic
- Acid para-aminobenzoic
- Acid salicylic
- Acid tranexamic
- Acid valproic
- Acid zoledronic
- Acitretin
- Aclasta
- Aclon
- Actapulgite
- Actelsar
- Actelsar HCT
- Actemra
- Actilyse
- Acular
- Acupan
- Acuvail
- Acyclovir STADA
- Acyclovir STADA Cream
- Adalat
- Adenosin
- Adenosin Ebewe
- Adipiodon
- Advagraf
- Aerius
- Afinitor
- Agicarvir
- Agifovir-E
- Agilosart
- Agilosart-H
- Agimepzol
- Agimosarid
- Agimstan
- Agimstan-H
- Agiremid
- Agivastar
- Aibezym
- Air-X
- Alaxan
- Albendazol
- Albiomin
- Albumin
- Albumin người Grifols 20%
- Albuminar
- AlbuRx
- Albutein
- Alcuronium chloride
- Aldesleukin
- Alendronat
- Alertin
- Alfa-Lipogamma 600 Oral
- Alfuzosin hydrochlorid
- Algotra
- Alimemazin
- Alimta
- Allipem
- Allopurinol
- Allopurinol STADA
- Aloxi
- Alprazolam
- Alpha Chymotrypsin
- Alpha tocopherol
- Alphachymotrypsin Glomed
- Alphagan-P
- Aluvia
- Alzental
- Amaryl
- Ambroco
- Ambroxol
- Amcinol-Paste
- Amigold
- Amikacin
- Aminocaproic acid
- Aminoleban
- Aminoleban Oral
- Aminosteril N-Hepa
- Amiparen
- Amitriptyline
- Amiyu
- Amlodipine
- Amlor
- Amoxicillin
- Amoxicillin & clavulanate
- Ampicillin
- Amquitaz
- Anaferon for children
- Anargil
- Anaropin
- Andriol Testocaps
- Anepzil
- Anyfen
- Apaisac
- Apidra SoloStar
- Apitim 5
- Aprovel
- Aquaphil
- Arcalion
- Arcoxia
- Aricept Evess
- Arimidex
- Arnetine
- Artrodar
- A-Scabs
- Ascorbic acid
- Asperlican/Candinazol
- Aspilets EC
- Aspirin
- Asthmatin
- Atelec
- Atocib 120
- Atocib 90
- Atosiban PharmIdea
- Atozet
- Attapulgite
- Atussin
- Atropin
- Augbactam
- Augmentin Sachet
- Augmentin SR
- Augmentin Tablets
- Augmex
- Avamys
- Avastin
- Avelox Dịch truyền
- Avelox Viên nén
- Avodart
- Axcel Cefaclor-125 Suspension
- Axcel Cetirizine Syrup
- Axcel Chlorpheniramine
- Axcel Dexchlorpheniramine
- Axcel Dicyclomine-S Syrup
- Axcel Diphenhydramine Paediatric Syrup
- Axcel Erythromycin ES
- Axcel Eviline
- Axcel Fungicort Cream
- Axcel Fusidic acid Cream
- Axcel Fusidic acid-B Cream
- Axcel Hydrocortisone Cream
- Axcel Lignocaine 2% Sterile Gel
- Axcel Loratadine
- Axcel Miconazole Cream
- Axcel Paracetamol
- Axcel Urea Cream
- Axitan
- Azenmarol
- Azicine
- Aziphar
- Azithromycin