Nhà sản xuất
Boehringer Ingelheim
Thành phần
Mỗi viên (có thể bẻ đôi): Pramipexole dihydrochloride monohydrate 0,25mg hay 1mg (tương đương 0,18mg hay 0,7mg pramipexole).
Mỗi viên (phóng thích chậm): Pramipexole dihydrochloride monohydrate 0,375mg, 0,75mg hay 1,5mg (tương đương 0,26mg, 0,52mg hay 1,05mg pramipexole).
Dược lực học
Pramipexole là chất đồng vận dopamine kết gắn chọn lọc và đặc hiệu cao với phân nhóm thụ thể dopamin D2, trong đó có ái lực ưu tiên với thụ thể D3; hoạt chất này có hoạt tính nội tại hoàn toàn.
Pramipexole làm giảm bớt các khiếm khuyết vận động của bệnh nhân trong bệnh Parkinson bằng cách kích thích các thụ thể dopamine trong thể vân. Các nghiên cứu trên động vật cho thấy pramipexole ức chế sự tổng hợp, phóng thích và chuyển hóa dopamine.
Cơ chế tác động của SIFROL trong điều trị hội chứng chân không yên chưa được biết rõ. Bằng chứng dược lý học thần kinh gợi ý rằng có sự can dự chủ yếu của hệ thống dopaminergic.
Trên người tình nguyện, giảm prolactin phụ thuộc liều dùng cũng đã được ghi nhận. Đã quan sát thấy tăng huyết áp và nhịp tim trong một nghiên cứu lâm sàng trên những người tình nguyện khỏe mạnh, liều dùng của SIFROL viên nén phóng thích chậm được điều chỉnh nhanh hơn (mỗi 3 ngày) với liều khuyến cáo lên tới 4,5mg dạng muối. Những tác dụng như vậy không quan sát thấy trên những bệnh nhân nghiên cứu.
Pramipexole giảm bớt các dấu hiệu và triệu chứng của bệnh nhân Parkinson vô căn. Các thử nghiệm lâm sàng có đối chứng bao gồm khoảng 1800 bệnh nhân dùng viên nén phóng thích chậm (hoặc 2100 bệnh nhân dùng viên nén) với thang điểm Hoehn và Yahr giai đoạn I-V điều trị với pramipexole. Ngoài ra, có xấp xỉ 1000 bệnh nhân dùng viên nén phóng thích chậm (hoặc khoảng 900 bệnh nhân dùng viên nén) trong giai đoạn bệnh tiến triển, đã được điều trị kèm liệu pháp levodopa và có biến chứng vận động.
Trong giai đoạn sớm và tiến triển của bệnh Parkinson, hiệu quả của pramipexole trong các thử nghiệm lâm sàng có đối chứng được duy trì trong suốt thời gian khoảng 6 tháng. Trong các nghiên cứu mở tiếp theo, hiệu quả kéo dài hơn 3 năm mà không thấy dấu hiệu suy giảm hiệu quả điều trị. Trong thử nghiệm lâm sàng mù đôi có đối chứng kéo dài 2 năm điều trị khởi đầu với pramipexole làm trì hoãn đáng kể sự xuất hiện các biến chứng và giảm thiểu tái phát so với điều trị khởi đầu bằng levodopa. Việc chậm xuất hiện các biến chứng vận động khi điều trị bằng pramipexole cần được cân nhắc với sự cải thiện đáng kể các chức năng vận động khi điều trị bằng levodopa (đo bằng sự thay đổi trung bình của thang điểm UPDRS). Tỷ lệ mới xuất hiện ảo giác và buồn ngủ cao hơn trong giai đoạn tăng liều trong nhóm dùng pramipexole. Tuy nhiên không có sự khác biệt có ý nghĩa trong giai đoạn duy trì liều. Đây là điểm cần xem xét khi điều trị khởi đầu bằng pramipexole cho bệnh nhân Parkinson.
Tính an toàn và hiệu quả của SIFROL viên nén phóng thích chậm trong điều trị bệnh Parkinson đã được đánh giá trong chương trình phát triển dược phẩm đa quốc gia bao gồm ba nghiên cứu có kiểm soát, ngẫu nhiên. Hai thử nghiệm được tiến hành trên những bệnh nhân mắc bệnh Parkinson giai đoạn sớm và một thử nghiệm tiến hành trên những bệnh nhân Parkinson giai đoạn tiến triển.
Tính vượt trội của SIFROL viên nén phóng thích chậm so với giả dược đã được mô tả sau 18 tuần điều trị dựa vào cả hai tiêu chí hiệu quả chính (thang điểm UPDRS phần II + III) và tiêu chí phụ then chốt (tỷ lệ đáp ứng CGI-I và PGI-I) trong một thử nghiệm mù đôi, có so sánh giả dược bao gồm 539 bệnh nhân mắc bệnh Parkinson giai đoạn sớm. Hiệu quả duy trì đã cho thấy ở những bệnh nhân được điều trị 33 tuần. SIFROL viên nén phóng thích chậm không thua kém so với viên nén pramipexole phóng thích nhanh khi đánh giá trên thang điểm UPDRS Phần II + III ở tuần thứ 33.
Trong một nghiên cứu lâm sàng mù đôi, có so sánh với giả dược bao gồm 517 bệnh nhân mắc bệnh Parkinson tiến triển đã được điều trị đồng thời với levodopa cho thấy tính ưu việt của SIFROL viên nén phóng thích chậm so với giả dược sau 18 tuần điều trị dựa trên các tiêu chí hiệu quả chính (thang điểm UPDRS Phần II+III) và tiêu chí phụ then chốt chủ yếu (thời gian không đáp ứng với thuốc).
Tính hiệu quả và khả năng dung nạp khi chuyển từ dạng SIFROL viên nén sang dạng viên nén phóng thích kéo dài tại cùng một liều dùng hàng ngày đã được đánh giá trong một nghiên cứu lâm sàng mù đôi ở những bệnh nhân mắc bệnh Parkinson giai đoạn sớm.
Hiệu quả đã được duy trì ở 87 trong số 103 bệnh nhân chuyển sang dùng SIFROL viên nén phóng thích chậm. Trong số 87 bệnh nhân này, 82,8% số bệnh nhân không thay đổi liều dùng, 13,8% tăng và 3,4% giảm liều dùng. Trong một nửa số 16 bệnh nhân không đáp ứng tiêu chí về hiệu quả duy trì theo thang điểm UPDRS phần II + III, sự thay đổi so với thời điểm bắt đầu không có ý nghĩa về mặt lâm sàng.
Chỉ có một bệnh nhân chuyển sang sử dụng SIFROL viên nén phóng thích chậm là có tác dụng không mong muốn liên quan đến thuốc và phải ngừng thuốc.
Hiệu quả của SIFROL đã được đánh giá trong bốn thử nghiệm lâm sàng đối chứng với giả dược trên khoảng 1.000 bệnh nhân có hội chứng chân không yên vô căn từ mức trung bình đến rất nặng. Hiệu quả được chứng minh trong các thử nghiệm có đối chứng trên bệnh nhân được điều trị đến 12 tuần. Hiệu quả duy trì của SIFROL chưa được nghiên cứu đầy đủ.
Thay đổi trung bình so với ban đầu của thang điểm IRLS (Restless Legs Syndrome Rating Scale) và thang điểm CGI-I (Clinical Global Impression-Improvement) là tiêu chí đánh giá chính cho hiệu quả. Ở cả hai tiêu chí đánh giá chính, có sự khác biệt có ý nghĩa thống kê giữa nhóm dùng liều pramipexole 0,25 mg, 0,5 mg và 0,75 mg so với nhóm dùng giả dược. Sau 12 tuần điều trị, điểm cơ bản IRLS cải thiện từ 23,5 còn 14,1 điểm ở nhóm giả dược và từ 23,4 còn 9,4 điểm ở nhóm dùng pramipexole (liều phối hợp). Sự khác biệt của giá trị trung bình được điều chỉnh là -4,3 điểm (CI 95%: -6,4; -2,1 điểm, p < 0,0001). Tỷ lệ người có đáp ứng với CGI-I (cải thiện, rất cải thiện) tương ứng là 51, 2% và 72,0% cho nhóm giả dược và nhóm dùng pramipexole (sự khác biệt là 20%, CI 95%: 8,1%; 31,8%, p < 0,0005).
Hiệu quả điều trị của 0,125 mg dạng muối/ngày xuất hiện ngay sau tuần đầu điều trị.
Trong nghiên cứu về những thay đổi sinh lý trong giấc ngủ (polysomnography study) có đối chứng giả dược, sau 3 tuần điều trị SIFROL có sự giảm đáng kể hiện tượng vận động chi thể theo chu kỳ khi ngủ (Periodic Limb Movements).
Dược động học
Pramipexole được hấp thu nhanh và hoàn toàn sau khi uống. Sinh khả dụng tuyệt đối lớn hơn 90%.
Trong một thử nghiệm giai đoạn I, khi đánh giá pramipexole viên nén phóng thích nhanh và viên nén phóng thích chậm ở trạng thái đói, nồng độ cực tiểu và nồng độ đỉnh trong huyết tương (Cmin, Cmax) và diện tích dưới đường cong (AUC) của cùng liều dùng hàng ngày của SIFROL viên nén phóng thích chậm dùng một lần trong ngày và SIFROL viên nén dùng 3 lần một ngày là tương đương nhau.
Dùng một lần mỗi ngày SIFROL viên nén phóng thích chậm làm giảm sự dao động thường xuyên hàm lượng pramipexole huyết tương trong 24 giờ so với khi dùng SIFROL viên nén phóng thích nhanh 3 lần mỗi ngày.
Nồng độ đỉnh trong huyết tương đạt được sau khoảng 6 giờ sau khi dùng SIFROL viên nén phóng thích chậm một lần mỗi ngày và sau 1 đến 3 giờ sau khi dùng SIFROL viên nén. Trạng thái cân bằng đạt được muộn nhất sau 5 ngày điều trị liên tục.
Dùng cùng với thức ăn nhìn chung không ảnh hưởng tới sinh khả dụng của pramipexole.
Ăn thức ăn có độ béo cao làm tăng nồng độ đỉnh (Cmax) khoảng 24% sau khi dùng liều đơn và khoảng 20% sau khi dùng đa liều và làm chậm thời gian đạt được nồng độ đỉnh ở người tình nguyện khỏe mạnh khoảng 2 giờ. Diện tích dưới đường cong toàn phần (AUC) không bị ảnh hưởng khi dùng cùng với thức ăn. Việc tăng Cmax được xem như không có ý nghĩa về mặt lâm sàng. Trong các nghiên cứu lâm sàng giai đoạn III xác lập tính an toàn và hiệu quả của SIFROL viên nén phóng thích chậm, bệnh nhân được hướng dẫn dùng thuốc được nghiên cứu mà không cần để ý đến bữa ăn.
Trọng lượng cơ thể không có ảnh hưởng lên AUC, nhưng ảnh hưởng trên thể tích phân bố và do vậy ảnh hưởng lên nồng độ đỉnh Cmax. Giảm trọng lượng cơ thể khoảng 30kg dẫn đến làm tăng Cmax khoảng 45%. Tuy nhiên, trong các nghiên cứu lâm sàng giai đoạn III ở những bệnh nhân mắc bệnh Parkinson cho thấy không có ảnh hưởng có ý nghĩa lâm sàng của cân nặng trên hiệu quả điều trị và khả năng dung nạp SIFROL viên nén phóng thích chậm.
Pramipexole cho thấy dược động học tuyến tính và nồng độ trong huyết tương ít thay đổi trên bệnh nhân. Ở người, pramipexole liên kết với protein ở tỷ lệ rất thấp (< 20%) và thể tích phân bố lớn (400 L). Đã quan sát thấy nồng độ trong mô não cao ở chuột cống (xấp xỉ 8 lần so với nồng độ trong huyết tương).
Trên người, pramipexole chỉ được chuyển hóa ở một mức độ nhỏ.
Pramipexole được đào thải chủ yếu qua thận dưới dạng không chuyển hóa. Khoảng 90% lượng thuốc được đánh dấu với 14C được bài tiết qua thận, trong khi ít hơn 2% được tìm thấy trong phân. Tổng thanh thải của pramipexole vào khoảng 500 mL/phút và độ thanh thải ở thận vào khoảng 400 mL/phút. Thời gian bán thải (t½) thay đổi từ 8 giờ ở người còn trẻ đến 12 giờ ở người cao tuổi.
Chỉ định/Công dụng
* SIFROL được chỉ định điều trị các dấu hiệu và triệu chứng của bệnh Parkinson vô căn, dùng đơn trị liệu (không cùng levodopa) hoặc kết hợp với levodopa, nghĩa là có thể dùng trong suốt đợt điều trị, cho đến cả giai đoạn muộn khi levodopa mất dần tác dụng (wear off) hay trở nên không ổn định và xuất hiện sự dao động trong hiệu quả điều trị (cuối liều hay dao động bật tắt "on off").
* SIFROL viên nén được chỉ định điều trị triệu chứng cho hội chứng "chân không yên vô căn" vừa đến nặng với liều lượng đến 0,75 mg dạng muối (xem phần Liều lượng và cách dùng).
Liều lượng & Cách dùng
Bệnh Parkinson
SIFROL viên nén: Uống thuốc với nước, có thể dùng cùng thức ăn hoặc không. Liều hằng ngày được chia đều để uống 3 lần trong ngày.
SIFROL viên nén phóng thích chậm: là dạng bào chế đường uống của pramipexole dùng một lần duy nhất trong ngày. Nên uống nguyên cả viên với nước, và không được nhai, chia nhỏ hoặc nghiền nát. Có thể dùng cùng hoặc không cùng với thức ăn và nên dùng hàng ngày tại một thời điểm nhất định. Khi quên không uống một liều, nên uống bù SIFROL viên nén phóng thích chậm trong vòng 12 giờ kể từ thời điểm dùng thường xuyên theo lịch. Nếu quá 12 giờ, nên bỏ qua liều bị quên và liều tiếp theo nên được sử dụng vào ngày hôm sau theo đúng lịch trình thuốc.
Điều trị khởi đầu
Liều dùng tăng dần từ từ, liều khởi đầu là 0,375 mg dạng muối mỗi ngày, rồi tăng liều dần mỗi 5-7 ngày. Nếu bệnh nhân không gặp các tác dụng phụ quá khó chịu, nên chỉnh liều dần cho đến khi đạt được tác dụng điều trị tối đa.
- xem Bảng 1.
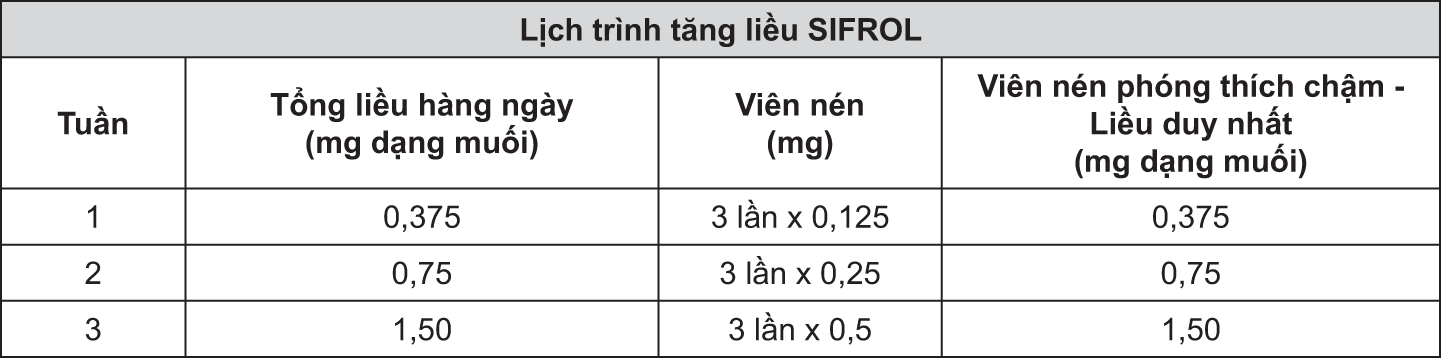
Nếu cần tăng liều thêm nữa, mỗi tuần nên tăng liều hàng ngày thêm 0,75 mg dạng muối cho đến liều tối đa là 4,5 mg dạng muối một ngày. Tuy nhiên, cần lưu ý rằng tỉ lệ buồn ngủ sẽ tăng lên khi liều cao hơn 1,5 mg/ngày (xem phần Tác dụng ngoại ý).
Bệnh nhân đã dùng SIFROL viên nén có thể chuyển qua sử dụng SIFROL viên phóng thích chậm chỉ sau 1 đêm, với cùng một liều lượng dùng hàng ngày. Sau khi chuyển qua dùng SIFROL viên nén phóng thích chậm, liều lượng có thể điều chỉnh dựa vào đáp ứng điều trị của bệnh nhân (xem mục Tính chất dược lý).
Điều trị duy trì
Liều dùng cho từng bệnh nhân nên ở trong khoảng từ 0,375 mg dạng muối đến tối đa là 4,5 mg dạng muối mỗi ngày. Trong quá trình tăng liều ở các nghiên cứu then chốt cho thấy hiệu quả đạt được bắt đầu từ liều 1,5 mg dạng muối. Việc chỉnh liều thêm nữa cần dựa trên đáp ứng lâm sàng và sự xuất hiện của các tác dụng ngoại ý. Trong các thử nghiệm lâm sàng, có khoảng 5% bệnh nhân được điều trị ở liều thấp hơn 1,5 mg dạng muối. Trong điều trị bệnh Parkinson giai đoạn tiến triển, liều cao hơn 1,5 mg dạng muối/ngày có thể hữu ích cho bệnh nhân khi có dự định giảm liều levodopa. Giảm liều levodopa được khuyến cáo trong cả hai trường hợp tăng liều hoặc điều trị duy trì SIFROL tùy thuộc vào phản ứng của từng bệnh nhân.
Ngừng điều trị
Ngừng đột ngột liệu pháp dopaminergic có thể dẫn đến xuất hiện hội chứng ác tính do thuốc chống loạn thần. Vì vậy, cần giảm liều pramipexole từ từ ở mức 0,75 mg dạng muối mỗi ngày cho đến khi liều hàng ngày giảm còn 0,75 mg dạng muối. Sau đó, cứ mỗi ngày nên giảm liều bớt 0,375 mg dạng muối mỗi ngày (xem phần Cảnh báo).
Liều dùng trên bệnh nhân suy thận
Sự thải trừ pramipexole phụ thuộc vào chức năng thận. Dưới đây là liều lượng được gợi ý khi khởi đầu điều trị: Bệnh nhân có độ thanh thải creatinin trên 50mL/phút không cần phải giảm liều hay số lần dùng thuốc hàng ngày.
(a) Viên nén phóng thích chậm: Trên bệnh nhân có độ thanh thải creatinine từ 30 đến 5mL/phút, bắt đầu với liều 0,375mg dạng muối SIFROL viên nén phóng thích chậm mỗi ngày. Nên lưu ý và đánh giá cẩn thận đáp ứng điều trị và mức độ dung nạp trước khi tăng liều dùng hàng ngày sau một tuần. Nếu việc tăng thêm liều dùng là cần thiết, liều dùng nên được tăng là 0,375mg dạng muối cho mỗi tuần cho đến liều tối đa là 2,25 mg dạng muối mỗi ngày. Không khuyến cáo điều trị ở những bệnh nhân có độ thanh thải creatinine dưới 30mL/phút với SIFROL viên nén phóng thích chậm do dữ liệu không có sẵn cho nhóm bệnh nhân này. Nên cân nhắc khi sử dụng SIFROL viên nén trong trường hợp này. Nên tuân theo các khuyến cáo đưa ra ở trên nếu chức năng thận suy giảm trong quá trình điều trị duy trì.
(b) Viên nén: Trên bệnh nhân có độ thanh thải creatinin dưới 20mL/phút, liều hàng ngày của SIFROL nên được uống một lần, bắt đầu với liều 0,125 mg dạng muối mỗi ngày. Liều tối đa hàng ngày không nên vượt quá 1,5 mg pramipexole. Nếu chức năng thận suy giảm trong thời gian điều trị duy trì, cần giảm liều SIFROL hàng ngày theo cùng một tỉ lệ với sự suy giảm của độ thanh thải creatinin, tức là nếu độ thanh thải creatinin giảm 30%, thì cũng giảm 30% liều SIFROL hàng ngày. Liều hàng ngày có thể chia ra uống hai lần nếu độ thanh thải creatinin ở trong khoảng từ 20 đến 50mL/phút và nên uống một lần duy nhất trong ngày nếu độ thanh thải creatinin dưới 20mL/phút.
Liều dùng trên bệnh nhân suy gan
Không cần thiết phải giảm liều trên bệnh nhân suy gan vì khoảng 90% hoạt chất được hấp thu sẽ được bài tiết qua thận. Tuy nhiên, ảnh hưởng của suy gan đối với dược động học của SIFROL vẫn chưa được nghiên cứu.
Liều dùng ở trẻ em và thanh thiếu niên
Không khuyến cáo sử dụng SIFROL viên nén phóng thích chậm ở trẻ em và thanh thiếu niên dưới 18 tuổi do còn thiếu dữ liệu về tính an toàn và hiệu quả.
Hội chứng chân không yên
Viên thuốc được uống với nước, và có thể uống cùng hay không cùng thức ăn.
Liều khởi đầu được khuyến nghị của SIFROL là 0,125 mg dạng muối uống mỗi ngày một lần, dùng 2-3 giờ trước khi đi ngủ. Đối với bệnh nhân cần giảm nhẹ triệu chứng thêm nữa, có thể tăng liều cách mỗi 4-7 ngày (khoảng cách giữa các bước tăng liều), đến tối đa là 0,75 mg dạng muối/ngày.
- xem Bảng 2.
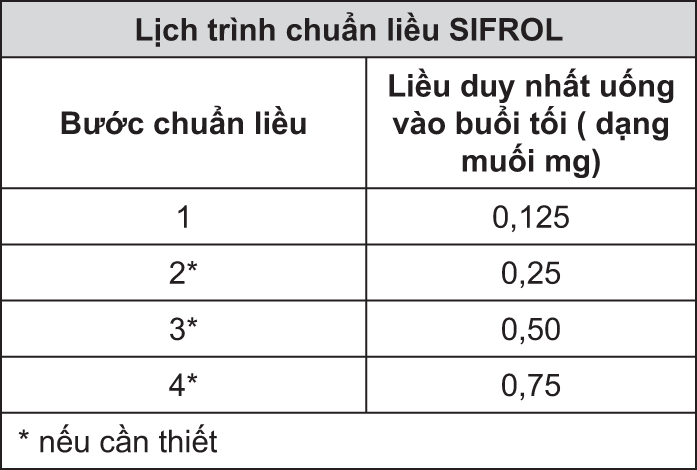
Do hiệu quả lâu dài của SIFROL trong điều trị "hội chứng chân không yên" chưa được thử nghiệm đầy đủ, cần đánh giá đáp ứng của bệnh sau ba tháng điều trị và cân nhắc việc có tiếp tục dùng thuốc hay không. Nếu điều trị bị gián đoạn trong vài ngày, cần bắt đầu chuẩn liều lại theo như bảng trên.
Ngừng điều trị
Không cần giảm liều SIFROL từ từ do liều điều trị hàng ngày hội chứng "chân không yên vô căn" không quá 0,75 mg dạng muối. Không loại trừ hiện tượng bật ngược (rebound, tình trạng tệ hơn của các triệu chứng sau khi ngừng thuốc đột ngột).
Liều dùng trên bệnh nhân suy thận
Sự thải trừ pramipexole phụ thuộc vào chức năng thận. Bệnh nhân có độ thanh thải creatinin trên 20mL/phút không cần phải giảm liều hàng ngày. Việc sử dụng SIFROL trên bệnh nhân có hội chứng chân không yên đang chạy thận nhân tạo hoặc bệnh nhân suy thận nặng chưa được nghiên cứu.
Liều dùng trên bệnh nhân suy gan
Không cần thiết phải giảm liều trên bệnh nhân suy gan, vì khoảng 90% lượng thuốc đã hấp thu được bài tiết qua thận.
Liều dùng ở trẻ em và thiếu niên
Khuyến cáo không dùng SIFROL cho trẻ em và thiếu niên dưới 18 tuổi do chưa có đủ số liệu chứng minh tính an toàn và hiệu quả của thuốc SIFROL đối với nhóm đối tượng này.
Cảnh báo
Khi kê toa SIFROL cho bệnh nhân Parkinson bị suy thận, nên giảm liều như hướng dẫn ở mục Liều lượng và Cách dùng.
Ảo giác là tác dụng phụ đã biết của thuốc đồng vận dopamin và của levodopa. Bệnh nhân cần được thông báo rằng có thể xảy ra ảo giác (phần lớn là ảo thị).
Ở bệnh nhân Parkinson giai đoạn bệnh tiến triển, khi điều trị phối hợp với levodopa, rối loạn vận động có thể gặp khi bắt đầu chuẩn liều SIFROL. Nếu điều này xảy ra, cần giảm liều levodopa.
SIFROL có liên quan đến buồn ngủ và khởi phát ngủ gật, đặc biệt ở bệnh nhân Parkinson. Ngủ gật trong các hoạt động hàng ngày mà trong một vài trường hợp không biết hoặc không có dấu hiệu báo trước thì ít gặp. Bệnh nhân cần được thông báo và khuyên thận trọng khi lái xe hoặc vận hành máy móc khi điều trị bằng SIFROL. Bệnh nhân có xuất hiện buồn ngủ hoặc ngủ gật cần hạn chế lái xe hoặc vận hành máy móc. Bên cạnh đó, cần cân nhắc giảm liều hoặc ngừng điều trị. Do có thể có các tác dụng khác cần khuyến cáo bệnh nhân nếu họ có sử dụng các thuốc an thần hoặc rượu (alcohol) cùng pramipexole (xem mục Tác động đối với khả năng lái xe và vận hành máy móc và Tác dụng ngoại ý).
Bệnh nhân và người chăm sóc nên nhận biết về các hành vi bất thường (phản ánh các triệu chứng của rối loạn kiểm soát xung lực và các hành vi xung lực cưỡng bức) như ăn nhiều (ăn uống vô độ), mua sắm quá độ (compulsive shopping), tăng hoạt động tình dục và cờ bạc bệnh lý đã được báo cáo ở những bệnh nhân điều trị với thuốc dopaminergic.
Nên xem xét giảm liều/ngưng thuốc từ từ.
Chỉ điều trị thuốc đồng vận dopamine cho bệnh nhân có rối loạn tâm thần nếu như lợi ích thu được cao hơn nguy cơ.
Cần tránh việc sử dụng đồng thời các thuốc chống loạn thần với pramipexole (xem mục Tương tác).
Cần kiểm tra mắt định kỳ hoặc khi có bất thường thị lực.
Cần thận trọng trong trường hợp có bệnh tim mạch nặng. Nên theo dõi huyết áp, đặc biệt là khi bắt đầu điều trị, vì nguy cơ chung là hạ huyết áp tư thế liên quan đến liệu pháp dopaminergic. Sự xuất hiện của các triệu chứng trong hội chứng an thần kinh ác tính cũng được ghi nhận khi ngừng đột ngột liệu pháp dopaminergic (xem phần Liều lượng và Cách dùng).
Các báo cáo trong y văn cho thấy điều trị hội chứng chân không yên bằng thuốc đồng vận dopaminergic có thể gây tăng hội chứng chân không yên.
Hiện tượng gia tăng biểu hiện bằng sự khởi phát triệu chứng sớm hơn vào buổi tối (hoặc thậm chí buổi chiều), tăng các triệu chứng và triệu chứng lan rộng đến các chi khác. Các thử nghiệm có đối chứng của SIFROL trên bệnh nhân có hội chứng chân không yên thường không kéo dài đủ thời gian để ghi nhận hiện tượng gia tăng này. Tần suất gia tăng sau một thời gian dài sử dụng SIFROL và việc xử lý thích hợp của những biến cố này chưa được đánh giá trong các thử nghiệm lâm sàng có đối chứng.
Ảnh hưởng trên khả năng lái xe và vận hành máy móc:
SIFROL có ảnh hưởng lớn đến khả năng lái xe và vận hành máy móc.
Có thể xuất hiện ảo giác hoặc buồn ngủ.
Bệnh nhân sử dụng SIFROL có xuất hiện buồn ngủ và/hoặc cơn ngủ gật bất thình lình cần được cảnh báo để ngừng lái xe hoặc tham gia vào các hoạt động mà sự mất tỉnh táo có thể gây thương tích hoặc tử vong cho bản thân họ và người khác (ví dụ khi vận hành máy móc) cho đến khi giải quyết được cơn buồn ngủ và ngủ gật (xem phần Cảnh báo, Tương tác và Tác dụng ngoại ý).
Quá Liều
Không có thông tin lâm sàng về quá liều. Các tác dụng phụ có thể gặp là những biểu hiện liên quan đến đặc tính dược lực học của thuốc đồng vận dopamine, bao gồm buồn nôn, ói mửa, tăng động, ảo giác, kích động, và hạ huyết áp. Chưa có thuốc giải độc cho việc quá liều thuốc đồng vận dopamine. Nếu có các dấu hiệu kích thích thần kinh trung ương, có thể dùng thuốc an thần. Xử trí quá liều thường bằng các biện pháp hỗ trợ chung như rửa dạ dày, truyền dịch, dùng than hoạt và theo dõi điện tim.
Chống chỉ định
Mẫn cảm với pramipexole hoặc bất cứ thành phần nào của sản phẩm.
Sử dụng ở phụ nữ có thai và cho con bú
Ảnh hưởng trên phụ nữ có thai và cho con bú chưa được nghiên cứu ở người. Pramipexole không có tính sinh quái thai trên chuột và thỏ, nhưng có độc tính trên phôi chuột cống khi dùng liều độc cho chuột cống mẹ (xem phần An toàn tiền lâm sàng).
Không nên dùng SIFROL trong thai kỳ trừ khi thật cần thiết, nghĩa là chỉ điều trị nếu lợi ích cao hơn nguy cơ đối với thai nhi.
Vì pramipexole ức chế tiết prolactin trên người, nên có thể ức chế sự tiết sữa. Việc pramipexole vào sữa mẹ chưa được nghiên cứu ở phụ nữ. Ở chuột cống, nồng độ của chất có hoạt tính - liên quan đến hoạt tính phóng xạ được xác định trong sữa chuột mẹ cao hơn trong huyết tương. Do còn thiếu các dữ liệu trên người, không nên dùng SIFROL trong thời gian cho con bú. Tuy nhiên, nếu không thể tránh khỏi việc sử dụng thuốc trong thời gian này, hãy ngừng việc cho con bú.
Chưa có bất kỳ nghiên cứu nào được thực hiện trên khả năng sinh sản. Các nghiên cứu trên động vật không chỉ ra ảnh hưởng gây hại trực tiếp hoặc gián tiếp liên quan đến khả năng sinh sản trên giống đực.
Tương tác
* Gắn kết với protein huyết tương
Pramipexole gắn kết với protein huyết tương với tỉ lệ rất thấp (< 20%) và ít bị biến đổi sinh học ở người. Do đó, ít có khả năng xảy ra tương tác với những thuốc khác mà có ảnh hưởng đến sự gắn kết protein huyết tương hoặc sự thải trừ do biến đổi sinh học.
Mặc dù tương tác với các thuốc kháng cholinergic chưa được nghiên cứu nhưng vì các thuốc kháng cholinergic bị thải trừ do biến đổi sinh học nên khả năng tương tác là rất thấp. Không có tương tác dược động học với selegiline và levodopa.
* Ức chế/cạnh tranh của đường thải trừ chủ động qua thận
Cimetidine giảm độ thanh thải qua thận của pramipexole vào khoảng 34%, có lẽ do ức chế hệ thống vận chuyển bài tiết các cation (ion dương) ở ống thận. Vì vậy, các thuốc ức chế hoặc làm giảm sự bài tiết chủ động qua thận như cimetidine và amantadine, có thể tương tác với pramipexole kết quả là làm giảm độ thanh thải một hoặc của cả hai thuốc. Cần cân nhắc giảm liều pramipexole khi các thuốc này được dùng cùng với SIFROL.
* Dùng đồng thời với levodopa
Khi dùng SIFROL cùng với levodopa, cần giảm liều levodopa, giữ nguyên liều các thuốc trị bệnh Parkinson khác trong khi tăng liều SIFROL.
Do khả năng xảy ra tác dụng cộng hợp, cần khuyến cáo cẩn trọng cho bệnh nhân khi dùng đồng thời pramipexole với các thuốc an thần khác hoặc rượu (xem Cảnh báo, Ảnh hưởng trên khả năng lái xe và vận hành máy móc và Tác dụng ngoại ý).
* Thuốc chống loạn thần: Nên tránh việc sử dụng đồng thời thuốc chống loạn thần với pramipexole, ví dụ các ảnh hưởng tác động đối kháng có thể xảy ra (xem mục Cảnh báo).
Tác dụng ngoại ý
Các tác dụng không mong muốn có thể xảy ra
Các tác dụng không mong muốn sau có thể xảy ra sau khi dùng SIFROL: mơ bất thường, hay quên, suy tim, biểu hiện hành vi của hiện tượng rối loạn kiểm soát xung lực và hành vi xung lực cưỡng chế như ăn uống vô độ, mua sắm quá độ (compulsive shopping), tăng hoạt động tình dục và cờ bạc bệnh lý; lú lẫn, táo bón, hoang tưởng, chóng mặt, rối loạn vận động, khó thở, mệt mỏi, ảo giác, nhức đầu, nấc, tăng động, hạ huyết áp, tiết hormone kháng bài niệu không tương xứng, ăn nhiều (ăn uống vô độ), mất ngủ, rối loạn ham muốn tình dục, buồn nôn, hoang tưởng (paranoia), phù ngoại biên, viêm phổi, ngứa, phát ban và phản ứng quá mẫn khác; bồn chồn (không yên), buồn ngủ, ngủ gật bất thình lình, ngất, rối loạn thị lực bao gồm nhìn đôi, nhìn mờ và giảm thị lực, nôn, tăng cân, giảm cân kể cả giảm cảm giác ngon miệng, tăng cân.
Dựa trên phân tích các nghiên cứu thử nghiệm lâm sàng có đối chứng, bao gồm 1778 bệnh nhân bị Parkinson dùng pramipexole viên nén phóng thích chậm (hoặc 1923 bệnh nhân dùng viên nén) và 1297 bệnh nhân (hoặc tương ứng 1354 bệnh nhân) dùng giả dược, tác dụng phụ của thuốc được ghi nhận ở cả hai nhóm. 67% bệnh nhân dùng SIFROL viên nén phóng thích chậm và 54% (hoặc tương ứng 52% bệnh nhân) dùng giả dược cho biết gặp ít nhất một tác dụng phụ.
Các tác dụng không mong muốn được báo cáo trong bảng dưới đây là những tác dụng xuất hiện với tỷ lệ 0,1% hoặc cao hơn ở những bệnh nhân điều trị với pramipexole và được báo cáo thường xuyên hơn một cách đáng kể ở những bệnh nhân dùng pramipexole so với dùng giả dược, hoặc khi các hiện tượng đó được cân nhắc là có liên quan về mặt lâm sàng. Các tác dụng phụ chủ yếu có mức độ nhẹ đến trung bình, thường xuất hiện ở giai đoạn đầu khi điều trị và thường có xu hướng mất đi khi tiếp tục điều trị.
Theo phân loại hệ cơ quan trong cơ thể, các tác dụng không mong muốn được liệt kê theo mức độ tần xuất (số bệnh nhân được cho là có xuất hiện phản ứng), sử dụng phân loại sau: rất phổ biến (≥1/10), phổ biến (≥1/100 tới <1/10); không phổ biến (≥1/1.000 tới <1/100); hiếm (≥1/10.000 tới <1/1000), rất hiếm (<1/10.000); không biết (không thể ước đoán từ dữ liệu sẵn có).
- xem Bảng 3.
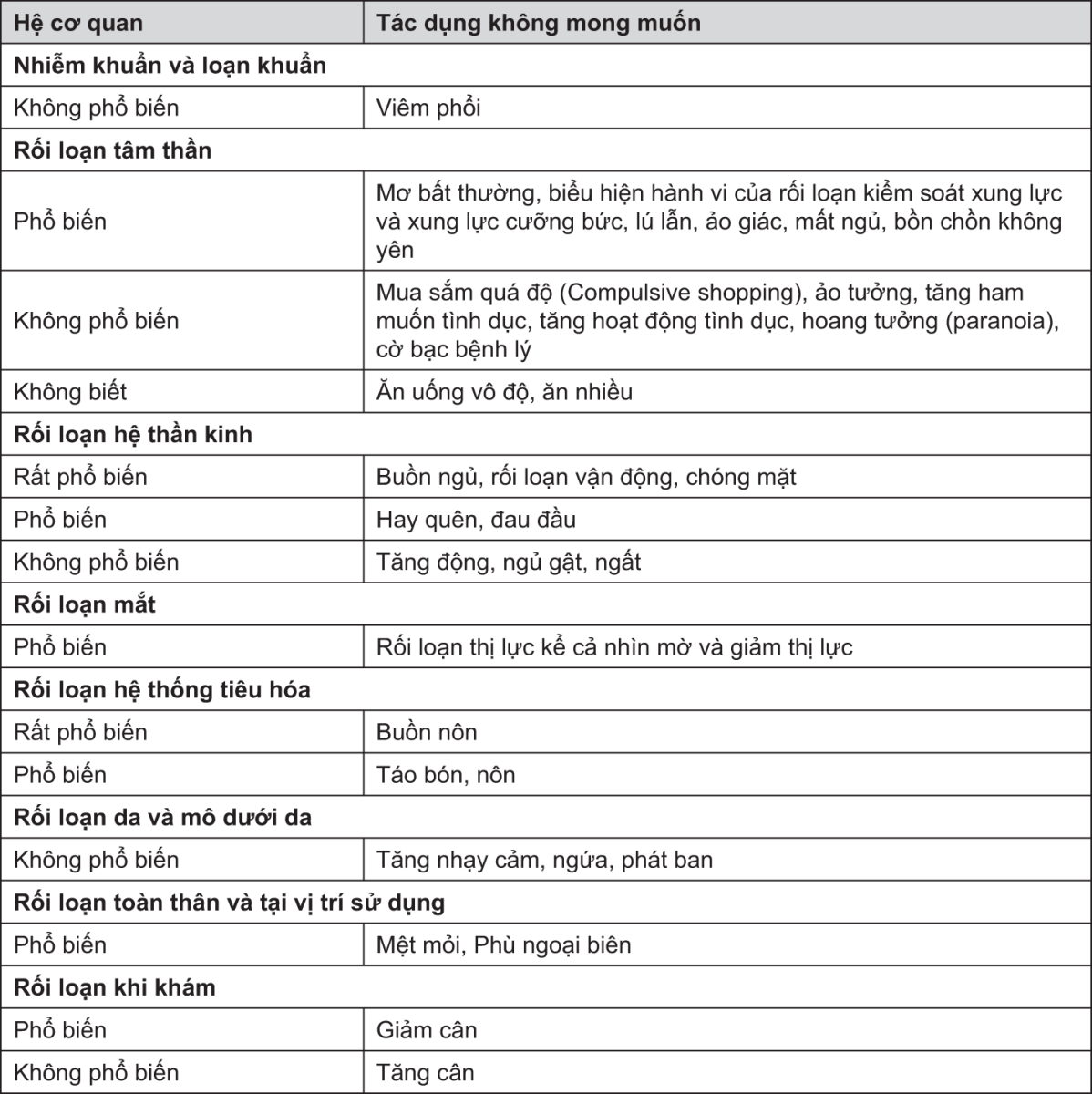
Các tác dụng không mong muốn thường gặp (≥ 5%) trên các bệnh nhân Parkinson dùng pramipexole nhiều hơn so với nhóm dùng giả dược là nôn, rối loạn vận động, hạ huyết áp, chóng mặt, buồn ngủ, mất ngủ, táo bón, ảo giác, đau đầu và mệt mỏi. Tỷ lệ buồn ngủ tăng lên khi liều cao hơn 1,5 mg dạng muối/ngày (xem phần Liều lượng và cách dùng). Tác dụng phụ thường gặp khi dùng kết hợp với levodopa là rối loạn vận động. Hạ huyết áp khi bắt đầu điều trị, đặc biệt khi tăng liều pramipexole quá nhanh.
Buồn ngủ
Tác dụng phụ phổ biến khi điều trị với pramipexole là buồn ngủ và không phổ biến là trạng thái buồn ngủ quá nhiều lúc ban ngày và ngủ gật (xem mục Cảnh báo).
Rối loạn tình dục
Không phổ biến có tác dụng không mong muốn gây rối loạn tình dục khi dùng pramipexole (tăng hoặc giảm)
Rối loạn kiểm soát xung lực và các hành vi xung lực cưỡng bức
Bệnh nhân điều trị bệnh Parkinson với các chất đối kháng dopamine, kể cả SIFROL, đặc biệt ở những liều cao đã được báo cáo xuất hiện những dấu hiệu của bệnh cờ bạc bệnh lý, tăng ham muốn tình dục và tăng hoạt động, nhìn chung thường hồi phục khi giảm liều hoặc ngừng điều trị (Xem mục Cảnh báo).
Trong các nghiên cứu lâm sàng và dữ liệu hậu mãi, đã có báo cáo suy tim ở những bệnh nhân điều trị với pramipexole. Trong một nghiên cứu dược dịch tễ học, sử dụng pramipexole có liên quan đến tăng nguy cơ suy tim so với những bệnh nhân không dùng pramipexole. Chưa giải thích được một mối liên quan giữa pramipexole và suy tim.
Trong một nghiên cứu hồi cứu cắt ngang và có kiểm soát trường hợp bao gồm 3.090 bệnh nhân mắc bệnh Pakinson, 13,6% bệnh nhân dùng trị liệu dopaminergic hoặc không dopaminergic có triệu chứng của một rối loạn kiểm soát xung lực trong vòng 6 tháng cuối. Các biểu hiện quan sát được bao gồm cờ bạc bệnh lý, mua sắm quá độ (compusive shopping), ăn uống vô độ, và có hành vi tình dục cưỡng bức (tăng hoạt động tình dục). Các yếu tố nguy cơ độc lập có thể của việc rối loạn kiểm soát xung lực kể cả khi điều trị với dopaminergic và dùng những liều cao dopaminergic, bệnh nhân ít tuổi (≤ 65 tuổi), chưa lập gia đình và gia đình có tiền sử đã được báo cáo là có những hành vi cờ bạc.
Lưu ý bệnh nhân thông báo cho bác sỹ biết các tác dụng không mong muốn gặp phải khi sử dụng thuốc.
Bảo quản
* Bảo quản dưới 30oC.
* Bảo quản nguyên trong bao bì tránh ánh sáng.
Phân loại ATC
N04BC05 - pramipexole
Trình bày/Đóng gói
Viên nén có thể bẻ đôi: hộp 3 vỉ x 10 viên.
Viên nén phóng thích chậm: hộp 3 vỉ x 10 viên.
- Abacavir
- Abernil
- Abiiogran
- Acarbose
- ACC
- Acebutolol
- Acenocoumarol
- Acetate Ringer's
- Acetazolamide
- Acetylcystein
- Acetylsalicylic acid
- Aciclovir
- Acid acetylsalicylic
- Acid aminocaproic
- Acid ascorbic
- Acid boric
- Acid chenodeoxycholic
- Acid ethacrynic
- Acid folic
- Acid fusidic
- Acid iopanoic
- Acid ioxaglic
- Acid nalidixic
- Acid pantothenic
- Acid para-aminobenzoic
- Acid salicylic
- Acid tranexamic
- Acid valproic
- Acid zoledronic
- Acitretin
- Aclasta
- Aclon
- Actapulgite
- Actelsar
- Actelsar HCT
- Actemra
- Actilyse
- Acular
- Acupan
- Acuvail
- Acyclovir STADA
- Acyclovir STADA Cream
- Adalat
- Adenosin
- Adenosin Ebewe
- Adipiodon
- Advagraf
- Aerius
- Afinitor
- Agicarvir
- Agifovir-E
- Agilosart
- Agilosart-H
- Agimepzol
- Agimosarid
- Agimstan
- Agimstan-H
- Agiremid
- Agivastar
- Aibezym
- Air-X
- Alaxan
- Albendazol
- Albiomin
- Albumin
- Albumin người Grifols 20%
- Albuminar
- AlbuRx
- Albutein
- Alcuronium chloride
- Aldesleukin
- Alendronat
- Alertin
- Alfa-Lipogamma 600 Oral
- Alfuzosin hydrochlorid
- Algotra
- Alimemazin
- Alimta
- Allipem
- Allopurinol
- Allopurinol STADA
- Aloxi
- Alprazolam
- Alpha Chymotrypsin
- Alpha tocopherol
- Alphachymotrypsin Glomed
- Alphagan-P
- Aluvia
- Alzental
- Amaryl
- Ambroco
- Ambroxol
- Amcinol-Paste
- Amigold
- Amikacin
- Aminocaproic acid
- Aminoleban
- Aminoleban Oral
- Aminosteril N-Hepa
- Amiparen
- Amitriptyline
- Amiyu
- Amlodipine
- Amlor
- Amoxicillin
- Amoxicillin & clavulanate
- Ampicillin
- Amquitaz
- Anaferon for children
- Anargil
- Anaropin
- Andriol Testocaps
- Anepzil
- Anyfen
- Apaisac
- Apidra SoloStar
- Apitim 5
- Aprovel
- Aquaphil
- Arcalion
- Arcoxia
- Aricept Evess
- Arimidex
- Arnetine
- Artrodar
- A-Scabs
- Ascorbic acid
- Asperlican/Candinazol
- Aspilets EC
- Aspirin
- Asthmatin
- Atelec
- Atocib 120
- Atocib 90
- Atosiban PharmIdea
- Atozet
- Attapulgite
- Atussin
- Atropin
- Augbactam
- Augmentin Sachet
- Augmentin SR
- Augmentin Tablets
- Augmex
- Avamys
- Avastin
- Avelox Dịch truyền
- Avelox Viên nén
- Avodart
- Axcel Cefaclor-125 Suspension
- Axcel Cetirizine Syrup
- Axcel Chlorpheniramine
- Axcel Dexchlorpheniramine
- Axcel Dicyclomine-S Syrup
- Axcel Diphenhydramine Paediatric Syrup
- Axcel Erythromycin ES
- Axcel Eviline
- Axcel Fungicort Cream
- Axcel Fusidic acid Cream
- Axcel Fusidic acid-B Cream
- Axcel Hydrocortisone Cream
- Axcel Lignocaine 2% Sterile Gel
- Axcel Loratadine
- Axcel Miconazole Cream
- Axcel Paracetamol
- Axcel Urea Cream
- Axitan
- Azenmarol
- Azicine
- Aziphar
- Azithromycin