Nhà sản xuất
Bayer Pharma AG
Nhà tiếp thị
Bayer (South East Asia)
Thành phần
Mỗi mL: Gadoxetate disodium 0,25mmol (tương đương với 181,43mg gadoxetate disodium).
Mô tả
Dung dịch tiêm trong suốt từ không màu tới màu vàng nhạt.
Dược lực học
Cơ chế tác dụng
Primovist là một chất đối quang thuận từ được sử dụng trong chụp cộng hưởng từ.
Tác dụng tăng đối quang qua trung gian của gadoxetate, một phức chất ion tạo bởi gadolinium (III) và liên kết ethoxybenzyl-diethylenetriamine-pentaacetic acid (EOB-DTPA).
Khi sử dụng chuỗi xung quét T1W trong chụp cộng hưởng từ proton, ion gadolinium làm rút ngắn thời gian thư giãn mạng lưới cấu trúc – spin của hạt nhân nguyên tử bị kích thích bị kích thích dẫn đến làm tăng cường độ tín hiệu và do đó tăng hình ảnh đối quang trên một số mô nhất định.
Tác dụng dược lực học
Gadoxetate disodium làm giảm rõ rệt thời gian thư giãn, ngay cả ở nồng độ thấp. Ở pH 7, cường độ từ trường là 0,47 T và 40°C, độ thư giãn (r1) được xác định dựa vào sự tác động lên thời gian thư giãn mạng lưới cấu trúc – spin (T1) của các proton trong huyết tương – vào khoảng 8,18 L/(mmol-giây) và độ thư giãn (r2) – được xác định dựa vào sự tác động lên thời gian thư giãn spin – spin (T2) – vào khoảng 8,56 L/(mmol-giây). Ở cường độ từ trường 1,5 T và 37°C, độ thư giãn trong huyết tương tương ứng là r1= 6,9 L/(mmol-giây) và r2 = 8,7 L/(mmol-giây). Độ thư giãn cho thấy sự phụ thuộc tỷ lệ nghịch nhẹ với cường độ từ trường.
Ethoxybenzyl-diethylenetriaminepentaacetat tạo thành một phức chất bền vững với ion gadolinium thuận từ có độ ổn định cực cao trong in vitro và in vivo (hằng số ổn định nhiệt động lực: log KGdl = 23,46).
Gadoxetate disodium tan nhiều trong nước, là một hợp chất ưa nước với hệ số tỷ lệ giữa n-butanol và chất đệm ở pH 7,6 là khoảng 0,011.
Do phân nửa là ethoxybenzyl ưa lipid nên phân tử gadoxetate disodium có phương thức hoạt động hai pha: ban đầu, sau khi tiêm khối thuốc (bolus) vào tĩnh mạch, thuốc phân phối trong khoảng ngoại bào; sau đó được hấp thu chọn lọc bởi các tế bào gan. Độ thư giãn r1 ở mô gan là 16,61/(mmol-giây) (ở 0,47 T) dẫn đến sự tăng cường độ tín hiệu ở mô gan. Tiếp theo đó gadoxetate disodium được thải vào mật.
Thuốc không thể hiện bất cứ tương tác ức chế rõ rệt nào với các enzym ở nồng độ thường dùng trên lâm sàng.
Hình ảnh học
Sau khi tiêm bolus Primovist, hình ảnh động trong thời gian của các pha động mạch, tĩnh mạch cửa và pha cân bằng sử dụng những kiểu tăng cản quang khác nhau theo thời gian của các tổn thương gan khác nhau là cơ sở để mô tả tổn thương trên X quang.
Sự tăng cản quang của nhu mô gan trong thời gian của pha tế bào gan hỗ trợ cho việc xác định số lượng, sự phân bố theo đoạn, hình dung và mô tả các tổn thương của gan, do đó, cải thiện sự phát hiện các tổn thương. Mô hình tăng cường cản quang/rửa trôi khác nhau của các tổn thương gan góp phần vào các thông tin từ pha động.
Pha muộn (tế bào gan) có thể được khảo sát ở thời điểm 20 phút sau khi tiêm, với cửa sổ hình ảnh kéo dài ít nhất 120 phút. Các kết quả về hiệu quả chẩn đoán và kỹ thuật của các thử nghiệm lâm sàng cho thấy sự cải thiện tối thiểu ở thời điểm 20 phút sau khi tiêm hơn các kết quả ở 10 phút sau khi tiêm. Ở bệnh nhân cần thẩm tách máu và bệnh nhân có các giá trị bilirubin tăng cao (>3 mg/dL), thì cửa sổ hình ảnh bị giảm đến 60 phút.
Sự bài tiết Primovist qua gan dẫn đến tăng cản quang các cấu trúc mật.

Bệnh nhân nhi
Một nghiên cứu quan sát được thực hiện trên 52 bệnh nhân nhi (tuổi >2 tháng tuổi và <18 tuổi). Bệnh nhân được chuyển đến để chụp MRI gan có tăng cường đối quang với Primovist để đánh giá các tổn thương nghi ngờ hoặc đã biết ở gan. Thông tin chẩn đoán bổ sung đạt được khi các hình ảnh cộng hưởng từ gan không tăng và tăng đối quang kết hợp với nhau được so sánh với hình ảnh cộng hưởng từ không tăng đối quang đơn độc. Các biến cố bất lợi nghiêm trọng được báo cáo tuy nhiên, không có báo cáo nào được đánh giá bởi bác sĩ nghiên cứu có liên quan tới Primovist. Do bản chất của nghiên cứu là hồi cứu và cỡ mẫu nhỏ, nên không thể có kết luận chắc chắn về tính an toàn và hiệu quả trên dân số bệnh nhân này.
Dược động học
Giới thiệu chung
Gadoxetate disodium hoạt động trong các cơ quan giống các hợp chất rất ưa nước, trơ về mặt sinh học, được thải qua thận và gan-mật khác.
Hấp thu và phân bố
Sau khi tiêm tĩnh mạch, đặc tính nồng độ gadoxetate disodium trong huyết tương theo thời gian được đặc trưng bởi sự giảm theo cấp số hai. Tổng thể tích phân bố của gadoxetate disodium ở trạng thái cân bằng khoảng 0,21 L/kg (khoảng ngoại bào). Tỷ lệ gắn kết với protein trong huyết tương khoảng 10%.
Hợp chất không qua được hàng rào máu não còn nguyên vẹn và khuếch tán qua hàng rào nhau thai chỉ ở một mức độ nhỏ như được chứng minh trên chuột.
Ở chuột đang cho con bú, dưới 0,5% liều dùng qua đường tĩnh mạch (0,1 mmol/kg) của gadoxetat đánh dấu phóng xạ thu lại được từ sữa trong dạ dày. Sự hấp thu sau khi uống ở chuột rất nhỏ, khoảng 0,4% của liều uống vào được thu lại từ nước tiểu.
Chuyển hóa
Gadoxetate disodium không được chuyển hóa.
Thải trừ
Gadoxetate disodium thải trừ hoàn toàn với qua đường thận và đường gan-mật với lượng như nhau trên người khỏe mạnh.
Bảy ngày sau khi tiêm tĩnh mạch gadoxetate, dưới 1% liều dùng còn tìm thấy trong cơ thể chuột và khỉ. Trong số đó, nồng độ cao nhất đo được ở thận và gan.
Thời gián bán thải hiệu quả trung bình của gadoxetate disodium (liều 0,01 tới 0,1 mmol/kg) ở người khỏe mạnh là khoảng 1 giờ.
Độ thanh thải toàn phần (CL) khoảng 250mL/phút. Độ thanh thải qua thận (CLR) tương ứng với khoảng 120mL/phút, tương tự với tốc độ lọc cầu thận người khỏe mạnh.
Tính chất tuyến tính/không tuyến tính
Gadoxetate disodium có tính dược động học tuyến tính nghĩa là các thông số dược động học thay đổi tỷ lệ với liều dùng (như Cmax, AUC) hoặc không phụ thuộc liều dùng (như Vss, t1/2) cho tới mức liều 100 µmol/kg cân nặng (0,4 mL/kg).
Thông tin bổ sung trên các quần thể bệnh nhân đặc biệt
Nghiên cứu lâm sàng pha III với liều Primovist là 0.1 mL cho mỗi kg cân nặng so sánh các đối tượng có các mức độ suy giảm chức năng gan, suy giảm chức năng thận khác nhau, người có cùng lúc suy gan và suy thận và người khỏe mạnh ở các độ tuổi khác nhau, bao gồm cả người cao tuổi.
Giới
Độ thanh thải toàn phần ở nữ (185mL/phút) thấp hơn ở nam (236mL/phút) khoảng 20%.
Người già (trên 65 tuổi)
Phù hợp theo những thay đổi sinh lý của chức năng thận theo tuổi, độ thanh thải huyết tương của gadoxetate disodium giảm từ 210mL/phút ở người chưa già xuống còn 163mL/phút ở người già từ 65 tuổi trở lên. Thời gian bán thải và phơi nhiễm toàn thân ở người cao tuổi cao hơn (2,3 giờ và 197 µmol-giờ/L theo thứ tự) so với ở nhóm đối chứng (1,8 giờ và 160 µmol-giờ/L theo thứ tự). Thuốc thải trừ hoàn toàn qua thận sau 24 giờ ở tất cả các đối tượng và không có sự khác biệt giữa những người già khỏe mạnh và những người chưa già.
Bệnh nhân suy giảm chức năng thận
Ở bệnh nhân suy giảm chức năng thận mức trung bình, AUC tăng đến 237 µmol-giờ/L (so với 160 μmol-giờ/L trên người tình nguyện khỏe mạnh) và thời gian bán thải tăng đến 2,2 giờ (so với 1,76 giờ trên người tình nguyện khỏe mạnh). Ở bệnh nhân suy thận giai đoạn cuối, thời gian bán thải kéo dài gấp 12 lần và AUC tăng khoảng 6 lần. Khoảng 55% liều dùng được tìm thấy trong phân trong vòng 6 ngày, phần lớn thải trừ trong vòng 3 ngày.
Bệnh nhân suy giảm chức năng gan
Ở bệnh nhân suy thận mức độ nhẹ hoặc trung bình, có sự tăng nhẹ đến vừa AUC huyết tương, thời gian bán thải và sự thải trừ qua nước tiểu, cũng như giảm thải trừ qua đường gan-mật so sánh với ở người khỏe mạnh.
Ở bệnh nhân suy gan nặng, đặc biệt những bệnh nhân có nồng độ bilirubin cao bất thường (>3 mg/dL), AUC tăng thành 259 µmol-giờ/L so với 160 µmol-giờ/L ở nhóm đối chứng. Thời gian bán thải tăng lên 2,6 giờ so với 1,8 giờ ở nhóm đối chứng. Sự thải trừ qua đường gan-mật giảm đi đáng kể, còn 5,7% liều dùng ở những bệnh nhân này.
Gadoxetate disodium có thể bị thải loại khỏi cơ thể qua thẩm tách máu. Khoảng 30% liều dùng bị thải trừ khỏi cơ thể khi tiến hành thẩm tách máu kéo dài 3 giờ bắt đầu sau 1 giờ tiêm thuốc. Ở bệnh nhân suy thận giai đoạn cuối, gadoxetate disodium được thải trừ gần như hoàn toàn nhờ sự thẩm tách và thải trừ qua mật trong thời gian 6 ngày. Có thể đo được nồng độ của gadoxetate disodium trong huyết tương tới 72 giờ sau khi dùng thuốc ở các bệnh nhân này (xem phần Cảnh báo).
An toàn tiền lâm sàng
Dữ liệu phi lâm sàng cho thấy không có mối nguy hại đặc biệt nào đối với người căn cứ trên các nghiên cứu quy ước về độc tính toàn thân, độc tính gen, khả năng mẫn cảm khi tiếp xúc.
Độc tính trên khả năng sinh sản
Trong các nghiên cứu về sự phát triển của phôi thai trên thỏ, Primovist đường tĩnh mạch sử dụng nhiều lần gây độc với phôi thai (tăng sảy thai sau khi trứng đã làm tổ) ở liều cao gấp 25,9 lần (tính theo diện tích bề mặt cơ thể) hoặc 80 lần (tính theo cân nặng cơ thể) so với liều đơn ở người.
Dung nạp tại chỗ
Các nghiên cứu thực nghiệm khả năng dung nạp Primovist tại chỗ cho thấy thuốc có khả năng dung nạp tốt sau khi đưa thuốc vào mạch (tĩnh mạch và động mạch) và cận tĩnh mạch.
Tuy nhiên, sử dụng thuốc đường tiêm bắp gây ra phản ứng không dung nạp tại chỗ do đó cần tuyệt đối tránh dùng trên người (xem phần Cảnh báo).
Chỉ định/Công dụng
Primovist được chỉ định để phát hiện các tổn thương khu trú ở gan và cung cấp thông tin về đặc điểm của các tổn thương trong chụp cộng hưởng từ xử lý hình ảnh T1 (MRI).
Thuốc này chỉ được dùng cho chẩn đoán bằng cách tiêm tĩnh mạch.
Liều lượng & Cách dùng
Cách dùng
Thuốc được dùng cho đường tĩnh mạch.
Tiêm thuốc vào tĩnh mạch (bolus). Sau khi tiêm chất đối quang, cần phải bơm rửa ống/đường tiêm tĩnh mạch bằng dung dịch nước muối sinh lý.
Tham khảo thông tin chi tiết về chẩn đoán hình ảnh trong phần Dược lực học.
Xem thêm các hướng dẫn trong phần “Hướng dẫn sử dụng/xử lý”.
Liều dùng
Người lớn
Liều khuyến cáo của Primovist
Người lớn: 0,1 mL Primovist trên 1kg cân nặng
Dùng lặp lại: Không có thông tin lâm sàng về dùng liều lặp lại Primovist.
Thông tin thêm về các đối tượng đặc biệt
Trẻ em
Tính an toàn và hiệu quả của Primovist chưa được thiết lập trên bệnh nhân dưới 18 tuổi. Các dữ liệu hiện có được miêu tả trong phần Dược lực học.
Người cao tuổi (từ 65 tuổi trở lên)
Không cần thiết phải chỉnh liều. Nên thận trọng trên người cao tuổi (xem phần Cảnh báo).
Bệnh nhân suy giảm chức năng gan
Không cần phải chỉnh liều.
Bệnh nhân suy giảm chức năng thận
Nên tránh sử dụng Primovist trên những bệnh nhân suy thận nặng (GFR <30mL/phút/1,73m2) và trên những bệnh nhân trong giai đoạn phẫu thuật cấy ghép gan trừ khi thông tin chẩn đoán là cần thiết và không có hình ảnh cộng hưởng từ không đối quang (xem phần Cảnh báo). Nếu không thể tránh việc sử dụng Primovist, thì liều sử dụng không được vượt quá 0,025 mmol/kg cân nặng. Không nên sử dụng quá một liều Primovist trong thời gian chụp. Do thiếu thông tin trên liều lặp lại, nên tránh tiêm lặp lại Primovist trừ khi khoảng cách giữa các lần tiêm ít nhất 7 ngày.
Cảnh báo
Quá mẫn
Cần đặc biệt thận trọng đánh giá nguy cơ-lợi ích ở những bệnh nhân được biết là quá mẫn với Primovist. Như với các thuốc đối quang khác sử dụng theo đường tĩnh mạch, Primovist có thể liên quan tới các phản ứng dạng phản vệ/quá mẫn hoặc phản ứng đặc ứng khác đặc trưng với các biểu hiện tim mạch, hô hấp, và da cho đến những phản ứng nghiêm trọng bao gồm cả sốc.
Nguy cơ gặp phản ứng quá mẫn sẽ cao hơn trong các trường hợp:
· có phản ứng trước đó với thuốc đối quang
· bệnh sử hen phế quản
· bệnh sử các rối loạn dị ứng.
Ở những bệnh nhân có nguy cơ dị ứng, trước khi quyết định sử dụng Primovist cần đặc biệt thận trọng đánh giá tỉ lệ nguy cơ-lợi ích.
Hầu hết các phản ứng này xảy ra trong vòng nửa giờ sau khi sử dụng. Do đó, cần theo dõi bệnh nhân sau khi tiến hành thủ thuật. Cần phải có thuốc điều trị các phản ứng quá mẫn cũng như chuẩn bị sẵn sàng các phương tiện cấp cứu cần thiết. Hiếm gặp những phản ứng muộn sau khi dùng thuốc vài giờ đến vài ngày (xem thêm phần Tác dụng ngoại ý).
Bệnh tim mạch
Cần thận trọng khi sử dụng Primovist ở bệnh nhân có các vấn đề về tim mạch nặng do dữ liệu hiện nay vẫn còn hạn chế.
Suy giảm chức năng thận
Trên người khỏe mạnh, gadoxetate disodium được thải trừ qua đường thận và đường gan-mật đều như nhau.
Trước khi sử dụng Primovist, nên tầm soát xem bệnh nhân có bị rối loạn chức năng thận bằng cách hỏi bệnh sử của bệnh nhân và/hoặc làm xét nghiệm.
Ở bệnh nhân suy thận nặng, cần cân nhắc cẩn thận lợi ích và nguy cơ có thể xảy ra, do thuốc đối quang thải trừ chậm ở những trường hợp này. Nên đảm bảo một khoảng thời gian đủ để thuốc đối quang thải trừ khỏi cơ thể trước khi tiếp tục sử dụng bất cứ một thuốc nào cho bệnh nhân suy thận.
Gadoxetate disodium có thể bị loại khỏi cơ thể qua thẩm tách máu. Khoảng 30% liều dùng bị thải trừ khỏi cơ thể nếu một giờ sau khi tiêm thuốc tiến hành một đợt thẩm tách máu kéo dài 3 giờ. Ở bệnh nhân suy thận giai đoạn cuối, gadoxetate disodium được thải trừ gần như hoàn toàn qua thẩm tách máu và thải trừ qua mật trong thời gian quan sát trong 6 ngày, phần lớn trong vòng 3 ngày.
Với bệnh nhân đang được thẩm tách máu khi dùng Primovist, nên cân nhắc bắt đầu tiến hành thẩm tách máu sau khi dùng Primovist để tăng cường thải trừ thuốc đối quang.
Đã có một số báo cáo về chứng xơ hóa toàn thân do thận (NSF) liên quan đến việc sử dụng thuốc đối quang có chứa gadolinium ở bệnh nhân có:
· suy thận cấp hoặc mạn tính mức độ nặng (GFR <30mL/phút/1.73m2) và
· suy giảm chức năng thận cấp tính ở bất cứ mức độ nào do hội chứng gan-thận hoặc đang trong thời kỳ phẫu thuật ghép gan.
Căn cứ trên mức liều dùng để chẩn đoán của Primovist cũng như hai đường thải trừ của thuốc (thận và gan mật), thì sự phơi nhiễm toàn thân với gadolinium là thấp tuy nhiên vẫn có khả năng xảy ra chứng xơ hóa toàn thân do thận khi dùng Primovist. Vì vậy, chỉ nên dùng Primovist ở những bệnh nhân này sau khi đánh giá cẩn thận nguy cơ/lợi ích (xem phần Tác dụng ngoại ý).
Không dung nạp tại chỗ
Cần hoàn toàn tránh việc sử dụng thuốc theo đường tiêm bắp do có thể gây ra các phản ứng không dung nạp tại chỗ bao gồm cả hoại tử khu trú (xem phần An toàn tiền lâm sàng).
Ảnh hưởng của thuốc lên khả năng lái xe, vận hành máy móc
Chưa có bằng chứng về ảnh hưởng của thuốc lên khả năng lái xe, vận hành máy móc.
Quá Liều
Liều đơn gadoxetate disodium cao tới 0,4 mL/kg (100 µmol/kg) cân nặng được dung nạp tốt. Chưa có báo cáo nào về quá liều khi sử dụng thuốc trên lâm sàng. Do đó, chưa nhận biết được các dấu hiệu và triệu chứng quá liều đặc trưng.
Bệnh nhân suy giảm chức năng thận và/hoặc suy giảm chức năng gan
Trong trường hợp sử dụng quá liều do bất cẩn ở bệnh nhân suy giảm chức năng thận và/hoặc chức năng gan nặng, có thể thải loại Primovist khỏi cơ thể bằng cách thẩm tách máu (xem phần Cảnh báo và Dược động học).
Chống chỉ định
Quá mẫn với các thành phần của thuốc.
Sử dụng ở phụ nữ có thai và cho con bú
Phụ nữ mang thai
Không có dữ liệu về sử dụng gadoxetat trên phụ nữ mang thai. Các nghiên cứu trên động vật cho thấy có độc tính trên chức năng sinh sản ở liều cao lặp lại (xem thêm phần An toàn tiền lâm sàng). Primovist không được sử dụng trong thời kỳ mang thai trừ khi bệnh lý lâm sàng của bệnh nhân phải sử dụng gadoxetate.
Phụ nữ cần cho con bú
Hiện chưa rõ liệu gadoxetate disodium có bài tiết vào sữa người hay không.
Bằng chứng từ dữ liệu phi lâm sàng cho thấy gadoxetate bài tiết vào sữa với một lượng rất nhỏ (ít hơn 0,5% liều dùng theo đường tĩnh mạch) và hấp thu kém qua đường tiêu hóa (khoảng 0,4% liều dùng đường uống được thải trừ qua đường nước tiểu).
Ở liều dùng trên lâm sàng, chưa dự đoán được ảnh hưởng của thuốc đến trẻ nhỏ và có thể dùng Primovist trong thời kỳ cho con bú.
Tương tác
Tương tác với các thuốc ức chế polypeptide vận chuyển anion hữu cơ (OATP) qua màng tế bào
Các nghiên cứu trên động vật cho thấy các hợp chất thuộc nhóm thuốc anionic như rifampicin làm cản trở sự hấp thu của Primovist ở gan, do đó làm giảm hiệu quả đối quang gan. Trong trường hợp này, tác dụng mong muốn đạt được của việc tiêm Primovist có thể bị hạn chế. Chưa có tương tác nào với các thuốc khác được biết từ các nghiên cứu trên động vật.
Một nghiên cứu về tương tác được thực hiện trên người tình nguyện khỏe mạnh cho thấy việc dùng đồng thời chất ức chế OATP erythromycin không làm ảnh hưởng đến hiệu quả và dược động học của Primovist.
Chưa có thêm các nghiên cứu lâm sàng với các thuốc khác được thực hiện.
Tương tác với bilirubin hoặc ferritin huyết thanh tăng cao ở bệnh nhân
Nồng độ bilirubin (>3 mg/dL) hoặc ferritin tăng cao có thể làm giảm hiệu quả đối quang gan của Primovist. Nếu sử dụng Primovist ở những bệnh nhân này, cần hoàn tất việc chụp cộng hưởng từ trong vòng 60 phút sau khi tiêm Primovist.
Tương tác với các test chẩn đoán
Trong 24 giờ sau khi tiến hành chẩn đoán với Primovist, xác định nồng độ sắt huyết thanh bằng phương pháp đo phức chất (như phương pháp phức chất Ferrocine) có thể dẫn đến giá trị cao hoặc thấp sai lệch bởi vì phức chất tự do caloxetate trisodium có trong dung dịch chất đối quang.
Tương kỵ
Do không có các nghiên cứu về tính tương kỵ của thuốc, không trộn lẫn thuốc này với các thuốc khác.
Tác dụng ngoại ý
Tóm tắt dữ liệu về độ an toàn
Độ an toàn nói chung của Primovist được dựa trên dữ liệu thu được từ hơn 1900 bệnh nhân trong các thử nghiệm lâm sàng và từ các giám sát hậu mãi.
Các phản ứng có hại thường gặp nhất (≥0.5%) ở bệnh nhân sử dụng Primovist là buồn nôn, đau đầu, cảm giác nóng, tăng huyết áp và choáng váng.
Phản ứng có hại nghiêm trọng nhất ở bệnh nhân sử dụng Primovist là sốc dạng phản vệ. Hiếm gặp phản ứng giống dị ứng muộn (từ vài giờ đến vài ngày sau khi dùng thuốc).
Phần lớn các tác dụng không mong muốn ở mức độ nhẹ đến trung bình.
Bảng liệt kê các phản ứng có hại
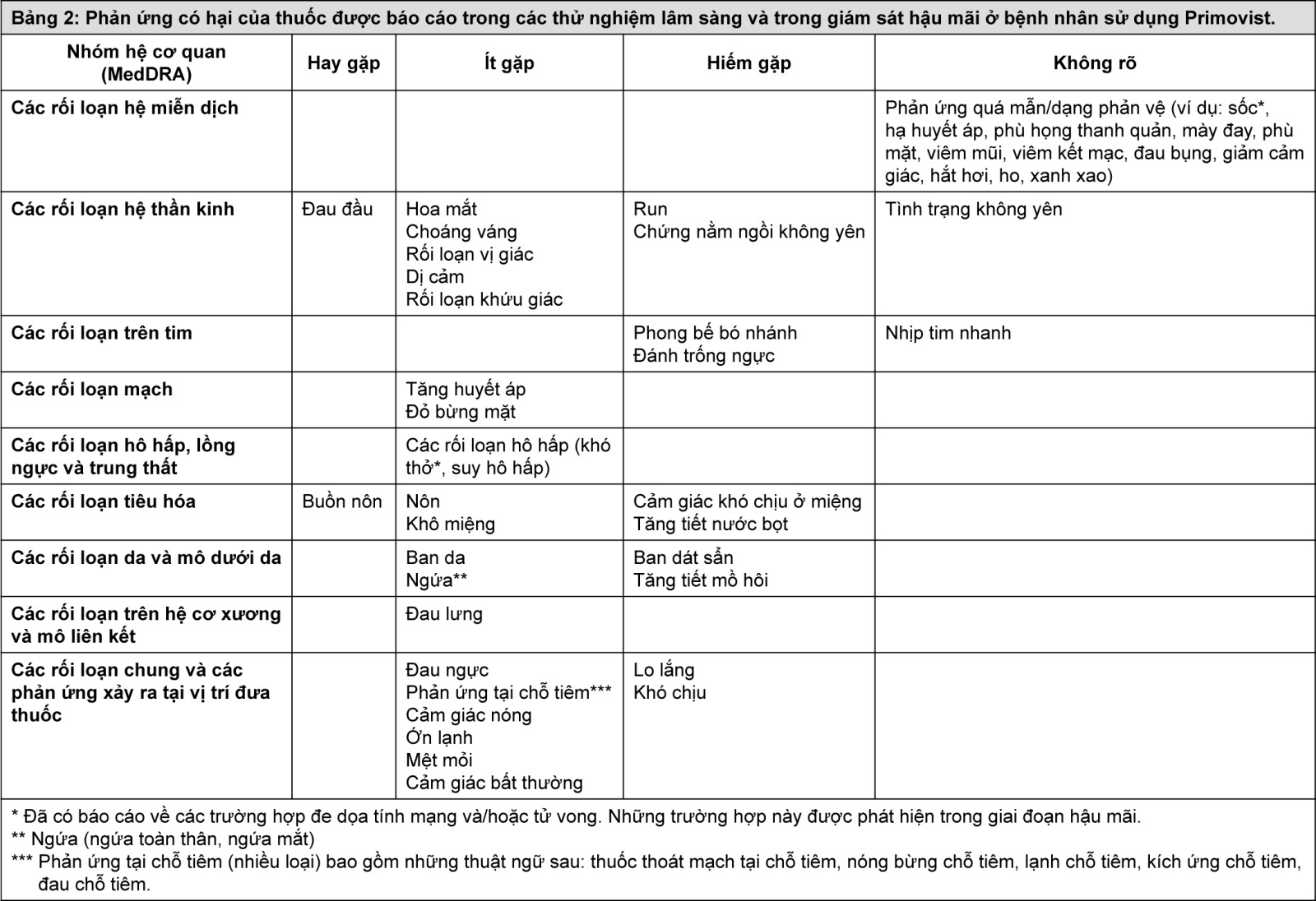
Những phản ứng có hại của Primovist được thể hiện trong bảng dưới đây. Các phản ứng này được phân loại theo nhóm hệ cơ quan. Các thuật ngữ MedDRA thích hợp nhất được sử dụng để mô tả một phản ứng nhất định và những từ đồng nghĩa và những tình trạng lâm sàng có liên quan.
Các phản ứng có hại của thuốc ghi nhận từ các thử nghiệm lâm sàng được phân loại theo tần suất xảy ra: hay gặp: ≥1/100 đến <1/10; ít gặp: ≥1/1.000 đến <1/100; hiếm gặp: ≥1/10.000 đến <1/1.000. Các phản ứng có hại chỉ được phát hiện trong giai đoạn giám sát hậu mãi nên một tần suất xảy ra mà không thể ước tính thì được xếp vào nhóm “không rõ”.
Trong mỗi nhóm phân loại theo tần suất, các tác dụng không mong muốn được sắp xếp theo thứ tự mức độ nghiêm trọng giảm dần.
- xem Bảng 2.
Mô tả một số phản ứng có hại
Đã có báo cáo về những trường hợp mắc chứng xơ hóa toàn thân do thận (NSF) khi sử dụng một số chất đối quang có chứa gadolinium (xem thêm phần Cảnh báo).
Tăng các giá trị sắt và bilirubin trong huyết thanh được báo cáo ít hơn 1% bệnh nhân sau khi truyền Primovist. Tuy nhiên, các giá trị này không tăng vượt quá 2-3 lần các giá trị lúc ban đầu và trở lại mức ban đầu trong vòng 1 đến 4 ngày.
Bảo quản
Không bảo quản thuốc trên 30oC.
Phân loại ATC
V08CA10
Trình bày/Đóng gói
Dung dịch tiêm: hộp 1 bơm tiêm chứa sẵn thuốc 10mL.
- Abacavir
- Abernil
- Abiiogran
- Acarbose
- ACC
- Acebutolol
- Acenocoumarol
- Acetate Ringer's
- Acetazolamide
- Acetylcystein
- Acetylsalicylic acid
- Aciclovir
- Acid acetylsalicylic
- Acid aminocaproic
- Acid ascorbic
- Acid boric
- Acid chenodeoxycholic
- Acid ethacrynic
- Acid folic
- Acid fusidic
- Acid iopanoic
- Acid ioxaglic
- Acid nalidixic
- Acid pantothenic
- Acid para-aminobenzoic
- Acid salicylic
- Acid tranexamic
- Acid valproic
- Acid zoledronic
- Acitretin
- Aclasta
- Aclon
- Actapulgite
- Actelsar
- Actelsar HCT
- Actemra
- Actilyse
- Acular
- Acupan
- Acuvail
- Acyclovir STADA
- Acyclovir STADA Cream
- Adalat
- Adenosin
- Adenosin Ebewe
- Adipiodon
- Advagraf
- Aerius
- Afinitor
- Agicarvir
- Agifovir-E
- Agilosart
- Agilosart-H
- Agimepzol
- Agimosarid
- Agimstan
- Agimstan-H
- Agiremid
- Agivastar
- Aibezym
- Air-X
- Alaxan
- Albendazol
- Albiomin
- Albumin
- Albumin người Grifols 20%
- Albuminar
- AlbuRx
- Albutein
- Alcuronium chloride
- Aldesleukin
- Alendronat
- Alertin
- Alfa-Lipogamma 600 Oral
- Alfuzosin hydrochlorid
- Algotra
- Alimemazin
- Alimta
- Allipem
- Allopurinol
- Allopurinol STADA
- Aloxi
- Alprazolam
- Alpha Chymotrypsin
- Alpha tocopherol
- Alphachymotrypsin Glomed
- Alphagan-P
- Aluvia
- Alzental
- Amaryl
- Ambroco
- Ambroxol
- Amcinol-Paste
- Amigold
- Amikacin
- Aminocaproic acid
- Aminoleban
- Aminoleban Oral
- Aminosteril N-Hepa
- Amiparen
- Amitriptyline
- Amiyu
- Amlodipine
- Amlor
- Amoxicillin
- Amoxicillin & clavulanate
- Ampicillin
- Amquitaz
- Anaferon for children
- Anargil
- Anaropin
- Andriol Testocaps
- Anepzil
- Anyfen
- Apaisac
- Apidra SoloStar
- Apitim 5
- Aprovel
- Aquaphil
- Arcalion
- Arcoxia
- Aricept Evess
- Arimidex
- Arnetine
- Artrodar
- A-Scabs
- Ascorbic acid
- Asperlican/Candinazol
- Aspilets EC
- Aspirin
- Asthmatin
- Atelec
- Atocib 120
- Atocib 90
- Atosiban PharmIdea
- Atozet
- Attapulgite
- Atussin
- Atropin
- Augbactam
- Augmentin Sachet
- Augmentin SR
- Augmentin Tablets
- Augmex
- Avamys
- Avastin
- Avelox Dịch truyền
- Avelox Viên nén
- Avodart
- Axcel Cefaclor-125 Suspension
- Axcel Cetirizine Syrup
- Axcel Chlorpheniramine
- Axcel Dexchlorpheniramine
- Axcel Dicyclomine-S Syrup
- Axcel Diphenhydramine Paediatric Syrup
- Axcel Erythromycin ES
- Axcel Eviline
- Axcel Fungicort Cream
- Axcel Fusidic acid Cream
- Axcel Fusidic acid-B Cream
- Axcel Hydrocortisone Cream
- Axcel Lignocaine 2% Sterile Gel
- Axcel Loratadine
- Axcel Miconazole Cream
- Axcel Paracetamol
- Axcel Urea Cream
- Axitan
- Azenmarol
- Azicine
- Aziphar
- Azithromycin