Nhà sản xuất
Hasan-Dermapharm
Thành phần
Mỗi viên: Entecavir monohydrat 0,5mg hoặc 1mg.
Trình bày/Đóng gói
Viên nén bao phim: hộp 3 vỉ x 10 viên, hộp 5 vỉ x 10 viên, hộp 10 vỉ x 10 viên.
Dược lực học
Nulesavir 0.5mg
- Entecavir là một thuốc tổng hợp tương tự nucleosid purin dẫn xuất từ guanin có hoạt tính kháng virus viêm gan B ở người (HBV). Thuốc được các enzym trong tế bào phosphoryl hóa để chuyển thành một chất chuyển hóa có hoạt tính, là entecavir triphosphat. Bằng cách cạnh tranh với cơ chất tự nhiên deoxyguanosin triphosphat, entecavir triphosphat ức chế DNA polymerase (enzym phiên mã ngược) của virus viêm gan B ở người, do đó đã ngăn chặn được mọi giai đoạn hoạt tính của enzym.
- Entecavir có hoạt tính in vitro và in vivo chống lại HBV, bao gồm cả một số chủng HBV kháng lamivudin. Thuốc cũng có tác dụng hạn chế in vitro chống một số virus ở người, bao gồm virus Herpes simplex typ 1 và 2 (HSV-1 và HSV-2), virus Varicella zoster và cytomegalovirus nhưng thuốc không chứng tỏ có hiệu quả trong lâm sàng. Entecavir có một vài tác dụng đối với HIV-1.
- Khi điều trị lâu dài ở một số bệnh nhân, một số chứng cứ cho thấy HBV chậm giảm nhạy cảm với entecavir.
- Các liệu pháp hiện có để điều trị HBV mạn tính (như entecavir, adefovir, lamivudin, telbivudin, tenofovir, interferon alfa, peginterferon alfa) chưa điều trị tiệt căn được HBV mà chỉ có tác dụng ức chế sự phát triển của virus. Do đó, quyết định thời gian thích hợp để bắt đầu điều trị phải dựa vào độ tuổi của bệnh nhân, mức độ tổn thương gan, khả năng đáp ứng với điều trị, khả năng xuất hiện chủng HBV kháng thuốc, khả năng tác dụng phụ, biến chứng và nồng độ DNA-HBV trong huyết thanh. Mục đích lâu dài của điều trị là để ngăn chặn xơ gan, suy gan và carcinom tế bào gan.
Nulesavir 1mg
Phân loại dược lý: Thuốc kháng virus dùng toàn thân, ức chế sao chép ngược nucleotid và nucleosid.
Mã ATC: J05AF10.
Cơ chế tác dụng
- Entecavir là chất tương tự nucleosid guanosin có hoạt tính kháng enzym HBV polymerase. Entecavir được phosphoryl hóa thành dạng triphosphat có hoạt tính, có chu kỳ bán hủy nội bào là 15 giờ. Bằng cách cạnh tranh với chất nền deoxyguanosin triphosphat tự nhiên, entecavir triphosphat ức chế 3 hoạt động của enzym polymerase của virus: (1) quá trình mồi của enzym HBV polymerase; (2) quá trình sao chép ngược chuỗi ADN xoắn nghịch từ ARN thông tin; (3) quá trình tổng hợp chuỗi ADN xoắn thuận của HBV. Entecavir triphosphat có hằng số ức chế (Ki) đối với ADN polymerase của HBV là 0,0012 μM. Entecavir triphosphat là một chất ức chế yếu α, β, δ ADN polymerase với giá trị Ki 18-40 μM. Ngoài ra, nồng độ cao entecavir không có tác động bất lợi đến quá trình tổng hợp enzym γ ADN polymerase hoặc ADN ti thể trong tế bào Hep G2 (một dòng tế bào ung thư gan ở người) (Ki > 160 μM).
- Hoạt tính kháng virus: Nồng độ entecavir ức chế tổng hợp ADN của HBV 50% (EC50) là 0,004 μM trên tế bào Hep G2 được lây nhiễm virus HBV ở tự nhiên. Giá trị trung bình EC50 của entecavir kháng HBV đề kháng lamivudin (LVDr) (có L180M và M240V ở enzym phiên mã ngược) là 0,026 μM. Các virus tái tổ hợp mã hóa đề kháng adefovir ở cả N236T và A181V của enzym phiên mã ngược vẫn nhạy cảm với ntecavir.
Một phân tích về tác động ức chế của entecavir chống lại các chủng HIV-1 trên lâm sàng và trong phòng thí nghiệm thực hiện trên nhiều tế bào và các điều kiện thí nghiệm khác nhau đã cho thấy giá trị EC50 của entecavir nằm trong khoảng từ 0,026 đến > 10 μM. Một số trường hợp có giá trị EC50 thấp hơn khi giảm số lượng virus. Trong nuôi cấy tế bào, entecavir tác động chọn lọc đối với sự thay thế M184I ở nồng độ μmol, xác nhận rằng nồng độ cao entecavir làm tăng khả năng ức chế. Các dòng HIV có chứa M184V giảm nhạy cảm với entecavir.
Trong các thử nghiệm kết hợp nuôi cấy HBV trong tế bào, abacavir, didanosin, lamivudin, stavudin, tenofovir hoặc zidovudin không đối kháng tác động chống HBV của entecavir ở khoảng nồng độ rộng. Trong các thử nghiệm kháng virus HIV, entecavir ở nồng độ μmol không đối kháng với tác động chống HBV của 6 chất ức chế enzym sao chép ngược nucleosid nêu trên hoặc emtricitabin.
- Kháng thuốc trong nuôi cấy tế bào: So sánh với các HBV không đột biến, virus LVDr có chứa rtM204V và rtL180M trong quá trình phiên mã ngược giảm nhạy cảm với entecavir 8 lần. Việc kết hợp các acid amin kháng entecavir (ETVr) thêm vào làm thay đổi rtT184, rtS202 hoặc rtM250, dẫn dến giảm nhạy cảm của entecavir trong nuôi cấy tế bào. Các thay đổi trong các chủng phân lập lâm sàng (T184A, C, F, G, I, L, M hoặc S; S202 C, G hoặc I và/hoặc M205 I, L hoặc V) làm giảm nhạy cảm với entecavir từ 16-741 lần so với chủng virus không đột biến. Những thay đổi ETVr trên phần còn lại của rtT184, rtS202 và rtM250 riêng lẻ tác động không nhiều đến sự nhạy cảm với entecavir và không ảnh hưởng đến sự nhạy cảm của entecavir trên những bệnh nhân không có những thay thế đề kháng lamivudin (quan sát trên 1000 bệnh nhân). Quá trình đề kháng này thực hiện gián tiếp do làm giảm liên kết của các chất ức chế với enzym phiên mã ngược đã biến đổi của HBV. Điều này làm giảm khả năng nhân đôi của virus HBV trong nuôi cấy tế bào.
Dược động học
Nulesavir 0.5mg
- Hấp thu: Entecavir hấp thu nhanh qua đường tiêu hóa sau khi uống. Sinh khả dụng của thuốc viên bằng sinh khả dụng của dung dịch uống nên hai thuốc này có thể thay thế nhau. Nồng độ đỉnh đạt được trong vòng 30-90 phút sau khi uống một liều và đạt được nồng độ ổn định sau 6-10 ngày điều trị. Ở người khỏe mạnh, khi uống liều 0,5mg, Cmax đạt khoảng 4,2 nanogam/mL; uống liều 1mg, Cmax đạt khoảng 8,2 nanogam/mL. Với một liều trong 1 ngày, thời gian bán thải trong huyết thanh khoảng 24 giờ. Thức ăn làm chậm và giảm hấp thu entercavir.
- Phân bố: Thể tích phân bố biểu kiến ước lượng vượt toàn bộ nước cơ thể, cho thấy entecavir phân bố rộng rãi trong các mô. In vitro, khoảng 13% entecavir gắn vào protein huyết tương.
- Chuyển hóa: Entecavir không bị hệ thống cytochrom P450 chuyển hóa. Một lượng nhỏ các chất liên hợp glucuronic và sulfat được tạo thành.
- Thải trừ: Entecavir đào thải chủ yếu qua thận nhờ lọc cầu thận và tiết tích cực qua ống thận. Thời gian bán thải là 128-149 giờ. Thẩm phân máu có thể loại bỏ được một phần entecavir.
Nulesavir 1mg
- Hấp thu: Entecavir được hấp thu nhanh qua đường tiêu hóa sau khi uống, nồng độ đỉnh trong huyết tương đạt được từ 0,5-1,5 giờ. Sinh khả dụng tuyệt đối chưa được xác định. Dựa trên sự bài tiết qua nước tiểu của thuốc dưới dạng không thay đổi, sinh khả dụng được ước tính ít nhất là 70%. Giá trị Cmax và AUC tăng tuyến tính với liều trong khoảng liều 0,1-1 mg. Khi dùng liều đơn, trạng thái ổn định đạt được sau 6-10 ngày với sự tích lũy gần gấp đôi. Cmax và Cmin ở trạng thái ổn định lần lượt là 4,2-0,3 ng/mL đối với liều 0,5 mg và 8,2-0,5 ng/mL đối với liều 1 mg. Dùng liều 0,5 mg entecavir cùng với bữa ăn nhiều chất béo (945 kCal; 54,6 g chất béo) hoặc ăn kiêng (379 kCal; 8,2 g chất béo) làm chậm hấp thu nhẹ entecavir, giảm Cmax 44-46%, giảm AUC 18-20%. Nồng độ Cmax và AUC thấp hơn không ảnh hưởng trên lâm sàng đến bệnh nhân chưa từng dùng thuốc nucleosid nhưng có tác động đến bệnh nhân đề kháng lamivudin.
- Phân bố: Thể tích phân bố ước tính của entecavir lớn hơn tổng lượng nước trong cơ thể. Liên kết với protein huyết tương khoảng 13% trong in vitro.
- Chuyển hóa: Entecavir không là chất nền, chất ức chế hay chất cảm ứng của hệ enzym CYP 450. Sau khi uống 1 liều entecavir-C14, không xuất hiện chất chuyển hóa oxy hóa hoặc acetyl hóa và chỉ một lượng nhỏ chất chuyển hóa pha II như liên hợp glucuronic và sulfat.
- Thải trừ: Entecavir được thải trừ chủ yếu qua thận, khoảng 75% liều dùng ở trạng thái ổn định, dưới dạng không chuyển hóa. Độ thanh thải của thận không phụ thuộc liều. Entecavir thải trừ qua cầu thận lẫn ống thận khi độ thanh thải thận 360-471 mL/phút. Sau khi đạt nồng độ đỉnh, nồng độ entecavir trong huyết tương giảm theo hàm mũ bậc 2 với thời gian bán hủy 128-149 giờ. Chỉ số tích lũy thuốc gấp khoảng 2 lần khi dùng liều đơn hàng ngày, thời gian bán hủy tích lũy của thuốc khoảng 24 giờ.
Dược động học ở một số đối tượng lâm sàng đặc biệt:
- Bệnh nhân suy gan: Các thông số dược động học ở những bệnh nhân suy gan trung bình đến nặng giống với những bệnh nhân có chức năng gan bình thường.
- Bệnh nhân suy thận: Giảm độ thanh thải creatinin dẫn đến giảm độ thanh thải entecavir. Quá trình thẩm phân máu trong 4 giờ loại bỏ khoảng 13% liều dùng, và 0,3% liều dùng được loại bỏ khi thẩm phân phúc mạc liên tục (CAPD). Thông số dược động học của bệnh nhân suy thận (không kèm viêm gan B mạn tính) khi uống liều entecavir 1 mg như sau:
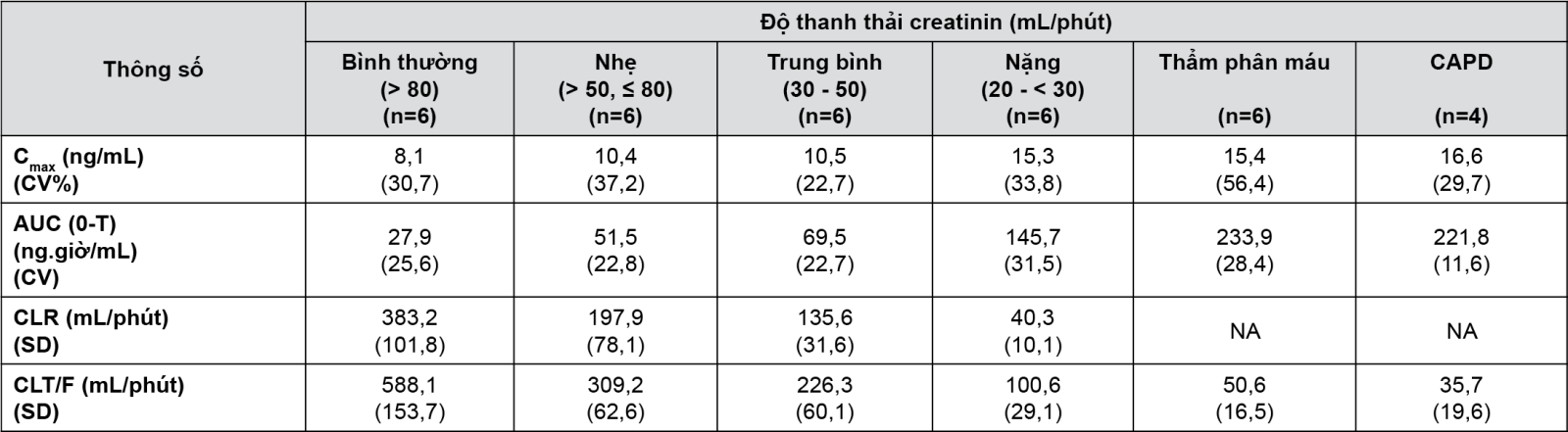
- Bệnh nhân sau ghép gan: Khi dùng phối hợp với liều cố định cyclosporin A hoặc tacrolimus, nồng độ entecavir gấp 2 lần so với bệnh nhân khỏe mạnh có chức năng thận bình thường. Chức năng thận thay đổi làm tăng nồng độ entecavir.
- Giới tính: AUC ở nữ giới cao hơn nam giới 14% do sự khác biệt về chức năng thận và cân nặng.
- Chủng tộc: Sự khác biệt chủng tộc không ảnh hưởng đáng kể đến dược động học của entecavir.
- Người cao tuổi: AUC ở người cao tuổi cao hơn người trẻ khoảng 12,5% sau khi điều chỉnh sự khác biệt về chức năng thận và cân nặng. Như vậy tuổi tác không ảnh hưởng đáng kể đến dược động học của entecavir.
- Trẻ em: Trạng thái ổn định dược động học của entecavir được nghiên cứu trên 24 trẻ em chưa từng dùng thuốc nucleosid và 19 trẻ em có HbeAg dương tính đã từng dùnglamivudin trong khoảng 2 tuổi – < 18 tuổi có bệnh gan còn bù. Khi dùng một liều duy nhất 0,015 mg/kg/ngày – 0,5 mg/ngày ở trẻ chưa từng dùng thuốc nucleosid, nồng độentecavir tương tự với người lớn khi dùng một liều 0,5 mg/ngày. Cmax, AUC(0-24) và Cmin ở những trẻ em này lần lượt là 6,31 ng/mL, 18,33 ng/mL và 0,28 ng/mL. Khi dùng một liều duy nhất entecavir từ 0,03 mg/kg/ngày đến liều tối đa 1,0 mg/ngày ở trẻ em đã dùng lamivudin, nồng độ entecavir tương tự với người lớn khi dùng liều 1,0 mg/ngày. Cmax, AUC(0-24) và Cmin ở những trẻ em này lần lượt là 14,48 ng/mL, 38,58 ng/mL và 0,47 ng/mL.
Chỉ định/Công dụng
Nulesavir 0.5mg
- Điều trị nhiễm virus viêm gan B (HBV) mạn tính ở người lớn và trẻ em ≥ 16 tuổi có chứng cứ HBV tích cực sao chép làm tăng cao DNA-HBV trong máu và tăng dai dẳng nồng độ aminotransferase huyết thanh (ALT hoặc AST) hoặc có chứng cứ mô học về bệnh gan đang hoạt động. Chỉ định này là dựa vào đáp ứng về mô học, virus học, sinh hóa, huyết thanh học ở người lớn và trẻ em ≥ 16 tuổi trước đây chưa dùng thuốc kháng virus nucleosid và ở người lớn có HBV kháng lamivudin đồng thời có HBeAg dương tính hoặc HBeAg âm tính kèm theo chức năng gan còn bù. Dùng entecavir để điều trị viêm gan B mạn tính và virus viêm gan B kháng lamivudin.
- Các dữ liệu còn hạn chế liên quan đến bệnh nhân đồng nhiễm HBV và HIV.
Nulesavir 1mg
- Người lớn: Điều trị viêm gan B mạn tính (HBV) ở người lớn có:
. Bệnh gan mất bù
. Bệnh gan còn bù có bằng chứng về sự nhân lên tích cực của virus, tăng liên tục nồng độ alanin aminotransferase huyết thanh (ALT) và các bằng chứng mô học về bệnh gan đang hoạt động và/hoặc xơ gan.
Đối với cả bệnh gan còn bù hoặc mất bù, chỉ định này được dựa trên thử nghiệm lâm sàng ở những bệnh nhân chưa từng dùng nucleosid bị nhiễm HBV dương tính hoặc không với HBeAg. Nulesavir cũng dùng điều trị viêm gan B ở bệnh nhân đã dùng lamivudin.
- Trẻ em (2 – < 18 tuổi): Điều trị viêm gan B mạn tính ở trẻ chưa dùng thuốc nucleosid, có bệnh gan còn bù, có bằng chứng về sự nhân lên tích cực của virus, tăng liên tục ALT huyết thanh, và các bằng chứng mô học về bệnh gan đang hoạt động và/hoặc xơ gan.
Liều lượng & Cách dùng
Nulesavir 0.5mg
Liều lượng:
- Người lớn và trẻ em ≥ 16 tuổi nhiễm HBV mạn tính chưa bao giờ điều trị bằng các thuốc tương tự nucleosid: 0,5 mg/lần/ngày.
- Người lớn và trẻ em ≥ 16 tuổi có tiền sử nhiễm HBV máu trong khi điều trị lamivudin hoặc có HBV được biết kháng lamivudin hoặc telbivudin: 1 mg/lần/ngày.
- Thời gian dùng thuốc tối ưu chưa biết nhưng ít nhất phải 1 năm.
- Có thể ngừng điều trị: Ở người HBeAg dương tính, phải điều trị ít nhất cho tới khi chuyển đổi huyết thanh HBe (mất HBeAg và DNA của HBV trở nên âm tính (dưới ngưỡng phát hiện), kèm theo phát hiện kháng thể kháng HBe ở 2 lần lấy máu liên tiếp cách nhau ít nhất 3 đến 6 tháng) hoặc tới khi chuyển đổi huyết thanh HBs hoặc trong trường hợp không có tác dụng sau 1 năm. Ở người HBeAg âm tính, phải điều trị ít nhất tới khi nồng độ DNA HBV âm tính (dưới ngưỡng phát hiện) và chuyển đổi huyết thanh HBs hoặc cho tới khi không thấy tác dụng. Trong trường hợp điều trị kéo dài trên 2 năm, cần phải thường xuyên đánh giá lại để xác định tiếp tục điều trị có thích hợp với bệnh nhân không.
Liều dùng đối với một số đối tượng lâm sàng đặc biệt:
- Người cao tuổi: Không cần điều chỉnh liều. Tuy nhiên, cần thận trọng do chức năng thận thường suy giảm ở người cao tuổi.
- Tổn thương gan: Không cần điều chỉnh liều.
- Suy thận: Phải điều chỉnh liều dựa vào độ thanh thải creatinin huyết thanh. Giảm liều bằng cách dùng dung dịch uống hoặc tăng khoảng cách giữa các liều. Bệnh nhân thẩm phân máu phải uống liều entecavir sau buổi thẩm phân. Liều khuyến cáo ở người chưa dùng nucleosid và người kháng lamivudin như sau:
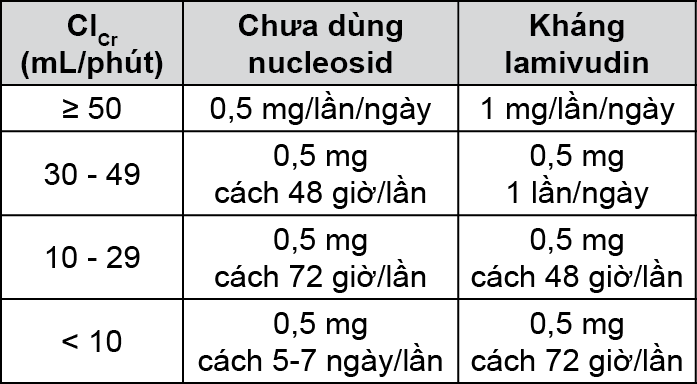
Cách dùng:
- Việc sử dụng thuốc phải do thầy thuốc chuyên khoa chỉ định và theo dõi.
- Uống thuốc vào lúc đói, ít nhất 2 giờ trước hoặc 2 giờ sau bữa ăn.
Nulesavir 1mg
Liều lượng
- Bệnh gan còn bù:
. Bệnh nhân chưa từng dùng nucleosid: Liều khuyến cáo ở người lớn là 0,5 mg/lần/ngày, kèm hoặc không kèm thức ăn.
. Bệnh nhân đã dùng lamivudin [có bằng chứng virus trong máu khi dùng lamivudin hoặc có đột biến đề kháng lamivudin (LVDr)]: Liều khuyến cáo ở người lớn là 1 mg/lần/ngày, nên uống vào lúc đói (2 giờ trước hoặc sau khi ăn). Trong trường hợp có đột biến đề kháng với lamivudin, nên dùng phối hợp entecavir với thuốc kháng virus thứ hai (không đề kháng chéo với lamivudin hoặc entecavir).
- Bệnh gan mất bù: Liều khuyến cáo cho người lớn là 1 mg/lần/ngày, dùng lúc đói (2 giờ trước hoặc sau khi ăn).
Liều lượng ở một số đối tượng lâm sàng đặc biệt:
- Bệnh nhân cao tuổi: Không cần chỉnh liều theo tuổi mà chỉnh liều theo chức năng thận.
- Bệnh nhân suy thận: Sự đào thải entecavir giảm khi độ thanh thải creatinin giảm. Cần chỉnh liều ở bệnh nhân có độ thanh thải creatinin < 50mL/phút, bao gồm bệnh nhân chạy thận nhân tạo hoặc thẩm phân phúc mạc liên tục theo khuyến cáo sau:

Chú ý: Nên uống entecavir sau khi chạy thận nhân tạo.
- Bệnh nhân suy gan: Không cần điều chỉnh liều.
- Giới tính và chủng tộc: Không cần điều chỉnh liều.
- Trẻ em: Việc quyết định điều trị với entecavir ở trẻ em phải được đánh giá cẩn thận dựa trên những bằng chứng mô học. Chỉ sử dụng thuốc khi lợi ích ức chế virus lâu dài cao hơn nguy cơ khi điều trị kéo dài, bao gồm xuất hiện đề kháng virus viêm gan B. Trẻ em có bệnh gan còn bù phải có ALT tăng liên tục ít nhất 6 tháng do viêm gan B mạn tính dương tính với HbeAg; hoặc ALT tăng liên tục ít nhất 12 tháng ở bệnh nhân trẻ em âm tính với HbeAg mới được chỉ định entecavir.
. Trẻ em có cân nặng ≥ 32,6kg: Liều khuyến cáo thông thường là 0,5 mg/lần/ngày, uống kèm hoặc không kèm thức ăn.
. Trẻ em có cân nặng < 32,6kg: Nên sử dụng dung dịch uống.
Thời gian điều trị: Thời gian điều trị tối ưu không rõ. Việc ngừng điều trị có thể được xem xét như sau:
- Người lớn hoặc trẻ em:
. Dương tính với HBeAg, nên điều trị ít nhất 12 tháng sau khi chuyển đổi huyết thanh HBe (mất HBeAg và ADN của HBV kèm theo phát hiện kháng thể kháng HBe khi xét nghiệm Hbe ở 2 lần lấy mẫu liên tiếp cách nhau ít nhất 3-6 tháng) hoặc sau khi chuyển đổi HBs hoặc trong trường hợp không có tác dụng điều trị. Ở trẻ em, nên theo dõi ALT và ADN của HBV trong huyết thanh thường xuyên sau khi ngừng điều trị.
. Âm tính với HBeAg, nên điều trị cho tới khi chuyển đổi huyết thanh HBs hoặc trường hợp không có hiệu quả điều trị. Khi điều trị kéo dài hơn 2 năm, cần đánh giá thườngxuyên để khẳng định việc tiếp tục điều trị có phù hợp với bệnh nhân hay không.
- Bệnh gan mất bù hoặc xơ gan: Không khuyến cáo ngừng điều trị.
- Trẻ em bị suy gan hoặc suy thận: Chưa được nghiên cứu.
Cách dùng: Việc sử dụng thuốc phải do bác sĩ chuyên khoa chỉ định và theo dõi. Uống thuốc chung với nước, có thể bẻ viên theo vạch ngang để chia liều nếu cần thiết.
Cảnh báo
Nulesavir 1mg
- Bệnh nhân suy thận: Chỉnh liều theo chức năng thận. Cần theo dõi chặt chẽ đáp ứng kháng virus của bệnh nhân.
- Viêm gan kịch phát: Các cơn viêm gan tự phát trầm trọng hơn ở những bệnh nhân viêm gan B mạn tính thường gặp và đặc trưng bởi sự tăng ALT huyết thanh tạm thời. Sau khi bắt đầu điều trị bằng thuốc kháng virus, ALT huyết thanh có thể tăng ở một số bệnh nhân trong khi ADN HBV giảm. Các đợt bệnh nặng ở một số bệnh nhân điều trị bằng entecavir có thời gian khởi phát từ 4-5 tuần. Ở những bệnh nhân mắc bệnh gan còn bù, ALT huyết thanh tăng thường không đi kèm với tăng bilirubin huyết thanh hoặc làm gan mất bù. Người mắc bệnh gan tiến triển hoặc xơ gan có nguy cơ cao bị gan mất bù sau khi bệnh nặng lên, do đó cần theo dõi chặt chẽ bệnh nhân trong quá trình điều trị. Một số trường hợp bệnh trở nặng do ngưng điều trị viêm gan B với entecavir. Bệnh nặng sau khi ngừng entecavir thường kết hợp với tăng nồng độ huyết thanh ADN của HBV và đa số trường hợp tự khỏi, nhưng một số trường hợp đã tử vong. Trong số những bệnh nhân chưa từng dùng nucleosid được điều trị bằng entecavir, các đợt viêm gan nặng lên có thời gian khởi phát trung bình 23-24 tuần sau khi ngừng điều trị với entecavir, và hầu hết được báo cáo ở những bệnh nhân có HBeAg âm tính. Cần theo dõi chức năng gan đều đặn thông qua xét nghiệm và lâm sàng ít nhất 6 tháng sau khi ngưng điều trị viêm gan B. Nếu cần, có thể bắt đầu điều trị lại viêm gan B.
- Bệnh gan mất bù: Những phản ứng có hại nghiêm trọng của gan (bất kể nguyên nhân) ở những bệnh nhân bị gan mất bù xảy ra với tỷ lệ cao, đặc biệt ở bệnh nhân phân loại C theo thang điểm Child-Turcotte-Pugh, khi so với những bệnh nhân có gan còn bù. Những bệnh nhân bị gan mất bù có nguy cơ cao nhiễm acid lactic và hội chứng gan thận. Cần theo dõi chặt chẽ các thông số xét nghiệm và lâm sàng ở nhóm bệnh nhân này.
- Nhiễm acid lactic và gan to nhiễm mỡ: Xuất hiện nhiễm acid lactic (không kèm theo thiếu oxy huyết) thường liên quan đến gan to và gan nhiễm mỡ khi dùng các thuốc tương tự như nucleosid (không loại trừ entecavir), đôi khi gây tử vong. Ngưng dùng các thuốc tương tự nucleosid (entecavir) khi nồng độ transaminase tăng cao, gan to tiến triển hoặc nhiễm acid lactic mà không rõ nguyên nhân. Các triệu chứng nhẹ trên hệ tiêu hóa như buồn nôn, nôn mửa và đau bụng có thể là triệu chứng nhiễm acid lactic. Các trường hợp tử vong có liên quan đến viêm tụy, suy gan/gan nhiễm mỡ, suy thận và nồng độ lactat huyết thanh cao. Cần thận trọng khi kê đơn entecavir cho những bệnh nhân bị gan to, viêm gan hoặc các yếu tố nguy cơ khác đã biết về bệnh gan (đặc biệt chú ý ở phụ nữ béo phì). Cần theo dõi chặt chẽ những bệnh nhân này.
- Sự xuất hiện đề kháng và những lưu ý đặc biệt với bệnh nhân đã dùng lamivudin: Đột biến xảy ra trên HBV polymerase (mã hóa những thay thế đề kháng lamivudin) dẫn đến bùng phát những thay thế thứ phát sau đó bao gồm cả đề kháng entecavir (ETVr). Thay thế ETVr ở phần còn lại của rtT184, rtS202 hoặc rtM250 xuất hiện trong số ít bệnh nhân đã dùng lamivudin. Bệnh nhân viêm gan đề kháng lamivudin có nguy cơ cao đề kháng entecavir. Khả năng tích lũy gen kháng entecavir trộn lẫn sau 1, 2, 3, 4 và 5 năm ở những bệnh nhân đã dùng lamivudin lần lượt là 6%, 15%, 36%, 47%, 51%. Cần theo dõi thường xuyên đáp ứng kháng virus và khả năng đề kháng ở bệnh nhân đã dùng lamivudin. Những bệnh nhân có đáp ứng kháng virus dưới mức tối ưu sau 24 tuần điều trị với entecavir nên được xem xét thay đổi điều trị. Khi bắt đầu điều trị HBV ở bệnh nhân kháng lamivudin hay bệnh nhân có bệnh gan, nên phối hợp entecavir với một thuốc kháng virus thứ 2 (không đề kháng chéo với lamivudin hoặc entecavir). Vì bệnh nhân HBV có tiền sử kháng lamivudin tăng nguy cơ đề kháng entecavir thứ phát không liên quan tới mức độ nặng của bệnh gan và bệnh nhân có bệnh gan mất bù dễ mắc phải những biến chứng bệnh gan nghiêm trọng trên lâm sàng nếu không kiểm soát được đáp ứng kháng virus.
- Trẻ em: Đáp ứng kháng virus ở trẻ em có mức nền ADN HBV ≥ 8,0 log IU/mL có tỷ lệ 10 thấp (< 50 IU/mL). Chỉ sử dụng entecavir khi lợi ích điều trị cao hơn nguy cơ (đề kháng).
- Bệnh nhân nhận ghép gan: Cần đánh giá chức năng thận trước và trong khi điều trị bằng entecavir ở những người ghép gan có dùng cyclosporin hoặc tacrolimus.
- Bệnh nhân nhiễm đồng thời viêm gan C và D: Không có dữ liệu về hiệu quả của entecavir.
- Bệnh nhân nhiễm đồng thời HIV/HBV mà không dùng đồng thời thuốc kháng virus sao chép ngược (ART): Khi điều trị bằng entecavir ở những người nhiễm HIV mà không dùng thuốc ART hoạt tính cao, xuất hiện kháng HIV. Do đó, không dùng entecavir trong trường hợp này.
- Bệnh nhân nhiễm đồng thời HIV/HBV có dùng đồng thời thuốc ART: Không có dữ liệu về hiệu quả của entecavir ở những bệnh nhân có HBeAg âm tính đồng nhiễm HIV.
- Việc điều trị bằng entecavir không làm giảm nguy cơ lây nhiễm HBV, do đó vẫn cần thực hiện các biện pháp phòng ngừa.
- Chế phẩm có chứa tá dược lactose monohydrat. Bệnh nhân có các vấn đề di truyền hiếm gặp về không dung nạp galactose, thiếu hụt men Lapp lactase hoặc kém hấp thu glucose – galactose không nên dùng thuốc này.
- Không có nghiên cứu về ảnh hưởng của entecavir đối với công việc. Tuy nhiên, chóng mặt, mệt mỏi và buồn ngủ là các triệu chứng thường gặp có thể ảnh hưởng đến khả năng lái xe và vận hành máy móc.
Quá Liều
Nulesavir 0.5mg: Dữ liệu về quá liều hiện nay còn hạn chế. Khi uống quá liều, cần theo dõi diễn biến để xử trí.
Nulesavir 1mg:
- Có ít kinh nghiệm về quá liều entecavir. Một người khỏe mạnh dùng liều lên tới 20 mg/ngày trong vòng 14 ngày, hoặc liều đơn 40 mg/ngày không xảy ra những phản ứng có hại bất ngờ. Nếu xảy ra tình trạng quá liều, bệnh nhân cần được theo dõi triệu chứng và điều trị hỗ trợ nếu cần thiết.
- Với liều entecavir 1 mg, quá trình thẩm phân máu trong 4 giờ loại bỏ khoảng 13% lượng entecavir.
Chống chỉ định
Nulesavir 0.5mg/Nulesavir 1mg: Quá mẫn với entecavir hay với bất kỳ thành phần nào của thuốc.
Nulesavir 0.5mg: Phụ nữ mang thai, phụ nữ đang cho con bú, trẻ em dưới 16 tuổi.
Sử dụng ở phụ nữ có thai và cho con bú
Nulesavir 0.5mg
Phụ nữ mang thai: Chưa có nghiên cứu nào ở phụ nữ mang thai và cũng chưa có số liệu nào về tác dụng của entecavir đối với lây truyền bệnh HBV từ mẹ sang con; con sinh ra từ mẹ nhiễm HBV thường được khuyến cáo dùng phác đồ phối hợp vắc xin HBV và globulin miễn dịch viêm gan B (HBIG).
Phụ nữ cho con bú: Chưa biết entecavir có vào sữa mẹ hay không. Ngừng cho bú hoặc ngừng thuốc tùy theo tầm quan trọng của thuốc đối với người mẹ.
Nulesavir 1mg
Phụ nữ mang thai: Các nghiên cứu trên động vật cho thấy độc tính sinh sản khi dùng liều cao entecavir. Những nguy cơ đối với con người chưa được xác định. Không nên dùng entecavir trong thai kỳ trừ khi cần thiết. Không có dữ liệu về tác dụng của entecavir đối với việc truyền HBV từ mẹ sang trẻ sơ sinh. Do đó, cần can thiệp thích hợp để ngăn ngừa nhiễm HBV sơ sinh.
Phụ nữ cho con bú: Không rõ entecavir được bài tiết qua sữa mẹ hay không. Có dữ liệu trên động vật cho thấy entecavir bài tiết qua sữa, do đó không loại trừ nguy cơ trên người. Ngưng cho trẻ bú mẹ khi dùng entecavir.
Tương tác
Nulesavir 0.5mg
- Chưa có tương tác nào cần khuyến cáo tránh dùng đồng thời với entecavir.
- Hàm lượng và tác dụng của entecavir có thể tăng bởi ganciclovir, valganciclovir, ribavirin.
- Entecavir không phải là cơ chất và không ức chế hoặc kích thích các isoenzym cytochrom P450 (CYP). Ít có khả năng tương tác về dược động với các thuốc chuyển hóa do các isoenzym CYP.
- Thuốc tác động đến thận hoặc đào thải qua thận: có khả năng tương tác dược động với các thuốc làm giảm chức năng thận hoặc cạnh tranh với entecavir để tiết tích cực qua ống thận. Nồng độ huyết thanh entecavir hoặc thuốc phối hợp có thể tăng. Cần phải theo dõi các tai biến phụ.
- Thuốc ức chế miễn dịch: có khả năng tương tác về dược động (nồng độ huyết thanh entecavir tăng vì chức năng thận bị thay đổi) với cyclosporin hoặc tacrolimus. Phải giám sát chức năng thận trước và trong khi điều trị entecavir ở người đang dùng cyclosporin, tacrolimus (ghép gan) hoặc các thuốc ức chế miễn dịch khác có thể ảnh hưởng đến chức năng thận.
Nulesavir 1mg
- Do entecavir được đào thải qua thận. Việc dùng chung với các thuốc làm giảm chức năng thận hoặc cạnh tranh đào thải qua ống thận có thể làm tăng nồng độ huyết thanh của cả hai thuốc. Ngoài lamivudin, adefovir dipivoxil và tenofovir disoproxil fumarat, việc phối hợp entecavir với các thuốc bài tiết qua thận hoặc ảnh hưởng đến chức năng thận chưa được đánh giá. Cần theo dõi chặt chẽ những tác động có hại đối với bệnh nhân khi phối hợp entecavir với các thuốc này.
- Không có tương tác dược động học giữa entecavir và lamivudin, adefovir hoặc tenofovir.
- Entecavir không là chất nền, chất ức chế hoặc chất cảm ứng CYP450. Do đó, không xảy ra tương tác thuốc qua trung gian CYP450.
- Các tương tác chỉ được nghiên cứu trên người lớn.
Tác dụng ngoại ý
Nulesavir 0.5mg
Trong thử nghiệm lâm sàng, 3% hoặc hơn số bệnh nhân được báo cáo có tác dụng không mong muốn như nhức đầu, mệt mỏi, chóng mặt, buồn nôn, tiêu chảy, khó tiêu, nôn, buồn ngủ và mất ngủ cũng đã được báo cáo.
- Thường gặp: Tiểu ra máu, tăng creatinin, glucose niệu; mất ngủ, nhức đầu, chóng mặt; nôn, tiêu chảy, buồn nôn, khó tiêu; tăng transaminase, tăng lipase, tăng amylase, tăng bilirubin huyết; mệt mỏi.
- Ít gặp: Phát ban, rụng tóc; đầy bụng, khó tiêu.
- Hiếm gặp: Phản ứng phản vệ. Một số trường hợp nhiễm toan acid lactic được báo cáo thường kết hợp với gan mất bù hoặc một bệnh nội khoa nặng khác hoặc đang dùng một thuốc khác. Dùng entecavir liên tục trung bình 96 tuần chưa thấy dung nạp thuốc thay đổi.
Các bất thường về xét nghiệm phổ biến nhất trong thử nghiệm lâm sàng entecavir là tăng ALT (lớn hơn 5 lần mức cao của bình thường: ULN), tiểu ra máu, tăng lipase (ít nhất 2,1 lần ULN), tiểu ra glucose, tăng bilirubin huyết (lớn hơn gấp 2 lần ULN), tăng ALT (lớn hơn gấp 10 lần ULN và gấp 2 lần nồng độ lúc bắt đầu điều trị trong huyết thanh), tăng glucose huyết lúc đói (trên 250 mg/dL), và tăng creatinin (ít nhất 0,5 mg/dL).
Nulesavir 1mg
Ở bệnh nhân có bệnh gan còn bù, tác dụng không mong muốn thường gặp là: đau đầu, mệt mỏi, chóng mặt và buồn nôn. Những đợt kịch phát của bệnh viêm gan đã được báo cáo khi ngưng điều trị entecavir.
Tác dụng không mong muốn được phân nhóm theo tần suất: rất thường gặp (ADR ≥ 1/10), thường gặp (1/100 ≤ ADR < 1/10), ít gặp (1/1000 ≤ ADR < 1/100), hiếm gặp (1/10000 ≤ ADR < 1/1000), rất hiếm gặp (ADR < 1/10000).
- Hệ miễn dịch: Phản ứng phản vệ (hiếm gặp).
- Tâm thần: Mất ngủ (thường gặp).
- Thần kinh: Nhức đầu, chóng mặt, buồn ngủ (thường gặp).
- Dạ dày – ruột: Nôn mửa, tiêu chảy, buồn nôn, khó tiêu (thường gặp).
- Gan – mật: Tăng transaminase (thường gặp).
- Da – mô dưới da: Phát ban, rụng tóc (ít gặp).
- Các rối loạn thông thường: Mệt mỏi (thường gặp).
Nhiễm acid lactic cũng được báo cáo ở những bệnh nhân có bệnh gan mất bù hoặc bệnh nội khoa nặng khác hoặc đang dùng một số thuốc khác.
Điều trị với entecavir liên tục trong thời gian trung bình 96 tuần chưa được chứng minh an toàn.
Thận trọng
Nulesavir 0.5mg
- Viêm gan tự phát trở thành trầm trọng hay xảy ra và thường biểu hiện bằng tăng nhất thời nồng độ huyết thanh ALAT. Sau khi bắt đầu điều trị kháng virus, nồng độ huyết thanh ALAT có thể tăng ở bệnh nhân trong khi nồng độ DNA-HBV huyết thanh giảm. Trong số các bệnh nhân điều trị bằng entecavir, các đợt bệnh nặng lên xuất hiện trung bình 4-5 tuần sau khi bắt đầu điều trị. Ở bệnh nhân có bệnh gan còn bù, nồng độ huyết thanh ALAT tăng thường không kèm theo tăng bilirubin huyết như bệnh gan mất bù. Nếu bệnh nhân đã có xơ gan, có nguy cơ cao gan mất bù sau khi bệnh nặng lên. Do đó, trong khi điều trị, phải theo dõi chặt chẽ bệnh nhân về lâm sàng và sinh hóa.
- Một số trường hợp bệnh nặng lên do ngừng điều trị chống viêm gan B bằng entecavir đã được báo cáo. Bệnh nặng lên sau khi ngừng entecavir thường kết hợp với tăng nồng độ huyết thanh DNA-HBV và đa số trường hợp tự khỏi, nhưng một số trường hợp đã tử vong. Trong số những bệnh nhân trước đây chưa dùng thuốc tương tự nucleosid nay được điều trị bằng entecavir, các trường hợp nặng lên xuất hiện trung bình 23-24 tuần sau khi ngừng điều trị. Phần lớn các trường hợp xảy ra ở người có HbeAg âm tính. Phải theo dõi gan đều đặn cả về lâm sàng và sinh hóa ít nhất 6 tháng sau khi ngừng điều trị. Nếu tăng DNA-HBV hoặc nếu cần, cho điều trị lại 1 đợt khác.
- Thận trọng khi điều trị cho bệnh nhân có gan mất bù vì nhiều tai biến phụ, có nguy cơ cao bị nhiễm toan acid lactic.
- Thận trọng khi điều trị entecavir cho bệnh nhân nhiễm HBV mạn tính mà không phát hiện người đó cũng nhiễm HIV vì có nguy cơ làm xuất hiện các chủng HIV kháng các thuốc nucleosid ức chế enzym phiên mã ngược (NRTI). Trước khi bắt đầu điều trị entecavir, phải làm test HIV. Do có thể có nguy cơ làm xuất hiện HIV kháng NRTI nên không dùng entecavir để điều trị nhiễm HBV mạn tính ở bệnh nhân nhiễm HIV.
- Phải thận trọng khi dùng entecavir để điều trị viêm gan B mạn tính vì có thể gây ra nhiễm toan acid lactic, gan to nhiều kèm nhiễm mỡ gan ở bệnh nhân dùng duy nhất các thuốc tương tự nucleosid hoặc phối hợp với các thuốc kháng virus khác. Đa số các trường hợp xảy ra ở phụ nữ; béo phì và điều trị lâu dài bằng các thuốc nucleosid ức chế enzym phiên mã ngược cũng có thể là yếu tố nguy cơ. Phải dùng thận trọng các thuốc tương tự nucleosid cho người được biết có nguy cơ cao về bệnh gan, nhưng nhiễm toan acid lactic, gan to nhiều và nhiễm mỡ cũng đã xảy ra ở người không có nguy cơ nào. Ngừng ngay entecavir ở bất cứ bệnh nhân nào có dấu hiệu lâm sàng và xét nghiệm gợi ý nhiễm toan lactic hoặc nhiễm độc gan nặng ngay cả khi transaminase không tăng.
- Chưa biết về độ an toàn và hiệu quả của entecavir đối với người ghép gan. Nếu phải dùng entecavir cho người ghép gan đã hoặc đang dùng một thuốc ức chế miễn dịch có thể tác động đến chức năng thận như cyclosporin, tacrolimus, phải giám sát cẩn thận chức năng thận trước và trong khi điều trị entecavir.
- Đối với người cao tuổi từ 65 tuổi trở lên, kinh nghiệm còn ít chưa đủ để xác định xem đáp ứng có khác với người trẻ tuổi không. Do entecavir chủ yếu đào thải qua thận nên nguy cơ nhiễm độc do entecavir có thể tăng ở người suy thận. Người cao tuổi thường có chức năng thận suy giảm, cần điều chỉnh liều theo mức độ suy thận và phải theo dõi chức năng thận.
- Điều chỉnh liều được khuyến cáo đối với bệnh nhân có ClCr < 50 mL/phút, bao gồm cả thẩm phân máu hoặc thẩm phân màng bụng ngoại trú.
- Entecavir không làm giảm nguy cơ lây truyền virus sang người khác nên các biện pháp dự phòng truyền bệnh phải được thực hiện.
- Thuốc có thể gây nhức đầu, mệt mỏi, chóng mặt, buồn ngủ, cần thận trọng khi vận hành tàu xe, máy móc.
Bảo quản
Nơi khô, dưới 30oC. Tránh ánh sáng
Phân loại ATC
J05AF10
- Abacavir
- Abernil
- Abiiogran
- Acarbose
- ACC
- Acebutolol
- Acenocoumarol
- Acetate Ringer's
- Acetazolamide
- Acetylcystein
- Acetylsalicylic acid
- Aciclovir
- Acid acetylsalicylic
- Acid aminocaproic
- Acid ascorbic
- Acid boric
- Acid chenodeoxycholic
- Acid ethacrynic
- Acid folic
- Acid fusidic
- Acid iopanoic
- Acid ioxaglic
- Acid nalidixic
- Acid pantothenic
- Acid para-aminobenzoic
- Acid salicylic
- Acid tranexamic
- Acid valproic
- Acid zoledronic
- Acitretin
- Aclasta
- Aclon
- Actapulgite
- Actelsar
- Actelsar HCT
- Actemra
- Actilyse
- Acular
- Acupan
- Acuvail
- Acyclovir STADA
- Acyclovir STADA Cream
- Adalat
- Adenosin
- Adenosin Ebewe
- Adipiodon
- Advagraf
- Aerius
- Afinitor
- Agicarvir
- Agifovir-E
- Agilosart
- Agilosart-H
- Agimepzol
- Agimosarid
- Agimstan
- Agimstan-H
- Agiremid
- Agivastar
- Aibezym
- Air-X
- Alaxan
- Albendazol
- Albiomin
- Albumin
- Albumin người Grifols 20%
- Albuminar
- AlbuRx
- Albutein
- Alcuronium chloride
- Aldesleukin
- Alendronat
- Alertin
- Alfa-Lipogamma 600 Oral
- Alfuzosin hydrochlorid
- Algotra
- Alimemazin
- Alimta
- Allipem
- Allopurinol
- Allopurinol STADA
- Aloxi
- Alprazolam
- Alpha Chymotrypsin
- Alpha tocopherol
- Alphachymotrypsin Glomed
- Alphagan-P
- Aluvia
- Alzental
- Amaryl
- Ambroco
- Ambroxol
- Amcinol-Paste
- Amigold
- Amikacin
- Aminocaproic acid
- Aminoleban
- Aminoleban Oral
- Aminosteril N-Hepa
- Amiparen
- Amitriptyline
- Amiyu
- Amlodipine
- Amlor
- Amoxicillin
- Amoxicillin & clavulanate
- Ampicillin
- Amquitaz
- Anaferon for children
- Anargil
- Anaropin
- Andriol Testocaps
- Anepzil
- Anyfen
- Apaisac
- Apidra SoloStar
- Apitim 5
- Aprovel
- Aquaphil
- Arcalion
- Arcoxia
- Aricept Evess
- Arimidex
- Arnetine
- Artrodar
- A-Scabs
- Ascorbic acid
- Asperlican/Candinazol
- Aspilets EC
- Aspirin
- Asthmatin
- Atelec
- Atocib 120
- Atocib 90
- Atosiban PharmIdea
- Atozet
- Attapulgite
- Atussin
- Atropin
- Augbactam
- Augmentin Sachet
- Augmentin SR
- Augmentin Tablets
- Augmex
- Avamys
- Avastin
- Avelox Dịch truyền
- Avelox Viên nén
- Avodart
- Axcel Cefaclor-125 Suspension
- Axcel Cetirizine Syrup
- Axcel Chlorpheniramine
- Axcel Dexchlorpheniramine
- Axcel Dicyclomine-S Syrup
- Axcel Diphenhydramine Paediatric Syrup
- Axcel Erythromycin ES
- Axcel Eviline
- Axcel Fungicort Cream
- Axcel Fusidic acid Cream
- Axcel Fusidic acid-B Cream
- Axcel Hydrocortisone Cream
- Axcel Lignocaine 2% Sterile Gel
- Axcel Loratadine
- Axcel Miconazole Cream
- Axcel Paracetamol
- Axcel Urea Cream
- Axitan
- Azenmarol
- Azicine
- Aziphar
- Azithromycin





