Ung thư vú
Ung thư biểu mô ống tuyến vú hoặc tiểu thùy
- Ung thư vú tại chỗ và xâm lấn
- Các loại ung thư vú xâm lấn đặc biệt
Các loại ung thư vú ít phổ biến hơn
Các yếu tố nguy cơ và phòng ngừa ung thư vú
Phát hiện và chẩn đoán sớm ung thư vú
Khuyến nghị của Hiệp hội Ung thư Hoa Kỳ để phát hiện sớm ung thư vú
Các xét nghiệm hình ảnh để chẩn đoán ung thư vú
- Xét nghiệm chẩn đoán hình ảnh khác
Các dấu hiệu và triệu chứng của ung thư vú
Phát hiện ung thư vú trong thời kỳ mang thai
Các thuật ngữ quan trọng trong chẩn đoán ung thư vú
Bộ nhiễm sắc thể và tăng sinh tế bào ung thư vú
Tình trạng thụ thể hormone của tế bào ung thư vú
Tình trạng protein HER2 của tế bào ung thư vú
Xét nghiệm biểu hiện gen ung thư vú
Các phương pháp điều trị phổ biến
- Điều trị ung thư vú theo giai đoạn
- Điều trị ung thư vú bộ ba âm tính
- Điều trị ung thư vú dạng viêm
- Điều trị ung thư vú trong thời kỳ mang thai
---------------------------------
TỔNG QUAN VỀ UNG THƯ VÚ
1. Ung thư vú là bệnh gì?
Ung thư vú là loại ung thư bắt đầu ở vú, có thể một hoặc cả hai bên vú.
Ung thư bắt đầu khi các tế bào phát triển ngoài tầm kiểm soát. (Để tìm hiểu thêm về cách ung thư khởi phát và xâm lấn hay di căn, hãy xem Ung thư)
Ung thư vú hầu như chỉ xãy ra ở phụ nữ, nhưng nam giới cũng có thể bị ung thư vú.
Phần lớn các khối u ở vú đều lành tính chứ không phải ung thư (ác tính). Các khối u lành tính ở vú là sự phát triển bất thường nhưng chỉ khu trú tại vú và xâm lấn ra những nơi khác ngoài vú và không đe dọa tính mạng, nhưng cũng có loại u vú lành tính có thể làm tăng nguy cơ bị ung thư vú ở phụ nữ. Do đó, khi có bất kỳ khối u hoặc thay đổi nào ở vú thì cần đến cơ sở y tế để được thăm khám xem là lành tính hay ác tính và liệu nó có thể ảnh hưởng đến nguy cơ ung thư trong tương lai hay không.
Ung thư vú bắt đầu từ đâu?
Ung thư vú có thể bắt đầu từ nhiều cấu trúc khác nhau bên trong vú. Vú là cơ quan nằm phía trước các xương sườn và cơ ngực. Mỗi vú được cấu tạo chủ yếu bởi các tuyến, ống tuyến vú và mô mỡ. Ở phụ nữ, vú tạo sữa để nuôi trẻ sơ sinh và trẻ nhỏ. Lượng mô mỡ ở vú quyết định kích thước của mỗi vú.
Vú có nhiều cấu trúc khác nhau:
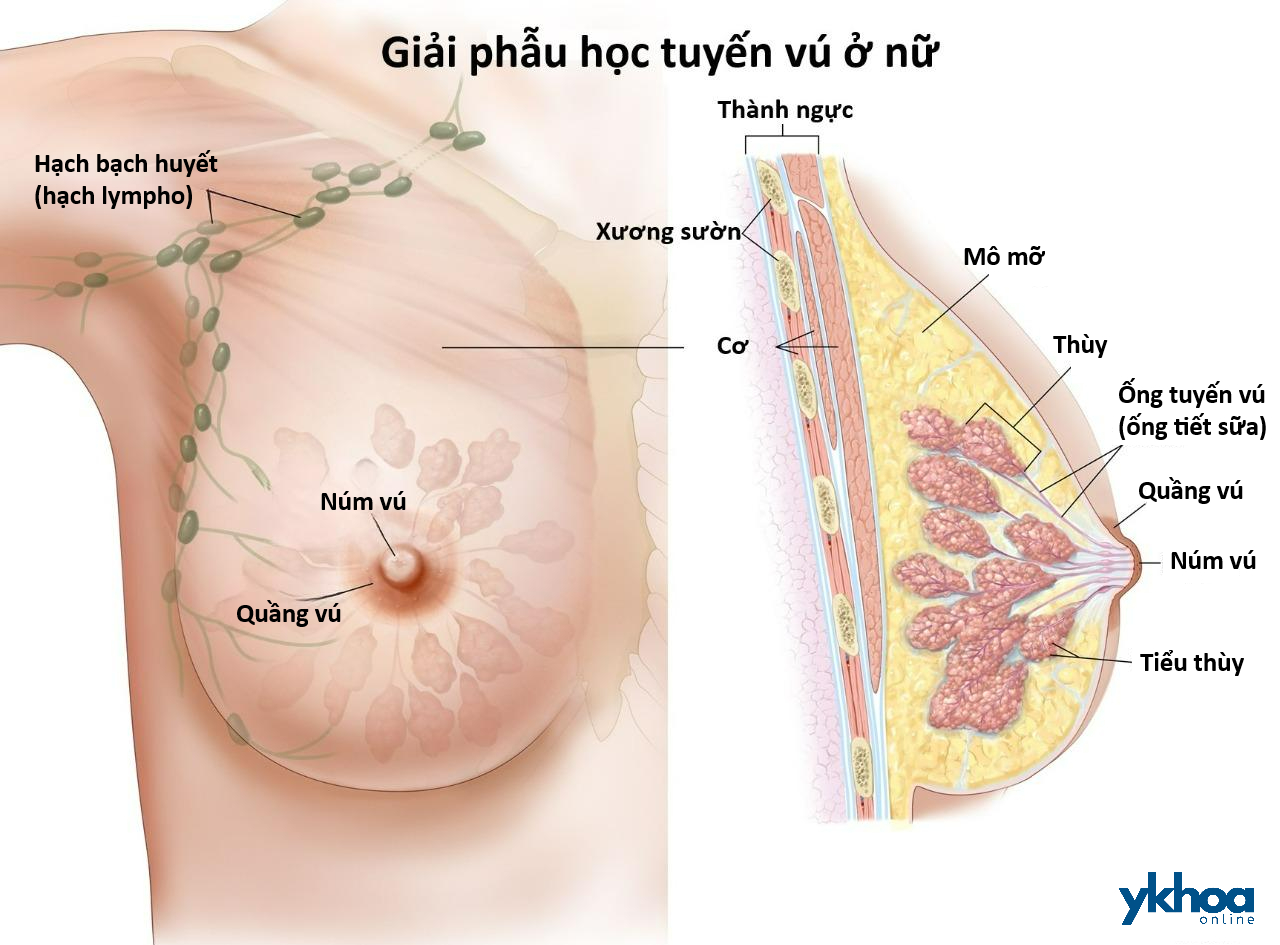
Cấu trúc mô tuyến vú. Ảnh: cancer.org
- Tiểu thùy là các tuyến ở vú tạo ra sữa mẹ. Ung thư bắt đầu từ đây được gọi là ung thư tiểu thùy.
- Ống tuyến vú là những ống nhỏ từ các tiểu thùy dẫn sữa đến núm vú (đôi khi còn được gọi là ống dẫn sữa hay ống tiết sữa). Ống tuyến vú là nơi khởi phát ung thư vú phổ biến nhất. Ung thư bắt đầu ở đây được gọi là ung thư ống tuyến vú.
- Núm vú là những lỗ hở trên da vú, nơi các ống tuyến vú kết hợp với nhau tạo thành các ống lớn hơn để dẫn sữa ra ngoài. Núm vú được bao quanh bởi lớp da dày hơn một chút gọi là quầng vú. Một loại ung thư vú ít phổ biến hơn gọi là bệnh Paget vú có thể bắt đầu ở núm vú.
- Chất béo và mô liên kết (chất đệm) bao quanh các ống tuyến vú và tiểu thùy và giúp giữ chúng đúng vị trí. Ung thư vú có thể bắt đầu ở mô đệm nhưng ít gặp hơn.
- Mạch máu và mạch bạch huyết cũng hiện diện trong vú. Angiosarcoma là một loại ung thư vú ít phổ biến hơn, có thể bắt đầu ở niêm mạc của các mạch máu này. Hệ thống bạch huyết được mô tả ở hình dưới đây.
Ung thư vú lan rộng như thế nào?
Ung thư vú có thể lan rộng khi các tế bào ung thư xâm nhập vào máu hoặc hệ bạch huyết và sau đó đến các bộ phận khác của cơ thể.
Hệ bạch huyết là một phần của hệ miễn dịch trong cơ thể. Đó là một mạng lưới các hạch bạch huyết (kích thước cỡ hạt đậu), mạch bạch huyết và các cơ quan phối hợp với nhau để thu thập và vận chuyển bạch huyết trong suốt qua các mô của cơ thể rồi đến máu. Dịch bạch huyết trong suốt bên trong mạch bạch huyết chứa các sản phẩm của mô, chất thải và các tế bào của hệ miễn dịch.
Các mạch bạch huyết mang dịch bạch huyết ra khỏi vú. Trong ung thư vú, tế bào ung thư có thể xâm lấn vào các mạch bạch huyết và bắt đầu phát triển trong các hạch bạch huyết. Hầu hết các mạch bạch huyết của vú chảy vào:
- Hạch bạch huyết dưới cánh tay (hạch nách)
- Các hạch bạch huyết bên trong ngực gần xương ức (hạch cạnh ức)
- Các hạch bạch huyết xung quanh xương đòn gồm hạch thượng đòn (phía trên xương đòn) và các hạch hạ đòn (phía dưới xương đòn)
Nếu tế bào ung thư đã xâm nhập hạch bạch huyết thì nhiều khả năng các tế bào đó đã di chuyển qua hệ thống bạch huyết và di căn (lan rộng) sang các bộ phận khác trong cơ thể. Tuy nhiên, không phải tất cả trường hợp có tế bào ung thư trong hạch bạch huyết đều bị di căn và ngược lại, không có tế bào ung thư trong hạch bạch huyết cũng có thể bị di căn sau này.
2. Nguyên nhân gây ung thư vú
Nguyên nhân gây ung thư vú chưa được biết rõ, nhưng có nhiều yếu tố nguy cơ gây ung thư vú đã được xác định. Ví dụ, các yếu tố nguy cơ liên quan đến lối sống, nội tiết tố… cũng có liên quan trong nhiều trường hợp ung thư vú.
Các tế bào vú bình thường có thể trở thành tế bào ung thư do những biến đổi hoặc đột biến gen. Nhưng chỉ có khoảng 1/10 bệnh ung thư vú (10%) có liên quan đến các gen đột biến đã biết được truyền từ cha mẹ (di truyền). Nhiều gen vẫn chưa được phát hiện, vì vậy những phụ nữ có tiền sử gia đình mắc bệnh ung thư vú có thể đã thừa hưởng gen bất thường. Nhưng đa số trường hợp ung thư vú (khoảng 90%) bắt nguồn từ những biến đổi gen mắc phải (không phải di truyền) vẫn chưa được xác định.
Đột biến gen di truyền
Một số gen đột biến được truyền từ cha mẹ sang. Có nghĩa là các đột biến đều hiện diện trong tất cả các tế bào của trẻ sơ sinh.
Một số loại đột biến gen di truyền có thể làm tăng đáng kể nguy cơ ung thư. Ví dụ các gen BRCA (BReast CAncer) như BRCA1 và BRCA2 là những gen ức chế khối u. Khi một trong những gen này bị đột biến thì nó không còn khả năng ngăn chặn sự phát triển của tế bào bất thường và ung thư có nhiều khả năng xuất hiện hơn.
Xét nghiệm di truyền có thể xác định một số phụ nữ có đột biến di truyền ở gen ức chế khối u BRCA1 hoặc BRCA2 cũng như các gen ít phổ biến khác như PALB2, ATM hoặc CHEK2. Những phụ nữ mang gen đột biến này cần được theo dõi và thực hiện những bước tầm soát phù hợp theo các khuyến nghị để giúp phát hiện ung thư ở giai đoạn sớm hơn, dễ điều trị hơn. Do những dạng đột biến này cũng thường liên quan đến ung thư ở các cơ quan khác (ngoài vú), nên những phụ nữ mang những đột biến này cũng có thể cân nhắc tầm soát sớm và thực hiện các biện pháp phòng ngừa đối với các bệnh ung thư ở cơ quan khác.
Đột biến gen mắc phải
Hầu hết các đột biến gen liên quan đến ung thư vú đều mắc phải. Có nghĩa là đột biến xãy ra ở tế bào vú tại một thời điểm nào đó trong đời, chứ không phải do di truyền từ cha mẹ.
Đột biến mắc phải của gen gây ung thư và/hoặc gen ức chế khối u có thể là hậu quả của các yếu tố khác, như tia xạ hoặc hóa chất gây ung thư. Nhưng đột biến gen cũng có thể chỉ là những sự kiện ngẫu nhiên xảy ra bên trong tế bào mà không có nguyên nhân bên ngoài. Cho đến nay, nguyên nhân của hầu hết các đột biến mắc phải có thể dẫn đến ung thư vú vẫn chưa được biết rõ. Hầu hết các bệnh ung thư vú đều có một số đột biến gen mắc phải.
CÁC LOẠI UNG THƯ VÚ
Ung thư vú được phân loại dựa vào loại tế bào ở vú phát triển thành ung thư.
1. Ung thư biểu mô ống tuyến vú hoặc tiểu thùy
Hầu hết ung thư vú là ung thư biểu mô (carcinoma), nghĩa là những khối u bắt nguồn từ các tế bào biểu mô lót bên trong các mô cơ quan của cơ thể. Ung thư vú còn được gọi cụ thể hơn là ung thư biểu mô tuyến (adenocarcinoma) do ung thư bắt nguồn từ các tế bào trong ống tuyến vú hoặc tiểu thùy (là những tuyến tạo ra sữa ở vú).
1.1. Ung thư vú tại chỗ và xâm lấn
Khi đề cập đến ung thư vú, bác sĩ thường đánh giá xem ung thư chỉ tại chỗ hay đã xâm lấn, di căn đến nơi khác.
1.1.1. Ung thư vú tại chỗ: Ung thư biểu mô ống tuyến vú tại chỗ (Ductal carcinoma in situ - DCIS) là loại tiền ung thư, bắt đầu từ các tế bào biểu mô trong ống tuyến vú và chưa xâm lấn vào những cấu trúc khác của mô vú.
Ung thư biểu mô ống tuyến vú tại chỗ (DCIS)
Khoảng 1/5 trường hợp ung thư vú mới thuộc loại ung thư biểu mô ống tuyến vú tại chỗ. Gần như tất cả trường hợp ung thư vú giai đoạn đầu này đều có thể được chữa dứt.
Ung thư biểu mô ống tuyến vú tại chỗ còn được gọi là ung thư vú giai đoạn 0. Đây là loại ung thư vú không xâm lấn hoặc tiền xâm lấn, có nghĩa là các tế bào lót trong lòng các ống tuyến vú đã bị biến đổi thành tế bào ung thư nhưng chúng chưa xâm lấn qua thành ống tuyến vú để vào mô vú xung quanh.
Ung thư biểu mô ống tuyến vú tại chỗ chưa xâm lấn vào các mô vú xung quanh nên nó không thể di căn ra ngoài vú đến các bộ phận khác của cơ thể. Tuy nhiên, theo thời gian nó có thể diễn tiến thành dạng ung thư xâm lấn. Khi đó, ung thư không còn khu trú bên trong ống tuyến vú mà sẽ xâm lấn vào các mô lân cận và từ đó di căn đến các nơi khác trong cơ thể.
Không thể biết chắc chắn trường hợp nào sẽ trở thành hay không trở thành ung thư xâm lấn, do đó gần như tất cả trường hợp ung thư biểu mô ống tuyến vú tại chỗ cần được điều trị.
1.1.2. Ung thư vú xâm lấn
Các tế bào ung thư đã lan sang mô vú xung quanh được gọi là ung thư vú xâm lấn.
Hầu hết các trường hợp ung thư vú đều xâm lấn, nhưng có nhiều loại ung thư vú xâm lấn khác nhau. Hai loại phổ biến nhất là ung thư biểu mô ống tuyến vú xâm lấn và ung thư biểu mô tiểu thùy vú xâm lấn.
Ung thư biểu mô ống tuyến vú xâm lấn (Invasive ductal carcinoma - IDC)
Đây là loại ung thư vú phổ biến nhất. Khoảng 8/10 trường hợp ung thư vú xâm lấn là loại ung thư biểu mô ống tuyến vú xâm lấn.
Ung thư biểu mô ống tuyến vú xâm lấn bắt đầu từ các tế bào biểu mô lót trong lòng ống tuyến vú. Từ đó, xuyên qua thành ống và xâm lấn vào các mô vú lân cận. Ngoài ra, tế bào ung thư có thể xâm nhập vào máu và hệ bạch huyết để di căn sang các cơ quan khác trong cơ thể.
Ung thư biểu mô tiểu thùy xâm lấn (Invasive lobular carcinoma - ILC)
Khoảng 1/10 ca ung thư vú xâm lấn là loại ung thư biểu mô tiểu thùy xâm lấn. Ung thư bắt đầu ở tế bào biểu mô trong tuyến vú tạo ra sữa (tiểu thùy), và cũng có thể xâm lấn và di căn sang các nơi khác trong cơ thể. Ung thư biểu mô tiểu thùy xâm lấn thường khó phát hiện hơn ung thư biểu mô ống tuyến vú xâm lấn khi khám thực thể và chụp nhũ ảnh. Ngoài ra, ung thư biểu mô tiểu thùy xâm lấn có nhiều khả năng ảnh hưởng đến cả hai vú hơn so với các loại ung thư biểu mô xâm lấn khác. Khoảng 1/5 phụ nữ bị ung thư biểu mô tiểu thùy xâm lấn có thể bị ung thư ở cả hai vú vào thời điểm được chẩn đoán.
Các loại ung thư vú xâm lấn ít phổ biến hơn
Các loại ung thư này ít phổ biến và mỗi loại thường chiếm < 5% trong tổng số các trường hợp ung thư vú. Một số loại có tiên lượng tốt hơn ung thư biểu mô ống tuyến vú xâm lấn như:
- Ung thư biểu mô nang dạng tuyến
- Ung thư biểu mô tuyến tế bào vảy cấp độ thấp (đây là một loại ung thư biểu mô dị sản)
- Ung thư biểu mô tủy
- Ung thư biểu mô nhầy
- Ung thư biểu mô tế bào gai (tế bào nhú)
- Ung thư biểu mô tiểu ống
Một số loại phụ có tiên lượng tương tự hoặc có thể xấu hơn ung thư biểu mô ống tuyến vú xâm lấn, như:
- Ung thư biểu mô dị sản (hầu hết các loại, ngoại trừ ung thư biểu mô tuyến tế bào vảy cấp độ thấp)
- Ung thư biểu mô vi nhú
- Ung thư biểu mô hỗn hợp (có đặc điểm của cả hai thể ung thư ống tuyến vú xâm lấn và thể tiểu thùy xâm lấn)
Nhìn chung, tất cả các loại ung thư này vẫn được điều trị như ung thư biểu mô ống tuyến vú xâm lấn.
1.2. Các loại ung thư vú xâm lấn đặc biệt
Một số bệnh ung thư vú xâm lấn có những điểm đặc biệt hoặc phát triển theo những cách khác nhau ảnh hưởng đến điều trị và tiên lượng bệnh. Những loại ung thư này ít phổ biến hơn nhưng có thể nặng hơn các loại ung thư vú khác.
1.2.1. Ung thư vú bộ ba âm tính (Triple-negative breast cancer - TNBC)
Chiếm khoảng 10-15% trường hợp ung thư vú. Đây là loại ung thư vú mà các tế bào ung thư không có thụ thể estrogen, không có thụ thể progesterone và cũng không tạo ra protein có tên là HER2 (thụ thể yếu tố tăng trưởng biểu bì 2 ở người). Do cả ba xét nghiệm trên đều âm tính nên gọi là Ung thư vú bộ ba âm tính. Loại ung thư vú này phổ biến hơn ở phụ nữ dưới 40 tuổi, người da đen hoặc những người có đột biến BRCA1.
Ung thư vú bộ ba âm tính có thể có các dấu hiệu và triệu chứng giống như các loại ung thư vú phổ biến khác. Tuy nhiên nó khác với các loại ung thư vú xâm lấn khác là có xu hướng phát triển và xâm lấn nhanh hơn, có ít lựa chọn điều trị hơn và thường có tiên lượng xấu hơn.
Chẩn đoán ung thư vú bộ ba âm tính: Sau khi ung thư vú được chẩn đoán bằng xét nghiệm hình ảnh và sinh thiết, các tế bào ung thư sẽ được kiểm tra một số protein nhất định. Nếu các tế bào không có thụ thể estrogen hoặc progesterone, đồng thời không tạo ra protein HER2, thì ung thư đó được chẩn đoán là ung thư vú bộ ba âm tính.
1.2.2. Ung thư vú dạng viêm (Inflammatory breast cancer - IBC)
Loại này rất hiếm và chỉ chiếm từ 1% đến 5% trong số tất cả các trường hợp ung thư vú. Mặc dù thuộc loại ung thư biểu mô ống tuyến vú xâm lấn nhưng các triệu chứng, tiên lượng và cách điều trị của nó lại khác. Trong ung thư vú dạng viêm, các tế bào ung thư làm tắc nghẽn các mạch bạch huyết gây ra các triệu chứng viêm vú như sưng và đỏ.
Ung thư vú dạng viêm khác với các loại ung thư vú khác ở nhiều điểm:
- Không giống một bệnh ung thư vú điển hình vì thường không có khối u ở vú và có thể không hiển thị trên ảnh chụp X quang tuyến vú, làm cho việc chẩn đoán khó khăn hơn.
- Thường gặp ở phụ nữ trẻ (dưới 40 tuổi).
- Phụ nữ da đen thường bị nhiều hơn phụ nữ da trắng.
- Phổ biến hơn ở những phụ nữ thừa cân hoặc béo phì.
- Có xu hướng phát triển và xâm lấn nhanh hơn nhiều so với các loại ung thư vú phổ biến.
- Khi được chẩn đoán lần đầu thì bệnh có thể vào giai đoạn III vì các tế bào ung thư đã vào các mạch bạch huyết, làm tắc nghẽn và gây triệu chứng giống như vú bị viêm.
Khoảng 1/3 trường hợp khi được chẩn đoán thì ung thư đã di căn xa đến các cơ quan khác trong cơ thể, khiến việc điều trị trở nên khó khăn hơn.
Loại ung thư này thường có tiên lượng xấu hơn so với các loại ung thư vú phổ biến khác.
Dấu hiệu và triệu chứng của ung thư vú dạng viêm
Dấu hiệu và triệu chứng thường phát triển nhanh chóng (trong vòng 3 đến 6 tháng), bao gồm:
- Sưng và đỏ ở vú
- Da vú bị rỗ hoặc dày giống như vỏ cam
- Núm vú thụt vào trong
- Một bên vú trông to hơn bên kia vì sưng
- Một bên vú có cảm giác nóng hơn và nặng hơn bên kia
- Vú có thể mềm, đau hoặc ngứa
- Sưng to hạch bạch huyết dưới cánh tay (hạch nách) hoặc các hạch gần xương đòn
Nếu có bất kỳ triệu chứng nào trên đây thì không có nghĩa là bị ung thư dạng viêm. Bệnh nhân nên đi đến cơ sở y tế để được thăm khám ngay. Sưng, nóng, đỏ, đau cũng là những triệu chứng phổ biến của nhiễm trùng hoặc viêm vú, chẳng hạn như viêm vú khi đang mang thai hoặc cho con bú. Vì những tình trạng này phổ biến hơn nhiều so với ung thư vú dạng viêm, nên ban đầu bác sĩ có thể nghi ngờ nhiễm trùng là nguyên nhân và điều trị bằng kháng sinh.
Nếu các triệu chứng không thuyên giảm sau 7 đến 10 ngày dùng kháng sinh thì cần phải làm xét nghiệm để tìm ung thư. Khả năng bị ung thư vú dạng viêm nên được đánh giá kỹ lưỡng hơn nếu những triệu chứng này xuất hiện ở những phụ nữ không đang mang thai, cho con bú hay đã qua thời kỳ mãn kinh.
Ung thư vú dạng viêm thường phát triển và di căn nhanh chóng. Tế bào ung thư có thể đã xâm lấn các hạch bạch huyết lân cận vào thời điểm xuất hiện các triệu chứng, có thể gây sưng hạch bạch huyết dưới cánh tay (hạch nách) hoặc phía trên xương đòn (hạch thượng đòn). Nếu việc chẩn đoán bị trì hoãn thì ung thư có thể di căn đến các nơi xa hơn.
Chẩn đoán ung thư vú dạng viêm:
- Chẩn đoán hình ảnh
Nếu nghi ngờ ung thư vú dạng viêm, một hoặc nhiều xét nghiệm hình ảnh sau đây có thể được thực hiện:
Chụp X quang tuyến vú (nhũ ảnh)
Siêu âm vú
Chụp MRI (chụp cộng hưởng từ) vú
- Sinh thiết
Ung thư vú dạng viêm được chẩn đoán bằng sinh thiết, lấy ra một mảnh mô vú nhỏ và quan sát trong phòng thí nghiệm. Chỉ có làm sinh thiết mới có thể biết chắc chắn rằng đó là ung thư.
Các tế bào ung thư thu được bằng sinh thiết sẽ được xem trong phòng thí nghiệm để xác định mức độ và sẽ được kiểm tra một số protein cụ thể để quyết định phương pháp điều trị phù hợp. Những trường hợp tế bào ung thư vú có thụ thể nội tiết tố sẽ được điều trị bằng liệu pháp nội tiết tố. Hoặc tế bào ung thư có quá nhiều protein HER2 sẽ được điều trị bằng thuốc nhắm vào HER2.
2. Các loại ung thư vú ít phổ biến hơn
Có một số loại ung thư vú bắt đầu ở các loại tế bào khác trong vú. Những loại ung thư này ít phổ biến hơn nhiều và đôi khi cần các phương pháp điều trị khác nhau.
2.1. Bệnh Paget vú
Đây là một loại ung thư vú hiếm gặp liên quan đến da núm vú và quầng vú. Bệnh Paget thường chỉ ảnh hưởng đến một bên vú. Trong 80-90% trường hợp, bệnh Paget thường xuất hiện cùng với ung thư biểu mô ống tuyến vú tại chỗ hoặc xâm lấn.
Dấu hiệu và triệu chứng:
Da ở núm vú và quầng vú thường đóng vảy và đỏ. Có thể có máu hoặc chất lỏng màu vàng chảy ra từ núm vú. Đôi khi núm vú phẳng hoặc thụt vào trong, có thể bị rát bỏng hoặc ngứa. Ban đầu, bác sĩ có thể nghĩ đây là bệnh chàm và nếu không cải thiện thì có thể sinh thiết.
Chẩn đoán:
Hầu hết những người mắc bệnh Paget ở vú cũng có khối u ở cùng một vú. Một hoặc nhiều xét nghiệm hình ảnh sau đây có thể được thực hiện để kiểm tra những thay đổi khác ở vú:
- Chụp X quang tuyến vú (Nhũ ảnh)
- Siêu âm vú
- Chụp MRI (chụp cộng hưởng từ) vú
Bệnh Paget ở vú được chẩn đoán bằng sinh thiết, lấy ra một mảnh mô vú nhỏ và quan sát kỹ trong phòng thí nghiệm. Trong một số trường hợp, toàn bộ núm vú có thể bị cắt bỏ. Chỉ có sinh thiết mới có thể chắc chắn rằng đó là ung thư.
Điều trị bệnh Paget vú
Bệnh Paget có thể được điều trị bằng cách cắt bỏ toàn bộ vú (phẫu thuật cắt trọn vú) hoặc phẫu thuật bảo tồn vú, sau đó là xạ trị toàn bộ vú. Nếu thực hiện phẫu thuật bảo tồn vú, thì toàn bộ vùng núm vú và quầng vú được cắt bỏ. Nếu phát hiện ung thư xâm lấn, các hạch bạch huyết dưới cánh tay sẽ được kiểm tra ung thư.
Nếu không có khối u nào trong mô vú và kết quả sinh thiết cho thấy ung thư chưa lan rộng trong mô vú thì tiên lượng sẽ rất tốt.
Nếu ung thư đã xâm lấn trong mô vú thì tiên lượng sẽ không tốt và khi đó ung thư sẽ được phân loại và điều trị giống như ung thư biểu mô ống tuyến vú xâm lấn.
2.2. Angiosarcoma vú
Đây là một loại ung thư hiếm gặp, xuất phát từ các tế bào lót trong lòng mạch máu hoặc mạch bạch huyết. Nhiều khi nguyên nhân là do biến chứng của xạ trị vú trước đó, có thể xảy ra 8-10 năm sau khi xạ trị tuyến vú.
Các dấu hiệu và triệu chứng:
Angiosarcoma vú có thể làm thay đổi về da như các nốt màu tím và/hoặc khối u ở vú. Triệu chứng này cũng có thể xảy ra ở cánh tay bị phù bạch huyết, nhưng không phổ biến. Phù bạch huyết là tình trạng sưng tấy có thể xuất hiện sau phẫu thuật hoặc xạ trị để điều trị ung thư vú.
Chẩn đoán:
Một hoặc nhiều xét nghiệm chẩn đoán hình ảnh có thể được thực hiện để kiểm tra những thay đổi ở vú:
- Chụp nhũ ảnh chẩn đoán
- Siêu âm vú
- Chụp MRI vú
Angiosarcoma vú được chẩn đoán bằng sinh thiết, lấy ra một mảnh mô vú nhỏ và xem xét kỹ trong phòng thí nghiệm. Chỉ có sinh thiết mới có thể biết chắc chắn đó là ung thư.
Điều trị:
Angiosarcoma vú có xu hướng phát triển và lây lan nhanh chóng. Điều trị thường là phẫu thuật cắt bỏ vú. Các hạch bạch huyết ở nách thường không bị cắt bỏ. Xạ trị có thể được chỉ định trong một số trường hợp không liên quan đến xạ trị vú trước đó.
2.3. U phyllodes
U phyllodes còn được gọi là u diệp thể vì các tế bào giống hình chiếc lá. Đây là loại u vú hiếm gặp bắt đầu từ mô liên kết (mô đệm) của vú chứ không phải từ các ống hay tuyến vú, vốn là những nơi khởi đầu của hầu hết các trường hợp ung thư vú. Đa số các u diệp thể là lành tính, chỉ một số ít là ác tính (ung thư).
U phyllodes phổ biến nhất ở phụ nữ ở độ tuổi 40, nhưng phụ nữ ở mọi lứa tuổi đều có thể mắc phải. Phụ nữ mắc hội chứng Li-Fraumeni (một tình trạng di truyền hiếm gặp) có nguy cơ mắc bệnh cao hơn.
U phyllodes thường được chia thành 3 nhóm, dựa trên hình dạng của chúng dưới kính hiển vi:
- U lành tính (không gây ung thư) chiếm hơn một nửa. Những khối u này ít có khả năng phát triển nhanh chóng hoặc lan rộng.
- U ranh giới có những đặc điểm nằm giữa khối u lành tính và ác tính (ung thư).
- U ác tính (ung thư) chiếm khoảng 1/4 trường hợp, có xu hướng phát triển nhanh và xâm lấn, di căn hoặc tái phát sau khi điều trị.
Chẩn đoán
U phyllodes thường có cảm giác như một khối u ở vú có mật độ chắc, không đau, nhưng một số có thể gây đau. Thường phát triển lớn khá nhanh và làm căng da.
Đôi khi u diệp thể đầu tiên được phát hiện khi làm xét nghiệm hình ảnh (như siêu âm hoặc chụp nhũ ảnh), thường khó phân biệt với u xơ tuyến vú.
Chẩn đoán thường bằng sinh thiết bằng kim nhỏ, để biết liệu nó có ác tính hay không.
Có khối u lành tính thì không ảnh hưởng đến nguy cơ ung thư vú. Nếu có khối u phyllodes ác tính thì nó không ảnh hưởng đến nguy cơ mắc các loại ung thư vú khác. Tuy nhiên, bệnh nhân cần được theo dõi chặt chẽ hơn và kiểm tra thường xuyên bằng xét nghiệm chẩn đoán hình sau khi điều trị, vì những khối u này đôi khi có thể tái phát sau phẫu thuật.
Điều trị
Các khối u phyllodes thường cần phải được loại bỏ hoàn toàn bằng phẫu thuật.
Nếu khối u là lành tính, chỉ cần thực hiện sinh thiết cắt bỏ là đủ, miễn là khối u đã được cắt bỏ hoàn toàn.
Nếu khối u ở ranh giới hoặc ác tính thì thường cũng cần phải loại bỏ một phần rìa rộng hơn (vùng mô bình thường xung quanh khối u). Có thể phẫu thuật bảo tồn vú (chỉ cắt bỏ khối u hoặc cắt bỏ một phần vú) hoặc phẫu thuật cắt toàn bộ vú (cắt trọn vú) khi không thể phẫu thuật bảo tồn vú. Có thể phải xạ trị sau phẫu thuật.
Nếu khối u là ác tính thì nó thường khác với các loại ung thư vú phổ biến vì ít có khả năng đáp ứng với các phương pháp điều trị thường thông thường, như liệu pháp hormone hoặc hóa trị. Các khối u phyllodes đã xâm lấn sang các bộ phận khác của cơ thể thường được điều trị giống như ung thư loại sarcoma (ung thư mô mềm) hơn là ung thư vú.
U phyllodes đôi khi tái phát ở cùng một vị trí nên phải theo dõi chặt chẽ bằng khám vú và xét nghiệm hình ảnh thường xuyên sau khi điều trị.
YẾU TỐ NGUY CƠ VÀ PHÒNG NGỪA UNG THƯ VÚ
1. Các yếu tố nguy cơ ung thư vú
Yếu tố nguy cơ là bất cứ điều gì làm tăng khả năng mắc bệnh. Nhưng việc có một hoặc nhiều yếu tố nguy cơ của ung thư vú không có nghĩa là chắc chắn mắc bệnh ung thư vú. Có 2 loại yếu tố nguy cơ: thay đổi được (ví dụ như liên quan lối sống) và không thay đổi được (ví dụ như tuổi, giới tính…).
1.1. Các yếu tố nguy cơ không thể thay đổi
Giới tính nữ
Đây là yếu tố nguy cơ chính gây ung thư vú. Nam giới cũng có thể bị ung thư vú, nhưng bệnh phổ biến ở nữ giới hơn.
Tuổi tác
Khi già đi, nguy cơ mắc bệnh ung thư vú sẽ tăng lên. Đa số ung thư vú được phát hiện ở phụ nữ từ 55 tuổi trở lên.
Đột biến gen di truyền
Khoảng 5% đến 10% trường hợp ung thư vú được cho là do di truyền, nghĩa là ung thư vú có nguyên nhân từ những đột biến gen được truyền từ cha mẹ.
- BRCA1 và BRCA2: Nguyên nhân phổ biến nhất gây ra ung thư vú di truyền là đột biến di truyền ở gen BRCA1 hoặc BRCA2. Trong các tế bào bình thường, những gen này giúp tạo ra các protein sửa chữa DNA bị hư hỏng. Các phiên bản đột biến của những gen này có thể dẫn đến sự phát triển bất thường của tế bào, và gây ung thư.
Nếu được thừa hưởng một bản sao đột biến của một trong hai gen này từ cha mẹ, bạn có nguy cơ mắc ung thư vú cao hơn.
Trung bình, một phụ nữ có đột biến gen BRCA1 hoặc BRCA2 có tới 7/10 khả năng mắc ung thư vú trước 80 tuổi. Nguy cơ này tăng lên nếu có nhiều thành viên trong gia đình bị ung thư vú.
Phụ nữ có một trong những đột biến này có nhiều khả năng ung thư vú ở độ tuổi trẻ hơn, cũng như ung thư ở cả hai bên vú.
Phụ nữ có một trong những thay đổi gen này cũng có nguy cơ bị ung thư buồng trứng và một số loại ung thư khác cao hơn. Nam giới thừa hưởng một trong những đột biến gen này cũng có nguy cơ mắc bệnh ung thư vú và một số bệnh ung thư khác cao hơn.
Ở Hoa Kỳ, đột biến BRCA phổ biến hơn ở người Do Thái gốc Ashkenazi (Đông Âu) so với các nhóm chủng tộc và dân tộc khác.
- Các gen khác: Đột biến các gen khác cũng có thể dẫn đến ung thư vú di truyền. Những đột biến gen này ít phổ biến hơn nhiều và hầu hết chúng không làm tăng nguy cơ ung thư vú nhiều như gen BRCA.
ATM: Gen ATM thường giúp sửa chữa DNA bị hư hỏng (hoặc giúp tiêu diệt tế bào nếu không thể sửa chữa được chúng). Việc thừa hưởng một bản sao bất thường của gen này có liên quan đến tăng tỷ lệ ung thư vú.
PALB2: Gen PALB2 tạo ra một loại protein tương tác với protein do gen BRCA2 tạo ra. Đột biến gen này cũng làm tăng nguy cơ ung thư vú.
TP53: Gen TP53 giúp ngăn chặn sự phát triển của các tế bào có DNA bị hư hỏng. Các đột biến di truyền của gen này gây ra hội chứng Li-Fraumeni. Những người mắc hội chứng này tăng nguy cơ ung thư vú, cũng như một số loại ung thư khác như bệnh bạch cầu, u não và ung thư xương. Đột biến này là nguyên nhân hiếm gặp gây ung thư vú.
CHEK2: Gen CHEK2 là một gen khác, giúp sửa chữa DNA. Đột biến CHEK2 làm tăng nguy cơ ung thư vú.
PTEN: Gen PTEN thường giúp điều chỉnh sự phát triển của tế bào. Các đột biến di truyền gen này có thể gây ra hội chứng Cowden, một rối loạn hiếm gặp làm tăng nguy cơ cả 2 loại u ác tính và u lành tính ở vú.
CDH1: Các đột biến di truyền gen này gây ra ung thư dạ dày lan tỏa di truyền, là một loại ung thư dạ dày hiếm gặp. Phụ nữ mang gen đột biến này cũng cũng bị tăng nguy cơ ung thư vú tiểu thùy xâm lấn.
STK11: Các đột biến gen này có thể gây ra hội chứng Peutz-Jeghers với các triệu chứng là xuất hiện các đốm sắc tố trên môi và trong miệng, polyp trong đường tiết niệu và đường tiêu hóa, và tăng nguy cơ bị nhiều loại ung thư, bao gồm ung thư vú.
Tư vấn và xét nghiệm di truyền: Xét nghiệm di truyền có thể được thực hiện để tìm kiếm các đột biến di truyền ở gen BRCA1 và BRCA2 (hoặc ít phổ biến hơn ở các gen như PTEN, TP53 hoặc các gen khác được đề cập ở trên). Đây có thể là một lựa chọn cho phụ nữ đã được chẩn đoán mắc bệnh ung thư vú, cũng như phụ nữ có các yếu tố nguy cơ mắc bệnh ung thư vú. Mặc dù xét nghiệm di truyền có ích trong một số trường hợp nhưng không phải mọi phụ nữ đều cần làm xét nghiệm, hơn nữa những ưu và nhược điểm cần được xem xét cẩn thận.
Có tiền sử gia đình mắc ung thư vú
Cần lưu ý là đa số phụ nữ bị ung thư vú không có tiền sử gia đình bị bệnh này. Nhưng nếu phụ nữ có thành viên gia đình bị ung thư vú thì họ sẽ có nguy cơ bị ung thư vú cao hơn, cụ thể:
- Có 1 người thân cấp độ một (mẹ, chị gái hoặc con gái) bị ung thư vú thì nguy cơ tăng gần gấp đôi. Có 2 người thân cấp độ một bị ung thư vú thì nguy cơ tăng lên khoảng gấp 3.
- Những phụ nữ có cha hoặc anh trai mắc ung thư vú cũng có nguy cơ mắc ung thư vú cao hơn.
Có tiền sử cá nhân mắc ung thư vú
Một phụ nữ bị ung thư vú một bên thì nguy cơ bị ung thư bên vú kia hoặc ung thư vú cùng bên ở vị trí khác sẽ tăng cao hơn. Điều này khác với tình trạng tái phát của ung thư ban đầu.
Chủng tộc và dân tộc
Phụ nữ da trắng có nguy cơ ung thư vú cao hơn một chút so với phụ nữ Mỹ gốc Phi. Ở những phụ nữ dưới 40 tuổi, ung thư vú phổ biến hơn ở phụ nữ Mỹ gốc Phi. Phụ nữ Mỹ gốc Phi cũng có tỷ lệ tử vong do ung thư vú cao hơn ở mọi lứa tuổi. Phụ nữ châu Á, gốc Tây Ban Nha và người Mỹ bản địa có nguy cơ bị bệnh và tử vong do ung thư vú thấp hơn.
Nguy cơ ở các nhóm chủng tộc khác nhau cũng khác nhau tùy theo loại ung thư vú. Ví dụ, phụ nữ Mỹ gốc Phi có nguy cơ ung thư vú bộ ba âm tính cao hơn.
Chiều cao
Nhiều nghiên cứu đã phát hiện ra rằng phụ nữ cao hơn có nguy cơ mắc ung thư vú cao hơn phụ nữ thấp. Chưa có giải thích rõ ràng cho điều này, nhưng có thể liên quan đến các yếu tố ảnh hưởng đến sự phát triển sớm, chẳng hạn như dinh dưỡng khi còn nhỏ, cũng như các yếu tố về nội tiết tố hoặc di truyền.
Có mô vú đậm đặc
Vú được tạo thành từ mô mỡ, mô xơ và mô tuyến. Vú trông đậm đặc (dày) hơn trên phim chụp nhũ ảnh khi chúng có nhiều mô tuyến và mô xơ hơn và ít mô mỡ hơn. Phụ nữ có mô vú đặc trên phim chụp nhũ ảnh có nguy cơ mắc ung thư vú cao hơn so với phụ nữ có mật độ vú trung bình. Ngoài ra, mô vú đặc cũng có thể khiến việc phát hiện ung thư trên phim chụp nhũ ảnh khó khăn hơn.
Một số yếu tố có thể ảnh hưởng đến mật độ vú, chẳng hạn như tuổi tác, tình trạng mãn kinh, sử dụng một số loại thuốc (ví dụ liệu pháp hormone mãn kinh), thai kỳ và di truyền.
Có bệnh tuyến vú lành tính
Phụ nữ được chẩn đoán bệnh lý tuyến vú lành tính (không phải ung thư) có thể có nguy cơ ung thư vú cao hơn. Bác sĩ thường chia các bệnh lý lành tính này thành các nhóm khác nhau, tùy theo nguy cơ gây ung thư vú:
Các tổn thương không tăng sinh: Những tình trạng này thường không ảnh hưởng đến nguy cơ ung thư vú hoặc nếu có, thì chỉ tăng nguy cơ rất nhỏ. Chúng bao gồm:
- Xơ hóa và/hoặc u nang đơn giản
- Tăng sản nhẹ
- Bệnh tuyến của vú (phì đại tuyến vú, không xơ hóa)
- U phyllodes (lành tính)
- U gai (nhú) đơn lẻ
- Hoại tử mô mỡ
- Dãn ống tuyến vú
- Xơ hóa quanh ống tuyến vú
- Vôi hóa liên quan đến biểu mô
- Các khối u khác (u mỡ, u mô thừa vú, u máu, u xơ thần kinh, u cơ biểu mô tuyến vú)
Viêm vú (nhiễm trùng vú) không phải là khối u và không làm tăng nguy cơ ung thư vú.
Tổn thương tăng sinh không có dị sản (bất thường tế bào): Các tế bào trong ống tuyến vú hoặc tiểu thùy của vú phát triển quá mức, nhưng trông không quá bất thường. Những tình trạng này dường như làm tăng nhẹ nguy cơ ung thư vú ở phụ nữ. Chúng bao gồm:
- Tăng sản ống tuyến vú (không có dị sản)
- U xơ tuyến vú (Bướu sợi tuyến vú)
- Bệnh tuyến của tuyến vú xơ cứng
- U nhiều nhú
- Sẹo tỏa tia (radial scar)
Tổn thương tăng sinh có dị sản: Các tế bào trong ống tuyến vú hoặc tiểu thùy của mô vú phát triển quá mức và một số trong số chúng không còn trông bình thường nữa. Những loại tổn thương này bao gồm:
- Tăng sản ống dẫn tuyến vú không điển hình
- Tăng sản tiểu thùy không điển hình
Nguy cơ ung thư vú cao hơn khoảng 4 đến 5 lần so với bình thường ở những phụ nữ có những thay đổi này. Nếu một phụ nữ cũng có tiền sử gia đình bị ung thư vú và tăng sản hoặc tăng sản không điển hình, thì cô ấy có nguy cơ mắc ung thư vú thậm chí còn cao hơn.
Ung thư biểu mô tiểu thùy tại chỗ
Trong ung thư biểu mô tiểu thùy tại chỗ, các tế bào trông giống tế bào ung thư đang phát triển trong các tiểu thùy của tuyến sản xuất sữa ở vú, nhưng chúng không phát triển xuyên qua thành tiểu thùy. Ung thư biểu mô tiểu thùy tại chỗ không được xem là ung thư và thường không phát triển ra ngoài tiểu thùy (tức là không trở thành ung thư vú xâm lấn) nếu không được điều trị. Nhưng phụ nữ mắc ung thư biểu mô tuyến tại chỗ có nguy cơ mắc ung thư vú cao hơn từ 7 đến 12 lần (có thể ở cả hai bên vú).
Có kinh sớm
Phụ nữ có nhiều chu kỳ kinh nguyệt hơn vì có kinh nguyệt sớm (đặc biệt là trước 12 tuổi) có nguy cơ ung thư vú cao hơn một chút. Nguy cơ tăng có thể là do tiếp xúc lâu hơn với các hormone estrogen và progesterone trong suốt cuộc đời.
Mãn kinh muộn
Phụ nữ có nhiều chu kỳ kinh nguyệt hơn vì mãn kinh muộn (thường là sau 55 tuổi) có nguy cơ mắc ung thư vú cao hơn một chút. Nguy cơ tăng có thể là do tiếp xúc lâu hơn với các hormone estrogen và progesterone trong suốt cuộc đời.
Xạ trị ở ngực
Phụ nữ được điều trị bằng xạ trị ở ngực để điều trị một loại ung thư khác (như u lympho Hodgkin hoặc không phải Hodgkin) khi còn trẻ có nguy cơ mắc ung thư vú cao hơn đáng kể. Nguy cơ này phụ thuộc vào độ tuổi khi được xạ trị. Nguy cơ cao nhất ở phụ nữ xạ trị trong độ tuổi thiếu niên hoặc thanh niên, khi ngực vẫn đang phát triển. Xạ trị ở phụ nữ lớn tuổi (sau khoảng 40 đến 45 tuổi) dường như không làm tăng nguy cơ mắc ung thư vú.
Tiếp xúc với chất diethylstilbestrol (DES)
Từ những năm 1940 đến đầu những năm 1970, một số phụ nữ mang thai đã được dùng một loại thuốc giống estrogen có tên là DES vì được cho rằng nó có thể làm giảm nguy cơ sẩy thai. Những phụ nữ này có nguy cơ mắc ung thư vú cao hơn một chút. Những phụ nữ có mẹ dùng DES trong khi mang thai cũng có thể có nguy cơ mắc ung thư vú cao hơn một chút.
1.2. Các yếu tố nguy cơ liên quan đến lối sống (có thể thay đổi)
Một số yếu tố nguy cơ ung thư vú có liên quan đến hành vi hay thói quen cá nhân, chẳng hạn như chế độ ăn uống và hoạt động thể chất, quyết định có con và dùng thuốc có chứa hormone…
Uống rượu
Uống rượu rõ ràng có liên quan đến việc tăng nguy cơ ung thư vú. Nguy cơ tăng lên theo lượng rượu tiêu thụ. Phụ nữ uống 1 ly rượu mỗi ngày có nguy cơ tăng nhẹ (khoảng 7% đến 10%) so với những người không uống rượu, trong khi những phụ nữ uống 2 đến 3 ly mỗi ngày có nguy cơ cao hơn khoảng 20%. Rượu cũng có liên quan đến việc tăng nguy cơ mắc các loại ung thư khác.
Tốt nhất là không nên uống rượu. Phụ nữ nếu có uống rượu thì không nên uống quá 1 ly mỗi ngày.
Thừa cân hoặc béo phì
Thừa cân hoặc béo phì sau mãn kinh làm tăng nguy cơ ung thư vú.
Trước thời kỳ mãn kinh, hầu hết estrogen đều được sản xuất từ buồng trứng và chỉ một lượng nhỏ được tạo từ mô mỡ. Sau thời kỳ mãn kinh (khi buồng trứng ngừng sản xuất estrogen), hầu hết estrogen là từ mô mỡ. Có nhiều mô mỡ sau khi mãn kinh có thể làm tăng nồng độ estrogen và tăng nguy cơ mắc bệnh ung thư vú.
Phụ nữ thừa cân cũng thường có lượng insulin trong máu cao hơn và có liên quan đến một số bệnh ung thư, bao gồm ung thư vú.
Một số nghiên cứu cho thấy thừa cân sau mãn kinh có liên quan với tăng nguy cơ ung thư vú dương tính với thụ thể hormone, trong khi thừa cân trước khi mãn kinh có thể làm tăng nguy cơ mắc bệnh ung thư loại ít gặp hơn là ung thư vú bộ ba âm tính.
Hiệp hội Ung thư Hoa Kỳ khuyến nghị nên duy trì cân nặng hợp lý trong suốt cuộc đời và tránh tăng cân quá mức bằng cách cân bằng lượng thức ăn và đồ uống cùng với hoạt động thể chất.
Không hoạt động thể chất
Ngày càng có nhiều bằng chứng cho thấy hoạt động thể chất thường xuyên làm giảm nguy cơ ung thư vú, đặc biệt ở phụ nữ đã mãn kinh.
Hiện chưa rõ chính xác hoạt động thể chất có thể làm giảm nguy cơ ung thư vú như thế nào nhưng có thể là do tác động của nó lên cân nặng của cơ thể, tình trạng viêm và nồng độ hormone.
Hiệp hội Ung thư Hoa Kỳ khuyến nghị người lớn nên dành mỗi tuần từ 150 đến 300 phút để hoạt động với cường độ vừa phải hoặc 75 đến 150 phút hoạt động với cường độ cao (hoặc kết hợp cả hai).
Không có con
Nhìn chung, những phụ nữ chưa có con hoặc sinh con đầu lòng sau 30 tuổi có nguy cơ ung thư vú cao hơn một chút. Mang thai nhiều lần và mang thai khi còn trẻ làm giảm nguy cơ ung thư vú.
Tuy nhiên, tác động của việc mang thai đến nguy cơ ung thư vú rất phức tạp. Ví dụ, nguy cơ ung thư vú cao hơn trong khoảng thập kỷ đầu tiên sau khi có con, nhưng sau đó sẽ giảm dần theo thời gian.
Không cho con bú
Hầu hết các nghiên cứu cho thấy rằng việc cho con bú có thể làm giảm nhẹ nguy cơ ung thư vú, đặc biệt nếu thời gian cho con bú kéo dài từ một năm trở lên. Lợi ích của việc cho con bú được giải thích là có thể làm giảm tổng số chu kỳ kinh nguyệt trong đời của người phụ nữ (giống như việc bắt đầu có kinh ở độ tuổi muộn hoặc mãn kinh sớm).
Tránh thai
Một số phương pháp ngừa thai sử dụng hormone có thể làm tăng nguy cơ ung thư vú.
- Thuốc tránh thai đường uống: Hầu hết các nghiên cứu đều phát hiện ra rằng phụ nữ sử dụng thuốc tránh thai đường uống có nguy cơ mắc ung thư vú cao hơn một chút so với những phụ nữ chưa bao giờ sử dụng chúng.
- Thuốc ngừa thai đường tiêm: Một số nghiên cứu (chứ không phải tất cả các nghiên cứu) cho thấy việc tiêm progesterone tác dụng kéo dài (như Depo-Provera) 3 tháng một lần để ngừa thai có thể làm tăng nguy cơ ung thư vú.
Các cách ngừa thai khác như que cấy tránh thai, dụng cụ trong tử cung, miếng dán da, vòng âm đạo…cũng sử dụng hormone, theo lý thuyết có làm tăng nguy cơ ung thư vú.
Liệu pháp hormone mãn kinh
Liệu pháp hormone cho phụ nữ mãn kinh bằng estrogen (thường kết hợp với progesterone) đã được sử dụng trong nhiều năm để giúp giảm các triệu chứng mãn kinh và giúp ngăn ngừa loãng xương. Phương pháp điều trị này còn có các tên khác, chẳng hạn như liệu pháp hormone sau mãn kinh và liệu pháp thay thế hormone.
Có 2 loại liệu pháp hormone chính:
Đối với những phụ nữ vẫn còn tử cung (dạ con), bác sĩ thường kê toa estrogen và progesterone (được gọi là liệu pháp hormone kết hợp hoặc liệu pháp hormone). Phối hợp với Progesterone là cần thiết vì nếu chỉ một mình estrogen thì có thể làm tăng nguy cơ ung thư tử cung.
Đối với những phụ nữ đã cắt bỏ tử cung, chỉ có thể sử dụng estrogen. Đây được gọi là liệu pháp thay thế estrogen hoặc liệu pháp estrogen.
- Liệu pháp hormone kết hợp: Sử dụng liệu pháp hormone kết hợp sau mãn kinh làm tăng nguy cơ ung thư vú. Nguy cơ này thường thấy sau khoảng 4 năm sử dụng.
Nguy cơ ung thư vú do liệu pháp hormone kết hợp thường liên quan ở phụ nữ hiện đang sử dụng và sử dụng gần đây. Nguy cơ ung thư vú ở giảm xuống khoảng 5 năm sau khi ngừng điều trị, mặc dù nguy cơ này không biến mất hoàn toàn.
Liệu pháp hormone sinh học: Từ “sinh học” đôi khi được sử dụng để mô tả các phiên bản estrogen và progesterone có cấu trúc hóa học giống như những hormone được tìm thấy tự nhiên ở người (trái ngược với các phiên bản hormone hơi khác có trong hầu hết các loại thuốc). Việc sử dụng các hormone này đã được quảng cáo là một cách an toàn để điều trị các triệu chứng mãn kinh. Nhưng vì không có nhiều nghiên cứu so sánh hormone “sinh học” hoặc “tự nhiên” với các phiên bản hormone tổng hợp nên không có bằng chứng nào cho thấy chúng an toàn hơn hoặc hiệu quả hơn. Cần nhiều nghiên cứu hơn để có kết luận chắc chắn.
- Liệu pháp estrogen: Các nghiên cứu về việc chỉ sử dụng estrogen sau mãn kinh cho kết quả khác nhau. Một số nghiên cứu thấy nguy cơ ung thư vú có tăng cao hơn một chút, trong khi những nghiên cứu khác thì thấy không tăng hoặc thậm chí giảm.
Tính đến thời điểm này, ngoài lợi ích là giảm các triệu chứng mãn kinh trong thời gian ngắn thì không có nhiều lý do chính đáng để sử dụng liệu pháp hormone sau mãn kinh (kết hợp hoặc chỉ một mình estrogen). Ngoài việc tăng nguy cơ ung thư vú, liệu pháp hormone kết hợp cũng có thể làm tăng nguy cơ mắc bệnh tim, tạo huyết khối và đột quỵ mặc dù nó làm giảm nguy cơ ung thư đại trực tràng và loãng xương. Do đó việc sử dụng liệu pháp hormone kết hợp cần được cân nhắc kỹ. Đối với liệu pháp estrogen, mặc dù chưa rõ liệu có làm tăng nguy cơ ung thư vú hay không nhưng nó làm tăng nguy cơ đột quỵ.
Trong trường hợp cần phải dùng liệu pháp hormone để điều trị các triệu chứng mãn kinh, thì tốt nhất nên sử dụng ở liều thấp nhất có hiệu quả và trong thời gian ngắn nhất có thể.
Phẫu thuật nâng ngực
Cấy túi ngực không liên quan đến tăng nguy cơ đối với các loại ung thư vú phổ biến.
Tuy nhiên, trong một số trường hợp hiếm thì có liên quan đến một số loại ung thư khác, bao gồm u lympho tế bào lớn không biệt hóa và các loại u lympho khác, cũng như ung thư biểu mô tế bào vảy. Những loại ung thư này có thể hình thành trong mô sẹo (vỏ nang) xung quanh túi độn và chúng có thể biểu hiện dưới dạng cục u, tụ dịch, sưng hoặc đau, hoặc thay đổi vùng da gần túi độn hoặc dưới dạng thay đổi về kích thước hoặc hình dạng vú.
1.3. Các yếu tố có tác động không rõ ràng đến nguy cơ ung thư vú
Có một số yếu tố có thể liên quan nguy cơ gây ung thư vú, nhưng nghiên cứu vẫn chưa có kết luận rõ ràng.
Chế độ ăn và vitamin
Mặc dù thừa cân hoặc béo phì và không hoạt động thể chất có liên quan đến nguy cơ ung thư vú, nhưng mối liên hệ có thể có giữa chế độ ăn và nguy cơ ung thư vú vẫn chưa rõ ràng. Kết quả của một số nghiên cứu cho thấy chế độ ăn có thể đóng một vai trò, trong khi những nghiên cứu khác không phát hiện ra rằng chế độ ăn ảnh hưởng đến nguy cơ ung thư vú.
Các nghiên cứu về phụ nữ ở Hoa Kỳ chưa tìm thấy mối liên hệ nhất quán giữa chế độ ăn nhiều chất béo và mắc ung thư vú, mặc dù một số nghiên cứu đã phát hiện ra mối liên hệ có thể có giữa chế độ ăn nhiều chất béo và nguy cơ tử vong do ung thư vú cao hơn. Các nghiên cứu cũng phát hiện ra rằng ung thư vú ít phổ biến hơn ở những quốc gia có chế độ ăn điển hình là ít chất béo nói chung, ít chất béo không bão hòa đa và ít chất béo bão hòa. Vẫn chưa có cách giải thích chắc chắn cho phát hiện này.
Chế độ ăn nhiều chất béo có thể dẫn đến tình trạng thừa cân hoặc béo phì, đây là một yếu tố nguy cơ ung thư vú đã biết. Chế độ ăn nhiều chất béo cũng là một yếu tố nguy cơ đối với một số loại ung thư khác và tăng nguy cơ mắc bệnh tim mạch.
Một số nghiên cứu cho thấy chế độ ăn nhiều trái cây, rau củ và các sản phẩm từ sữa giàu canxi nhưng ít thịt đỏ và thịt chế biến có thể làm giảm nguy cơ ung thư vú. Đây vẫn là một lĩnh vực nghiên cứu đang được quan tâm.
Cho đến nay, không có bằng chứng đáng tin cậy nào cho thấy việc dùng vitamin (hoặc bất kỳ loại thực phẩm bổ sung nào khác) có thể làm giảm nguy cơ ung thư vú.
Việc thiếu mối liên hệ chặt chẽ giữa chế độ ăn uống và ung thư vú trong các nghiên cứu cho đến nay không có nghĩa là không cần một chế độ ăn uống lành mạnh. Một chế độ ăn ít chất béo, thịt đỏ và thịt chế biến nhưng nhiều trái cây và rau củ có thể mang lại nhiều lợi ích cho sức khỏe, bao gồm cả việc giảm nguy cơ mắc một số loại ung thư khác.
Hóa chất trong môi trường
Rất nhiều nghiên cứu đã được báo cáo và nhiều nghiên cứu khác đang được thực hiện để hiểu rõ những ảnh hưởng có thể có của môi trường đối với nguy cơ ung thư vú.
Các hóa chất trong môi trường có đặc tính giống estrogen được quan tâm đặc biệt. Ví dụ, các chất có trong một số loại nhựa, một số loại mỹ phẩm và sản phẩm chăm sóc cá nhân, thuốc trừ sâu và PCB (polychlorinated biphenyls) dường như có những đặc tính như vậy. Về mặt lý thuyết, những chất này có thể ảnh hưởng đến nguy cơ ung thư vú.
Hiện tại, nghiên cứu không chỉ ra mối liên hệ rõ ràng giữa nguy cơ ung thư vú và việc tiếp xúc với những chất này, nhưng rất khó để nghiên cứu những tác động như vậy ở người. Cần có nhiều nghiên cứu hơn nữa trong lĩnh vực này.
Khói thuốc lá
Một số nghiên cứu đã phát hiện ra rằng hút thuốc lá nhiều trong thời gian dài có thể liên quan đến nguy cơ ung thư vú cao hơn một chút. Trong một số nghiên cứu, nguy cơ cao nhất là ở phụ nữ bắt đầu hút thuốc trước khi sinh con đầu lòng. Báo cáo năm 2014 của Tổng giám đốc Y khoa Hoa Kỳ về hút thuốc kết luận rằng có bằng chứng "gợi ý nhưng chưa đủ" cho thấy hút thuốc làm tăng nguy cơ ung thư vú.
Làm việc ca đêm
Phụ nữ làm việc vào ban đêm, chẳng hạn như y tá làm ca đêm, có thể có nguy cơ mắc ung thư vú cao hơn. Đây là một lĩnh vực nghiên cứu đang được quan tâm. Tác động này có thể là do sự thay đổi nồng độ melatonin, một loại hormone bị ảnh hưởng bởi sự tiếp xúc của cơ thể với ánh sáng. Các hormone khác cũng đang được nghiên cứu.
1.4. Các yếu tố nguy cơ gây ung thư vú chưa được chứng minh hoặc gây tranh cãi
Có một số yếu tố mà nghiên cứu đã chỉ ra là không liên quan đến ung thư vú. Có nhiều thông tin trực tuyến hoặc truyền miệng về các yếu tố nguy cơ chưa được chứng minh hoặc gây tranh cãi này. Điều quan trọng là phải tìm hiểu sự thật.
Thuốc chống mồ hôi
Nhiều ý kiến cho rằng cho rằng các hóa chất trong thuốc chống mồ hôi dưới cánh tay (hay được gọi là lăn nách) được hấp thụ qua da, cản trở quá trình lưu thông bạch huyết và khiến độc tố tích tụ trong vú, cuối cùng dẫn đến ung thư vú.
Dựa trên các bằng chứng hiện có (bao gồm cả những gì đã biết về cách cơ thể hoạt động), có rất ít hoặc không có lý do gì để tin rằng thuốc chống mồ hôi làm tăng nguy cơ ung thư vú.
Áo ngực
Nhiều ý kiến cho rằng áo ngực gây ung thư vú bằng cách cản trở lưu thông bạch huyết. Không có cơ sở khoa học hoặc lâm sàng nào cho tuyên bố này và một nghiên cứu năm 2014 trên hơn 1.500 phụ nữ không tìm thấy mối liên hệ nào giữa việc mặc áo ngực và nguy cơ ung thư vú.
Phá thai
Nhiều nghiên cứu lớn kết luận không có mối liên hệ nào giữa phá thai và nguy cơ ung thư vú.
2. Có cách nào ngăn ngừa ung thư vú không?
Không có phương pháp ngăn ngừa ung thư vú triệt để, nhưng có những cách có thể làm để giảm nguy cơ bị ung thư vú. Điều này rất quan trọng đối với những phụ nữ có một số yếu tố nguy cơ mắc ung thư vú, chẳng hạn như có tiền sử gia đình bị ung thư vú hoặc mang gen đột biến di truyền. Các phương pháp giảm nguy cơ ung thư vú bao gồm:
- Tư vấn di truyền và xét nghiệm nguy cơ ung thư vú
- Quyết định có nên sử dụng thuốc để giảm nguy cơ ung thư vú hay không
- Tamoxifen và Raloxifene để giảm nguy cơ ung thư vú
- Thuốc ức chế aromatase để giảm nguy cơ ung thư vú
- Phẫu thuật phòng ngừa để giảm nguy cơ ung thư vú
Bác sĩ sẽ đánh giá và thảo luận từng trường hợp cụ thể trước khi thực hiện một trong các phương pháp trên nếu thấy cần thiết.
PHÁT HIỆN VÀ CHẨN ĐOÁN SỚM UNG THƯ VÚ
Ung thư vú đôi khi được phát hiện sau khi các triệu chứng xuất hiện, nhưng nhiều trường hợp ung thư vú không có triệu chứng. Do đó tầm soát ung thư vú định kỳ rất quan trọng để giúp phát hiện ung thư vú giai đoạn sớm.
Xét nghiệm tầm soát ung thư vú là gì?
Tầm soát (hay sàng lọc) là làm các xét nghiệm để tìm bệnh ở những người không có bất kỳ triệu chứng nào. Mục tiêu của tầm soát ung thư vú là phát hiện sớm, trước khi nó gây ra các triệu chứng (chẳng hạn như có thể sờ thấy khối u ở vú). Phát hiện sớm có nghĩa là tìm và chẩn đoán bệnh sớm hơn so với khi đợi các triệu chứng bắt đầu xuất hiện.
Ung thư vú được phát hiện qua các xét nghiệm tầm soát có nhiều khả năng nhỏ hơn và ít có khả năng lan ra ngoài vú. Kích thước của khối ung thư vú và mức độ lan rộng của nó là một số yếu tố quan trọng nhất trong việc dự đoán tiên lượng của bệnh.
1. Khuyến nghị của Hiệp hội Ung thư Hoa Kỳ để phát hiện sớm ung thư vú
Ung thư vú được phát hiện sớm, khi khối u còn nhỏ và chưa lan rộng sẽ dễ điều trị thành công hơn. Làm xét nghiệm tầm soát định kỳ là cách đáng tin cậy nhất để phát hiện sớm ung thư vú. Hiệp hội Ung thư Hoa Kỳ có hướng dẫn tầm soát dành cho phụ nữ có nguy cơ mắc ung thư vú trung bình và cao.
1.1. Khuyến nghị tầm soát của Hiệp hội Ung thư Hoa Kỳ dành cho phụ nữ có nguy cơ ung thư vú trung bình
Một phụ nữ được xem là có nguy cơ ung thư vú trung bình nếu không có: tiền sử cá nhân mắc bệnh ung thư vú, tiền sử gia đình mắc bệnh ung thư vú hoặc đột biến gen được biết là làm tăng nguy cơ ung thư vú (VD gen BRCA) và chưa xạ trị ngực trước 30 tuổi. (Xem bên dưới để biết hướng dẫn dành cho phụ nữ có nguy cơ cao.)
- Phụ nữ từ 40 đến 44 tuổi có thể bắt đầu tầm soát bằng chụp nhũ ảnh (X quang tuyến vú) hàng năm.
- Phụ nữ từ 45 đến 54 tuổi nên chụp nhũ ảnh hàng năm.
- Phụ nữ từ 55 tuổi trở lên có thể chụp nhũ ảnh hai năm một lần hoặc có thể tiếp tục chụp nhũ ảnh hàng năm. Việc tầm soát nên tiếp tục miễn là người phụ nữ có sức khỏe tốt và dự kiến sẽ sống thêm ít nhất 10 năm nữa.
- Tất cả phụ nữ cần được giải thích rõ về vai trò và khả năng của chụp nhũ ảnh trong tầm soát ung thư vú.
Khám vú lâm sàng không được khuyến khích để tầm soát ung thư vú ở phụ nữ có nguy cơ trung bình ở mọi lứa tuổi.
1.1.1. Chụp nhũ ảnh
Chụp nhũ ảnh là chụp X-quang tuyến vú. Chụp nhũ ảnh có thể giúp phát hiện ung thư vú ở giai đoạn đầu, khi điều trị có nhiều khả năng thành công nhất. Kỹ thuật này có thể giúp phát hiện những thay đổi ở vú có thể là ung thư trước nhiều năm khi các triệu chứng thực thể bắt đầu xuất hiện. Kết quả từ nhiều thập kỷ nghiên cứu cho thấy những phụ nữ chụp nhũ ảnh thường xuyên thì có nhiều khả năng phát hiện ung thư vú sớm hơn, và ít cần các phương pháp điều trị tích cực hơn như phẫu thuật cắt trọn vú và hóa trị, và cũng có nhiều khả năng khỏi bệnh hơn.
Cần lưu ý là chụp nhũ ảnh không phải là phương pháp tầm soát hoàn hảo vì nó có thể không phát hiện ra ung thư vú. Ngược lại, khi chụp nhũ ảnh phát hiện thấy có bất thường hay nghi ngờ thì bác sĩ có thể yêu cầu thêm xét nghiệm khác như siêu âm vú hoặc chụp thêm nhũ ảnh…
Chụp nhũ ảnh 2D và 3D
Gần đây, kỹ thuật hình chụp nhũ ảnh mới hơn thường được gọi là chụp nhũ ảnh ba chiều (3D) đã trở nên phổ biến hơn nhiều và thường có giá cao hơn chụp nhũ ảnh 2D.
Theo Hiệp hội Ung thư Hoa Kỳ (ACS) thì chụp nhũ ảnh 2D hay 3D cũng đều phù hợp để tầm soát ung thư vú.
1.1.2. Khám vú lâm sàng và tự khám vú
Nghiên cứu chưa cho thấy lợi ích rõ ràng của việc khám vú định kỳ do chuyên gia y tế thực hiện (khám lâm sàng vú) hoặc do chính phụ nữ thực hiện (tự khám vú). Thông thường, phụ nữ có thể phát hiện ra triệu chứng ung thư (ví dụ như khối u ở vú) qua các sinh hoạt thường ngày như tắm rửa hoặc mặc quần áo. Phụ nữ nên làm quen với hình dáng và cảm giác bình thường của bộ ngực và nên đi bác sĩ nếu có dấu hiệu bất thường.
Mặc dù theo Hiệp hội Ung thư Hoa Kỳ, khám vú lâm sàng định kỳ (bởi bác sĩ) hoặc tự khám vú không phải là bước tầm soát ung thư vú được khuyến nghị nhưng điều đó không có nghĩa là những thăm khám đó là không cần thiết. Ví dụ, trong một số trường hợp, đặc biệt đối với những phụ nữ có nguy cơ ung thư vú cao hơn mức trung bình, khám vú lâm sàng bởi bác sĩ vẫn là cần thiết, cùng với việc tư vấn về nguy cơ và cách phát hiện sớm ung thư vú.
1.2. Khuyến nghị tầm soát của Hiệp hội Ung thư Hoa Kỳ dành cho phụ nữ có nguy cơ cao
Những phụ nữ có nguy cơ cao bị ung thư vú nên chụp MRI vú và chụp nhũ ảnh hàng năm, thường bắt đầu khi 30 tuổi. Phụ nữ có nguy cơ bị ung thư vú cao là những người:
- Có nguy cơ mắc bệnh ung thư vú trong suốt cuộc đời khoảng 20% đến 25% hoặc cao hơn, theo các công cụ đánh giá nguy cơ chủ yếu dựa trên tiền sử gia đình
- Có đột biến gen BRCA1 hoặc BRCA2 đã biết (dựa trên kết quả xét nghiệm gen)
- Có người thân thế hệ thứ nhất (cha mẹ, anh chị em ruột hoặc con) bị đột biến gen BRCA1 hoặc BRCA2 và bản thân họ chưa được xét nghiệm di truyền
- Đã xạ trị ngực trước 30 tuổi
- Mắc hội chứng Li-Fraumeni, hội chứng Cowden hoặc hội chứng Bannayan-Riley-Ruvalcaba hoặc có người thân thế hệ thứ nhất mắc một trong những hội chứng này
Hiệp hội Ung thư Hoa Kỳ khuyến cáo không nên tầm soát MRI đối với những phụ nữ có nguy cơ mắc bệnh ung thư vú trong cuộc đời dưới 15%.
Nếu phải chụp MRI, thì nó là bổ sung chứ không phải thay thế cho chụp nhũ ảnh vì mặc dù MRI có nhiều khả năng phát hiện ung thư hơn chụp nhũ ảnh nhưng nó vẫn có thể bỏ sót một số bệnh ung thư mà chụp nhũ ảnh có thể phát hiện.
Hầu hết phụ nữ có nguy cơ cao nên bắt đầu tầm soát bằng MRI và chụp nhũ ảnh khi họ 30 tuổi và tiếp tục miễn là họ có sức khỏe tốt.
Công cụ dùng để đánh giá nguy cơ ung thư vú
Một số công cụ đánh giá nguy cơ có thể giúp các chuyên gia y tế ước tính nguy cơ ung thư vú của phụ nữ. Những công cụ này đưa ra ước tính sơ bộ về nguy cơ ung thư vú, dựa trên sự kết hợp của các yếu tố nguy cơ. Ước tính nguy cơ ung thư vú cũng có thể thay đổi theo thời gian.
Bác sĩ có thể thảo luận với phụ nữ về việc lựa chọn sử dụng công cụ đánh giá nguy cơ và kết quả đánh giá.
2. Các xét nghiệm hình ảnh để chẩn đoán ung thư vú
Có nhiều xét nghiệm hình ảnh khác nhau có thể được sử dụng để phát hiện và chẩn đoán ung thư vú. Nếu bác sĩ thấy có bất thường khi xem kết quả khi chụp nhũ ảnh hoặc nếu triệu chứng nghi ngờ ung thư vú, bác sĩ có thể sẽ yêu cầu làm thêm xét nghiệm để giúp chẩn đoán.
2.1. Chụp nhũ ảnh
Vì sao cần chụp nhũ ảnh?
Chụp nhũ ảnh là xét nghiệm hình ảnh tầm soát ở những phụ nữ không có triệu chứng hoặc ở những phụ nữ có các triệu chứng nghi ngờ ung thư. Chụp nhũ ảnh có thể phát hiện hoặc phát hiện sớm ung thư vú, khi nó còn nhỏ và thậm chí trước khi có thể sờ thấy khối u. Đây là lúc điều trị dễ nhất.
Mục đích của chụp nhũ ảnh là gì?
- Chụp nhũ ảnh tầm soát: để tìm kiếm các dấu hiệu ung thư vú ở những phụ nữ không có bất kỳ triệu chứng nào ở vú. Mỗi bên vú đều được chụp X- quang, thường từ 2 góc khác nhau.
- Chụp nhũ ảnh chẩn đoán: để quan sát vú khi có các triệu chứng ở vú hoặc nếu thấy điều gì đó bất thường trên kết quả chụp nhũ ảnh tầm soát. Khi đó gọi là chụp nhũ ảnh chẩn đoán. Góc chụp của chụp nhũ ảnh chẩn đoán có thể khác với khi chụp nhũ ảnh tầm soát, để có thêm hình ảnh của vú ở nhiều hướng khác nhau. Ngoài ra, chụp chụp nhũ chẩn đoán cũng được sử dụng để tầm soát những phụ nữ đã được điều trị ung thư vú trước đây.
Thấy gì khi chụp nhũ ảnh?
Chụp nhũ ảnh có thể cho thấy những vùng bất thường ở vú. Dù không thể biết chắc liệu vùng bất thường có phải là ung thư hay không, nhưng nó giúp bác sĩ đánh giá bước đầu và quyết định xem có cần làm thêm xét nghiệm (chẳng hạn như sinh thiết vú) hay không. Chụp nhũ ảnh có thể thấy một số bất thường của vú như:
- Vôi hóa
- Khối u ở vú
- Bất đối xứng
- Biến dạng
Chụp nhũ ảnh hoạt động như thế nào?
Chụp nhũ ảnh được thực hiện bằng một máy được thiết kế chỉ dành riêng để chụp mô vú bằng tia X. Máy chụp tia X với liều thấp hơn so với tia X thông thường dùng để chụp các cơ quan trong cơ thể như chụp X-quang phổi hoặc xương. Máy chụp nhũ ảnh có 2 tấm ép phẳng vú để các mô vú cách xa nhau, giúp cho hình ảnh rõ hơn và sử dụng ít tia X hơn.
Trước đây, chụp nhũ ảnh thường được in trên các tấm phim lớn. Ngày nay, chụp nhũ ảnh kỹ thuật số phổ biến hơn. Hình ảnh kỹ thuật số được ghi lại và lưu dưới dạng tập tin trong máy tính.
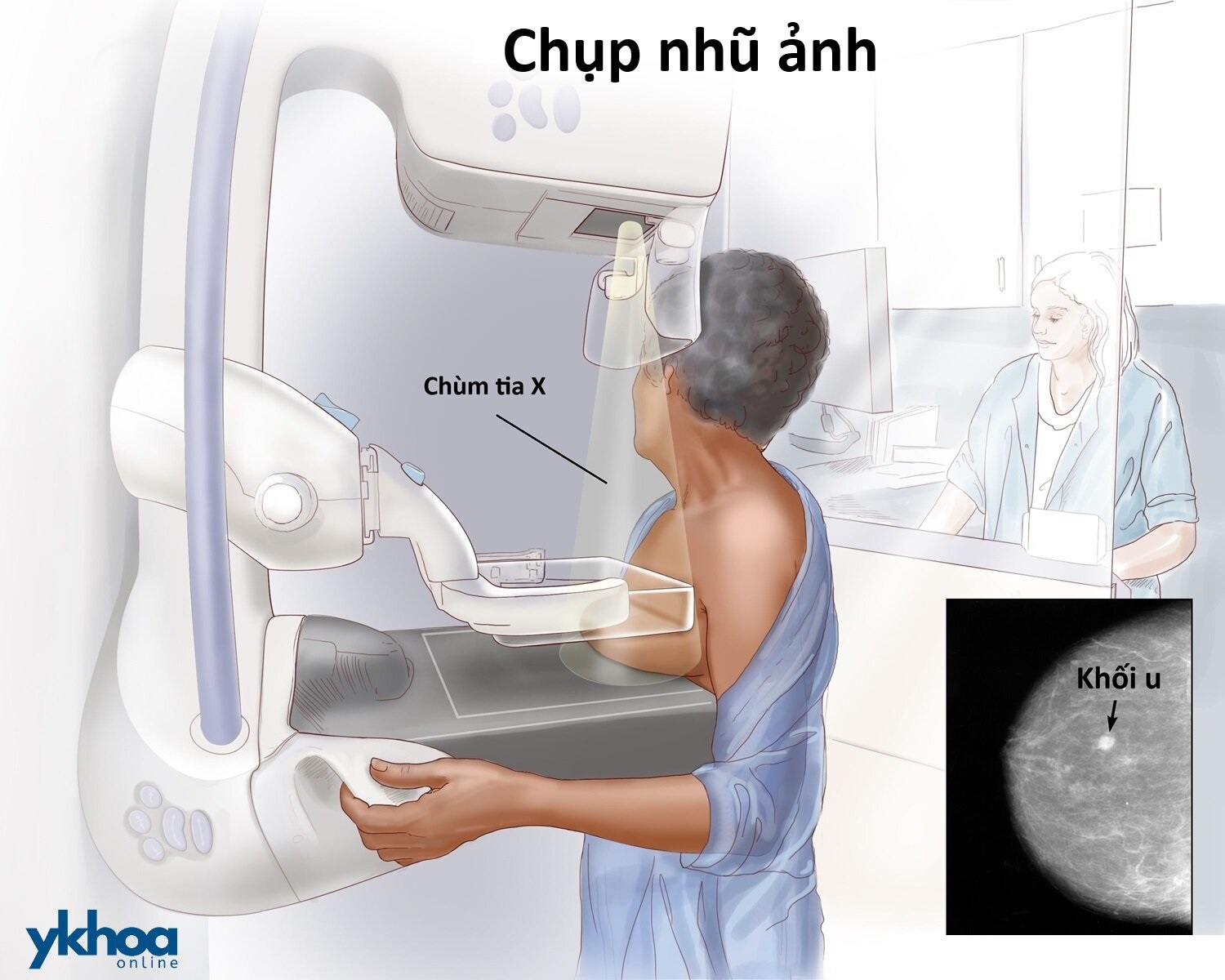
Minh họa chụp nhũ ảnh. Ảnh: cancer.gov
Chụp nhũ ảnh 3D (ba chiều) là gì?
Chụp nhũ ảnh 3D còn được gọi là chụp cắt lớp vú hoặc chụp cắt lớp vú kỹ thuật số. Đối với chụp nhũ ảnh 2D thông thường, khi chụp thì mỗi bên vú được ép từ hai góc khác nhau (một lần từ trên xuống dưới và một lần từ 2 bên). Nhưng đối với chụp nhũ ảnh 3D, máy sẽ chụp nhiều tia X liều thấp khi di chuyển theo một vòng cung nhỏ xung quanh vú. Sau đó, máy tính sẽ ghép các hình ảnh lại thành một loạt các lát cắt mỏng giúp nhìn rõ hơn mô vú trong không gian ba chiều.

Minh họa chụp nhũ ảnh 3D. Ảnh: broadwaymedicalclinic.com
Chụp nhũ ảnh có an toàn không?
Chụp nhũ ảnh làm vú tiếp xúc với một lượng nhỏ tia xạ. Nhưng lợi ích của chụp nhũ ảnh lớn hơn bất kỳ tác hại nào có thể xảy ra do tiếp xúc với tia xạ. Các máy móc hiện đại sử dụng liều tia xạ thấp để chụp X-quang vú có chất lượng hình ảnh cao. Trung bình, tổng liều cho một lần chụp nhũ ảnh thông thường với 2 góc chụp của mỗi bên vú là khoảng 0,4 millisieverts, hay mSv. (MSv là đơn vị đo liều bức xạ.) Liều bức xạ từ chụp nhũ ảnh 3D có thể dao động từ thấp hơn một chút đến cao hơn một chút so với chụp nhũ ảnh 2D thông thường.
Để hiểu rõ hơn về liều bức xạ, mỗi năm người dân ở Hoa Kỳ thường tiếp xúc với trung bình khoảng 3 mSv bức xạ từ môi trường tự nhiên, được gọi là bức xạ nền. Liều bức xạ được sử dụng để chụp nhũ ảnh tầm soát cả hai bên vú tương đương lượng bức xạ nền từ môi trường tự nhiên trong khoảng 7 tuần.
Nếu nghi ngờ có thể có thai, hãy cho bác sĩ và kỹ thuật viên chụp nhũ ảnh biết. Mặc dù nguy cơ đối với thai nhi là rất nhỏ và chụp nhũ ảnh thường được cho là an toàn trong thai kỳ, nhưng chụp nhũ ảnh tầm soát không được thực hiện thường quy ở phụ nữ mang thai không có nguy cơ ung thư vú cao.
Cần lưu ý gì trước khi chụp nhũ ảnh?
Nếu có thể, hãy đến cơ sở y tế chuyên chụp nhũ ảnh.
Cố gắng đến cùng một cơ sở mỗi lần để có thể dễ dàng so sánh kết quả chụp nhũ ảnh qua từng năm.
Trong trường hợp mới đến một cơ sở y tế lần đầu, hãy mang theo những giấy tờ liên quan (VD chỉ định cho chụp nhũ ảnh của bác sĩ, kết quả sinh thiết hoặc bất kỳ xét nghiệm nào khác liên quan đến vú) đã từng thực hiện trước đó.
Nếu trước đây đã chụp nhũ ảnh tại một cơ sở khác, nhớ mang theo phim và kết quả đến cơ sở mới để so sánh hình ảnh hiện tại và trước đây.
Nên lên lịch hẹn chụp nhũ ảnh vào thời điểm vú không bị đau hoặc sưng, để không có cảm giác quá khó chịu lúc chụp và để có được hình ảnh đẹp. Nên tránh chụp vào tuần lễ ngay trước kỳ kinh.
Vào ngày chụp, không thoa chất khử mùi, chất chống mồ hôi, phấn, kem dưỡng da, hoặc nước hoa dưới cánh tay, trên hoặc dưới ngực vì chúng có thể chứa các chất sẽ hiển thị trên phim chụp X-quang dưới dạng các đốm trắng.
Nên mặc váy hoặc quần sẽ thuận lợi hơn vì chỉ cần cởi áo và áo ngực để chụp nhũ ảnh
Nếu có bất kỳ thay đổi nào gần đây ở vú, hãy báo cho bác sĩ biết trước khi chụp nhũ ảnh vì khi đó có thể phải cần chụp nhũ ảnh chẩn đoán thay vì chụp nhũ ảnh tầm soát để có thể chụp rõ những vị trí đang nghi ngờ.
Cần khai báo với bác sĩ những thông tin tiền sử bệnh lý có thể ảnh hưởng đến nguy cơ ung thư vú, chẳng hạn như phẫu thuật, sử dụng hormone, tiền sử gia đình có người thân bị ung thư vú hoặc nếu bạn đã từng bị ung thư vú trước đây.
Những điều cần nói với kỹ thuật viên chụp nhũ ảnh?
Để có được kết quả chụp chất lượng tốt, hãy thông báo cho kỹ thuật viên:
- Về bất kỳ thay đổi hoặc đang có bất kỳ vấn đề nào ở vú
- Nếu có phẫu thuật thẩm mỹ
- Nếu gặp khó khăn khi đứng một mình (khi không có gậy chống)
- Nếu đang cho con bú hoặc nghĩ mình có thể đang mang thai.
- Nếu cảm thấy choáng váng hoặc chóng mặt khi chụp nhũ ảnh.
Những điều cần biết về quá trình chụp nhũ ảnh
Cần phải cởi áo và áo ngực để chụp nhũ ảnh.
Người được chụp và kỹ thuật viên sẽ là những người duy nhất trong phòng trong quá trình chụp nhũ ảnh.
Để có được hình ảnh chất lượng cao, vú cần bị ép lại. Sau khi đặt vú lên máy, kỹ thuật viên sẽ hạ tấm plastic phía trên xuống ép vú trong khoảng 10 đến 15 giây để chụp. Sau đó, vú sẽ được ép từ 2 bên để chụp tiếp.
Nếu chụp nhũ ảnh 3D thì quy trình cũng giống như trên, nhưng máy sẽ di chuyển theo một vòng cung nhỏ, ở phía trên vú hoặc dọc theo bên ngực, cho mỗi lần chụp. Kỹ thuật viên có thể yêu cầu người được chụp nín thở.
Toàn bộ quy trình mất khoảng 20 phút. Thời gian ép vú thực tế chỉ kéo dài khoảng 10 đến 15 giây cho mỗi hình. Vú bị ép có thể gây khó chịu hoặc đau. Hãy báo kỹ thuật viên nếu thấy đau để họ điều chỉnh lực ép sao cho thoải mái.
Nếu là chụp nhũ ảnh tầm soát thì mỗi bên vú sẽ được chụp hai góc. Nhưng đối với một số trường hợp như có túi độn ngực hoặc vú có kích thước lớn, thì có thể cần chụp nhiều ảnh hơn.
Chụp nhũ ảnh giúp phát hiện gì?
Bác sĩ X quang sẽ xem và đọc kết quả của phim chụp nhũ ảnh. Thông thường là xem vú có bị thay đổi hay có gì bất thường không, ví dụ như các đốm trắng nhỏ gọi là vôi hóa, các vùng bất thường gọi là khối u hay các bất thường khác có thể là dấu hiệu của ung thư.
Nếu có thể, bác sĩ sẽ so sánh phim chụp nhũ ảnh lần này với phim chụp nhũ ảnh cũ để xem có phát hiện nào mới không. Các thay đổi ở vú mà bác sĩ sẽ tìm kiếm bao gồm:
- Vôi hóa: là các cặn canxi nhỏ trong mô vú, nhìn giống như các đốm trắng nhỏ trên phim chụp nhũ ảnh, có thể do hoặc không do ung thư gây ra. Có 2 loại vôi hóa.
Vôi hóa đại thể: Các nốt vôi hóa có kích thước lớn, nhiều khả năng là do lão hóa động mạch vú, do chấn thương cũ hoặc do viêm. Các cặn lắng canxi này thường không phải do ung thư và không cần làm sinh thiết vú. Vôi hóa đại thể phổ biến hơn ở phụ nữ lớn tuổi (đặc biệt là sau 50 tuổi).
Vôi hóa vi thể: Là những đốm canxi nhỏ trong vú, thường đáng lo ngại hơn vôi hóa đại thể, nhưng không phải lúc nào cũng là bị ung thư. Hình dạng và vị trí xuất hiện của vôi hóa có (VD gần khối u) sẽ giúp bác sĩ X quang đánh giá trường hợp vôi hóa vi thể này có phải là do ung thư gây ra hay không.
Trong hầu hết các trường hợp, vôi hóa vi thể không cần phải kiểm tra bằng sinh thiết. Nhưng nếu nghi ngờ, bác sĩ cũng có thể cho làm sinh thiết vú để kiểm tra ung thư.
- Khối u trong vú: là vùng mô vú bất thường có hình dạng và các bờ ranh giới khiến nó trông khác so với phần còn lại của mô vú trên phim chụp nhũ ảnh. Khối u có thể có hoặc không có vôi hóa. Khối u có thể là dạng u nang (túi chứa dịch không phải ung thư), hoặc u đặc lành tính không phải ung thư (như u xơ tuyến vú, còn gọi là bướu sợi tuyến vú), hay cũng có thể là khối u ác tính (ung thư.)
U nang là túi chứa dịch. U nang đơn giản (túi chứa dịch có thành mỏng) không phải là ung thư và thường không cần phải kiểm tra bằng sinh thiết. Nếu khối u không phải là u nang đơn giản thì đáng ngại hơn, có thể cần sinh thiết để chắc chắn rằng đó không phải là ung thư.
Khối u đặc thì đáng lo hơn u nang, nhưng hầu hết các khối u đặc ở vú không phải là ung thư.
U nang và u đặc có thể có cảm giác giống nhau khi thăm khám bằng tay. Đôi khi nhìn cũng giống nhau trên phim chụp nhũ ảnh. Trong những trường hợp này, bác sĩ có thể cho siêu âm vú vì siêu âm có thể biết bên trong khối u là đặc hay chứa đầy dịch.
Nếu siêu âm vẫn khó phân biệt u đặc hay u nang thì có thể đưa một cây kim nhỏ vào khối u trong quá trình siêu âm để cố gắng hút dịch ra. Nếu khối u biến mất trên siêu âm khi dịch được hút ra, thì đó là u nang và không cần phải kiểm tra thêm.
Nếu khối u không phải là u nang đơn giản (nghĩa là có một phần khối u là đặc hoặc có điểm đáng nghi nào khác), thì có thể cần thêm các xét nghiệm hình ảnh để xem có phải là ung thư hay không. Ví dụ như theo dõi khối u có thay đổi theo theo thời gian hay không bằng chụp nhũ ảnh hoặc siêu âm thường xuyên, hoặc có thể làm sinh thiết.
- Bất đối xứng: hiện diện các vùng màu trắng nhìn thấy trên phim chụp nhũ ảnh khác với mô vú bình thường (ví dụ như vú bên kia). Có nhiều loại: bất đối xứng cục bộ, bất đối xứng đang tiến triển và bất đối xứng toàn bộ. Cần phải theo dõi hoặc cần làm thêm xét nghiệm hình ảnh chẩn đoán khác để loại trừ ung thư.
Chụp nhũ ảnh tầm soát hàng năm trên cùng một bệnh nhân (từ trái qua phải tương ứng phim chụp nhũ ảnh từ cũ nhất đến mới nhất) phát hiện hình ảnh bất đối xứng tiến triển, nghi ngờ là do ung thư. Ảnh: healthimaging.com
- Cấu trúc biến dạng: Một vùng mô vú bị biến dạng hoặc bị co kéo về một điểm nào đó. Nguyên nhân có thể là do vị trí của vú trong quá trình chụp nhũ ảnh, do chấn thương hoặc thủ thuật đã thực hiện trên vú trước đó và cũng có thể là dấu hiệu của ung thư vú.
- Mật độ mô vú: Chụp nhũ ảnh cũng giúp đánh giá mật độ vú. Mật độ mô vú là thông số đo lượng mô xơ và mô tuyến trong vú so với mô mỡ. Mật độ này không liên quan đến kích thước hoặc độ săn chắc của vú.
Mô vú được gọi là “đặc” nếu có nhiều mô xơ và mô tuyến hơn so với mô mỡ trong vú.
Khoảng một nửa số phụ nữ có mô vú đặc. Mô vú đặc không phải là bất thường, nhưng có nguy cơ mắc ung thư vú cao hơn một chút.
Mô vú đặc cũng có thể gây khó khăn trong việc phát hiện ung thư trên chụp nhũ ảnh. Nguyên nhân là do mô xơ và mô tuyến vú có màu trắng trên chụp nhũ ảnh, có thể che giấu hình ảnh khối u ác tính cũng có màu trắng. Tuy vậy, không cần làm thêm các xét nghiệm nào khác ngoài chụp nhũ ảnh ở những phụ nữ có mô vú đặc nhưng không có nguy cơ mắc ung thư vú (VD như có đột biến gen, tiền sử ung thư vú trong gia đình hoặc có các yếu tố nguy cơ khác).
Tìm hiểu kết quả chụp nhũ ảnh
Các bác sĩ sử dụng một hệ tiêu chuẩn gọi là Hệ thống dữ liệu và báo cáo hình ảnh vú (BIRADS: Breast Imaging Reporting & Data System) để mô tả những gì họ thấy trên phim chụp nhũ ảnh.
BIRADS là gì?
Là một hệ thống tiêu chuẩn để mô tả các phát hiện và kết quả chụp nhũ ảnh. BI-RADS sắp xếp các kết quả thành các mức độ được đánh số từ 0 đến 6.
Với cách phân độ này, bác sĩ có thể mô tả những gì họ nhìn thấy trên phim chụp nhũ ảnh bằng cùng một thuật ngữ. Điều này giúp việc trao đổi kết quả và theo dõi sau khi chụp nhũ ảnh thuận lợi hơn.
(Lưu ý: Phân độ theo BI-RADS cũng được sử dụng để mô tả kết quả siêu âm vú hoặc chụp MRI vú.)
Các mức độ theo BIRADS:
- BIRADS 0: Dữ liệu chưa đủ để kết luận chính xác, cần bổ sung thêm hình ảnh cũ để so sánh hoặc cần thêm xét nghiệm hình ảnh khác.
- BIRADS 1: Âm tính.
Đây là kết quả xét nghiệm bình thường. Vú trông giống nhau, không có khối u, cấu trúc không bị biến dạng hoặc vôi hóa đáng ngờ. Trong trường hợp này, âm tính có nghĩa là không phát hiện gì mới hoặc bất thường.
- BIRADS 2: Lành tính (không phải ung thư).
Trên phim nhũ ảnh cho thấy có một hay nhiều tổn thương lành tính như vôi hóa lành tính, hach bạch huyết, khối u lành tính.
- BIRADS 3: Có thể là lành tính – Đề nghị theo dõi trong thời gian ngắn.
Tổn thương xác định được trên hình ảnh có thể là lành tính, xác suất ác tính của tổn thương này dưới 2%. Bướu sợi tuyến vú thường được xếp vào nhóm này. Có hai lựa chọn trong trường hợp này là: sinh thiết ngay để có kết quả chắc chắn hoặc tái khám sau 6 tháng để đánh giá lại.
- BIRADS 4: Nghi ngờ ác tính, nên sinh thiết.
Phát hiện bất thường không chắc chắn giống ung thư nhưng có thể là ung thư. Bác sĩ X quang có thể đề nghị sinh thiết. BIRADS 4 có 3 phân độ:
4A: Khả năng ung thư là thấp (hơn 2% nhưng không quá 10%)
4B: Khả năng ung thư là trung bình (hơn 10% nhưng không quá 50%)
4C: Khả năng ung thư là cao (hơn 50% nhưng dưới 95%), không cao như BIRADS 5
- BIRADS 5: Rất có khả năng ác tính – Cần có biện pháp phù hợp.
Phát hiện bất thường giống như ung thư và có khả năng cao (ít nhất 95%) là ung thư. Cần phải làm sinh thiết.
- BIRADS 6: Khối u đã được sinh thiết và đã có kết quả xác định là ác tính (ung thư). Cần lên kế hoạch điều trị thích hợp.
Hạn chế của chụp nhũ ảnh
Chụp nhũ ảnh là phương pháp tầm soát ung thư vú tốt nhất hiện nay. Nhưng chụp nhũ ảnh cũng có những hạn chế. Ví dụ, chụp nhũ ảnh không chính xác 100% trong việc xác định có bị ung thư vú hay không; có thể bỏ sót một số loại ung thư và đôi khi phát hiện bất thường tưởng là ung thư nhưng hóa ra không phải là ung thư.
- Kết quả âm tính giả
Chụp nhũ ảnh âm tính giả là hình ảnh trông bình thường mặc dù có ung thư vú.
Phụ nữ có mô vú đặc có nhiều khả năng nhận được kết quả âm tính giả hơn.
Chụp nhũ ảnh âm tính giả có thể khiến phụ nữ có cảm giác an toàn sai lầm, nghĩ rằng họ không bị ung thư vú trong khi thực tế là họ bị.
Điều quan trọng là phải đi khám bác sĩ nếu có các triệu chứng mới ở vú, ngay cả khi đã chụp nhũ ảnh tầm soát gần đây cho kết quả bình thường. Có thể cần phải làm thêm các xét nghiệm như chụp nhũ ảnh chẩn đoán và/hoặc siêu âm vú để quan sát kỹ hơn vùng bất thường.
- Kết quả dương tính giả
Chụp nhũ ảnh dương tính giả là hình ảnh trông bất thường mặc dù không có ung thư vú. Chụp nhũ ảnh phát hiện bất thường thì thường đòi hỏi phải xét nghiệm thêm (chụp nhũ ảnh chẩn đoán, siêu âm và đôi khi là chụp MRI hoặc thậm chí là sinh thiết vú) để xem có phải là ung thư hay không.
Kết quả dương tính giả thường gặp hơn ở những phụ nữ trẻ, có mô vú đặc, đã từng sinh thiết vú, có người thân trong gia đình bị ung thư vú hoặc đang dùng estrogen.
- Chụp nhũ ảnh có thể không hữu ích cho tất cả phụ nữ
Giá trị của chụp nhũ ảnh tầm soát phụ thuộc vào sức khỏe tổng thể của phụ nữ. Phát hiện sớm ung thư vú có thể không giúp sống lâu hơn nếu bệnh nhân có bệnh lý nặng đi kèm như bệnh lý tim, thận, gan hoặc phổi. Hướng dẫn tầm soát ung thư vú của Hiệp hội Ung thư Hoa Kỳ nhấn mạnh rằng phụ nữ có các bệnh lý nặng đi kèm (bệnh đồng mắc) hoặc thời gian sống còn ngắn nên thảo luận với bác sĩ xem có nên tiếp tục chụp nhũ ảnh hay không.
Điều cần lưu ý là mặc dù chụp nhũ ảnh có thể phát hiện ra các khối u vú nhỏ khó có thể cảm nhận được bằng sờ nắn, nhưng việc điều trị khối u nhỏ không phải luôn luôn có thể chữa dứt vì có loại ung thư phát triển nhanh hoặc có thể đã di căn, ngay cả khi khối u ở vú vẫn còn nhỏ.
- Chẩn đoán quá mức và điều trị quá mức
Chụp nhũ ảnh tầm soát thường có thể phát hiện ung thư vú xâm lấn và ung thư ống tuyến vú tại chỗ (DCIS) cần được điều trị. Nhưng cũng có trường hợp một số loại ung thư xâm lấn và ung thư ống tuyến vú tại chỗ phát hiện trên chụp nhũ ảnh sẽ không bao giờ tiến triển hoặc lan rộng. Những loại ung thư này không đe dọa đến tính mạng và sẽ không bao giờ được phát hiện hoặc được điều trị nếu không chụp nhũ ảnh. Vấn đề là bác sĩ không thể phân biệt được những loại ung thư này với những loại ung thư sẽ tiến triển và lan rộng.
Chẩn đoán quá mức có thể dẫn đến điều trị quá mức (điều trị không thực sự cần thiết ), vì ung thư sẽ không bao giờ gây ra bất kỳ vấn đề nào. Bác sĩ không phải lúc nào cũng có thể biết loại ung thư nào có thể đe dọa hay không đe dọa tính mạng. Do đó bác sĩ khuyên nên điều trị tất cả các loại ung thư vú. Điều này khiến một số phụ nữ phải chịu tác dụng phụ của việc điều trị ung thư, mặc dù thực tế là không cần thiết.
Tuy nhiên, tỷ lệ chẩn đoán quá mức không cao, nhưng ước tính dao động từ 1% đến 10%.
- Phơi nhiễm tia xạ
Vì chụp nhũ ảnh là chụp bằng tia X (X- quang) nên vú có tiếp xúc với tia xạ. Lượng tia xạ từ mỗi lần chụp nhũ ảnh là thấp, nhưng vẫn có thể tăng lên theo thời gian.
2.2. Siêu âm vú
Siêu âm vú sử dụng sóng âm để tạo ra hình ảnh của mô vú. Siêu âm giúp phát hiện một số thay đổi ở vú, như u nang chứa đầy dịch mà có thể khó phát hiện bằng chụp nhũ ảnh.
Khi nào cần siêu âm vú?
Siêu âm vú thường không được sử dụng như một xét nghiệm tầm soát thường quy cho ung thư vú, nhưng có ích trong một số trường hợp như khối u (đặc biệt là những khối u có thể sờ thấy nhưng không nhìn thấy trên phim chụp nhũ ảnh). Siêu âm có thể hữu ích ở những phụ nữ có mô vú đặc, khiến việc nhìn thấy các vùng bất thường trên phim chụp nhũ ảnh trở nên khó khăn. Siêu âm cũng có thể được sử dụng để quan sát kỹ hơn vùng nghi ngờ được phát hiện trên phim chụp nhũ ảnh.
Siêu âm vú hữu ích vì nó có thể phân biệt giữa các khối u chứa đầy dịch như u nang và các khối u đặc.
Siêu âm cũng được dùng để hướng dẫn đưa kim sinh thiết chính xác vào một vùng của vú để lấy tế bào ra và xét nghiệm ung thư, hoặc trong sinh thiết các hạch bạch huyết phì đại ở vùng dưới cánh tay.
Siêu âm được sử dụng rộng rãi, dễ thực hiện, không tiếp xúc với tia xạ và ít tốn kém hơn các xét nghiệm hình ảnh khác.
Siêu âm vú được thực hiện như thế nào?
Thông thường, siêu âm được thực hiện bằng một dụng cụ cầm tay gọi là đầu dò. Đầu tiên, một loại gel được bôi lên da và/hoặc đầu dò, bác sĩ siêu âm sẽ di chuyển đầu dò trên bề mặt da vú. Siêu âm phát ra sóng âm và thu lại tiếng dội của sóng âm từ các mô vú sâu hơn dưới da. Những tiếng dội của sóng âm này sẽ tạo thành hình ảnh trên màn hình máy tính. Có thể cảm thấy chút áp lực khi đầu dò di chuyển xung quanh da, nhưng sẽ không đau.
Siêu âm vú tự động (ABUS: Automated breast ultrasound) là một lựa chọn tại một số trung tâm chẩn đoán hình ảnh. Kỹ thuật này sử dụng đầu dò lớn hơn nhiều để chụp hàng trăm hình ảnh bao phủ gần như toàn bộ vú. Siêu âm vú tự động thường được sử dụng để tầm soát cho những phụ nữ có mô vú đặc. Nó cũng có thể được sử dụng cho những phụ nữ có phát hiện bất thường trên các xét nghiệm hình ảnh khác hoặc có các triệu chứng ở vú. Đôi khi cần phải siêu âm đầu dò cầm tay lại nếu có phát hiện vùng bất thường khi siêu âm vú tự động để chụp thêm hình ảnh của vùng bất thường này.
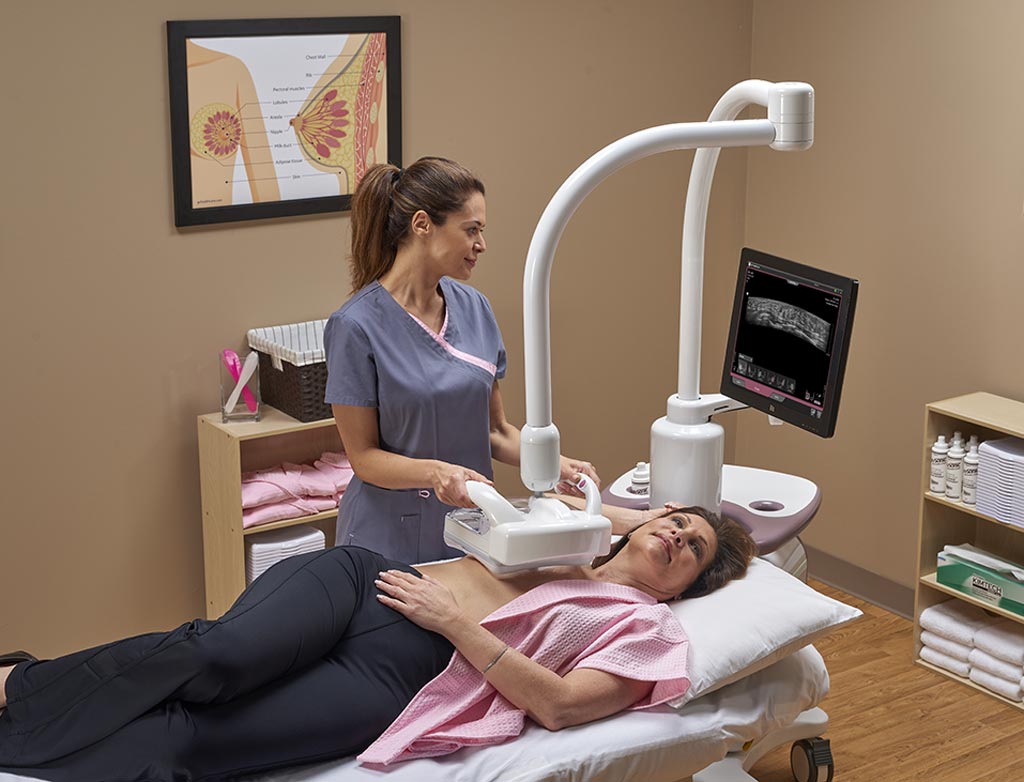
Siêu âm vú tự động. Ảnh: globetechcdn.com.
Kết quả siêu âm vú được ghi nhận như thế nào?
Các bác sĩ sử dụng cùng một hệ thống tiêu chuẩn để mô tả kết quả chụp nhũ ảnh, siêu âm vú và MRI vú là BIRADS, chia thành các mức độ đánh số từ 0 đến 6. Xem thêm chi tiết về BIRADS ở phần chụp nhũ ảnh.
2.3. Chụp MRI vú
Chụp MRI vú (chụp cộng hưởng từ) sử dụng sóng vô tuyến và nam châm mạnh để tạo ra hình ảnh chi tiết bên trong vú.
Khi nào cần chụp MRI vú?
MRI vú có thể được sử dụng trong các tình huống khác nhau như dưới đây.
- Để tầm soát: Đối với một số phụ nữ có nguy cơ mắc ung thư vú cao, nên chụp MRI vú tầm soát cùng với chụp nhũ ảnh hàng năm. MRI không được khuyến khích là xét nghiệm tầm soát riêng lẻ vì nó có thể bỏ sót một số loại ung thư mà chụp nhũ ảnh có thể phát hiện.
Mặc dù MRI có thể phát hiện một số loại ung thư không thấy trên chụp nhũ ảnh, nhưng nó cũng có khả năng cho kết quả dương tính giả, từ đó dẫn đến một số xét nghiệm và/hoặc sinh thiết không cần thiết. Đây là lý do tại sao MRI không được khuyến khích là xét nghiệm tầm soát cho những phụ nữ có nguy cơ mắc ung thư vú trung bình.
- Để chẩn đoán: Có thể chụp MRI để kiểm tra xem có phải là ung thư vú hay không trong trường hợp nghi ngờ ung thư vú (dựa trên các triệu chứng hoặc phát hiện khi khám, chẳng hạn như tiết dịch núm vú bất thường). Các xét nghiệm hình ảnh khác như chụp nhũ ảnh và siêu âm vú thường được thực hiện trước, nhưng MRI có thể được thực hiện nếu kết quả của các xét nghiệm hình ảnh này không rõ ràng.
- Để xác định mức độ ung thư vú: Nếu ung thư vú đã được chẩn đoán, đôi khi chụp MRI vú được thực hiện để giúp xác định kích thước và vị trí chính xác của ung thư, để tìm các khối u khác ở vú và để kiểm tra các khối u ở vú bên kia. MRI vú không phải lúc nào cũng hữu ích nên không phải mọi phụ nữ được chẩn đoán ung thư vú đều cần chụp MRI vú.
- Để kiểm tra rò rỉ túi độn ngực bằng silicon: Có thể sử dụng MRI vú để kiểm tra rò rỉ túi độn ngực bằng silicon. Lưu ý: MRI không được sử dụng cho những phụ nữ có túi độn ngực bằng nước muối.
Những điều cần biết về chụp MRI vú
Cũng giống như chụp nhũ ảnh được thực hiện bằng máy chụp X-quang được thiết kế riêng cho vú, chụp MRI vú cũng cần thiết bị đặc biệt. Máy chụp MRI vú có một thiết bị đặc biệt gọi là cuộn dây ngực chuyên dụng để chụp ảnh vú. Không phải tất cả các cơ sở y tế đều có thiết bị chụp MRI vú chuyên dụng. Nếu cần chụp MRI vú thì nên đến một cơ sở có thiết bị chuyên dụng và có thể thực hiện sinh thiết vú dưới sự hướng dẫn của MRI nếu cần.
MRI sử dụng nam châm mạnh thay vì bức xạ để tạo ra hình ảnh cắt ngang rất chi tiết của cơ thể. Máy quét MRI chụp ảnh từ nhiều góc độ, tạo ra nhiều lát cắt hình ảnh của cơ thể như nhìn từ phía trước, từ bên hoặc từ đỉnh đầu. MRI có thể tạo ra hình ảnh rõ nét của các mô mềm trong cơ thể, mà khó nhìn thấy bằng các xét nghiệm hình ảnh khác.
Không giống như chụp nhũ ảnh hoặc siêu âm vú, chụp MRI vú yêu cầu phải tiêm thuốc tương phản vào tĩnh mạch trước khi chụp để nhìn thấy rõ hơn những vùng bất thường ở vú.
Cần chuẩn bị gì trước khi chụp MRI vú?
Hãy tìm hiểu về vấn đề chi trả bảo hiểm y tế trước khi chụp MRI vì đây là xét nghiệm tốn kém.
- Làm theo hướng dẫn: Thường không cần ăn kiêng hoặc chuẩn bị gì đặc biệt trước khi chụp MRI, chỉ cần làm theo hướng dẫn.
- Nếu có vấn đề với không gian kín: Chụp MRI vú thường được thực hiện với tư thế nằm sấp bên trong một ống dài và hẹp với hai tay duỗi thẳng qua đầu. Nếu người có vấn đề khi ở trong một không gian chật hẹp thì có thể phải cần dùng thuốc an thần trong khi nằm trong máy chụp MRI. Hãy báo cho kỹ thuật viên MRI biết.
- Tháo bỏ các vật bằng kim loại: Trước khi chụp, kỹ thuật viên sẽ yêu cầu cởi đồ và mặc áo choàng hoặc quần áo khác không có khóa kéo hoặc kim loại. Hãy nhớ tháo những vật dụng đang mang, đeo bằng kim loại như kẹp tóc, đồ trang sức, dụng cụ nha khoa và khuyên xỏ trên cơ thể...
- Nếu có kim loại trong cơ thể: Trước khi quét, kỹ thuật viên sẽ hỏi xem có bất kỳ vật dụng, thiết bị bằng kim loại nào trong người không. Một số vật bằng kim loại sẽ không gây ra vấn đề, nhưng một số khác thì có thể.
Hãy cho kỹ thuật viên biết nếu có bất kỳ thiết bị nào được cấy ghép trong cơ thể vì có thể bị ảnh hưởng nếu chụp MRI như:
- Máy khử rung tim hoặc máy tạo nhịp tim
- Kẹp dùng cho phình động mạch não
- Cấy ghép ốc tai
- Stent kim loại (để nong) lòng mạch máu (như stent mạch vành)
Các bước chụp MRI vú như thế nào?
Chụp MRI thường được thực hiện tại bệnh viện hoặc phòng khám ngoại trú. Đầu tiên, một đường truyển tĩnh mạch sẽ được đặt ở cánh tay để có thể tiêm thuốc tương phản trong quá trình chụp.
Bệnh nhân nằm sấp trên một chiếc bàn phẳng hẹp với hai tay duỗi thẳng qua đầu. Ngực sẽ thòng xuống một lỗ trên bàn để không bị đè ép khi chụp. Kỹ thuật viên có thể sử dụng gối để giúp bạn thoải mái và không bị di chuyển. Sau đó, bàn sẽ trượt vào một ống dài và hẹp.
Chụp MRI không gây đau, nhưng phải nằm yên bên trong ống hẹp, có khi được yêu cầu nín thở hoặc giữ nguyên tư thế trong một số thời điểm. Máy có thể phát ra tiếng động, tiếng lách cách và tiếng vo ve… Một số cơ sở y tế có cung cấp nút nhét tai hoặc tai nghe để giúp đỡ ồn trong trong quá trình chụp.
Khi chụp MRI vú để tìm ung thư vú, có một chất tương phản tên là gadolinium được tiêm vào tĩnh mạch ở cánh tay để giúp hiển thị rõ vùng bất thường của mô vú. Chất này khác với thuốc tương phản được sử dụng trong chụp cắt lớp CT. Nếu đã từng bị di ứng với chất tương phản khi chụp các xét nghiệm chẩn đoán hình ảnh trước đây thì hãy cho kỹ thuật viên biết.
Mỗi bộ ảnh thường mất vài phút và toàn bộ quá trình chụp MRI thường mất khoảng 30 đến 45 phút. Sau khi chụp, có khi phải đợi thêm một lát để kỹ thuật viên kiểm tra hình ảnh, xem có cần chụp thêm không.
Đối với kỹ thuật MRI mới hơn, thì số lượng ảnh có thể chụp ít hơn, do đó quá trình quét mất ít thời gian hơn (thường khoảng 10 phút).
Kết quả MRI vú được ghi nhận như thế nào?
Các bác sĩ sử dụng cùng một hệ thống tiêu chuẩn để mô tả kết quả chụp nhũ ảnh, siêu âm vú và MRI vú là BIRADS, chia thành các mức độ đánh số từ 0 đến 6. Xem thêm chi tiết về BIRADS ở phần chụp nhũ ảnh.
2.4. Các xét nghiệm hình ảnh khác
Các xét nghiệm hình ảnh vú được sử dụng phổ biến nhất hiện nay là chụp nhũ ảnh, siêu âm và chụp MRI vú. Các xét nghiệm hình ảnh khác hạn như chụp CT, chụp xương hoặc chụp PET đôi khi được thực hiện để xem ung thư vú đã di căn hay chưa.
Đối với chụp cắt lớp phát xạ positron (PET: positron emission tomography), có một chất đánh dấu phóng xạ sẽ được tiêm vào máu, thường được sử dụng là một dạng đường phóng xạ có tên gọi là FDG (Fluoro-Deoxy-Glucose). PET được thực hiện nếu nghi ngờ ung thư vú có thể đã di căn sang các cơ quan khác trong cơ thể. Một loại chất đánh dấu phóng xạ mới hơn, là fluoroestradiol F-18, hiện đã có sẵn để chụp PET tìm di căn ung thư vú tiến triển dương tính với thụ thể estrogen (ER).
3. Các dấu hiệu và triệu chứng của ung thư vú
Mặc dù việc tầm soát ung thư vú thường xuyên là quan trọng, nhưng chụp nhũ ảnh không phát hiện ra mọi loại ung thư vú. Do đó, việc tự nhận biết bất kỳ thay đổi nào ở vú và biết được các dấu hiệu và triệu chứng của ung thư vú là rất quan trọng.
Triệu chứng phổ biến nhất của ung thư vú là một khối u mới xuất hiện (mặc dù hầu hết các khối u ở ngực không phải là ung thư). Một khối u cứng, không đau có các bờ không đều có nhiều khả năng là ung thư, nhưng ung thư vú cũng có thể mềm, tròn, nhạy cảm hoặc thậm chí gây đau.
Các triệu chứng khác có thể có của ung thư vú bao gồm:
- Sưng toàn bộ hoặc một phần vú (kể cả khi không sờ thấy khối u)
- Da có những vết lõm (trông giống như vỏ cam)
- Đau vú hoặc núm vú
- Núm vú thụt vào trong
- Núm vú hoặc da vú đỏ, khô, bong tróc hoặc dày lên
- Tiết dịch núm vú (không phải sữa mẹ)
- Sưng to hạch bạch huyết dưới cánh tay hoặc gần xương đòn (Đôi khi đây có thể là dấu hiệu của ung thư vú di căn ngay cả trước khi khối u ở vú đủ lớn để sờ thấy.)
Nhiều triệu chứng trong số này cũng có thể do các bệnh lành tính (không phải ung thư) ở vú gây nên. Quan trọng là phải kiểm tra bất kỳ khối u nào xuất hiện, hoặc bất kỳ thay đổi nào ở vú với chuyên gia y tế.
Cần lưu ý là tự thăm khám và nhận biết sự thay đổi của vú không thể thay thế cho việc tầm soát ung thư vú định kỳ. Chụp nhũ ảnh tầm soát có thể giúp phát hiện sớm ung thư vú, trước khi có bất kỳ triệu chứng nào xuất hiện. Phát hiện sớm ung thư vú sẽ có cơ hội điều trị thành công cao hơn.
4. Sinh thiết
Nếu các triệu chứng ở vú hoặc kết quả xét nghiệm hình ảnh (như chụp nhũ ảnh) cho thấy có thể bị ung thư vú, bác sĩ có thể chỉ định sinh thiết vú.
Sinh thiết vú là gì?
Sinh thiết vú là thủ thuật được thực hiện để lấy một phần mô vú hoặc khối u, được gọi là mẫu. Trong quá trình sinh thiết, bác sĩ sẽ lấy mẫu từ vùng nghi ngờ ung thư để gửi phòng thí nghiệm xem mẫu mô có chứa tế bào ung thư hay không.
Cần làm sinh thiết vú không có nghĩa là chắc chắn bị ung thư, mà chỉ là nghi ngờ ung thư. Sinh thiết là cách duy nhất để chẩn đoán xác định là ung thư.
Các loại sinh thiết vú
Có nhiều loại sinh thiết vú khác nhau. Bác sĩ sẽ chỉ định loại sinh thiết tùy vào các yếu tố:
- Bất thường ở vú qua thăm khám lâm sàng
- Kích thước khối u
- Vị trí khối u
- Có nhiều vùng nghi ngờ ung thư không
- Sức khỏe tổng thể của bệnh nhân
- Lựa chọn của bệnh nhân
Có các loại sinh thiết như sau:
- Chọc hút bằng kim nhỏ (FNA: Fine Needle Aspiration)
- Sinh thiết bằng kim lõi (CNB: Core Needle Biospy)
- Sinh thiết bằng phẫu thuật
- Sinh thiết hạch bạch huyết
4.1. Chọc hút bằng kim nhỏ (FNA)
Thủ thuật này thường được thực hiện nếu vùng nghi ngờ có khả năng là một túi chứa đầy dịch (u nang). Dùng kim hút bỏ dịch có thể giúp giảm đau do u nang. Chọc hút bằng kim nhỏ cũng có thể hữu ích nếu bác sĩ không chắc chắn liệu vùng nhìn thấy trên hình ảnh là u nang hay u đặc.
Trong thủ thuật chọc hút bằng kim nhỏ, bác sĩ sử dụng một cây kim rỗng rất nhỏ gắn vào ống tiêm để rút (hút) một lượng nhỏ mô vú hoặc dịch từ một vùng khả nghi để kiểm tra.
Nếu có thể cảm nhận được vùng cần sinh thiết, bác sĩ có thể vừa cảm nhận vừa đưa kim vào.
Nếu khó cảm nhận khối u (ví dụ khối u nằm sâu trong mô vú), bác sĩ có thể đưa kim vào chọc hút theo hướng dẫn của siêu âm. Đây được gọi là chọc hút bằng kim nhỏ có siêu âm hướng dẫn.
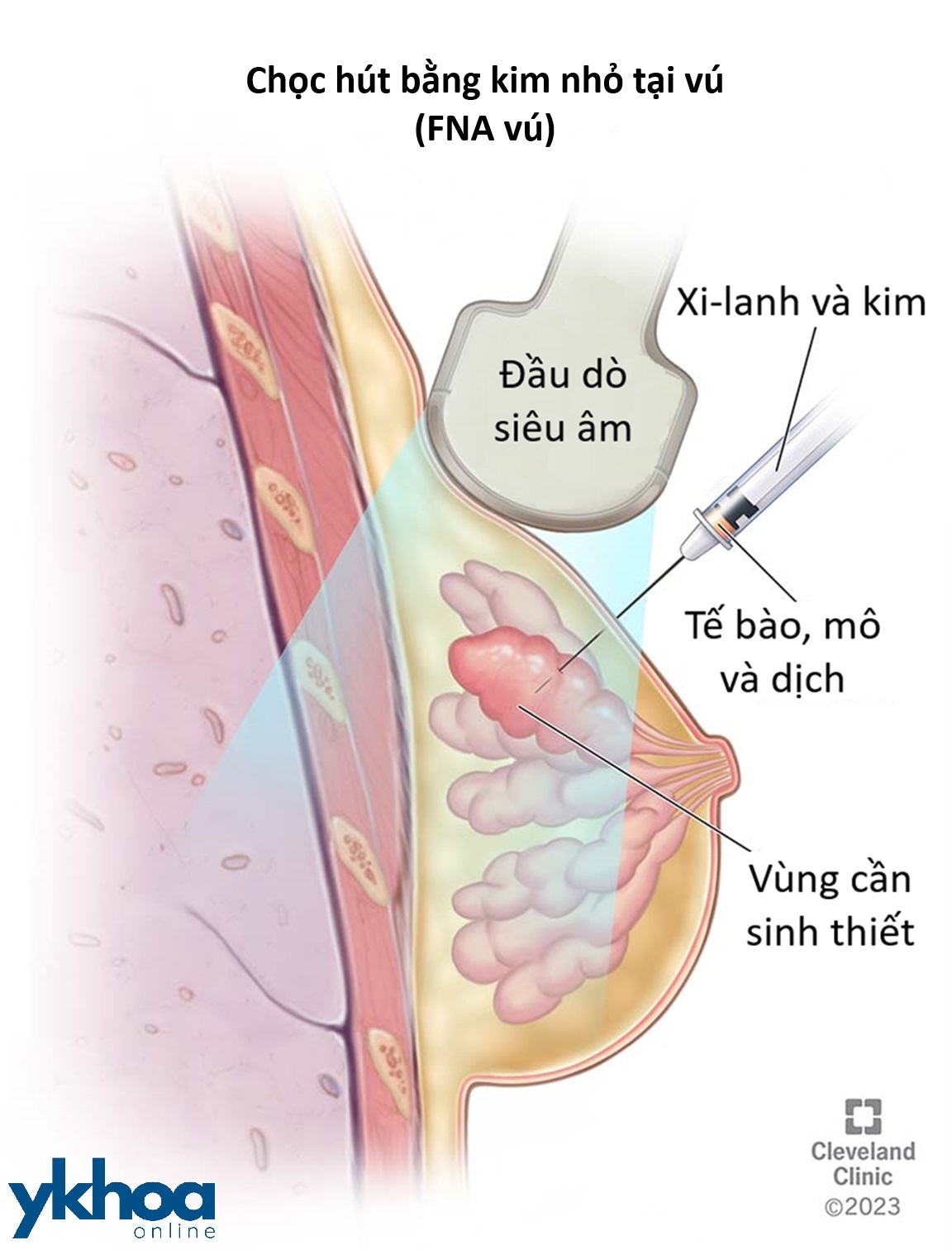
Minh họa thủ thuật chọc hút bằng kim nhỏ (FNA) có siêu âm hướng dẫn. Ảnh: clevelandclinic.org
Mẫu được chọc hút bằng kim nhỏ sau đó sẽ được kiểm tra xem có tế bào ung thư không. Một nhược điểm của FNA là nó chỉ chọc hút một lượng nhỏ mô và tế bào, vì vậy mẫu thường cần được kiểm tra ngay dưới kính hiển vi để tránh phải lấy thêm mẫu.
Các bước tiến hành
FNA là một thủ thuật ngoại trú (không cần nằm viện). Bác sĩ có thể dùng hay không dùng thuốc gây tê tại chỗ tùy từng trường hợp vì kim dùng để sinh thiết rất nhỏ nên việc dùng kim tiêm thuốc gây tê có khi còn đau hơn cả khi sinh thiết.
Bạn sẽ nằm ngửa và nằm im khi bác sĩ thực hiện FNA.
Có thể cảm thấy một chút áp lực từ đầu dò nếu bác sĩ có sử dụng siêu âm hướng dẫn. Sau đó bác sĩ sẽ đưa kim vào vùng cần chọc hút sinh thiết. Khi kim đã vào đúng vị trí, bác sĩ sẽ sử dụng ống tiêm để kéo ra một lượng nhỏ mô và/hoặc dịch. Có thể lặp lại thao tác này vài lần để lấy một số mẫu. Sau khi hoàn tất thủ thuật, vùng đó sẽ được băng hoặc gạc vô trùng.
Chọc hút để lấy một mẫu sinh thiết thường mất khoảng 15 giây. Toàn bộ quy trình từ đầu đến cuối thường mất khoảng 20 đến 30 phút nếu có siêu âm hướng dẫn.
Sau khi làm FNA
Bác sĩ hoặc y tá sẽ hướng dẫn cách chăm sóc vùng đã làm sinh thiết, những việc có thể làm và những việc cần tránh trong thời gian chờ vết thương lành lại. Hoạt động gắng sức có thể được yêu cầu phải hạn chế trong khoảng một ngày, sau đó có thể quay lại bình thường.
Đôi khi, sinh thiết gây chảy máu, bầm tím hoặc sưng tấy, làm cho khối u ở vú trông to hơn sau khi sinh thiết. Thông thường, không cần lo lắng về điều này và tình trạng bầm tím và sưng tấy sẽ biến mất theo thời gian. Bác sĩ hoặc y tá sẽ hướng dẫn những điều lưu ý và khi nào thì cần liên lạc bác sĩ.
Biết được gì khi làm thủ thuật chọc hút bằng kim nhỏ?
Bác sĩ giải phẫu bệnh sẽ xem xét mẫu mô hoặc dịch sinh thiết để tìm xem có tế bào ung thư trong đó không.
Ưu điểm chính của thủ thuật này là nhanh, thường không cần gây tê và không cần rạch da, do đó không cần khâu và không để lại sẹo. Ngoài ra, trong một số trường hợp, có thể có ngay kết quả ngay trong ngày.
Tuy nhiên, đôi khi có thể bỏ sót ung thư nếu kim không đi đúng vào vùng có tế bào ung thư hoặc nếu không lấy đủ tế bào. Ngay cả khi tìm thấy ung thư, lượng tế bào ung thư được chọc hút bằng kim nhỏ cũng có thể không đủ để thực hiện một số xét nghiệm khác nếu cần.
Nếu kết quả chọc hút sinh thiết bằng kim nhỏ không đưa ra chẩn đoán rõ ràng hoặc nếu bác sĩ vẫn còn lo ngại, có thể bác sĩ sẽ chỉ định một loại sinh thiết rộng hơn, như sinh thiết bằng kim lõi hoặc sinh thiết bằng phẫu thuật.
4.2. Sinh thiết bằng kim lõi
Nếu xét nghiệm hoặc chẩn đoán hình ảnh nghi ngờ ung thư vú, bác sĩ có thể chỉ định làm sinh thiết bằng kim lõi. Đây là loại sinh thiết thường được sử dụng nếu nghi ngờ ung thư vú, vì nó lấy được nhiều mô vú hơn so với chọc hút bằng kim nhỏ mà không cần phẫu thuật.
Với thủ thuật này, bác sĩ sử dụng kim rỗng để lấy các mảnh mô vú từ vùng nghi ngờ mà bác sĩ đã cảm nhận khi khám hoặc đã thấy trên xét nghiệm hình ảnh. Kim được gắn vào một lò xo để có thể di chuyển ra vào mô vú nhanh chóng hoặc có thể được gắn vào một thiết bị hút giúp hút kéo mô vú vào kim (được gọi là sinh thiết lõi có hút chân không).
Mỗi lần sẽ lấy một mẫu mô hình trụ nhỏ (lõi). Thường bác sĩ sẽ lấy nhiều mẫu mô.
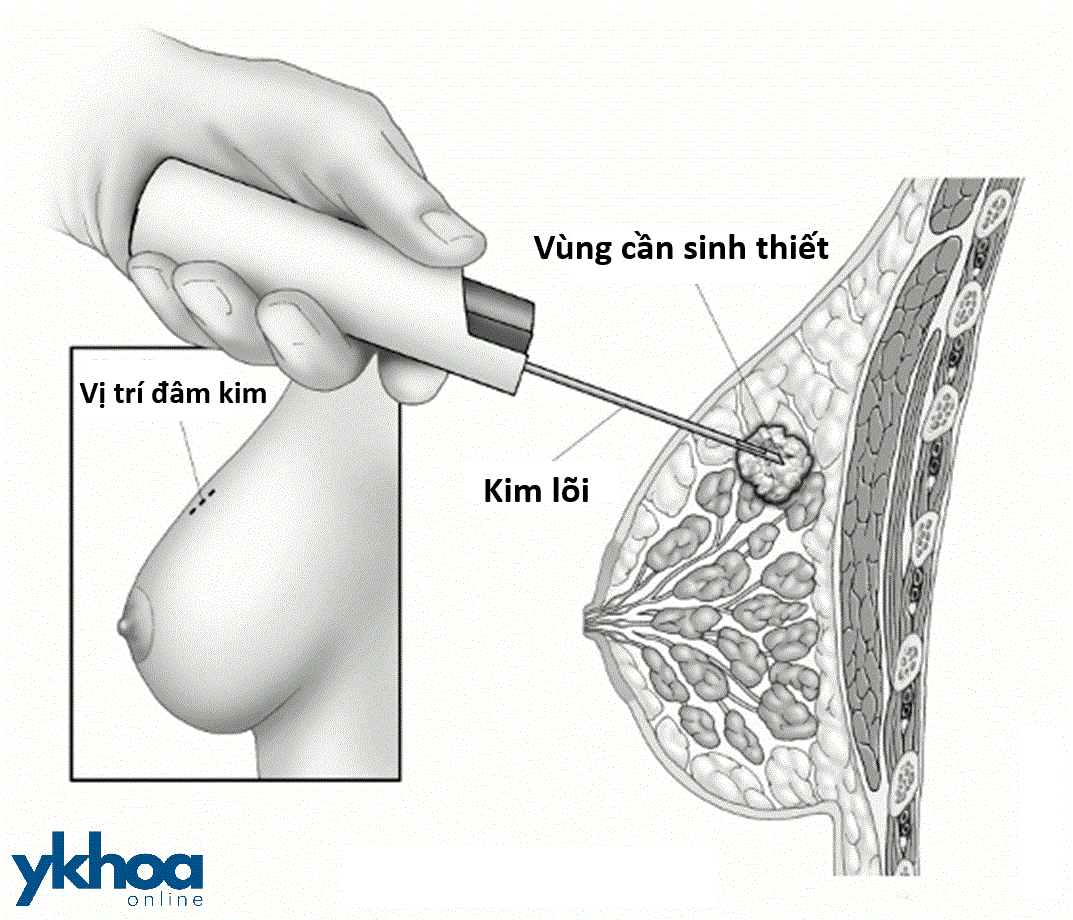
Sinh thiết vú bằng kim lõi. Ảnh: cancer.org
Bác sĩ có thể đưa kim vào vùng bất thường bằng cách sờ khối u. Nhưng cũng có thể bác sĩ sẽ sử dụng một số loại xét nghiệm hình ảnh để hướng dẫn kim vào đúng vị trí như chụp nhũ ảnh (hoặc chụp cắt lớp vú), MRI hay siêu âm vú.
Các bước thực hiện
Đây là thủ thuật ngoại trú, không cần nhập viện. Bản thân thủ thuật này thường khá nhanh, nhưng có thể mất nhiều thời gian hơn nếu cần có xét nghiệm hình ảnh hỗ trợ hoặc tiến hành loại sinh thiết bằng kim lõi đặc biệt.
Nếu sinh thiết bằng kim lõi được thực hiện bằng hướng dẫn hình ảnh, tư thế của bệnh nhân tùy thuộc vào loại xét nghiệm hình ảnh được sử dụng.
Đầu tiên bác sĩ sẽ tiêm thuốc tê vào khu vực cần sinh thiết, đôi khi sau đó cần rạch một vết nhỏ trên da vú (khoảng 5-6mm). Kim sinh thiết được đưa vào mô vú thông qua vết cắt này để lấy mẫu mô. Bác sĩ sẽ đưa kim vào, có thể cùng với hướng dẫn của các xét nghiệm hình ảnh để giúp kim đến đúng vị trí để lấy mẫu mô.
Thường sau đó, bác sĩ sẽ đưa vào một dụng cụ nhỏ (kẹp) để đánh dấu vùng sinh thiết. Kẹp đánh dấu này sẽ hiển thị trên phim chụp nhũ ảnh hoặc các xét nghiệm hình ảnh khác, giúp xác định vị trí chính xác của khu vực cần điều trị thêm (nếu cần) hoặc để theo dõi. Kẹp này sẽ ở nguyên vị trí và an toàn khi chụp MRI.
Thường không cần khâu sau khi rút kim, nhưng có thể phải ấn trong thời gian ngắn để giúp hạn chế chảy máu. Sau đó, băng lại bằng băng vô trùng.
Sau khi sinh thiết bằng kim lõi
Hoạt động gắng sức có thể được yêu cầu phải hạn chế trong khoảng một ngày, sau đó có thể quay lại bình thường.
Thủ thuật này có thể gây chảy máu, bầm tím hoặc sưng tấy, làm cho khối u ở vú trông lớn hơn sau khi sinh thiết. Thường không cần quá lo lắng về điều này và vết bầm tím hay sưng sẽ biến mất theo thời gian. Bác sĩ hoặc y tá sẽ hướng dẫn những điều lưu ý và khi nào thì cần liên lạc bác sĩ.
Sinh thiết bằng kim lõi thường không để lại sẹo.
Biết được gì khi làm thủ thuật sinh thiết bằng kim lõi?
Bác sĩ giải phẫu bệnh sẽ kiểm tra mô sinh thiết dưới kính hiển vị để xem có tế bào ung thư trong đó không. Sinh thiết bằng kim lõi thường giúp phát hiện nếu có tế bào ung thư và cũng cung cấp đủ mẫu nếu cần thêm xét nghiệm khác. Tuy nhiên, nó vẫn có thể bỏ sót một số loại ung thư.
Nếu kết quả sinh thiết bằng kim lõi không đưa ra chẩn đoán rõ ràng hoặc nếu vẫn còn nghi ngời, bác sĩ có thể chỉ định làm lại sinh thiết bằng kim lõi, hoặc chỉ định loại sinh thiết khác rộng hơn như sinh thiết bằng phẫu thuật.
4.3. Sinh thiết bằng phẫu thuật
Nếu kết quả sinh thiết kim (kim nhỏ hoặc kim lõi) không rõ ràng, có thể bác sĩ sẽ cho chỉ định sinh thiết bằng phẫu thuật (đôi khi được gọi là sinh thiết mở).
Đối với loại sinh thiết này, phẫu thuật được sử dụng để cắt bỏ toàn bộ hoặc một phần của vùng nghi ngờ để kiểm tra xem có tế bào ung thư hay không.
Có 2 loại sinh thiết bằng phẫu thuật:
Sinh thiết một phần: chỉ cắt đi một phần khối u hoặc vùng mô vú bất thường.
Sinh thiết trọn: Cắt bỏ toàn bộ khối u hoặc vùng bất thường và một phần vùng mô bình thường xung quanh khối u (bờ hay viền khối u).
Các bước tiến hành
Sinh thiết bằng phẫu thuật thường phải gây tê tại chỗ hoặc gây mê toàn thân.
Bác sĩ phẫu thuật sẽ rạch da vú và cắt bỏ vùng mô nghi ngờ, sau đó khâu lại và băng vết thương bằng băng vô trùng.
Sau khi sinh thiết phẫu thuật
Sinh thiết bằng phẫu thuật có thể gây chảy máu, bầm tím hoặc sưng, có thể khiến vú to và sưng hơn sau phẫu thuật sinh thiết. Thường thì vết bầm tím và sưng sẽ biến mất theo thời gian. Bác sĩ hoặc y tá sẽ hướng dẫn cách chăm sóc vị trí sinh thiết phẫu thuật, và thời gian và mức độ cần hạn chế các hoạt động cũng như khi nào thì cần liên hệ bác sĩ nếu có vấn đề bất thường.
Sinh thiết bằng phẫu thuật có thể để lại sẹo. Hình dạng vú có thể thay đổi tùy thuộc vào lượng mô vú được cắt bỏ.
Biết được gì khi sinh thiết bằng phẫu thuật?
Bác sĩ giải phẫu bệnh sẽ kiểm tra mẫu mô được sinh thiết bằng phẫu thuật dưới kính hiển vi xem có tế bào ung thư không.
Hãy hỏi bác sĩ khi nào có kết quả sinh thiết. Các bước tiếp theo sẽ phụ thuộc vào kết quả sinh thiết.
Nếu không tìm thấy tế bào ung thư trong sinh thiết, bác sĩ sẽ trao đổi xem có cần làm thêm xét nghiệm khác không, thời điểm cần chụp nhũ ảnh tiếp theo và hẹn lần tái khám tới…
Nếu phát hiện thấy có tế bào ung thư, có thể bác sĩ sẽ yêu cầu làm thêm xét nghiệm khác để nhận biết loại ung thư và vạch kế hoạch điều trị phù hợp nhất. Có thể bác sĩ cũng sẽ đề nghị hội chẩn với bác sĩ chuyên khoa khác.
4.4. Sinh thiết hạch bạch huyết
Nếu ung thư vú lan rộng, trước tiên nó thường di căn đến các hạch bạch huyết gần đó, dưới cánh tay (nhóm hạch nách). Đôi khi di căn đến các hạch bạch huyết gần xương đòn hoặc gần xương ức (phần giữa phía trước của ngực). Biết được ung thư đã di căn đến các hạch bạch huyết hay chưa sẽ giúp đưa ra hướng điều trị tốt nhất.
Cắt bỏ một hoặc nhiều hạch bạch huyết dưới cánh tay (hạch nách) và kiểm tra trong phòng thí nghiệm để đánh giá xem ung thư đã di căn ra ngoài vú hay chưa. Việc này cũng giúp đánh giá giai đoạn của ung thư vú. Nếu các hạch bạch huyết có tế bào ung thư, thì khả năng tế bào ung thư cũng di căn xa đến các bộ phận khác của cơ thể sẽ cao hơn. Có thể thực hiện thêm các xét nghiệm hình ảnh nếu trường hợp này xảy ra.
Có thể cắt bỏ hạch bạch huyết theo nhiều cách khác nhau, tùy thuộc vào việc có hạch bạch huyết nào bị to ra không, khối u vú lớn đến mức nào và các yếu tố khác.
Sinh thiết hạch phì đại
Nếu bất kỳ hạch bạch huyết nào dưới cánh tay hoặc xung quanh xương đòn sưng to ra, thì có thể sinh thiết kim: chọc hút bằng kim nhỏ (FNA) hoặc sinh thiết bằng kim lõi. Trường hợp phẫu thuật để cắt bỏ hạch phì đại thì ít phổ biến hơn. Nếu phát hiện ung thư ở hạch bạch huyết, sẽ cần cắt bỏ nhiều hạch hơn.
Các loại phẫu thuật hạch bạch huyết
Các hạch bạch huyết lân cận cần được kiểm tra xem ung thư đã xâm lấn hay chưa, kể cả khi chúng không phì đại. Có 2 cách để kiểm tra:
- Sinh thiết hạch bạch huyết gác cửa: chỉ cắt bỏ một vài hạch.
- Cắt bỏ hạch nách: trong một số trường hợp, có thể cần phải cắt bỏ nhiều hạch hơn.
Cắt bỏ hạch bạch huyết thường được thực hiện trong ca phẫu thuật cắt bỏ khối u ung thư vú, nhưng cũng có khi được thực hiện như một ca phẫu thuật riêng biệt.
Sinh thiết hạch bạch huyết gác cửa
Bác sĩ phẫu thuật sẽ tìm và cắt bỏ hạch bạch huyết đầu tiên mà ung thư có khả năng di căn đến (gọi là hạch gác cửa hay gác cổng). Trong thủ thuật này, có một chất sẽ được tiêm vào khối u, vùng xung quanh khối u hoặc vùng xung quanh núm vú. Có thể thực hiện bằng:
- Chất phóng xạ và/hoặc thuốc nhuộm màu xanh, HOẶC
- Dung dịch chứa các hạt oxit sắt
Các mạch bạch huyết sẽ mang những chất này theo cùng một con đường mà ung thư có khả năng di căn. Hạch bạch huyết đầu tiên mà chất này di chuyển đến sẽ là hạch gác cửa.
Sau khi tiêm chất này, có thể xác định được hạch gác cửa bằng cách:
- Sử dụng một máy đặc biệt để phát hiện phóng xạ hoặc các hạt oxit sắt trong các hạch
- Tìm kiếm các hạch đã chuyển sang màu xanh (hoặc nâu nếu sử dụng dung dịch chứa các hạt oxit sắt)
Đôi khi, cả hai phương pháp đều được sử dụng.
Kế đến, bác sĩ phẫu thuật sẽ rạch vùng da phía trên và cắt bỏ hạch bạch huyết gác cửa.
Hạch gác cửa bị cắt bỏ sẽ được gửi đến bác sĩ giải phẫu bệnh để kiểm tra xem có chứa tế bào ung thư không. Nhiều khi xét nghiệm giải phẫu bệnh này được thực hiện ngay trong quá trình phẫu thuật. Lý do là nếu phát hiện thấy ung thư hiện diện trong hạch bạch huyết gác cửa, thì có khả năng ung thư cũng đã xâm lấn các hạch bạch huyết khác lân cận. Khi đó, bác sĩ phẫu thuật có thể cắt luôn hạch nách khi bệnh nhân vẫn còn đang trên bàn mổ. Còn nếu không thấy tế bào ung thư trong các hạch gác cửa tại thời điểm phẫu thuật hoặc nếu bác sĩ giải phẫu bệnh không thể kiểm tra tại thời điểm phẫu thuật, thì chúng sẽ được kiểm tra kỹ hơn trong vài ngày tiếp theo.
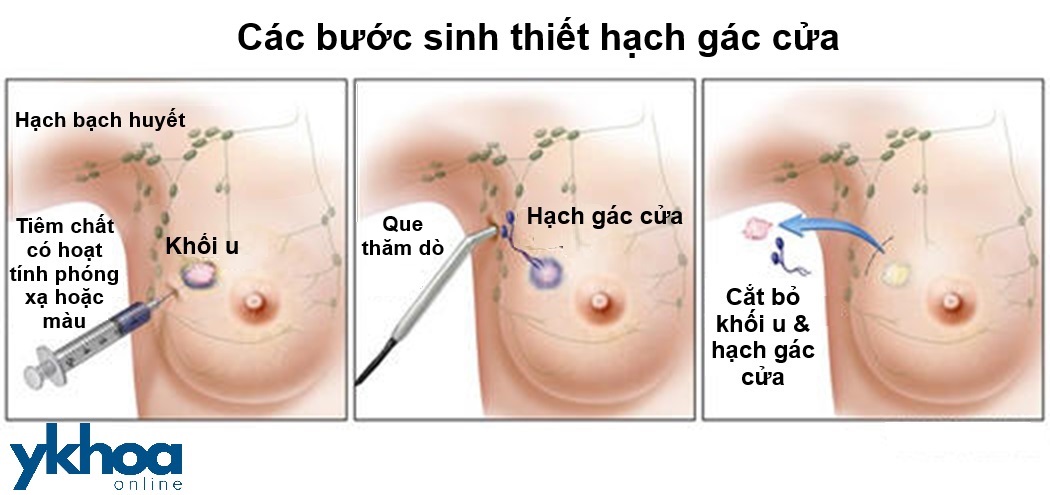 Các bước sinh thiết hạch gác cửa tại vú: Một chất phóng xạ và/hoặc thuốc nhuộm màu xanh được tiêm gần khối u. Chất được tiêm vào được định vị bằng mắt thường và/hoặc bằng thiết bị phát hiện phóng xạ. Hạch gác cửa (hạch bạch huyết đầu tiên tiếp nhận chất phóng xạ hoặc thuốc nhuộm) được cắt bỏ và kiểm tra xem có tế bào ung thư không. Ảnh: cancer.gov
Các bước sinh thiết hạch gác cửa tại vú: Một chất phóng xạ và/hoặc thuốc nhuộm màu xanh được tiêm gần khối u. Chất được tiêm vào được định vị bằng mắt thường và/hoặc bằng thiết bị phát hiện phóng xạ. Hạch gác cửa (hạch bạch huyết đầu tiên tiếp nhận chất phóng xạ hoặc thuốc nhuộm) được cắt bỏ và kiểm tra xem có tế bào ung thư không. Ảnh: cancer.gov
Nếu sau phẫu thuật, bác sĩ giải phẫu bệnh phát hiện ung thư có trong hạch gác cửa, bệnh nhân có thể được đề nghị phẫu thuật cắt bỏ hạch nách để kiểm tra xem có ung thư không. Tuy nhiên, cũng có trường hợp không cần phẫu thuật cắt hạch tùy vào đánh giá các yếu tố như kích thước của khối u vú, loại phẫu thuật được sử dụng để cắt bỏ khối u và phương pháp điều trị nào được lên kế hoạch sau phẫu thuật.
Các trường hợp sau có thể không cần phải phẫu thuật cắt hạch nách:
- Phụ nữ có khối u vú kích thước ≤ 5cm, có không quá 2 hạch gác cửa dương tính (có tế bào ung thư), đang được phẫu thuật bảo tồn vú sau đó là xạ trị và không hóa trị trước khi phẫu thuật.
- Phụ nữ có hạch bạch huyết với lượng ung thư rất nhỏ (≤2 mm) và đang được phẫu thuật cắt trọn vú.
Nếu không có ung thư ở hạch gác cửa, thì khả năng ung thư đã di căn đến các hạch nơi khác là rất thấp, do đó không cần phẫu thuật cắt hạch thêm nữa.
Sinh thiết hạch gác cửa thường được chỉ định cho trường hợp ung thư vú giai đoạn sớm, ung thư vú tiến triển tại chỗ trong một số trường hợp nhất định, chẳng hạn như sau khi điều trị tân bổ trợ và không áp dụng cho những phụ nữ bị ung thư vú dạng viêm.
Mặc dù đây là một thủ thuật phổ biến, nhưng nó đòi hỏi nhiều kỹ năng và cần được thực hiện bởi bác sĩ phẫu thuật giàu kinh nghiệm.
Phẫu thuật cắt bỏ hạch nách
Hạch bạch huyết vùng dưới cánh tay (hạch nách) được cắt bỏ và và kiểm tra giải phẫu bệnh xem bên trong có tế bào ung thư hay không. Cắt bỏ hạch nách thường được thực hiện cùng lúc với ca phẫu thuật điều trị cắt trọn vú hoặc phẫu thuật bảo tồn vú, nhưng cũng có khi thực hiện trong ca phẫu thuật lần hai. Phẫu thuật cắt hạch nách thường được chỉ định trong các trường hợp sau:
- Nếu sinh thiết hạch gác cửa trước đó cho thấy 3 hoặc nhiều hạch bạch huyết dưới cánh tay có tế bào ung thư
- Nếu hạch nách dưới cánh tay hoặc xương đòn sưng to có thể sờ thấy trước khi phẫu thuật hoặc nhìn thấy trên các xét nghiệm hình ảnh và chọc hút bằng kim nhỏ hoặc sinh thiết bằng kim lõi cho thấy tế bào ung thư
- Nếu ung thư đã phát triển đủ lớn và vượt khỏi hạch bạch huyết
- Nếu sinh thiết hạch gác cửa có kết quả dương tính với tế bào ung thư sau khi hóa trị trước phẫu thuật để thu nhỏ khối u (hóa trị bổ trợ)
Các biến cố không mong muốn của phẫu thuật cắt hạch
Sau phẫu thuật cắt hạch, có thể xảy ra tình trạng đau, sưng, chảy máu, huyết khối và nhiễm trùng.
- Phù bạch huyết
Một tác dụng phụ lâu dài có thể xảy ra của phẫu thuật cắt hạch bạch huyết là sưng ở cánh tay hoặc ngực, được gọi là phù bạch huyết. Nguyên nhân là vì lượng dịch dư thừa ở cánh tay thường sẽ đi ngược trở lại vào máu thông qua hệ bạch huyết, nên việc cắt bỏ các hạch bạch huyết đôi khi sẽ chặn đường dẫn lưu từ cánh tay, khiến dịch bị tích tụ, gây phù.
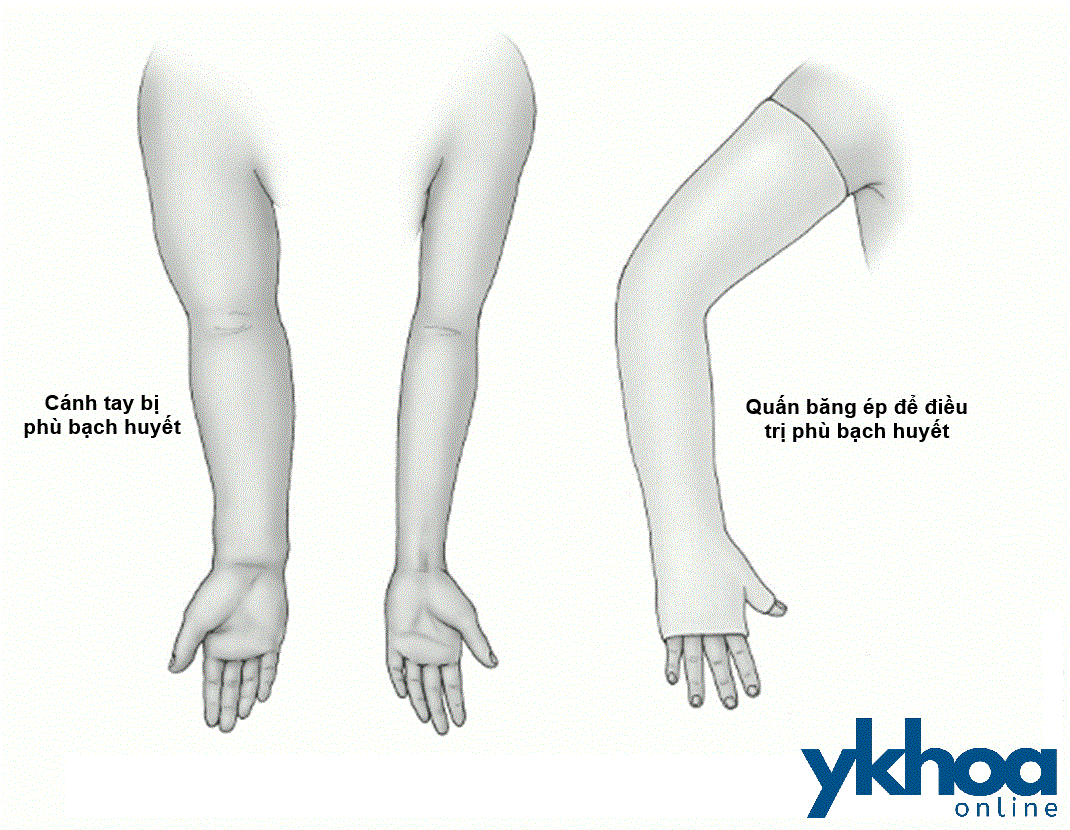
Minh họa cánh tay bị phù bạch huyết. Ảnh: cancer.org
Sinh thiết hạch gác cửa ít gây phù bạch huyết hơn so với phẫu thuật cắt bỏ hạch nách (5%-17% đối với sinh thiết hạch gác cửa và 20% - 30% đối với phẫu thuật cắt bỏ hạch nách). Phù bạch huyết phổ biến hơn nếu có xạ trị sau phẫu thuật hoặc ở những phụ nữ béo phì. Đôi khi triệu chứng phù chỉ kéo dài trong vài tuần rồi biến mất, nhưng cũng có trường hợp kéo dài rất lâu. Nếu cánh tay bị phù, cứng hoặc đau sau phẫu thuật cắt hạch bạch huyết, hãy báo ngay với bác sĩ.
- Hạn chế vận động vai và cánh tay
Hạn chế vận động ở cánh tay và vai sau phẫu thuật cũng là biến cố không mong muốn, phổ biến hơn ở phẫu thuật cắt hạch nách so với sinh thiết hạch gác cửa. Bệnh nhân sẽ được hướng dẫn cách tập thể dục để tránh các biến chứng lâu dài (như cứng khớp vai).
- Tê bì
Cảm giác tê da phần trên, bên trong cánh tay là một tác dụng phụ phổ biến vì dây thần kinh cảm giác ở đây đi qua vùng hạch bạch huyết.
5. Phát hiện ung thư vú trong thời kỳ mang thai
Ung thư vú trong thời kỳ mang thai không phổ biến (khoảng 1 trong 3.000 phụ nữ mang thai). Nhưng nếu phát hiện thấy khối u hoặc có bất thường ở vú, hãy đến cơ sở y tế để được thăm khám. Có nhiều xét nghiệm có thể thực hiện ở phụ nữ mang thai nếu nghi ngờ ung thư vú. Và cũng có nhiều lựa chọn để điều trị ung thư vú cho phụ nữ đang mang thai.
Ung thư vú trong thai kỳ là loại ung thư phổ biến nhất trong thời kỳ mang thai.
Ung thư vú có thể khó phát hiện hơn khi mang thai
Sự thay đổi nồng độ hormone trong thai kỳ khiến vú thay đổi: to hơn, sần sùi, đau… nên khó phát hiện khối u hơn.
Một lý do khác là nhiều phụ nữ không muốn tầm soát ung thư vú bằng chụp nhũ ảnh vì sợ ảnh hưởng đến thai nhi nên họ thường trì hoãn đến sau khi sinh. Ngoài ra, chụp nhũ ảnh trong thời kỳ mang thai hay cho con bú sẽ thấy hình ảnh mô vú đặc hơn, khiến việc phát hiện ung thư cũng khó khăn hơn.
Do những lý do trên, phụ nữ mang thai bị ung thư vú thường được chẩn đoán ở giai đoạn muộn hơn so với những phụ nữ không mang thai.
Chụp nhũ ảnh và các xét nghiệm hình ảnh khác có an toàn trong thai kỳ không?
Mối quan tâm chính đối với bất kỳ xét nghiệm hình ảnh nào trong thai kỳ là liệu tia xạ có tiếp xúc với thai nhi đang phát triển hay không, điều này có thể gây hại, đặc biệt là trong tam cá nguyệt đầu tiên.
Chụp nhũ ảnh có thể phát hiện hầu hết các bệnh ung thư vú bắt đầu khi phụ nữ mang thai và nhìn chung, chụp nhũ ảnh trong thai kỳ được cho là an toàn. Lượng bức xạ cần thiết để chụp nhũ ảnh là nhỏ và bức xạ tập trung vào vú, vì vậy hầu hết không chiếu đến các bộ phận khác của cơ thể. Để bảo vệ thêm, một tấm chắn bằng chì được đặt trên phần bụng dưới để giúp ngăn tia xạ chiếu đến tử cung. Tuy nhiên, một lượng nhỏ bức xạ có thể chiếu đến thai nhi và không biết liệu nó có an toàn hay gây hại đến thai nhi hay không.
Siêu âm vú không sử dụng bức xạ và được cho là an toàn trong thai kỳ. Đây thường là một xét nghiệm dễ thực hiện, vì vậy, đây thường là xét nghiệm đầu tiên được sử dụng để đánh giá sự thay đổi ở vú (chẳng hạn như có khối u) trong thai kỳ.
Các xét nghiệm khác, chẳng hạn như chụp PET, chụp xương và chụp cắt lớp vi tính (CT) có nhiều khả năng khiến thai nhi tiếp xúc với tia xạ.
Chụp cộng hưởng từ (MRI) vú không sử dụng tia xạ. Tuy nhiên, chụp MRI vú thường yêu cầu tiêm một chất tương phản gọi là gadolinium vào máu để có được hình ảnh rõ nét. Chất cản quang này có thể đi qua nhau thai và có thể gây hại đến thai nhi. Do đó, bác sĩ thường không khuyến nghị chụp MRI vú trong thời kỳ mang thai.
Sinh thiết vú trong thời kỳ mang thai
Nếu có một khối u mới ở vú hoặc kết quả xét nghiệm hình ảnh bất thường bị nghi ngờ có thể là ung thư, thì thường phải sinh thiết để lấy vùng mô vú bị nghi ngờ làm xét nghiệm giải phẩu bệnh.
Kỹ thuật sinh thiết vú phổ biến nhất là sinh thiết bằng kim lõi. Thông thường, thuốc gây tê tại chỗ được sử dụng để làm tê vùng vú nơi sẽ tiến hành sinh thiết, nên ít gây nguy hại đến thai nhi.
Trong trường hợp sinh thiết kim lõi không đưa ra câu trả lời rõ ràng, thì sinh thiết phẫu thuật thường là bước tiếp theo. Thai phụ sẽ phải được gây mê toàn thân. Khi đó có thể gây hại đến thai nhi.
Ung thư vú có thể di căn đến thai nhi không?
Ung thư vú chưa bao giờ được phát hiện là di căn từ mẹ sang thai nhi. Nhưng trong một số trường hợp hiếm hoi, ung thư đã di căn đến nhau thai và có thể ảnh hưởng đến lượng dinh dưỡng mà thai nhi nhận được từ mẹ.
CÁC THUẬT NGỮ QUAN TRỌNG TRONG CHẨN ĐOÁN UNG THƯ VÚ
Khi được chẩn đoán mắc ung thư vú, có lẽ bệnh nhân sẽ nghe rất nhiều thuật ngữ khác nhau được sử dụng để mô tả căn bệnh ung thư của mình.
1. Cấp độ ung thư vú (grade)
Cấp độ ung thư vú khác với giai đoạn ung thư vú.
Khi các tế bào ung thư được lấy ra khỏi vú, chúng sẽ được gửi phòng thí nghiệm kiểm tra dưới kính hiển vi để đánh giá về mô học.
Bác sĩ giải phẫu bệnh sẽ xem và đưa ra đánh giá về cấp độ dựa vào mức độ giống và khác nhau giữa các tế bào ung thư so với tế bào bình thường. Cấp độ được sử dụng để đánh giá khả năng tăng trưởng và xâm lấn của ung thư, giúp dự đoán tiên lượng và đưa ra phương pháp điều trị phù hợp nhất. Có 3 cấp độ:
- Cấp độ thấp (cấp độ 1): ung thư phát triển chậm và ít có khả năng lây lan hơn.
- Cấp độ cao (cấp độ 3): ung thư phát triển nhanh và có nhiều khả năng lây lan hơn.
- Cấp độ trung gian (cấp độ 2): ung thư phát triển nhanh hơn ung thư cấp độ 1 nhưng chậm hơn ung thư cấp độ 3.
Cách phân cấp độ ung thư vú
Ba đặc điểm của tế bào ung thư vú được đánh giá và chấm điểm. Mỗi đặc điểm được chấm từ 1-3 điểm. Sau đó, cộng các điểm số này lại, tổng số điểm sẽ dao động từ 3 đến 9 điểm. Thay vì mô tả các cấp độ ung thư vú bằng tổng số điểm, thường thì bác sĩ sẽ sử dụng các thuật ngữ “biệt hóa tốt”, “biệt hóa trung bình” và “biệt hóa kém” để mô tả cấp độ ung thư:
- Cấp độ 1 hoặc biệt hóa tốt (3 - 5 điểm). Các tế bào phát triển chậm hơn và trông giống tế bào vú bình thường hơn.
- Cấp độ 2 hoặc biệt hóa trung bình (6 - 7 điểm). Các tế bào phát triển với tốc độ trung bình và mức độ khác biệt giữa tế bào ung thư và tế bào bình thường ở đâu đó giữa cấp độ 1 và 3.
- Cấp độ 3 hoặc biệt hóa kém (8 – 9 điểm). Các tế bào ung thư trông rất khác so với tế bào bình thường và có thể sẽ phát triển và di căn nhanh hơn.
Cách phân cấp độ ung thư vú trên có thể áp dụng cho ung thư vú xâm lấn và ung thư biểu mô tuyến vú tại chỗ (DCIS).
2. Bộ nhiễm sắc thể và tăng sinh tế bào ung thư vú
Tìm hiểu thêm thông tin về DNA trong tế bào ung thư vú có thể giúp dự đoán tốc độ phân chia và phát triển của các tế bào ung thư đó. Nếu bạn muốn tìm hiểu thêm về DNA và ung thư vú, trước tiên bạn nên hiểu hai thuật ngữ quan trọng: đa bội và tăng sinh tế bào.
Bộ nhiễm sắc thể của tế bào ung thư: đề cập đến lượng DNA mà chúng chứa. Nếu có một lượng DNA bình thường trong các tế bào, gọi là lưỡng bội thì loại ung thư này có xu hướng phát triển và lây lan chậm hơn.
Nếu lượng DNA bất thường, gọi là dị bội thì loại ung thư này có xu hướng ác tính hơn, phát triển và lây lan nhanh hơn.
Các xét nghiệm về bộ nhiễm sắc thể có thể giúp đánh giá dự hậu về lâu dài, nhưng hiếm khi thay đổi phương pháp điều trị. Các xét nghiệm này được xem là tùy chọn, không được khuyến nghị là xét nghiệm thường quy trong ung thư vú.
Tăng sinh tế bào: Tăng sinh tế bào là tốc độ tế bào ung thư sao chép DNA của nó và phân chia thành 2 tế bào. Nếu các tế bào ung thư phân chia nhanh hơn, nghĩa là ung thư phát triển nhanh hơn hoặc ác tính hơn.
Xét nghiệm Ki-67 có thể ước tính tốc độ tăng sinh tế bào ung thư, từ đó giúp lập kế hoạch điều trị hoặc dự đoán kết quả điều trị. Ki-67 là một loại protein chỉ có trong các tế bào đang phân chia. Điểm Ki-67 cao có nghĩa là nhiều tế bào đang phân chia nhanh và ung thư có khả năng phát triển và lan rộng. Điểm Ki-67 trên 30% thường được coi là cao.
Tuy nhiên, kết quả xét nghiệm có thể khác nhau tùy thuộc vào những yếu tố như phòng xét nghiệm, phương pháp xét nghiệm và phần nào của khối u được xét nghiệm.
Một phương pháp khác cũng có thể xác định tốc độ phân chia tế bào là phân số giai đoạn S (S-phase fraction), đây là tỷ lệ phần trăm các tế bào đang sao chép DNA để chuẩn bị phân chia thành 2 tế bào mới. Trong chu kỳ phân chia tế bào, giai đoạn S (hay pha S) là giai đoạn tổng hợp DNA.
Nếu xét nghiệm phân số pha S hoặc chỉ số đánh dấu Ki-67cho kết quả cao, điều đó có nghĩa là các tế bào ung thư đang phân chia với tốc độ nhanh hơn.
3. Tình trạng thụ thể hormone của tế bào ung thư vú
Các tế bào ung thư vú được lấy ra trong quá trình sinh thiết hoặc phẫu thuật được xét nghiệm để tìm xem chúng có một số protein cụ thể (là thụ thể estrogen hoặc progesterone) hay không. Nếu tế bào ung thư có các thụ thể này, có nghĩa là khi các hormone estrogen và progesterone gắn vào các thụ thể, chúng sẽ kích thích tế ung thư phát triển.
Ung thư được gọi là thụ thể hormone dương tính hoặc thụ thể hormone âm tính dựa trên việc chúng có hay không có các thụ thể này.
Biết được tình trạng thụ thể hormone của ung thư là rất quan trọng, vì giúp xác định các phương án điều trị phù hợp.
Thụ thể estrogen và progesterone là gì?
Thụ thể là protein của tế bào có thể gắn với một số chất nhất định trong máu. Các tế bào vú bình thường và một số tế bào ung thư vú có thụ thể gắn với các nội tiết tố là estrogen và progesterone, và cần những hormone này gắn vào để tế bào phát triển.
Các tế bào ung thư vú có thể có một, cả hai hoặc không có thụ thể hormone nào.
- Thụ thể estrogen dương tính: Tế bào ung thư vú có thụ thể estrogen được gọi là ung thư vú thụ thể estrogen dương tính (hoặc ER+).
- Thụ thể progesterone dương tính: Tế bào ung thư vú có thụ thể progesterone được gọi là ung thư vú thụ thể progesterone dương tính (hoặc PR+).
- Thụ thể hormone dương tính: Tế bào ung thư có một hoặc cả hai thụ thể trên, được gọi là ung thư vú thụ thể hormone dương tính (hoặc HR+).
- Thụ thể hormone âm tính: Tế bào ung thư không có cả thụ thể estrogen và thụ thể progesterone, thì được gọi là ung thư vú thụ thể hormone âm tính (hoặc HR-).
Ngăn không cho hormone estrogen và progesterone gắn các thụ thể của chúng có thể giúp ngăn chặn diễn tiến của ung thư vú. Có những loại thuốc với cơ chế tác động này để điều trị ung thư vú (gọi là liệu pháp hormone, hay liệu pháp nội tiết tố).
Tại sao việc biết được tình trạng thụ thể hormone lại quan trọng?
Việc biết được tình trạng thụ thể hormone sẽ giúp bác sĩ quyết định cách điều trị. Nếu ung thư có một hoặc cả hai thụ thể hormone này, thuốc điều trị hormone sẽ được sử dụng để làm giảm nồng độ estrogen hoặc ngăn chặn estrogen gắn vào thụ thể trên các tế bào ung thư vú. Phương pháp điều trị này hiệu quả đối với các trường hợp ung thư vú dương tính với thụ thể hormone, nhưng không có tác dụng đối với các trường hợp ung thư vú âm tính với thụ thể hormone (âm tính với cả thụ thể estrogen và thụ thể progesterone).
Tất cả các trường hợp ung thư vú xâm lấn đều phải được xét nghiệm cả hai thụ thể hormone này trong mẫu sinh thiết hoặc trong khối u đã được phẫu thuật cắt bỏ. Khoảng 3/4 trường hợp ung thư vú có ít nhất một trong hai thụ thể này. Tỷ lệ này cao hơn ở phụ nữ lớn tuổi so với phụ nữ trẻ tuổi. Ung thư biểu mô ống tuyến vú tại chỗ (DCIS) cũng nên được kiểm tra các thụ thể hormone.
Xét nghiệm thụ thể hormone được thực hiện như thế nào?
Kỹ thuật xét nghiệm hóa mô miễn dịch thường được sử dụng nhất để tìm xem các tế bào ung thư có thụ thể estrogen và progesterone hay không.
Kết quả xét nghiệm thụ thể hormone có ý nghĩa gì?
Khối u được kết luận là thụ thể hormone dương tính nếu ít nhất 1% tế bào được xét nghiệm có thụ thể estrogen và/hoặc progesterone. Nếu không có, xét nghiệm sẽ kết luận là thụ thể hormone âm tính.
- Ung thư vú dương tính với thụ thể hormone: tế bào ung thư có thụ thể estrogen hoặc thụ thể progesterone hoặc cả hai. Loại ung thư vú này có thể được điều trị bằng liệu pháp hormone để làm giảm nồng độ estrogen hoặc chặn các thụ thể estrogen. Ung thư dương tính với thụ thể hormone thường phát triển chậm hơn so với loại ung thư âm tính với thụ thể hormone, và có tiên lượng tốt hơn trong thời gian ngắn, nhưng sau điều trị nhiều năm thường bị tái phát.
- Ung thư vú âm tính với thụ thể hormone: tế bào ung thư không có thụ thể estrogen hoặc progesterone nên điều trị bằng liệu pháp hormone không có tác dụng đối với những loại ung thư này. Đây là loại ung thư thường phát triển nhanh hơn các loại ung thư dương tính với thụ thể hormone. Nếu có tái phát sau khi điều trị, thì thường là trong vài năm đầu. Ung thư âm tính với thụ thể hormone phổ biến hơn ở những phụ nữ chưa mãn kinh.
- Ung thư vú bộ ba âm tính: tế bào ung thư không có thụ thể estrogen, không có thụ thể progesterone và cũng không tạo ra protein HER2 (thụ thể yếu tố tăng trưởng biểu bì 2 ở người). Ung thư này phổ biến hơn ở những phụ nữ dưới 40 tuổi, là người da đen hoặc có đột biến ở gen BRCA1, thường phát triển và lây lan nhanh hơn hầu hết các loại ung thư vú khác. Vì các tế bào ung thư không có thụ thể hormone nên liệu pháp hormone không hiệu quả đối với loại ung thư này. Và vì chúng không có nhiều HER2 nên các loại thuốc nhắm vào HER2 cũng không có tác dụng. Hóa trị vẫn có thể hữu ích. Xem thêm Ung thư vú ba âm tính để tìm hiểu thêm.
- Ung thư vú bộ ba dương tính: tế bào ung thư có cả thụ thể estrogen, thụ thể progesterone và và HER2. Các trường hợp ung thư này có thể được điều trị bằng thuốc hormone cũng như thuốc nhắm trúng đích HER2.
4. Tình trạng protein HER2 của tế bào ung thư vú
Khoảng 15% đến 20% trường hợp ung thư vú có mức protein HER2 cao. Những loại ung thư này được gọi là ung thư vú dương tính với HER2.
HER2 là gì và ý nghĩa của nó?
HER2 là một loại protein giúp các tế bào ung thư vú phát triển nhanh. Các tế bào ung thư vú có mức HER2 cao hơn bình thường được gọi là HER2 dương tính. Những loại ung thư này có xu hướng phát triển và lây lan nhanh hơn các loại ung thư vú âm tính với HER2, nhưng thường đáp ứng tốt hơn khi điều trị bằng thuốc nhắm vào protein HER2.
Tất cả các loại ung thư vú xâm lấn đều phải được xét nghiệm HER2 trên mẫu sinh thiết hoặc khi khối u được cắt bỏ bằng phẫu thuật.
Xét nghiệm HER2 được thực hiện như thế nào?
Xét nghiệm hóa mô miễn dịch (IHC: immunohistochemistry) hoặc kỹ thuật lai huỳnh quang tại chỗ (FISH: Fluorescent in situ hybridization) được sử dụng để đánh giá mức protein HER2 có cao hay không.
Kết quả xét nghiệm có nghĩa là gì?
Kết quả xét nghiệm HER2 sẽ giúp lựa chọn phương pháp điều trị phù hợp nhất.
Xét nghiệm lai huỳnh quang tại chỗ thường đắt hơn và mất nhiều thời gian hơn. Do đó, xét nghiệm bằng hóa mô miễn dịch (IHC) thường được thực hiện trước.
- Nếu kết quả IHC là 0: ung thư được coi là âm tính với HER2 và không đáp ứng với điều trị bằng thuốc nhắm trúng đích HER2.
- Nếu kết quả IHC là 1+: ung thư được coi là âm tính với HER2, nên thường không đáp ứng với điều trị bằng thuốc nhắm trúng đích HER2. Nhưng nghiên cứu mới cho thấy một số loại thuốc HER2 có thể có hiệu quả trong một số trường hợp.
- Nếu kết quả IHC là 2+: tình trạng HER2 của ung thư được gọi là "không rõ ràng", cần được xét nghiệm bằng FISH để làm rõ kết quả.
- Nếu kết quả IHC là 3+: ung thư dương tính với HER2, khi đó sẽ được điều trị bằng thuốc nhắm trúng đích HER2.
Một số trường hợp ung thư vú có kết quả IHC 1+ hoặc IHC 2+ cùng với xét nghiệm FISH âm tính có thể được gọi là ung thư HER2 thấp. Những trường hợp này còn đang được nghiên cứu, nhưng có vẻ như vẫn có đáp ứng với một số loại thuốc nhắm trúng đích HER2.
Các trường hợp ung thư vú bộ ba âm tính và ung thư vú bộ ba dương tính: đã được đề cập trong mục “Tình trạng thụ thể hormone” ngay phía trên.
5. Xét nghiệm biểu hiện gen ung thư vú
Xét nghiệm biểu hiện gen là một dạng y học cá nhân hóa (hay cá thể hóa), nghĩa là tìm hiểu rõ thêm để điều chỉnh phương pháp điều trị cho từng trường hợp ung thư vú.
Các xét nghiệm này được thực hiện trên các tế bào ung thư vú sau phẫu thuật hoặc sinh thiết để xem xét một số gen cụ thể. Xét nghiệm này đôi khi được gọi là lập hồ sơ biểu hiện gen.
Kết quả xét nghiệm biểu hiện gen có ý nghĩa gì?
Các kiểu biểu hiện gen có thể giúp dự đoán:
- Liệu một số loại ung thư vú giai đoạn sớm có khả năng tái phát sau khi điều trị ban đầu hay không.
- Những trường hợp nào mà hóa trị bổ trợ (sau phẫu thuật) có thể có hiệu quả. Liệu pháp hormone là phương pháp điều trị tiêu chuẩn cho ung thư vú dương tính với thụ thể hormone, nhưng việc nên hay không nên hóa trị không phải lúc nào cũng rõ ràng. Các xét nghiệm gen này có thể giúp ra quyết định. Tuy nhiên, không thể biết chắc liệu bệnh ung thư có tái phát hay không, khi có và không có hóa trị.
Vai trò của xét nghiệm về gen trong ung thư vú còn đang được tiếp tục nghiên cứu.
Các lựa chọn xét nghiệm:
Oncotype DX, MammaPrint và Prosigna là những ví dụ về các xét nghiệm gen ung thư để xem liệu có cần hóa trị để nguy cơ tái phát hay không. Loại xét nghiệm được sử dụng sẽ phụ thuộc vào từng trường hợp cụ thể. Lưu ý rằng các xét nghiệm này được sử dụng cho các bệnh ung thư giai đoạn đầu và không cần xét nghiệm trong mọi trường hợp. Ví dụ, nếu ung thư vú tiến triển thì rõ ràng là cần phải hóa trị, ngay cả khi không có xét nghiệm biểu hiện gen.
5.1. Oncotype DX: được sử dụng cho ung thư dương tính với thụ thể hormone giai đoạn I, II hoặc IIIa chưa di căn đến hơn 3 hạch bạch huyết và âm tính với HER2. Xét nghiệm này cũng có thể được sử dụng cho ung thư biểu mô ống tuyến vú tại chỗ (còn gọi là ung thư vú giai đoạn 0).
Xét nghiệm này xem xét một bộ 21 gen trong các tế bào ung thư từ mẫu sinh thiết khối u hoặc phẫu thuật để đánh giá khả năng tái phát theo thang điểm từ 0 đến 100. Điểm số phản ánh nguy cơ ung thư vú tái phát trong 9 năm tới nếu chỉ được điều trị bằng liệu pháp hormone và lợi ích có thể mang lại của hóa trị sau phẫu thuật.
Đối với phụ nữ > 50 tuổi và không có hạch bạch huyết bị ung thư xâm lấn:
Điểm số thấp (0-25) có nghĩa là nguy cơ tái phát thấp. Hầu hết phụ nữ có điểm số tái phát thấp không được hưởng lợi từ hóa trị và có kết quả tốt khi được điều trị bằng liệu pháp hormone.
Điểm số cao (26-100) có nghĩa là nguy cơ tái phát cao hơn. Phụ nữ có điểm tái phát cao có nhiều khả năng được hưởng lợi từ việc kết hợp hóa trị với liệu pháp hormone để giúp giảm nguy cơ ung thư tái phát.
Đối với phụ nữ ≤ 50 tuổi và không có hạch bạch huyết bị ung thư xâm lấn:
Điểm thấp (0-15) có nghĩa là nguy cơ tái phát thấp. Hầu hết những phụ nữ có điểm số tái phát thấp không được hưởng lợi từ hóa trị và có kết quả tốt khi được điều trị bằng liệu pháp hormone.
Điểm trung bình (16-25) có nghĩa là một số phụ nữ trong nhóm này có thể có lợi ích nhỏ khi kết hợp hóa trị với liệu pháp hormone để giảm nguy cơ ung thư tái phát. Hãy trao đổi với bác sĩ về các lựa chọn.
Điểm cao (26-100): có nghĩa là nguy cơ tái phát cao hơn. Phụ nữ có điểm tái phát cao có nhiều khả năng được hưởng lợi từ việc kết hợp hóa trị với liệu pháp hormone để giúp giảm nguy cơ ung thư tái phát.
Đối với phụ nữ ≤ 50 tuổi và có hạch bạch huyết bị ung thư xâm lấn:
Điểm thấp (0-25) có nghĩa là nguy cơ tái phát thấp hơn, nhưng phụ nữ trong nhóm này có thể hưởng lợi khi kết hợp hóa trị với liệu pháp hormone. Một lựa chọn khác có thể là ức chế buồng trứng cùng với tamoxifen hoặc chất ức chế aromatase.
Điểm cao (26-100) có nghĩa là nguy cơ tái phát cao hơn. Phụ nữ trong nhóm này có nhiều khả năng được hưởng lợi từ việc bổ sung hóa trị vào liệu pháp hormone để giúp giảm nguy cơ ung thư tái phát.
5.2. MammaPrint: được sử dụng để giúp xác định khả năng ung thư vú tái phát ở cơ quan xa vú sau khi điều trị. Xét nghiệm này được được sử dụng cho bất kỳ loại ung thư vú xâm lấn nào có kích thước khối u ≤ 5 cm và đã di căn không quá 3 hạch bạch huyết. Xét nghiệm này có thể được thực hiện bất kể độ tuổi hay tình trạng hormone hoặc HER2 của ung thư.
Xét nghiệm này xem xét 70 gen khác nhau để xác định xem ung thư có nguy cơ tái phát thấp hay cao trong 10 năm tới. Kết quả xét nghiệm trả về là "nguy cơ thấp" hoặc "nguy cơ cao". Xét nghiệm này cũng đang được nghiên cứu như một cách để xác định xem một số trường hợp có được hưởng lợi từ hóa trị hay không.
5.3. Prosigna: được sử dụng để dự đoán nguy cơ tái phát trong 10 năm tới ở những phụ nữ sau mãn kinh và có ung thư vú xâm lấn với thụ thể hormone dương tính và HER2 âm tính. Xét nghiệm này có thể được sử dụng để xét nghiệm các trường hợp ung thư giai đoạn đầu chưa xâm lấn hạch bạch huyết hoặc có không quá 3 hạch bạch huyết bị ung thư xâm lấn.
Xét nghiệm này xem xét 50 gen và phân loại kết quả thành nguy cơ tái phát thấp, trung bình hoặc cao.
5.4. Chỉ số ung thư vú: được thực hiện trên mẫu mô khối u từ khi chẩn đoán lần đầu để dự đoán nguy cơ tái phát trong vòng 5 đến 10 năm cho các trường hợp ung thư vú xâm lấn dương tính với thụ thể hormone và chưa xâm lấn đến các hạch lân cận hoặc xâm lấn không quá 3 hạch. Xét nghiệm này cũng có thể giúp dự đoán những trường hợp nào được hưởng lợi từ liệu pháp hormone khi dùng trong thời gian dài hơn 5 năm.
Xét nghiệm này xem xét 11 gen và phân loại kết quả thành nguy cơ tái phát thấp hoặc cao.
6. Các giai đoạn của ung thư vú
Sau khi chẩn đoán xác định ung thư vú, bác sĩ sẽ cố gắng tìm hiểu và đánh giá xem ung thư đã di căn hay chưa và nếu có thì di căn đến đâu. Quá trình này được gọi là phân giai đoạn. Biết được ung thư đang ở giai đoạn nào sẽ giúp xác định mức độ nghiêm trọng của bệnh, lựa chọn cách điều trị tốt nhất và đánh giá tiên lượng của bệnh nhân.
Có mấy giai đoạn ung thư vú?
Giai đoạn sớm nhất của ung thư vú là giai đoạn 0 (ung thư biểu mô tại chỗ). Sau đó là các giai đoạn từ I (1) đến IV (4).
Theo quy tắc, số càng thấp thì ung thư càng ít di căn. Số càng cao, chẳng hạn như giai đoạn IV, nghĩa là ung thư đã di căn nhiều hơn. Và trong mỗi giai đoạn, chữ cái càng sớm nghĩa là giai đoạn càng thấp. Mặc dù diễn tiến ung thư của mỗi người là khác nhau, nhưng các trường hợp ung thư cùng giai đoạn thường được điều trị giống nhau và tiên lượng cũng tương tự nhau.
Các giai đoạn ung thư được xác định như thế nào?
Hệ thống phân loại thường được sử dụng nhất cho ung thư vú là hệ thống TNM của Liên hiệp Ủy ban Ung thư Hoa Kỳ (AJCC). Hệ thống phân giai đoạn ung thư vú của AJCC mới nhất, có hiệu lực từ tháng 1 năm 2018, bao gồm cả phân giai đoạn lâm sàng và bệnh học:
- Phân giai đoạn bệnh học: được xác định bằng cách kiểm tra mô được cắt bỏ trong quá trình phẫu thuật.
- Phân giai đoạn lâm sàng: nếu không thể phẫu thuật ngay hoặc quá chỉ định phẫu thuật, ung thư sẽ được phân theo giai đoạn lâm sàng. Khi đó, sẽ dựa trên kết quả khám sức khỏe, sinh thiết và xét nghiệm hình ảnh. Phân giai đoạn lâm sàng giúp lập kế hoạch điều trị. Tuy nhiên, nhiều khi ung thư đã lan rộng hơn so với ước tính của giai đoạn lâm sàng và có thể không dự đoán được tiên lượng của bệnh nhân chính xác như phân giai đoạn bệnh lý.
Trong cả hai hệ thống phân loại, 7 yếu tố đánh giá chính được sử dụng:
T (Tumor: Khối u): Ung thư lớn đến mức nào? Nó đã phát triển sang các khu vực lân cận chưa?
N (Lymp Node: Hạch bạch huyết): Ung thư xâm lấn các hạch bạch huyết gần đó chưa? Nếu có, bao nhiêu hạch?
M (Metastasis: Di căn): Ung thư đã di căn xa đến các cơ quan khác như phổi hoặc gan chưa?
ER (Estrogen Receptor): Tình trạng thụ thể estrogen như thế nào? Tế bào ung thư có thụ thể estrogen không?
PR (Progesterone Receptor: Tình trạng thụ thể progesterone như thế nào? Tế bào ung thư có thụ thể progesterone không?
HER2: Tình trạng protein HER2 như thế nào? Tế bào ung thư có tạo ra nhiều HER2 không?
G (Grade: Cấp độ ung thư): Mức độ giống hay khác của tế bào ung thư so với tế bào bình thường như thế nào?
Hệ thống phân giai đoạn TNM gồm 3 chi tiết đầu tiên rất hay được sử dụng để phân giai đoạn của nhiều loại ung thư, kể cả ung thư vú.
Chi tiết về hệ thống phân loại TNM
Các số hoặc chữ cái sau T, N và M cung cấp thêm thông tin chi tiết về từng yếu tố này. Số càng cao có nghĩa là ung thư tiến triển hơn. Các thông tin bên dưới sử dụng các định nghĩa theo bệnh học.
T – Khối u
Theo sau T là một số từ 0 đến 4, mô tả kích thước của khối u nguyên phát và mức độ lan rộng đến da hoặc đến thành ngực dưới vú hay chưa. Các số T càng cao có nghĩa là khối u càng lớn và/hoặc lan rộng hơn đến các mô gần vú. Các giai đoạn của T bao gồm:
TX: Không thể đánh giá khối u nguyên phát.
T0: Không có bằng chứng về khối u nguyên phát.
Tis: Ung thư biểu mô tuyến vú tại chỗ (DCIS) hoặc bệnh Paget ở vú không có khối u
T1 (bao gồm T1a, T1b và T1c): Khối u có đường kính ≤ 2 cm.
T2: Khối u có đường kính > 2 cm nhưng ≤ 5 cm.
T3: Khối u có đường kính > 5 cm.
T4 (bao gồm T4a, T4b, T4c và T4d): Khối u có bất kỳ kích thước nào phát triển vào thành ngực hoặc da. Bao gồm ung thư vú dạng viêm.
N – Hạch bạch huyết
Theo sau N là một số từ 0 đến 3 cho biết ung thư có lan đến các hạch bạch huyết lân cận hay chưa? và nếu có thì bao nhiêu hạch?
Phân loại hạch bạch huyết đối với ung thư vú dựa trên việc quan sát hạch dưới kính hiển vi.
Một khối tế bào ung thư phải chứa ít nhất 200 tế bào hoặc có đường kính ít nhất 0,2 mm thì mới có thể thay đổi giai đoạn N. Nếu một vùng ung thư nhỏ hơn 0,2 mm (hoặc ít hơn 200 tế bào) không làm thay đổi giai đoạn, nhưng được ghi lại bằng các chữ viết tắt (i+ hoặc mol+) cho biết loại xét nghiệm đặc biệt được sử dụng để tìm kiếm sự lan rộng của tế bào ung thư vú đến hạch.
Nếu phần diện tích ung thư tại hạch ít nhất là 0,2 mm (hoặc 200 tế bào), nhưng vẫn không lớn hơn 2 mm, thì được gọi là di căn vi thể. Còn nếu phần diện tích ung thư tại hạch lớn hơn 2 mm thì được gọi là di căn đại thể (nhưng thường chỉ gọi là di căn) và sẽ làm thay đổi giai đoạn N.
Các giai đoạn của N bao gồm:
NX: Không thể đánh giá các hạch bạch huyết gần đó (ví dụ, nếu chúng đã được cắt bỏ trước đó).
N0: Ung thư chưa lan đến các hạch bạch huyết gần đó.
N0(i+): Vùng ung thư lan rộng chứa ít hơn 200 tế bào và nhỏ hơn 0,2 mm. Viết tắt "i+" có nghĩa là một số lượng nhỏ tế bào ung thư (gọi là tế bào khối u biệt lập) được nhìn thấy trong kỹ thuật nhuộm thông thường hoặc khi sử dụng một loại kỹ thuật nhuộm đặc biệt, gọi là hóa mô miễn dịch.
N0(mol+): Không thể nhìn thấy tế bào ung thư trong các hạch nách (kể cả khi sử dụng kỹ thuật nhuộm đặc biệt), nhưng dấu vết của tế bào ung thư đã được phát hiện bằng một kỹ thuật gọi là RT-PCR (Phản ứng tổng hợp chuỗi theo thời gian thực). RT-PCR là một xét nghiệm phân tử có thể tìm thấy một số lượng rất nhỏ các tế bào ung thư.
N1: Ung thư đã di căn đến 1 đến 3 hạch bạch huyết nách (dưới cánh tay) và/hoặc ung thư được tìm thấy trong các hạch bạch huyết vú trong (những hạch gần xương ức) khi sinh thiết hạch bạch huyết gác cửa.
N1mi: Có di căn vi thể trong các hạch bạch huyết dưới cánh tay. Các vùng ung thư lan rộng trong các hạch bạch huyết có đường kính ít nhất là 0,2mm, nhưng không lớn hơn 2mm.
N1a: Ung thư đã di căn đến 1 đến 3 hạch bạch huyết dưới cánh tay với ít nhất một vùng ung thư lan rộng hơn 2mm.
N1b: Ung thư đã lan đến các hạch bạch huyết vú trong cùng bên với ung thư, nhưng chỉ có thể được phát hiện khi làm sinh thiết hạch bạch huyết gác cửa (vì hạch vú trong chưa phì đại).
N1c: Có cả đặc điểm của N1a và N1b.
N2: Ung thư đã lan đến 4 đến 9 hạch bạch huyết dưới cánh tay hoặc ung thư đã làm phì đại các hạch bạch huyết vú trong
N2a: Ung thư đã lan đến 4 đến 9 hạch bạch huyết dưới cánh tay, với ít nhất một vùng ung thư lan rộng hơn 2 mm.
N2b: Ung thư đã lan đến một hoặc nhiều hạch bạch huyết vú trong, khiến chúng to (phì đại) ra.
N3: Bất kỳ trường hợp nào sau đây:
N3a:
Ung thư đã lan đến ≥10 hạch nách, với ít nhất một vùng ung thư lan rộng hơn 2 mm, HOẶC
Ung thư đã lan đến các hạch dưới xương đòn, với ít nhất một vùng ung thư lan rộng hơn 2 mm.
N3b:
Ung thư được tìm thấy ở ít nhất một hạch nách (có ít nhất một vùng ung thư lan rộng hơn 2 mm) và đã lan rộng đến các hạch vú trong, HOẶC
Ung thư đã lan đến 4 hạch nách trở lên (có ít nhất một vùng ung thư lan rộng hơn 2 mm) và đã đến các hạch vú trong khi làm sinh thiết hạch bạch huyết gác cửa.
N3c: Ung thư đã lan đến các hạch trên xương đòn (hạch thượng đòn) ở cùng bên khối u với ít nhất một vùng ung thư lan rộng hơn 2 mm.
M – Di căn
Theo sau M là 0 hoặc 1, cho biết ung thư đã di căn đến các cơ quan xa chưa, ví dụ như phổi, gan hoặc xương.
M0: Không phát hiện thấy di căn xa trên phim chụp X-quang (hoặc các xét nghiệm hình ảnh khác).
cM0(i+): Một số lượng nhỏ tế bào ung thư được tìm thấy trong máu hoặc tủy xương (chỉ phát hiện bằng các xét nghiệm đặc biệt) hoặc các vùng nhỏ của ung thư di căn (không lớn hơn 0,2 mm) được tìm thấy trong các hạch bạch huyết xa nách, xương đòn hoặc vú trong.
M1: Ung thư đã di căn xa đến các cơ quan khác (thường là xương, phổi, não hoặc gan), được phát hiện bằng các xét nghiệm hình ảnh hoặc khám lâm sàng và/hoặc sinh thiết một trong những vùng này chứng minh ung thư đã di căn và lớn hơn 0,2 mm.
ĐIỀU TRỊ UNG THƯ VÚ
1. Điều trị tại chỗ
Điều trị tại chỗ nghĩa là điều trị ngay tại khối u mà không ảnh hưởng đến những nơi khác của cơ thể. Phẫu thuật và xạ trị là điều trị tại chỗ.
Hầu hết phụ nữ bị ung thư vú sẽ phải được phẫu thuật để cắt bỏ khối u. Tùy vào loại ung thư vú và mức độ tiến triển của bệnh mà bác sĩ sẽ lựa chọn các cách điều trị khác nhau, có thể là trước hoặc sau phẫu thuật, hoặc đôi khi là cả trước và sau phẫu thuật.
1.1. Phẫu thuật ung thư vú
Đa số trường hợp ung thư vú đều cần phải phẩu thuật. Có nhiều loại phẫu thuật khác nhau, tùy thuộc vào tình trạng bệnh mà bác sĩ sẽ chọn phương pháp phù hợp. Ví dụ, phẫu thuật để:
- Cắt bỏ càng nhiều mô ung thư càng tốt (cắt rông
- Đánh giá xem ung thư đã di căn đến các hạch bạch huyết dưới cánh tay hay chưa (sinh thiết hạch gác cửa hoặc cắt bỏ hạch nách)
- Phục hồi hình dạng vú sau khi cắt bỏ khối u (tái tạo vú)
- Giảm các triệu chứng của ung thư tiến triển
Bác sĩ có thể đề nghị loại phẫu thuật dựa trên các đặc điểm ung thư vú và tiền sử bệnh lý của bệnh nhân.
1.1.1. Phẫu thuật cắt bỏ khối u ung thư vú:
Có hai loại phẫu thuật ung thư vú chính:
- Phẫu thuật bảo tồn vú: là phẫu thuật cắt bỏ ung thư cũng như một số mô bình thường xung quanh. Chỉ cắt bỏ phần vú có chứa ung thư. Lượng mô vú bị cắt bỏ phụ thuộc vào vị trí và kích thước của khối u và các yếu tố khác. Phẫu thuật này còn được gọi là cắt bỏ khối u, cắt bỏ một phần tư vú, cắt bỏ một phần vú.
- Cắt trọn vú: là phẫu thuật cắt bỏ toàn bộ vú, bao gồm tất cả các mô vú và đôi khi là các mô lân cận vú. Một số trường hợp cần cắt bỏ cả hai vú.
Lựa chọn giữa phẫu thuật bảo tồn vú và cắt bỏ vú
Ung thư giai đoạn đầu có thể lựa chọn giữa phẫu thuật bảo tồn vú và cắt trọn vú. Ưu điểm chính của phẫu thuật bảo tồn là giữ lại hầu hết mô vú, nhưng thường sẽ cần xạ trị sau đó. Trường hợp cắt trọn vú để điều trị ung thư giai đoạn đầu thì ít cần xạ trị hơn.
Đối với trường hợp kích thước khối u lớn, đã có xạ trị trước đó thì cắt trọn vú là lựa chọn phù hợp hơn so với phẫu thuật bảo tồn.
Một số bệnh nhân có thể lo lắng rằng phẫu thuật bảo tồn cắt bỏ ít mô hơn có thể làm tăng nguy cơ ung thư tái phát. Nhưng các nghiên cứu trên hàng nghìn phụ nữ trong hơn 20 năm cho thấy ở những người mắc ung thư giai đoạn đầu (có thể áp dụng cả hai loại phẫu thuật) thì tỷ lệ sống còn của phương pháp phẫu thuật bảo tồn kết hợp xạ trị cũng tương đương phương pháp cắt trọn vú.
1.1.2. Phẫu thuật cắt bỏ hạch bạch huyết lân cận
Để xem xét liệu ung thư vú có di căn đến các hạch bạch huyết dưới cánh tay (nách) hay chưa, bác sĩ sẽ phẫu thuật cắt bỏ một hoặc nhiều hạch bạch huyết này và gửi phòng xét nghiệm giải phẫu bệnh tìm tế bào ung thư. Cắt hạch có thể thực hiện ngay trong ca phẫu thuật ung thư vú hoặc được tiến hành như một ca phẫu thuật riêng biệt.
Có hai loại phẫu thuật chính để cắt bỏ các hạch bạch huyết là:
- Sinh thiết hạch gác cửa: Bác sĩ phẫu thuật sẽ tiêm thuốc nhuộm màu và sau đó chỉ cắt bỏ các hạch nách đã hấp thụ thuốc nhuộm màu. Các hạch bạch huyết gác cửa là hạch đầu tiên mà tế bào ung thư có khả năng di căn đến. Chỉ cắt bỏ một hoặc vài hạch sẽ làm giảm nguy cơ biến cố không mong muốn như sưng nách (phù bạch huyết) so với phương pháp cắt bỏ hạch nách (được mô tả bên dưới).
- Cắt bỏ hạch nách: là một thủ thuật không sử dụng thuốc nhuộm. Bác sĩ phẫu thuật cắt bỏ nhiều hạch nách dưới cánh tay (thường ít hơn 20). Mặc dù cắt bỏ hạch nách không được thực hiện thường xuyên như trước đây, nhưng nó vẫn là cách tốt nhất để đánh giá hạch trong một số trường hợp.
1.1.3. Tái tạo vú sau phẫu thuật
Nhiều phụ nữ có thể chọn phẫu thuật tái tạo vú sau phẫu thuật ung thư vú, mục đích là tái tạo gò vú giúp phục hồi hình dáng vú sau phẫu thuật. Trong một số ca phẫu thuật bảo tồn vú, có thể cấy mỡ vào vú để làm đầy vết lõm sau phẩu thuật.
Tùy thuộc vào tình trạng sức khỏe và sở thích cá nhân của bệnh nhân, có thể lựa chọn loại phẫu thuật tái tạo phù hợp: Tái tạo vú cùng lúc với phẫu thuật (tái tạo tức thì) hoặc một thời gian sau phẫu thuật (tái tạo chậm).
Nếu bệnh nhân đang nghĩ đến việc phẫu thuật tái tạo thì nên thảo luận với bác sĩ phẫu thuật vú và bác sĩ phẫu thuật thẩm mỹ trước ca phẫu thuật ung thư vú (cắt trọn vú hoặc phẫu thuật bảo tồn). Điều này giúp nhóm phẫu thuật có thời gian lập kế hoạch các phương án điều trị phù hợp nhất.
1.1.4. Phẫu thuật cho bệnh ung thư vú tiến triển
Mặc dù phẫu thuật rất khó chữa dứt ung thư vú đã di căn đến các bộ phận khác của cơ thể, nhưng nó vẫn có ích trong một số trường hợp, như làm chậm sự xâm lấn, lan rộng của ung thư hoặc giúp ngăn ngừa hay làm giảm các triệu chứng. Ví dụ, phẫu thuật có thể được sử dụng:
- Khi khối u vú gây ra vết thương hở ở vú
- Để điều trị một số vùng bị ung thư di căn, chẳng hạn như não
- Khi khối u ung thư chèn ép tủy sống hoặc di căn xương gây ra các biến chứng ở tủy sống hoặc làm gãy xương
- Để điều trị tắc nghẽn ở gan
- Để giảm đau hoặc các triệu chứng khác
Nếu bác sĩ có chỉ định phẫu thuật cho ung thư vú tiến triển, bệnh nhân cần biết mục đích của phẫu thuật là để cố gắng chữa bệnh ung thư hay để ngăn ngừa hoặc điều trị các triệu chứng, biến chứng do ung thư gây ra.
1.2. Xạ trị ung thư vú
Xạ trị là phương pháp điều trị bằng tia năng lượng cao (hoặc bằng các hạt) để tiêu diệt tế bào ung thư. Một số trường hợp ung thư vú sẽ cần xạ trị, ngoài các phương pháp điều trị khác.
Tùy thuộc vào giai đoạn ung thư vú và các yếu tố khác, xạ trị có thể được sử dụng trong một số trường hợp:
- Sau phẫu thuật bảo tồn vú, giúp giảm nguy cơ ung thư tái phát ở cùng một bên vú hoặc các hạch lân cận.
- Sau phẫu thuật cắt trọn vú, đặc biệt khi ung thư lớn hơn 5 cm, hoặc khi phát hiện thấy tế bào ung thư ở nhiều hạch bạch huyết, ở vùng rìa phẫu thuật như da hoặc cơ.
- Nếu ung thư đã di căn đến các bộ phận khác của cơ thể, chẳng hạn như xương, tủy sống hoặc não.
Các loại xạ trị ung thư vú:
Các loại xạ trị chính có thể được sử dụng để điều trị ung thư vú là:
Xạ trị chiếu ngoài
Xạ trị chiếu trong
- Xạ trị chiếu ngoài: là loại xạ trị phổ biến nhất đối với ung thư vú. Một máy chiếu tia xạ bên ngoài cơ thể sẽ tập trung bức xạ vào vùng bị ung thư.
Những vùng cần xạ trị tùy thuộc vào phương pháp phẫu thuật (cắt trọn vú hay phẫu thuật bảo tồn vú) và tình trạng hạch bạch huyết lân cận đã bị xâm lấn hay chưa.
Nếu là phẫu thuật cắt trọn vú và không có hạch bạch huyết bị ung thư xâm lấn thì xạ trị sẽ tập trung vào thành ngực, vết sẹo phẫu thuật cắt trọn vú và những vị trí ống dẫn lưu được đặt sau phẫu thuật.
Nếu là phẫu thuật bảo tồn vú, rất có thể bệnh nhân sẽ được xạ trị toàn bộ vú. Một đợt xạ trị tăng cường vào vùng mô ung thư vú đã được cắt bỏ (gọi là nền khối u) là cần thiết nguy cơ ung thư tái phát cao. Đợt xạ trị tăng cường thường được thực hiện sau khi kết thúc các đợt điều trị, sử dụng cùng một loại máy xạ trị, với lượng tia xạ thấp hơn tập trung vào nền khối u. Hầu hết bệnh nhân không nhận thấy sự khác nhau về tác dụng phụ giữa xạ trị tăng cường và xạ trị toàn bộ vú.
Nếu phát hiện ung thư ở các hạch bạch huyết dưới cánh tay (hạch nách), có thể xạ trị. Đôi khi, xạ trị cũng được chỉ định cho các hạch phía trên xương đòn (hạch thượng đòn) và các hạch bên dưới xương ức ở giữa ngực (hạch vú trong).
Thời gian bắt đầu xạ trị chiếu ngoài: thường sau khi lành vết mổ, khoảng một tháng hoặc lâu hơn. Nếu bệnh nhân đang được hóa trị, thì thường chờ đến khi hóa trị hoàn tất mới bắt đầu xạ trị. Một số phương pháp điều trị sau phẫu thuật, như liệu pháp hormone hoặc liệu pháp nhắm trúng đích HER2 có thể được thực hiện cùng lúc với xạ trị.
Tác dụng phụ có thể xảy ra của xạ trị chiếu ngoài
Các tác dụng phụ ngắn hạn chính của xạ trị chùm ngoài đối với vú là:
- Sưng ở vú
- Mệt mỏi
- Những thay đổi về da ở vùng được điều trị tương tự như cháy nắng (đỏ, bong tróc da, sạm da)
Bệnh nhân được khuyên tránh để vùng da được điều trị tiếp xúc với ánh nắng mặt trời vì có thể khiến những thay đổi về da trở nên tồi tệ hơn. Hầu hết những thay đổi về da sẽ cải thiện trong vòng vài tháng. Những thay đổi ở mô vú thường biến mất trong vòng 6 đến 12 tháng, nhưng có thể mất nhiều thời gian hơn.
Xạ trị chùm ngoài cũng có thể gây ra những tác dụng phụ về lâu dài:
- Vú nhỏ lại và da trở nên săn chắc hoặc sưng lên.
- Xạ trị có thể ảnh hưởng đến các lựa chọn tái tạo vú sau này. Xạ trị cũng có thể làm ảnh hưởng quá trình lành vết thương nếu xạ trị được thực hiện sau phẫu thuật tái tạo, đặc biệt là các thủ thuật vạt mô.
- Những phụ nữ đã xạ trị vú có thể không thể cho con bú từ vú đã xạ trị.
- Xạ trị vào vú đôi khi có thể làm tổn thương một số dây thần kinh ở cánh tay, gây bệnh lý đám rối thần kinh cánh tay và có thể gây tê, đau và yếu ở vai, cánh tay và bàn tay.
- Xạ trị vào các hạch dưới cánh tay có thể gây phù bạch huyết, gây đau và sưng ở cánh tay hoặc ngực.
- Trong một số trường hợp hiếm gặp, xạ trị có thể làm yếu và gãy xương sườn
- Trước đây, phổi và tim có nhiều khả năng bị tia xạ chiếu, có thể dẫn đến tổn thương lâu dài. Thiết bị xạ trị hiện đại ngày nay tập trung các chùm tia xạ tốt hơn so với các máy đời cũ, vì vậy những vấn đề này ngày nay rất hiếm gặp.
- Một biến chứng rất hiếm gặp của xạ trị vú là sự phát triển của một loại ung thư khác gọi là angiosarcoma (Sarcome mạch máu)
- Xạ trị chiếu trong: còn được gọi là xạ trị trong, là một cách khác để thực hiện liệu pháp xạ trị. Thay vì chiếu các chùm tia xạ từ bên ngoài cơ thể, một thiết bị chứa hạt hoặc viên phóng xạ được đặt vào mô vú trong một thời gian ngắn tại khu vực đã cắt bỏ khối u (nền khối u).
Tác dụng phụ có thể xảy ra của xạ trị chiếu trong
Giống như xạ trị chiếu ngoài, xạ trị chiếu trong có thể có tác dụng phụ, bao gồm:
- Đỏ và/hoặc bầm tím tại vị trí điều trị
- Đau vú
- Nhiễm trùng
- Tổn thương mô mỡ ở ngực
- Yếu và gãy xương sườn trong một số trường hợp hiếm gặp
- Tụ dịch trong vú
2. Điều trị toàn thân
Các loại thuốc dùng để điều trị ung thư vú được coi là liệu pháp toàn thân vì chúng có thể tiếp cận các tế bào ung thư ở hầu hết mọi nơi trong cơ thể. Một số thuốc được dùng qua đường uống, tiêm vào cơ (tiêm bắp) hoặc tiêm trực tiếp vào máu. Tùy thuộc vào loại ung thư vú, các loại thuốc điều trị khác nhau có thể được sử dụng, bao gồm:
- Hóa trị
- Liệu pháp hormone
- Liệu pháp nhắm trúng đích
- Liệu pháp miễn dịch
2.1. Hóa trị
Hóa trị sử dụng thuốc chống ung th, tiêm tĩnh mạch hoặc uống. Thuốc đi vào mạch máu để đến các tế bào ung thư ở hầu hết các bộ phận trong cơ thể.
Trường hợp tế bào ung thư di căn đến dịch não tủy và tủy sống, hóa trị có thể được đưa trực tiếp vào khu vực này, được gọi là hóa trị nội tủy.
Khi nào thì hóa trị được sử dụng cho bệnh ung thư vú?
Không phải tất cả bệnh nhân ung thư vú đều cần hóa trị, nhưng có một số trường hợp cần hóa trị.
- Sau phẫu thuật (hóa trị bổ trợ)
Hóa trị bổ trợ được dùng để cố gắng tiêu diệt tế bào ung thư còn sót lại hoặc đã di căn nhưng không thể nhìn thấy, ngay cả trên các xét nghiệm hình ảnh. Nếu những tế bào ung thư này phát triển, chúng có thể hình thành khối u mới ở những nơi khác trong cơ thể. Hóa trị bổ trợ giúp giảm nguy cơ ung thư vú tái phát.
- Trước phẫu thuật (hóa trị tân bổ trợ)
Hóa trị trước phẫu thuật giúp thu nhỏ khối u, để có thể cắt bỏ bằng phẫu thuật. Do đó, hóa trị trước phẫu thuật thường được sử dụng để điều trị các trường hợp ung thư có kích thước khối u quá lớn không thể phẫu thuật cắt bỏ khi mới được chẩn đoán, có nhiều hạch bạch huyết nghi bị ung thư xâm lấn hoặc là ung thư vú dạng viêm.
Nếu sau hóa trị tân bổ trợ và phẫu thuật xong mà các tế bào ung thư vẫn còn thì có thể tiếp tục dùng hóa trị bổ trợ để giảm nguy cơ ung thư tái phát.
Hóa trị tân bổ trợ còn được dùng trong các trường hợp sau:
- Bằng cách hóa trị trước khi cắt bỏ khối u, bác sĩ đánh giá ung thư phản ứng với hóa trị như thế nào. Nếu đợt thuốc hóa trị đầu tiên không làm khối u co nhỏ lại, thì cần phải dùng các loại thuốc khác. Hóa trị cũng sẽ tiêu diệt bất kỳ tế bào ung thư nào có thể đã di căn nhưng không thể nhìn thấy bằng mắt thường hoặc trên các xét nghiệm hình ảnh. Cũng giống như hóa trị bổ trợ, hóa trị tân bổ trợ có thể làm giảm nguy cơ ung thư vú tái phát.
- Một số trường hợp ung thư giai đoạn đầu được hóa trị tân bổ trợ có thể sống lâu hơn nếu ung thư biến mất hoàn toàn sau điều trị, thường thấy nhất ở những phụ nữ bị ung thư vú bộ ba âm tính hoặc ung thư vú HER2 dương tính.
Cần lưu ý không phải tất cả bệnh nhân ung thư vú đều phù hợp cho hóa trị tân bổ trợ.
- Ung thư vú di căn
Hóa trị là liệu pháp chính cho những trường hợp ung thư đã di căn ra khỏi vú và vùng nách, đến các cơ quan xa như gan, phổi... Hóa trị có thể được sử dụng khi ung thư vú được chẩn đoán hoặc sau các đợt điều trị ban đầu. Thời gian điều trị phụ thuộc vào hiệu quả của hóa trị và mức độ dung nạp của bệnh nhân.
Các thuốc hóa trị dùng cho ung thư vú
Trong hầu hết các trường hợp, hóa trị có hiệu quả cao nhất khi phối hợp đồng thời nhiều thuốc, thường là kết hợp 2 hoặc 3 loại thuốc.
Thuốc hóa trị bổ trợ và tân bổ trợ:
- Anthracycline, chẳng hạn như doxorubicin (Adriamycin) và epirubicin (Ellence)
- Taxane, chẳng hạn như paclitaxel (Taxol) và docetaxel (Taxotere)
- 5-fluorouracil (5-FU) hoặc capecitabine (Xeloda)
- Cyclophosphamide (Cytoxan)
- Carboplatin (Paraplatin)
Thuốc hóa trị cho ung thư vú đã di căn:
- Taxane: Paclitaxel (Taxol), docetaxel (Taxotere) và paclitaxel liên kết albumin (Abraxane)
- Ixabepilone (Ixempra)
- Eribulin (Halaven)
- Anthracycline: Doxorubicin (Adriamycin), doxorubicin dạng liposome (Doxil) và epirubicin (Ellence)
- Thuốc chứa bạch kim (Cisplatin, carboplatin)
- Vinorelbine (Navelbine)
- Capecitabine (Xeloda)
- Gemcitabine (Gemzar)
Đối với các loại ung thư dương tính với HER2, một hoặc nhiều loại thuốc nhắm trúng đích HER2 có thể được sử dụng cùng với hóa trị. (Xem Liệu pháp nhắm trúng đích bên dưới)
Hóa trị ung thư vú được thực hiện như thế nào?
Thuốc hóa trị ung thư vú thường được truyền vào tĩnh mạch bằng cách tiêm trong vài phút hoặc truyền trong thời gian dài hơn.
Thông thường, cần phải có một catheter (ống thông) được đặt trong tĩnh mạch (gọi là đường truyền trung tâm). Đường truyền này được sử dụng để đưa thuốc, chế phẩm của máu, chất dinh dưỡng hoặc dịch trực tiếp vào máu, và cũng được sử dụng để lấy máu làm xét nghiệm.
Ở bệnh nhân ung thư vú, đường truyền trung tâm thường được đặt ở bên đối diện với vú bị ung thư. Trong trường hợp ung thư cả hai bên vú, thì đường truyền trung tâm thường được đặt ở bên có ít hạch bạch huyết bị cắt bỏ do ung thư xâm lấn hơn.
Hóa trị được thực hiện theo chu kỳ, sau đó là thời gian nghỉ ngơi để bệnh nhân có thời gian phục hồi. Chu kỳ hóa trị thường kéo dài 2 hoặc 3 tuần. Lịch trình thay đổi tùy thuộc vào loại thuốc được sử dụng. Ví dụ, với một số loại thuốc, hóa trị chỉ được thực hiện vào ngày đầu tiên của chu kỳ. Với những loại thuốc khác, hóa trị được thực hiện một ngày một tuần, trong vài tuần liên tục hoặc cách tuần. Lịch trình hóa trị được lặp lại cho chu kỳ tiếp theo.
Hóa trị bổ trợ và tân bổ trợ thường được thực hiện trong tổng thời gian từ 3 đến 6 tháng, tùy thuộc vào loại thuốc được sử dụng. Thời gian điều trị ung thư vú di căn (giai đoạn 4) phụ thuộc vào hiệu quả và tác dụng phụ của thuốc.
Tác dụng phụ có thể xảy ra của hóa trị ung thư vú
Thuốc hóa trị có thể gây ra tác dụng phụ, tùy thuộc vào loại và liều lượng thuốc được sử dụng cũng như thời gian điều trị. Một số tác dụng phụ phổ biến bao gồm:
Rụng tóc
Thay đổi móng tay
Lở miệng
Mất cảm giác thèm ăn hoặc thay đổi cân nặng
Buồn nôn và nôn
Tiêu chảy
Mệt mỏi
Bốc hỏa và/hoặc khô âm đạo do mãn kinh do hóa trị (xem “Thay đổi kinh nguyệt và các vấn đề về khả năng sinh sản” bên dưới)
Tổn thương thần kinh (xem “”ổn thương thần kinh” bên dưới)
Hóa trị cũng có thể ảnh hưởng đến các tế bào tạo máu của tủy xương, có thể dẫn đến:
Tăng nguy cơ nhiễm trùng (do giảm bạch cầu)
Dễ bị bầm tím hoặc chảy máu (do giảm tiểu cầu)
Mệt mỏi (do giảm hồng cầu)
Những tác dụng phụ này thường biến mất sau khi kết thúc quá trình điều trị. Có nhiều cách để làm giảm những tác dụng phụ này. Ví dụ, dùng thuốc chống nôn để giúp ngăn hoặc giảm cảm giác buồn nôn và nôn.
Thay đổi kinh nguyệt và các vấn đề về khả năng sinh sản
Đối với phụ nữ trẻ, thay đổi chu kỳ kinh nguyệt là tác dụng phụ phổ biến của hóa trị. Hóa trị có thể gây mãn kinh sớm và vô sinh, khi đó nguy cơ mắc bệnh tim, mất xương, loãng xương cũng sẽ tăng lên. Có những thuốc có thể điều trị hoặc ngăn ngừa tình trạng mất xương.
Ngay cả khi mất kinh trong quá trình hóa trị thì bệnh nhân vẫn có thể mang thai. Mang thai trong khi đang hóa trị có gây dị tật bẩm sinh cho thai nhi và ảnh hưởng đến quá trình điều trị. Nếu bệnh nhân chưa mãn kinh trước khi điều trị và đang hoạt động tình dục, thì cần phải thảo luận với bác sĩ về các biện pháp tránh thai. Phụ nữ ung thư vú dương tính với thụ thể hormone không nên dùng thuốc tránh thai bằng hormone. Cần phải trao đổi với cả bác sĩ ung thư và bác sĩ sản phụ khoa về những lựa chọn phương pháp tránh thai phù hợp nhất. Khi phụ nữ đã hoàn tất hóa trị thì có thể sinh con một cách an toàn.
Nếu bệnh nhân muốn sinh con sau khi điều trị ung thư vú thì cần trao đổi với bác sĩ ngay sau khi được chẩn đoán và trước khi bắt đầu điều trị. Trong một số trường hợp có thể sử dụng một thuốc tương tự hormone phóng thích hormone hoàng thể hóa (LHRH), cùng với hóa trị, có thể giúp có thai sau khi điều trị ung thư.
Nếu bệnh nhân đang mang thai mắc ung thư vú thì vẫn có thể được điều trị. Một số loại thuốc hóa trị có thể được sử dụng an toàn trong 2 tam cá nguyệt cuối của thai kỳ. Xem thêm mục “Điều trị ung thư vú trong thai kỳ”.
Tổn thương tim
Mặc dù không phổ biến nhưng thuốc doxorubicin, epirubicin và một số loại thuốc hóa trị khác có thể gây tổn thương cơ tim vĩnh viễn (gọi là bệnh cơ tim). Nguy cơ cao nhất nếu thuốc được sử dụng trong thời gian dài hoặc dùng liều cao. Nguy cơ tổn thương cơ tim cũng tăng lên nếu các thuốc này được phối hợp với các loại thuốc khác có thể gây tổn thương tim (chẳng hạn như thuốc nhắm trúng đích HER2). Các yếu tố nguy cơ như tiền sử gia đình mắc bệnh tim, tăng huyết áp và bệnh tiểu đường cũng có thể làm tăng nguy cơ tổn thương tim khi dùng một trong những loại thuốc này.
Do đó, trước khi bắt đầu hóa trị bằng những thuốc này thì bệnh nhân sẽ được kiểm tra chức năng tim (như siêu âm tim). Bác sĩ cũng kiểm soát cẩn thận liều lượng, theo dõi các triệu chứng của bệnh tim và chức năng tim của bệnh nhân trong quá trình điều trị. Nếu chức năng tim bắt đầu suy giảm, bác sĩ sẽ ngưng tạm thời hoặc vĩnh viễn loại thuốc đang điều trị. Tuy nhiên, cũng có trường hợp các dấu hiệu tổn thương tim không xuất hiện cho đến nhiều tháng hoặc nhiều năm sau khi ngừng điều trị.
Tổn thương thần kinh (bệnh thần kinh ngoại biên)
Nhiều loại thuốc dùng để điều trị ung thư vú, bao gồm taxane (docetaxel, paclitaxel và paclitaxel gắn protein), thuốc chứa platinum (carboplatin, cisplatin), vinorelbine, eribulin và ixabepilone, có thể gây tổn thương thần kinh ở tay, cánh tay, bàn chân và chân. Khi đó bệnh nhân có thể bị tê, đau, yếu, cảm giác nóng rát hoặc ngứa, nhạy cảm với lạnh hoặc nóng. Trong hầu hết các trường hợp, các triệu chứng này sẽ biến mất sau khi ngừng điều trị, nhưng cũng có trường hợp có thể kéo dài hoặc tồn tại vĩnh viễn.
Hội chứng tay-chân
Một số loại thuốc hóa trị, chẳng hạn như capecitabine (Xeloda) và doxorubicin dạng liposome (Doxil), có thể gây kích ứng lòng bàn tay và lòng bàn chân, gọi là hội chứng tay-chân. Các triệu chứng ban đầu bao gồm tê, ngứa và đỏ. Nếu nặng hơn thì bàn tay và bàn chân có thể bị sưng hoặc thậm chí đau. Da có thể phồng rộp, dẫn đến bong tróc hoặc thậm chí là lở loét. Các triệu chứng này dần cải thiện khi ngừng thuốc hoặc giảm liều. Cách tốt nhất để ngăn ngừa hội chứng tay-chân nặng là báo cho bác sĩ biết khi các triệu chứng mới xuất hiện, để có thể thay đổi liều lượng hoặc có thể chuyển sang thuốc khác.
Tăng nguy cơ mắc bệnh bạch cầu
Rất hiếm khi một số loại thuốc hóa trị, chẳng hạn như doxorubicin (Adriamycin), có thể gây ra các bệnh về tủy xương, ví dụ như hội chứng loạn sản tủy hoặc thậm chí là bệnh bạch cầu tủy cấp tính, là một loại ung thư của tế bào bạch cầu. Nếu các biến chứng này xảy ra, thì thường là trong vòng 10 năm sau khi điều trị. Đối với hầu hết phụ nữ, lợi ích của hóa trị để ngừa ung thư vú tái phát hoặc kéo dài tuổi thọ vượt xa nguy cơ mắc biến chứng nặng hiếm gặp này.
Mệt mỏi do hóa trị
Mệt mỏi là một tác dụng phụ phổ biến của hóa trị. Nhiều phụ nữ cảm thấy không khỏe sau hóa trị, có cảm giác đau nhức cơ thể hoặc nhức mỏi và giảm chức năng thể chất nhẹ. Những thay đổi này thường diễn tiến chậm theo thời gian.
Tình trạng này có thể kéo dài từ vài tháng đến vài năm. Bệnh nhân cần báo cho bác sĩ biết về tình trạng này. Tập thể dục, ngủ trưa và tiết kiệm năng lượng có thể giúp cải thiện mệt mỏi. Cũng có khi bệnh nhân bị mất ngủ và cần điều trị. Đôi khi mệt mỏi có thể là dấu hiệu của bệnh trầm cảm, có thể được cải thiện bằng tư vấn và/hoặc dùng thuốc.
2.2. Liệu pháp hormone
Một số loại ung thư vú bị ảnh hưởng bởi nội tiết tố (hormone) như estrogen và progesterone. Các tế bào ung thư vú có các thụ thể gắn với estrogen và progesterone để giúp chúng phát triển. Các phương pháp điều trị để ngăn các hormone này gắn vào các thụ thể hoặc giảm nồng độ các hormone được gọi là liệu pháp hormone hoặc liệu pháp nội tiết.
Liệu pháp hormone có thể tiếp cận các tế bào ung thư hầu như ở mọi nơi trong cơ thể chứ không chỉ ở vú. Liệu pháp này được khuyến nghị cho những trường hợp ung thư vú dương tính với thụ thể hormone (tế bào ung thư có thụ thể hormone) nhưng không có tác dụng với những trường hợp ung thư âm tính với thụ thể hormone (tế bào ung thư không có thụ thể hormone).
Khi nào dùng liệu pháp hormone?
Liệu pháp hormone thường được sử dụng sau phẫu thuật (như liệu pháp bổ trợ) để giúp giảm nguy cơ ung thư tái phát. Đôi khi cũng được sử dụng trước phẫu thuật (như liệu pháp tân bổ trợ).
Liệu pháp hormone thường được sử dụng kéo dài, trong ít nhất 5 năm. Có thể hơn 5 năm cho những trường hợp có nguy cơ tái phát ung thư cao hơn. Có một xét nghiệm tên là “Chỉ số ung thư vú” có thể giúp đánh giá xem có nên dùng liệu pháp hormone kéo dài hơn 5 năm hay không.
Liệu pháp hormone cũng có thể được sử dụng để điều trị ung thư tái phát sau khi điều trị hoặc đã di căn đến cơ quan khác trong cơ thể.
Liệu pháp hormone hoạt động như thế nào?
Khoảng 2/3 trường hợp ung thư vú là dương tính với thụ thể hormone, nghĩa là các tế bào ung thư có thụ thể gắn với estrogen (ung thư dương tính với thụ thể estrogen) và/hoặc progesterone (ung thư dương tính với thụ thể progesterone) để giúp các tế bào ung thư phát triển và lan rộng.
Hầu hết các liệu pháp hormone hoạt động theo cơ chế: hoặc là làm giảm nồng độ estrogen hoặc là ngăn không cho estrogen gắn vào thụ thể (chặn thụ thể estrogen).
2.2.1. Thuốc chặn thụ thể estrogen
Những loại thuốc này ức chế sự phát triển ung thư vú bằng cách ngăn không cho estrogen gắn vào thụ thể của nó.
Thuốc điều biến thụ thể estrogen chọn lọc (SERM: Selective estrogen receptor modulators)
Thuốc nhóm này ngăn estrogen gắn kết với các tế bào ung thư và không cho chúng phát triển và phân chia. Những thuốc này có tác dụng chống estrogen trong các tế bào vú, nhưng lại hoạt động giống như estrogen trong các mô khác, như tử cung và xương.
Loại thuốc nhóm này là thuốc viên, dùng đường uống.
Tamoxifen: sử dụng để điều trị cho những phụ nữ bị ung thư vú đã hoặc chưa mãn kinh, có thể được sử dụng theo một số cách:
- Ở những phụ nữ có nguy cơ mắc ung thư vú cao, tamoxifen có thể được sử dụng để giúp giảm nguy cơ phát triển ung thư vú.
- Đối với những trường hợp ung thư biểu mô ống tuyến vú tại chỗ dương tính với thụ thể hormone đã được điều trị bằng phẫu thuật bảo tồn, dùng tamoxifen trong 5 năm sẽ làm giảm nguy cơ tái phát ở cùng một bên vú, giảm nguy cơ bị ung thư vú xâm lấn hoặc ung thư biểu mô ống tuyến vú tại chỗ ở cả hai bên vú.
- Đối với phụ nữ bị ung thư vú xâm lấn dương tính với thụ thể hormone đã được điều trị bằng phẫu thuật, tamoxifen có thể giúp giảm nguy cơ ung thư tái phát và cải thiện cơ hội sống lâu hơn. Thuốc cũng có thể làm giảm nguy cơ ung thư mới khởi phát ở vú còn lại. Có thể bắt đầu tamoxifen sau phẫu thuật (liệu pháp bổ trợ) hoặc trước phẫu thuật (liệu pháp tân bổ trợ). Thuốc thường được sử dụng trong 5 đến 10 năm nếu dùng sau phẫu thuật. Tamoxifen chủ yếu được sử dụng cho những phụ nữ bị ung thư vú giai đoạn đầu chưa mãn kinh. Nếu đã mãn kinh thì thuốc ức chế men aromatase (xem bên dưới) thường được sử dụng để thay thế.
- Đối với những trường hợp ung thư vú dương tính với hormone đã di căn đến các cơ quan khác trong cơ thể, tamoxifen có thể giúp làm chậm hoặc ngăn chặn sự phát triển của ung thư và thậm chí có thể làm co nhỏ khối u.
Toremifene (Fareston)
Toremifene là một thuốc điều biến thụ thể estrogen chọn lọc, có tác dụng tương tự tamoxifen, nhưng ít được sử dụng hơn và chỉ được chấp thuận để điều trị cho những phụ nữ sau mãn kinh bị ung thư vú di căn. Thuốc thường không có tác dụng nếu tamoxifen đã được sử dụng và không còn hiệu quả.
Tác dụng phụ của tamoxifen và toremifene
Các tác dụng phụ thường gặp nhất của tamoxifen và toremifene là:
Bốc hỏa
Âm đạo bị khô hoặc tiết dịch
Rối loạn chu kỳ kinh nguyệt
Ở một số ít phụ nữ bị ung thư vú đã di căn xương, khi bắt đầu điều trị bằng tamoxifen thì khối u xương có thể to hơn trong thời gian ngắn và có thể gây đau xương. Tình trạng này thường biến mất nhanh chóng, và hiếm khi gây canxi máu khó kiểm soát. Nhưng nếu có, thì có thể phải ngừng điều trị một thời gian.
Các tác dụng phụ hiếm gặp nhưng nghiêm trọng hơn cũng có thể xảy ra:
- Ở phụ nữ đã mãn kinh, thuốc điều biến thụ thể estrogen chọn lọc có thể làm tăng nguy cơ ung thư nội mạc tử cung và sarcoma tử cung. Hãy báo ngay cho bác sĩ nếu có chảy máu âm đạo bất thường. Chảy máu tử cung không hẳn là do ung thư, nhưng cần được phát hiện, và xử trí nhanh chóng.
- Tạo huyết khối (cục máu đông) là một tác dụng phụ hiếm gặp khác nhưng nghiêm trọng. Huyết khối thường được tạo thành ở chân (gọi là huyết khối tĩnh mạch sâu), nhưng có khi một cục máu đông ở chân có thể di chuyển lên trên và làm tắc động mạch ở phổi gây thuyên tắc phổi. Hãy báo ngay cho bác sĩ hoặc y tá nếu bị đau, đỏ hoặc sưng ở bắp chân (có thể là triệu chứng của huyết khối tĩnh mạch sâu), hoặc bị khó thở hay đau ngực (có thể là triệu chứng của thuyên tắc phổi). Tamoxifen hiếm khi có liên quan đến đột quỵ ở phụ nữ sau mãn kinh, nhưng nếu bệnh nhân đột nhiên bị đau đầu dữ dội, lú lẫn, nói khó, khó cử động hay đi đứng thì báo ngay cho bác sĩ.
- Đục thủy tinh thể đôi khi xãy ra khi dùng tamoxifen. Hãy chú ý đến thị lực và báo ngay nếu có bất thường.
- Tác động lên xương: Tamoxifen có thể khiến xương mỏng đi ở phụ nữ tiền mãn kinh. Tuy nhiên, lợi ích của thuốc này lớn hơn nguy cơ ở đa số phụ nữ bị ung thư vú dương tính với thụ thể hormone.
Thuốc phân hủy thụ thể estrogen chọn lọc (SERD: Selective estrogen receptor degraders)
Giống như thuốc điều biến thụ thể estrogen chọn lọc (SERM), các loại thuốc nhóm phân hủy thụ thể estrogen chon lọc (SERD) gắn vào thụ thể estrogen. Nhưng SERD gắn chặt hơn vào thụ thể và khiến chúng bị phân hủy. Thuốc nhóm này có tác dụng chống estrogen trong toàn bộ cơ thể.
SERD thường được sử dụng nhất ở những phụ nữ đã mãn kinh. Khi dùng cho phụ nữ tiền mãn kinh, cần kết hợp với chất chủ vận hormone giải phóng hormone hoàng thể (LHRH) để ức chế buồng trứng.
Fulvestrant (Faslodex)
Fulvestrant được chỉ định sử dụng trong các trường hợp sau:
- Chỉ dùng để điều trị ung thư vú tiến triển chưa được điều trị bằng liệu pháp hormone khác.
- Chỉ dùng để điều trị ung thư vú tiến triển sau khi các loại thuốc hormone khác (như tamoxifen và thường là thuốc ức chế aromatase) đã hết tác dụng.
- Kết hợp với thuốc ức chế CDK 4/6 hoặc thuốc ức chế PI3K để điều trị ung thư vú di căn như liệu pháp hormone ban đầu hoặc sau khi đã thử các liệu pháp hormone khác.
Thuốc được tiêm 2 mũi vào mông (dưới). Trong tháng đầu tiên, tiêm 2 mũi cách nhau 2 tuần. Sau đó, tiêm một mũi mỗi tháng.
Elacestrant (Orserdu)
Thuốc này được sử dụng để điều trị ung thư vú tiến triển, thụ thể estrogen dương tính, HER2 âm tính khi các tế bào ung thư có đột biến gen ESR1 và ung thư tiến triển sau ít nhất một loại liệu pháp hormone khác.
Elacestrant được uống hàng ngày dưới dạng viên nén.
Tác dụng phụ của fulvestrant và elacestrant
Các tác dụng phụ ngắn hạn phổ biến của những loại thuốc này có thể bao gồm:
- Bốc hỏa và/hoặc đổ mồ hôi đêm
- Đau đầu
- Buồn nôn
- Mệt mỏi
- Mất cảm giác thèm ăn
- Đau cơ, khớp hoặc xương
- Đau tại chỗ tiêm
- Elacestrant cũng có thể làm tăng cholesterol và mỡ máu.
2.2.2. Thuốc làm giảm nồng độ estrogen
Vì estrogen kích thích loại ung thư vú dương tính với thụ thể hormone phát triển, nên việc giảm nồng độ estrogen có thể giúp làm chậm sự phát triển của ung thư hoặc giúp ngăn ngừa ung thư tái phát.
Thuốc ức chế men aromatase
Thuốc ức chế aromatase là thuốc ngăn chặn hầu hết quá trình sản xuất estrogen trong cơ thể. Trước khi mãn kinh, hầu hết estrogen được tạo ra bởi buồng trứng. Nhưng ở những phụ nữ có buồng trứng không hoạt động (do mãn kinh hoặc do một số thuốc điều trị), estrogen vẫn được tạo ra trong mô mỡ do một loại enzyme gọi là aromatase. Thuốc ức chế aromatase tác động bằng cách ngăn aromatase tạo ra estrogen.
Những loại thuốc này phù hợp cho phụ nữ mãn kinh, và cũng có thể được sử dụng ở những phụ nữ tiền mãn kinh khi được phối hợp với thuốc ức chế buồng trứng (xem bên dưới).
Các loại thuốc ức chế aromatase là thuốc viên uống hàng ngày:
Letrozole (Femara)
Anastrozole (Arimidex)
Exemestane (Aromasin)
Tác dụng phụ:
Các tác dụng phụ phổ biến nhất của nhóm này là:
- Bốc hỏa
- Khô âm đạo
- Đau xương và khớp
- Đau cơ
Thuốc ức chế aromatase có tác dụng phụ khác với tamoxifen. Chúng không gây ung thư tử cung và rất hiếm tạo huyết khối. Tuy nhiên, nhóm thuốc này có thể gây đau cơ và cứng và/hoặc đau khớp. Đau khớp có thể tương tự như cảm giác bị viêm đa khớp cùng lúc và bệnh nhân có thể phải chuyển sang một thuốc ức chế aromatase khác như duloxetine (Cymbalta) hoặc tập thể dục thường xuyên và sử dụng thuốc kháng viêm không steroid (NSAID). Đôi khi đau cơ và khớp buộc phải ngưng điều trị. Khi đó, bác sĩ khuyên dùng tamoxifen để hoàn thành 5 đến 10 năm điều trị bằng hormone.
Thuốc nhóm này làm giảm đáng kể nồng độ estrogen ở phụ nữ sau mãn kinh, nên có thể gây loãng xương, và thậm chí gãy xương. Bệnh nhân dùng thuốc này thường xuyên được kiểm tra mật độ xương và có thể bác sĩ chỉ định sử dụng thuốc nhóm bisphosphonates (ví dụ như axit zoledronic [Zometa]) hoặc denosumab (Xgeva, Prolia) để tăng cường sức khỏe của xương.
Ức chế buồng trứng
Đối với phụ nữ tiền mãn kinh, việc cắt bỏ hoặc dùng thuốc ức chế buồng trứng (là nơi sản xuất estrogen chính) thực sự khiến họ trở thành phụ nữ sau mãn kinh. Khi đó có thể sử dụng một số liệu pháp hormone khác, chẳng hạn như thuốc ức chế aromatase. Ức chế buồng trứng cùng với tamoxifen hoặc thuốc ức chế aromatase có thể được khuyến nghị cho những phụ nữ bị ung thư vú có nguy cơ tái phát cao.
Có một số cách để cắt bỏ hoặc ức chế buồng trứng để điều trị ung thư vú:
- Cắt bỏ buồng trứng: Phẫu thuật để cắt bỏ buồng trứng vĩnh viễn.
- Thuốc chủ vận hormone phóng thích hormone hoàng thể hóa (LHRH): Những thuốc nhóm này còn được gọi là chất tương tự hormone phóng thích hormone hoàng thể hóa, và thường được sử dụng hơn phẫu thuật cắt bỏ buồng trứng. Cơ chế tác động của nhóm thuốc này là chặn tín hiệu gửi đến buồng trứng để sản xuất estrogen, gây ra tình trạng mãn kinh tạm thời. Các loại thuốc LHRH phổ biến bao gồm goserelin (Zoladex) và leuprolide (Lupron). Chúng có thể được sử dụng riêng lẻ như một liệu pháp nội tiết tố hoặc kết hợp với các loại thuốc nội tiết tố khác (tamoxifen, thuốc ức chế aromatase, fulvestrant) ở phụ nữ tiền mãn kinh.
- Thuốc hóa trị: Một số loại thuốc hóa trị có thể gây tổn thương và làm mất khả năng sản xuất estrogen của buồng trứng ở phụ nữ tiền mãn kinh. Chức năng của buồng trứng có thể được phục hồi sau nhiều tháng hoặc nhiều năm, nhưng cũng có trường hợp tổn thương buồng trứng là vĩnh viễn, không hồi phục và phụ nữ trở thành mãn kinh.
Tất cả các phương pháp trên đều có thể gây ra các triệu chứng mãn kinh, bao gồm bốc hỏa, đổ mồ hôi đêm, khô âm đạo và thay đổi tính khí.
2.2.3. Liệu pháp hormone sau phẫu thuật ung thư vú
Sau phẫu thuật, liệu pháp hormone có thể được áp dụng để giảm nguy cơ ung thư tái phát. Sử dụng thuốc ức chế aromatase dù là đơn lẻ hay sau khi sử dụng tamoxifen, đã được chứng minh là có hiệu quả hơn so với chỉ dùng tamoxifen trong 5 năm.
Các phác đồ điều trị bằng hormone dưới đây phù hợp ở những phụ nữ sau mãn kinh được chẩn đoán ung thư vú:
- Tamoxifen trong 2 đến 3 năm, sau đó là thuốc ức chế aromatase trong 2 đến 3 năm (tổng thời gian điều trị là 5 năm)
- Tamoxifen trong 2 đến 3 năm, sau đó là thuốc ức chế aromatase trong 5 năm (tổng thời gian điều trị là 7 đến 8 năm)
- Tamoxifen trong 4,5 đến 6 năm, sau đó là thuốc ức chế aromatase trong 5 năm (tổng thời gian điều trị là 9,5 đến 11 năm)
- Tamoxifen trong 5 đến 10 năm
- Thuốc ức chế aromatase trong 5 đến 10 năm
- Thuốc ức chế aromatase trong 2 đến 3 năm, sau đó là tamoxifen trong 2 đến 3 năm (tổng thời gian điều trị là 5 năm)
Đối với những phụ nữ không thể dùng thuốc ức chế aromatase, tamoxifen trong 5 đến 10 năm là một lựa chọn.
Đối với hầu hết những phụ nữ sau mãn kinh có ung thư dương tính với thụ thể hormone, hầu hết sẽ dùng thuốc ức chế aromatase vào một thời điểm nào đó trong quá trình điều trị bổ trợ (sau phẫu thuật). Phương pháp điều trị tiêu chuẩn là dùng những loại thuốc này trong khoảng 5 năm hoặc dùng kết hợp với tamoxifen trong 5 đến 10 năm. Đối với những phụ nữ có nguy cơ tái phát cao hơn, có thể khuyến nghị điều trị bằng hormone trong thời gian dài hơn 5 năm. Tamoxifen là một lựa chọn cho phụ nữ không thể dùng thuốc ức chế aromatase. Dùng tamoxifen trong 10 năm được coi là hiệu quả hơn dùng trong 5 năm, nhưng bác sĩ và bệnh nhân sẽ thảo luận và quyết định lộ trình điều trị tốt nhất cho từng trường hợp cụ thể.
Các phác đồ điều trị dưới đây phù hợp cho những phụ nữ tiền mãn kinh được chẩn đoán ung thư vú:
- Tamoxifen (có hoặc không có ức chế buồng trứng) trong 5 đến 10 năm.
- Tamoxifen (có hoặc không có ức chế buồng trứng) trong 5 năm, sau đó dùng thuốc ức chế aromatase trong 5 năm nếu bệnh nhân đã mãn kinh.
- Một thuốc ức chế aromatase phối hợp với ức chế buồng trứng trong 5 đến 10 năm.
Nếu bệnh nhân bị ung thư vú giai đoạn đầu và chưa mãn kinh khi được chẩn đoán lần đầu, bác sĩ khuyên dùng tamoxifen trước, sau đó dùng thuốc ức chế aromatase sau nếu bệnh nhân mãn kinh trong quá trình điều trị. Một lựa chọn khác là ức chế buồng trứng bằng cách dùng thuốc chủ vận hormone phóng thích hormone hoàng thể hóa (LHRH) phối hợp với thuốc ức chế aromatase. Phụ nữ tiền mãn kinh không nên dùng thuốc ức chế aromatase đơn trị liệu để điều trị ung thư vú vì nó không an toàn và có thể làm tăng nồng độ hormone.
2.2.4. Nếu ung thư tái phát hoặc đã di căn
Tamoxifen, thuốc ức chế aromatase, elacestrant và fulvestrant có thể được sử dụng để điều trị ung thư vú hormone dương tính tiến triển, đặc biệt là ở phụ nữ sau mãn kinh. Phụ nữ tiền mãn kinh được chỉ định dùng tamoxifen hoặc thuốc ức chế aromatase kết hợp với chất chủ vận hormone phóng thích hormone hoàng thể hóa để điều trị ung thư tiến triển.
2.2.5. Các loại liệu pháp hormone ít phổ biến hơn
Một số liệu pháp hormone khác thường được sử dụng trong quá khứ, nhưng hiện nay hiếm khi được sử dụng bao gồm:
Megestrol acetate (Megace), một loại thuốc giống progesterone
Androgen (hormone nam), giống như testosterone
Estradiol (một dạng estrogen)
Mặc dù những thuốc này thường gây ra nhiều tác dụng phụ nhưng đây có thể là những lựa chọn nếu các liệu pháp hormone khác không còn hiệu quả.
2.3. Liệu pháp nhắm trúng đích
Liệu pháp nhắm trúng đích là các loại thuốc nhắm vào mục tiêu là những protein (đích) trên các tế bào ung giúp chúng phát triển, di căn và sống lâu hơn. Thuốc nhắm trúng đích có tác dụng tiêu diệt hoặc làm chậm sự phát triển của các tế bào ung thư. Nhóm này có tác dụng phụ khác với hóa trị.
Các thuốc nhóm này đi vào máu và tiếp cận hầu hết mọi khu vực trong cơ thể giống như thuốc hóa trị để chống lại các tế bào ung thư đã di căn xa đến các cơ quan khác trong cơ thể. Thuốc nhắm trúng đích có thể có tác dụng ngay cả khi thuốc hóa trị không còn tác dụng. Một số loại thuốc nhắm trúng đích còn giúp tăng hiệu quả của các liệu pháp khác.
Có nhiều loại thuốc nhắm trúng đích trong điều trị ung thư vú như:
- Liệu pháp nhắm trúng đích cho ung thư vú dương tính với HER2
- Liệu pháp nhắm trúng đích cho ung thư vú dương tính với thụ thể hormone
- Liệu pháp nhắm trúng đích cho phụ nữ có đột biến gen BRCA
- Liệu pháp nhắm trúng đích cho ung thư vú có bộ ba âm tính (không có thụ thể estrogen, không có thụ thể progesterone, không có HER2)
2.3.1. Liệu pháp nhắm trúng đích cho ung thư vú dương tính với HER2
Trong khoảng 15% đến 20% trường hợp ung thư vú, các tế bào ung thư tạo ra nhiều protein là thụ thể yếu tố tăng trưởng biểu bì 2 (HER2), nên được gọi là ung thư vú dương tính với HER2. Loại ung thư vú này thường phát triển và di căn mạnh hơn so với ung thư vú âm tính với HER2. Có nhiều loại thuốc nhắm vào protein HER2:
2.3.1.1. Kháng thể đơn dòng
Kháng thể đơn dòng là phiên bản protein của hệ thống miễn dịch (kháng thể) do con người tạo ra, được thiết kế để gắn vào một mục tiêu cụ thể. Trong trường hợp này, chúng gắn vào protein HER2 trên các tế bào ung thư, để ngăn chúng phát triển.
Trastuzumab (Herceptin): là dạng thuốc được tiêm vào đường tĩnh mạch (IV), dùng để điều trị cả ung thư vú giai đoạn đầu và giai đoạn tiến triển. Thuốc thường được dùng cùng với hóa trị, nhưng cũng có thể được sử dụng đơn trị. Khi bắt đầu trước (tân bổ trợ) hoặc sau (bổ trợ) phẫu thuật để điều trị ung thư vú giai đoạn đầu, thuốc này thường được dùng trong 6 tháng đến một năm. Đối với ung thư vú giai đoạn tiến triển, việc điều trị thường được thực hiện trong thời gian thuốc còn hiệu quả.
Một dạng khác của trastuzumab, được gọi là thuốc tiêm trastuzumab và hyaluronidase (Tên biệt dược là Herceptin Hylecta), được tiêm dưới da.
Pertuzumab (Perjeta): Kháng thể đơn dòng HER2 tiêm vào tĩnh mạch (IV). Thuốc này có thể được tiêm cùng với trastuzumab và hóa trị, trước hoặc sau phẫu thuật để điều trị ung thư vú giai đoạn đầu hoặc để điều trị ung thư vú giai đoạn tiến triển. Thuốc này được tiêm vào tĩnh mạch (IV).
Thuốc tiêm trastuzumab, pertuzumab và hyaluronidase (Phesgo): Đây là sự kết hợp của các loại kháng thể đơn dòng, dạng tiêm dưới da.
Margetuximab (Margenza): Kháng thể đơn dòng HER2, tiêm tĩnh mạch (IV), có thể được sử dụng cùng với hóa trị để điều trị ung thư vú tiến triển, thường là sau khi đã thử ít nhất 2 loại thuốc nhắm trúng đích HER2 khác.
2.3.1.2. Liên hợp kháng thể - thuốc
Liên hợp kháng thể - thuốc là kháng thể đơn dòng liên kết với thuốc hóa trị. Cơ chế tác động của nhóm thuốc này là kháng thể kháng HER2 hoạt động như tín hiệu dẫn đường bằng cách gắn vào protein HER2 trên tế bào ung thư, đưa thuốc hóa trị trực tiếp đến và tiêu diệt tế bào ung thư.
Ado-trastuzumab emtansine (Kadcyla): Liên kết giữa kháng thể kháng HER2 là trastuzumab với thuốc hóa trị emtansine. Thuốc này được truyền qua tĩnh mạch (IV) để điều trị ung thư vú giai đoạn đầu sau phẫu thuật (khi hóa trị và trastuzumab được dùng trước khi phẫu thuật và ung thư vẫn còn tại thời điểm phẫu thuật) hoặc để điều trị ung thư vú tiến triển ở những phụ nữ đã được điều trị bằng trastuzumab và hóa trị.
Fam-trastuzumab deruxtecan (Enhertu): Liên kết giữa kháng thể kháng HER2 là trastuzumab với thuốc hóa trị deruxtecan. Thuốc này được truyền qua tĩnh mạch (IV) để điều trị ung thư vú không thể loại bỏ bằng phẫu thuật hoặc đã di căn đến nơi khác trong cơ thể, thường là sau khi đã thử ít nhất 1 loại thuốc nhắm trúng đích HER2 khác.
Fam-trastuzumab deruxtecan cũng có thể được sử dụng để điều trị ung thư vú có lượng HER2 thấp và không thể loại bỏ bằng phẫu thuật hoặc đã di căn đến nơi khác trong cơ thể, thường là sau khi đã thử hóa trị hoặc nếu ung thư tái phát trong vòng 6 tháng sau khi kết thúc hóa trị bổ trợ.
2.3.1.3. Thuốc ức chế kinase
HER2 thuộc một nhóm protein có tên gọi là kinase. Kinase có vai trò truyền tín hiệu chẳng hạn như ra lệnh cho tế bào tăng trưởng phát triển. Thuốc ức chế kinase ngăn chặn việc truyền tín hiệu này, do đó ngăn không cho tế bào ung thư phát triển.
Lapatinib (Tykerb): là dạng thuốc viên uống. Lapatinib được sử dụng để điều trị ung thư vú tiến triển, thường được dùng cùng với trastuzumab và thuốc hóa trị capecitabine.
Neratinib (Nerlynx): là dạng thuốc viên uống. Neratinib được sử dụng để điều trị ung thư vú giai đoạn đầu sau khi điều trị bằng trastuzumab trong một năm và thuốc thường được dùng trong một năm. Thuốc cũng có thể được dùng cùng với thuốc hóa trị capecitabine để điều trị cho những trường hợp di căn, thường là sau khi đã thử ít nhất 2 loại thuốc nhắm trúng đích HER2 khác.
Tucatinib (Tukysa): là dạng thuốc viên uống, thường là hai lần một ngày. Tucatinib được sử dụng để điều trị ung thư vú tiến triển, sau khi đã thử ít nhất một loại thuốc nhắm trúng đích HER2 khác. Thuốc này thường được dùng cùng với trastuzumab và thuốc hóa trị capecitabine.
Tác dụng phụ của liệu pháp thuốc nhắm trúng đích HER2
Tác dụng phụ của nhóm thuốc này thường nhẹ, nhưng vẫn có trường hợp nặng. Không nên dùng nhóm thuốc này nếu bệnh nhân đang mang thai vì chúng có thể gây hại và thậm chí gây tử vong cho thai nhi. Trong trường hợp có thể có thai, hãy trao đổi với bác sĩ về các biện pháp tránh thai hiệu quả trong khi dùng những loại thuốc này.
Kháng thể đơn dòng và liên hợp thuốc - kháng thể có thể làm tổn thương tim trong hoặc sau khi điều trị và có thể dẫn đến suy tim sung huyết. Đối với hầu hết (nhưng không phải tất cả) trường hợp, tác dụng này chỉ kéo dài trong thời gian ngắn và sẽ cải thiện khi ngưng thuốc. Nguy cơ sẽ còn cao hơn khi dùng phối hợp những loại thuốc này với thuốc hóa trị có thể gây tổn thương tim, như doxorubicin (Adriamycin) và epirubicin (Ellence). Các yếu tố khác có thể làm tăng nguy cơ trên tim là trên 50 tuổi, thừa cân hoặc béo phì, đang có các vấn đề về tim và dùng thuốc điều trị tăng huyết áp.
Do nguy cơ gây tổn thương tim của nhóm thuốc này nên bác sĩ thường kiểm tra chức năng tim của bệnh nhân (VD siêu âm tim) trước và trong quá trình điều trị. Hãy báo bác sĩ biết nếu có các triệu chứng như khó thở, nhịp tim nhanh, phù chân và mệt.
Lapatinib, neratinib, tucatinib và phối hợp giữa pertuzumab với trastuzumab có thể gây tiêu chảy nặng.
Lapatinib và tucatinib cũng có thể gây ra hội chứng bàn tay-bàn chân, làm cho bàn tay và bàn chân bị đau và đỏ, có thể phồng rộp và bong tróc.
Lapatinib, neratinib và tucatinib có thể gây ra tác dụng phụ trên gan. Bác sĩ sẽ làm xét nghiệm máu để kiểm tra chức năng gan trong quá trình điều trị. Cần để ý và báo ngay khi có các dấu hiệu hoặc triệu chứng liên quan đến gan, như ngứa da, vàng da hoặc vàng mắt, nước tiểu sẫm màu hoặc đau ở vùng bụng trên bên phải (vùng hạ sườn bên phải).
Fam-trastuzumab deruxtecan (Enhertu) có thể gây tác dụng phụ nặng trên đường hô hấp. Cần báo ngay nếu xuất hiện có các triệu chứng như ho, thở khò khè, khó thở hoặc sốt.
2.3.2. Liệu pháp nhắm trúng đích cho ung thư vú dương tính với thụ thể hormone
Khoảng 3/4 trường hợp ung thư vú là có dương tính với thụ thể hormone (estrogen hoặc progesterone). Đối với loại ung thư này, điều trị bằng liệu pháp hormone thường hiệu quả. Một số loại thuốc điều trị nhắm trúng đích có thể giúp tăng hiệu quả của liệu pháp hormone, và cũng có thể làm tăng tác dụng phụ.
2.3.2.1. Thuốc ức chế CDK4/6
Palbociclib (Ibrance), ribociclib (Kisqali) và abemaciclib (Verzenio) là những loại thuốc ức chế các protein trong tế bào được gọi là kinase phụ thuộc cyclin (CDK), đặc biệt là CDK4 và CDK6. Việc ức chế các protein CDK này trong các tế bào ung thư vú dương tính với thụ thể hormone sẽ giúp ngăn chặn các tế bào phân chia. Từ đó làm chậm sự phát triển của ung thư.
Những loại thuốc này được chấp thuận để điều trị một số loại ung thư vú dương tính với thụ thể hormone, âm tính với HER2.
Nhóm thuốc này được chỉ định sử dụng trong nhiều trường hợp:
- Dùng cùng với thuốc ức chế aromatase hoặc fulvestrant cho những phụ nữ bị ung thư vú tiến triển đã mãn kinh.
- Dùng cùng với fulvestrant hoặc chất ức chế aromatase cho những phụ nữ bị ung thư vú tiến triển vẫn còn kinh nguyệt đều đặn hoặc sắp mãn kinh. Tuy nhiên, những phụ nữ này phải dùng thuốc để ngăn buồng trứng sản xuất estrogen như thuốc chủ vận hormone phóng thích hormone hoàng thể hóa (LHRH) hoặc cắt bỏ buồng trứng bằng phẫu thuật.
- Abemaciclib được sử dụng cho những phụ nữ bị ung thư vú tiến triển đã từng được điều trị bằng liệu pháp hormone và hóa trị.
- Đối với những phụ nữ bị ung thư vú giai đoạn đầu đã di căn đến các hạch bạch huyết và có khả năng tái phát cao sau phẫu thuật, abemaciclib có thể được dùng như một phương pháp điều trị bổ trợ cùng với tamoxifen hoặc ức chế aromatase. Thuốc thường được dùng trong 2 năm.
- Đối với phụ nữ bị ung thư vú giai đoạn II hoặc giai đoạn III có nguy cơ tái phát cao sau phẫu thuật, ribociclib có thể được dùng kết hợp với thuốc ức chế aromatase như một phương pháp điều trị bổ trợ, thường là trong 3 năm. Phụ nữ tiền mãn kinh cũng phải dùng thuốc ngăn buồng trứng sản xuất estrogen hoặc cắt bỏ buồng trứng bằng phẫu thuật.
Các thuốc nhóm này thường là dạng viên, uống một hoặc hai lần mỗi ngày.
Các tác dụng phụ phổ biến nhất của thuốc ức chế CDK4/6 là giảm tế bào máu và mệt mỏi. Buồn nôn, nôn, lở miệng, rụng tóc, tiêu chảy và đau đầu là những tác dụng phụ ít phổ biến hơn. Tác dụng phụ hạ thấp bạch cầu có thể làm tăng nguy cơ nhiễm trùng nặng. Một tác dụng phụ khác hiếm gặp nhưng có thể đe dọa tính mạng là bệnh phổi mô kẻ.
2.3.2.2. Thuốc ức chế mTOR
mTOR là một loại protein trong tế bào giúp chúng phân chia và phát triển. Everolimus (Afinitor) ức chế mTOR, có thể ngăn chặn khối u phát triển.
Everolimus dạng viên uống, thường là một lần một ngày, được sử dụng cho những phụ nữ đã mãn kinh và bị ung thư vú dương tính với thụ thể hormone, âm tính với HER2 ở giai đoạn tiến triển. Thuốc được sử dụng với thuốc ức chế aromatase là exemestane (Aromasin) cho những trường hợp ung thư tiến triển khi đang được điều trị bằng letrozole hoặc anastrozole (hoặc nếu ung thư bắt đầu tiến triển ngay sau khi ngừng điều trị bằng các loại thuốc này). Thuốc cũng có thể được sử dụng với thuốc nhóm nội tiết là fulvestrant.
Các tác dụng phụ thường gặp của everolimus bao gồm loét miệng, phát ban, tiêu chảy, buồn nôn, cảm thấy yếu hoặc mệt mỏi, giảm số lượng tế bào máu, khó thở và ho. Everolimus cũng có thể làm tăng lipid máu (cholesterol và triglyceride) và tăng đường huyết, vì vậy bác sĩ sẽ cho bệnh nhân xét nghiệm máu thường xuyên trong thời gian dùng thuốc. Thuốc này cũng có thể làm tăng nguy cơ nhiễm trùng nặng.
2.3.2.3. Thuốc ức chế PI3K
Alpelisib (Piqray) ức chế một dạng protein là PI3K trong tế bào ung thư, giúp ngăn chặn chúng phát triển. Thuốc dạng viên uống, thường là một lần một ngày.
Thuốc này có thể được sử dụng cùng với thuốc nội tiết fulvestrant để điều trị cho phụ nữ bị ung thư vú tiến triển dương tính với thụ thể hormone, âm tính với HER2 có đột biến gen PIK3CA và bệnh tiến triển trong khi hoặc sau khi điều trị bằng thuốc ức chế aromatase. Gen PIK3CA là gen ra lệnh cho tế bào tạo ra protein PI3K. Bác sĩ sẽ xét nghiệm máu hoặc khối u để tìm đột biến này trước khi bắt đầu điều trị bằng thuốc này.
Tác dụng phụ của alpelisib gồm phát ban trên da, tăng đường huyết, các tác dụng phụ trên thận, gan hoặc tuyến tụy, tiêu chảy, số lượng tế bào máu thấp, buồn nôn và nôn, mệt mỏi, chán ăn, lở miệng, sụt cân, hạ canxi máu, các vấn đề về đông máu và rụng tóc.
Có thể xảy ra các phản ứng da rất nghiêm trọng, chẳng hạn như phát ban kèm theo bong tróc và phồng rộp và cần báo cho bác sĩ. Những người có tiền sử phản ứng da nghiêm trọng nên báo cho bác sĩ trước khi dùng alpelisib. Có thể bác sĩ dùng thuốc kháng histamine để giúp ngăn ngừa phát ban. Bệnh nhân cũng được kiểm tra thường xuyên đường huyết.
2.3.2.4. Thuốc ức chế AKT
Capivasertib (Truqap) ức chế các protein AKT, là một phần của con đường truyền tín hiệu bên trong tế bào (bao gồm cả tế bào ung thư) để giúp chúng phát triển. Các protein khác trong con đường này bao gồm protein PI3K và PTEN.
Thuốc này được sử dụng cùng với thuốc nội tiết tố fulvestrant để điều trị ung thư vú tiến triển dương tính với thụ thể nội tiết tố, âm tính với HER2 khi các tế bào ung thư có những thay đổi ở bất kỳ gen PIK3CA, AKT1 hoặc PTEN và ung thư tiến triển trong khi hoặc sau khi điều trị bằng liệu pháp nội tiết tố. Bác sĩ sẽ xét nghiệm máu hoặc khối u của bệnh nhân để tìm những đột biến này trước khi bắt đầu điều trị bằng thuốc này.
Thuốc này được uống dưới dạng viên, thường là hai lần một ngày trong 4 ngày, sau đó nghỉ 3 ngày mỗi tuần.
Tác dụng phụ của capivasertib bao gồm: Tăng đường huyết, tiêu chảy (có thể nghiêm trọng), phát ban da hoặc các phản ứng da khác. Có thể xảy ra các phản ứng da rất nghiêm trọng, chẳng hạn như phát ban kèm theo bong tróc và phồng rộp, và cần báo cho bác sĩ. Các tác dụng phụ có thể xảy ra khác bao gồm buồn nôn, nôn, lở miệng và thay đổi một số xét nghiệm máu.
2.3.2.5. Liên hợp kháng thể - thuốc
Liên hợp kháng thể - thuốc là kháng thể đơn dòng kết hợp với thuốc hóa trị. Kháng thể hoạt động như tín hiệu dẫn đường bằng cách gắn vào một protein cụ thể trên tế bào ung thư, đưa thuốc hóa trị trực tiếp đến tiêu diệt chúng.
Sacituzumab govitecan (Trodelvy): kháng thể đơn dòng gắn vào protein Trop-2 trên tế bào ung thư vú và đưa thuốc hóa trị trực tiếp đến tiêu diệt chúng. Một số tế bào ung thư vú có quá nhiều Trop-2, giúp chúng phát triển và lan rộng nhanh chóng.
Thuốc này được sử dụng để điều trị ung thư vú tiến triển dương tính với thụ thể hormone, âm tính với HER2, ở những người đã được điều trị bằng liệu pháp hormone và ít nhất 2 phác đồ hóa trị.
Thuốc được truyền tĩnh mạch (IV) hàng tuần trong 2 tuần, sau đó nghỉ một tuần, rồi bắt đầu lại.
Một số tác dụng phụ thường gặp của loại thuốc này bao gồm buồn nôn, nôn, tiêu chảy, táo bón, cảm thấy mệt mỏi, phát ban, chán ăn, rụng tóc, hạ hồng cầu và đau bụng. Các tác dụng phụ nghiêm trọng có thể bao gồm hạ bạch cầu nặng (làm tăng cao nguy cơ nhiễm trùng), tiêu chảy nặng và phản ứng truyền dịch (tương tự như phản ứng dị ứng) khi truyền thuốc. Thuốc thường được sử dụng trước mỗi đợt điều trị để giảm nguy cơ nôn và phản ứng truyền dịch.
2.3.3. Liệu pháp nhắm trúng đích cho phụ nữ có đột biến gen BRCA
Olaparib (Lynparza) và talazoparib (Talzenna) là những loại thuốc được gọi là chất ức chế PARP. Protein PARP giúp sửa chữa DNA bị hư hỏng bên trong tế bào. Các gen BRCA (BRCA1 và BRCA2) cũng giúp sửa chữa DNA nhưng theo một cơ chế khác. Đột biến ở một trong những gen BRCA ức chế quá trình sửa chữa DNA. Chất ức chế PARP hoạt động bằng cách chặn các protein PARP. Vì các tế bào khối u có gen BRCA đột biến đã gặp khó khăn trong việc sửa chữa DNA bị hư hỏng, nên việc chặn thêm các protein PARP sẽ làm chết tế bào khối u này. Thuốc nhóm này dạng viên, uống một hoặc hai lần một ngày, được chỉ định trong nhiều trường hợp:
- Dùng cho những phụ nữ có đột biến BRCA bị ung thư vú HER2 âm tính giai đoạn sớm sau phẫu thuật đã được điều trị bằng hóa trị (trước hoặc sau phẫu thuật) và có nguy cơ tái phát cao. Thuốc thường được dùng trong một năm.
- Olaparib và talazoparib có thể được sử dụng để điều trị ung thư vú HER2 âm tính tiến triển hoặc di căn ở phụ nữ có đột biến BRCA đã từng được hóa trị. Nếu là loại ung thư dương tính với thụ thể hormone, thì olaparib cũng có thể được sử dụng ở những phụ nữ đã từng được điều trị bằng liệu pháp hormone.
Chỉ một tỷ lệ nhỏ phụ nữ bị ung thư vú khi được sinh ra đã mang gen BRCA đột biến trong tất cả các tế bào của cơ thể. Còn trường hợp đột biến gen xuất hiện sau sinh thì khác: Đột biến gen chỉ có trong các tế bào ung thư. Bác sĩ sẽ cho làm xét nghiệm máu để xem có đột biến gen BRCA hay không, trước khi bắt đầu điều trị bằng các loại thuốc này.
Các tác dụng phụ của thuốc gồm buồn nôn, nôn, tiêu chảy, mệt mỏi, chán ăn, thay đổi vị giác, giảm hồng cầu (gây thiếu máu), giảm tiểu cầu và bạch cầu. Hiếm khi, thuốc ức chế PARP gây ung thư máu, chẳng hạn như hội chứng loạn sản tủy hoặc bệnh bạch cầu tủy cấp tính (AML).
2.3.4. Liệu pháp nhắm trúng đích cho ung thư vú bộ ba âm tính
Trong ung thư vú bộ ba âm tính, các tế bào ung thư không có thụ thể estrogen hoặc progesterone và chúng tạo ra rất ít hoặc không tạo ra protein HER2.
Liên hợp kháng thể-thuốc
Sacituzumab govitecan (Trodelvy): Phần kháng thể đơn dòng gắn vào protein Trop-2 trên tế bào ung thư vú và đưa thuốc hóa trị, trực tiếp đến tiêu diệt chúng.
Liên hợp kháng thể-thuốc này có thể được sử dụng riêng lẻ để điều trị ung thư vú bộ ba âm tính tiến triển, sau khi đã thử ít nhất 2 phác đồ hóa trị khác. Thuốc này được truyền tĩnh mạch (IV) hàng tuần trong 2 tuần, sau đó nghỉ một tuần, rồi bắt đầu lại.
Một số tác dụng phụ thường gặp của loại thuốc này gồm buồn nôn, nôn, tiêu chảy, táo bón, mệt mỏi, phát ban, chán ăn, rụng tóc, hạ hồng cầu và đau bụng. Các tác dụng phụ nghiêm trọng có thể gồm hạ bạch cầu nặng (làm tăng cao nguy cơ nhiễm trùng), tiêu chảy nặng và phản ứng truyền dịch (tương tự như phản ứng dị ứng) khi truyền thuốc. Thuốc thường được sử dụng trước mỗi đợt điều trị để giảm nguy cơ nôn và phản ứng truyền dịch.
2.4. Liệu pháp miễn dịch
Liệu pháp miễn dịch là sử dụng thuốc tăng cường hệ miễn dịch của cơ thể, để nhận diện và tiêu diệt tế bào ung thư. Liệu pháp miễn dịch thường tác động lên các protein chuyên biệt để tăng cường phản ứng miễn dịch. Các loại thuốc này có tác dụng phụ khác với hóa trị.
Một số loại thuốc thuộc liệu pháp miễn dịch, ví dụ như kháng thể đơn dòng, hoạt động theo nhiều cơ chế để kiểm soát tế bào ung thư và cũng có thể được xem là liệu pháp nhắm trúng đích vì chúng ức chế một loại protein đích chuyên biệt trên tế bào ung thư để ngăn không cho chúng phát triển.
Thuốc ức chế “trạm kiểm soát” miễn dịch
Một đặc tính quan trọng của hệ miễn dịch là khả năng tự ngăn không cho nó tấn công các tế bào bình thường trong cơ thể. Để làm được điều này, các “trạm kiểm soát” bản chất là các protein trên các tế bào miễn dịch sẽ được bật (hoặc tắt) để phát hiện tác nhân lạ như tế bào ung thư và khởi động phản ứng miễn dịch chống lại chúng. Tuy nhiên, các tế bào ung thư vú đôi khi “qua mặt” được các trạm kiểm soát này và không bị hệ miễn dịch tấn công. Các loại thuốc nhắm vào các protein trạm kiểm soát này giúp khôi phục phản ứng miễn dịch chống lại các tế bào ung thư vú.
Thuốc ức chế PD-1
Pembrolizumab (Keytruda) là một loại thuốc nhắm vào PD-1 (một loại protein trên tế bào lympho T của hệ miễn dịch, giúp ngăn chúng tấn công các tế bào khác trong cơ thể). Bằng cách ức chế PD-1, thuốc sẽ thúc đẩy phản ứng miễn dịch chống lại các tế bào ung thư vú, làm giảm kích thước khối u.
Thuốc có thể được sử dụng cùng với hóa trị để điều trị ung thư vú bộ ba âm tính trong các trường hợp:
- Trước và sau phẫu thuật đối với ung thư giai đoạn 2 hoặc 3
- Ung thư tái phát tại chỗ nhưng không thể phẫu thuật cắt bỏ
- Ung thư đã di căn sang các nơi khác trong cơ thể.
Thuốc này được truyền tĩnh mạch (IV), thường là 3 hoặc 6 tuần một lần. Trong một số trường hợp nhất định, bác sĩ có thể xét nghiệm tế bào ung thư của bệnh nhân để tìm protein PD-L1, khi đó ung thư có nhiều khả năng đáp ứng với điều trị bằng pembrolizumab.
Tác dụng phụ của thuốc ức chế trạm kiểm soát miễn dịch gồm mệt mỏi, ho, buồn nôn, phát ban trên da, chán ăn, táo bón và tiêu chảy.
Các tác dụng phụ nghiêm trọng ít xảy ra hơn.
Phản ứng truyền dịch: Một số người có thể bị phản ứng truyền dịch, giống như phản ứng dị ứng, bao gồm sốt, ớn lạnh, đỏ bừng mặt, phát ban, ngứa da, chóng mặt, thở khò khè và khó thở. Cần phải báo ngay cho bác sĩ hoặc y tá nếu có bất kỳ triệu chứng nào trong số này.
Phản ứng tự miễn: Loại thuốc này loại bỏ một trong những lớp bảo vệ của hệ miễn dịch trong cơ thể. Do đó, có đôi khi hệ miễn dịch tấn công các cơ quan trong cơ thể (như phổi, tiêu hóa, gan, thận, cơ quan nội tiết…), gây ra các triệu chứng nghiêm trọng hoặc thậm chí đe dọa tính mạng.
Điều đặc biệt quan trọng là phải báo cáo ngay cho bác sĩ hoặc y tá nếu xảy ra tác dụng phụ nghiêm trọng, có thể cần phải ngừng điều trị và bác sĩ có thể cho bệnh nhân sử dụng corticosteroid liều cao để ức chế hệ miễn dịch.
3. Các phương pháp điều trị phổ biến
Thông thường, phương pháp điều trị được chọn dựa trên loại và giai đoạn của ung thư vú. Các yếu tố khác, bao gồm sức khỏe tổng thể, tình trạng mãn kinh và mong muốn cá nhân của bệnh nhân cũng được cân nhắc.
3.1. Điều trị ung thư vú theo giai đoạn
Giai đoạn ung thư vú là một yếu tố quan trọng để đưa ra quyết định về các lựa chọn điều trị. Nhìn chung, ung thư vú càng xâm lấn thì càng cần điều trị nhiều hơn. Nhưng các yếu tố khác cũng có thể quan trọng, chẳng hạn như:
- Tế bào ung thư có thụ thể hormone không (tức là ung thư dương tính với thụ thể estrogen hoặc dương tính với thụ thể progesterone)
- Tế bào ung thư có lượng lớn protein HER2 không (tức là ung thư dương tính với HER2)
- Tế bào ung thư có đột biến gen không
- Sức khỏe tổng thể và mong muốn cá nhân của bệnh nhân
- Tình trạng kinh nguyệt (đã mãn kinh hay chưa)
- Tốc độ tiến triển của ung thư và có ảnh hưởng đến các cơ quan lớn như phổi hoặc gan hay chưa
Các giai đoạn ung thư vú:
Giai đoạn 0
Ung thư giai đoạn 0 chỉ giới hạn ở bên trong ống tuyến vú và không xâm lấn các mô lân cận.
Ung thư biểu mô ống tuyến vú tại chỗ (DCIS) là khối u vú giai đoạn 0.
Ung thư biểu mô tiểu thùy tại chỗ (LCIS) từng được phân loại là giai đoạn 0, nhưng điều này đã được thay đổi vì nó không phải là ung thư. Tuy nhiên, ung thư biểu mô tiểu thùy tại chỗ làm tăng nguy cơ ung thư vú.
Giai đoạn I-III
Điều trị ung thư vú giai đoạn I đến III thường bao gồm phẫu thuật và xạ trị, thường kết hợp với hóa trị hoặc các thuốc khác trước (tân bổ trợ) hoặc sau (bổ trợ) phẫu thuật.
- Giai đoạn I: U vẫn còn tương đối nhỏ và chưa di căn đến các hạch bạch huyết hoặc chỉ có một vùng nhỏ ung thư ở hạch bạch huyết gác cửa (hạch bạch huyết đầu tiên mà ung thư có thể di căn đến).
- Giai đoạn II: U giai đoạn này lớn hơn ung thư giai đoạn I và/hoặc đã di căn đến một vài hạch bạch huyết lân cận.
- Giai đoạn III: Khối u lớn hơn hoặc đang xâm lấn vào các mô xung quanh (da trên vú hoặc cơ bên dưới), hoặc đã di căn đến nhiều hạch bạch huyết lân cận.
Giai đoạn IV (ung thư vú di căn): Ung thư đã di căn khỏi vú và các hạch bạch huyết lân cận để đến các cơ quan khác trong cơ thể.
Ung thư vú tái phát
Ung thư được gọi là tái phát khi nó tái xuất hiện sau khi điều trị. Tái phát có thể là cục bộ (ở cùng một bên vú), vùng (ở các hạch bạch huyết lân cận) hoặc ở xa. Điều trị ung thư vú tái phát phụ thuộc vào vị trí khối u tái phát và những phương pháp điều trị trước đó.
3.1.1. Điều trị ung thư biểu mô ống tuyến vú tại chỗ
Ung thư biểu mô ống tuyến vú tại chỗ là các tế bào lót ống tuyến vú trở thành tế bào ung thư, nhưng không xâm lấn vào mô vú xung quanh nên được xem là ung thư vú không xâm lấn hoặc tiền xâm lấn. Mặc dù ung thư biểu mô ống tuyến vú tại chỗ thường không xâm lấn ra khỏi vú, nhưng cần được điều trị vì nếu không điều trị thì một số tế bào ung thư có thể biến đổi bất thường, khiến nó trở thành ung thư vú xâm lấn và có thể di căn.
Trong hầu hết các trường hợp ung thư biểu mô ống tuyến vú tại chỗ, có thể lựa chọn giữa phẫu thuật bảo tồn vú và phẫu thuật cắt trọn vú. Nhưng nếu tế bào ung thư hiện diện ở khắp vú, thì phẫu thuật cắt trọn vú phù hợp hơn.
Phẫu thuật bảo tồn vú
Bác sĩ cắt bỏ khối u và một lượng nhỏ mô vú bình thường xung quanh khối u. Thường không cần cắt bỏ hạch bạch huyết trong ca phẫu thuật bảo tồn vú.
Sau đó bệnh nhân sẽ được xạ trị để giảm nguy cơ tái phát ung thư ở cùng một bên vú. Phẫu thuật bảo tồn vú mà không có xạ trị không phải là phương pháp điều trị chuẩn, nhưng có thể là lựa chọn phù hợp cho phụ nữ lớn tuổi, phụ nữ có bệnh đồng mắc khác, hoặc phụ nữ có mô ung thư nhỏ và đã được cắt rộng (cắt nhiều mô lành xung quanh khối u).
Phẫu thuật cắt trọn vú
Bác sĩ thường chọn cách này nếu vùng mô ung thư lớn, hoặc có nhiều vùng mô ung thư riêng biệt ở các góc phần tư vú khác nhau, hay khi không thể cắt bỏ hoàn toàn mô ung thư bằng phẫu thuật bảo tồn. Khi phẫu thuật cắt trọn vú thì bác sĩ sẽ sinh thiết hạch lympho gác cửa vì thường là có xâm lấn hoặc thậm chí có thể phải cắt bỏ toàn bộ hạch nách.
Sau phẫu thuật cắt trọn vú đối thì thường không cần xạ trị và có thể chọn tái tạo vú ngay hoặc sau đó.
Liệu pháp hormone sau phẫu thuật vú
Nếu ung thư vú này dương tính với thụ thể hormone (estrogen hoặc progesterone), thì điều trị bằng tamoxifen (cho mọi phụ nữ) hoặc bằng thuốc ức chế aromatase, chẳng hạn như exemestane hoặc anastrozole (cho phụ nữ đã mãn kinh) trong 5 năm sau phẫu thuật có thể làm giảm nguy cơ tái phát hoặc xâm lấn.
3.1.2. Điều trị ung thư vú giai đoạn I
Những khối ung thư vú này vẫn còn khá nhỏ và chưa di căn đến các hạch bạch huyết hoặc chỉ di căn đến một vùng nhỏ hạch bạch huyết gác cửa.
Liệu pháp tại chỗ (phẫu thuật và xạ trị)
Phẫu thuật là phương pháp điều trị chính cho ung thư vú giai đoạn I. Có thể phẫu thuật bảo tồn hoặc cắt trọn vú. Bác sĩ phẫu thuật cũng cần kiểm tra hạch bạch huyết lân cận bằng cách sinh thiết hạch bạch huyết gác cửa hoặc cắt bỏ hạch bạch huyết nách.
Nếu bệnh nhân được phẫu thuật bảo tồn vú thì xạ trị thường được thực hiện sau phẫu thuật để giảm nguy cơ ung thư tái phát.
Một số trường hợp, tái tạo vú có thể được thực hiện ngay trong ca phẫu thuật ung thư vú. Nhưng nếu bệnh nhân cần xạ trị sau phẫu thuật, thì nên đợi đến khi xạ trị hoàn tất mới tiến hành phẫu thuật tái tạo vú.
Trường hợp phụ nữ ≥ 65 tuổi có thể cân nhắc phẫu thuật bảo tồn vú mà mà không cần xạ trị nếu có đủ các điều kiện dưới đây:
- Khối u có đường kính ≤ 3 cm và đã được cắt bỏ hoàn toàn.
- Không có hạch bạch huyết nào được cắt bỏ có tế bào ung thư.
- Ung thư có thụ thể estrogen dương tính hoặc thụ thể progesterone dương tính và sẽ được điều trị bằng liệu pháp hormone.
Nếu phẫu thuật cắt trọn vú thì thường không cần xạ trị. Tuy nhiên, vẫn có trường hợp cần phải xạ trị tùy theo đánh giá của bác sĩ.
Liệu pháp toàn thân (hóa trị và các loại thuốc khác)
Nếu ung thư vú dương tính với thụ thể hormone thì bác sĩ thường sẽ chỉ định sử dụng liệu pháp hormone (tamoxifen hoặc thuốc ức chế aromatase) sau khi phẫu thuật, gọi là hóa trị bổ trợ sau phẫu thuật, bất kể khối u nhỏ đến mức nào. Liệu pháp hormone thường được sử dụng trong ít nhất 5 năm.
Nhiều phụ nữ lớn tuổi sẽ được cân nhắc xem có nên hóa trị hay không. Nhiều bác sĩ cũng có thể đề nghị hóa trị cho các khối u nhỏ hơn, đặc biệt là khi khối u có đặc điểm bất lợi (VD ung thư phát triển nhanh; âm tính với thụ thể hormone, dương tính với HER2; hoặc xét nghiệm gen Oncotype DX có điểm số cao).
Sau phẫu thuật, một số trường hợp ung thư vú có HER2 dương tính sẽ được điều trị bằng trastuzumab (cùng với hoặc không cùng với pertuzumab) trong tối đa 1 năm.
Nhiều trường hợp ung thư vú HER2 dương tính sẽ được điều trị bằng hóa trị tân bổ trợ (trước phẫu thuật) và trastuzumab (cùng với hoặc không cùng với pertuzumab) sau đó là phẫu thuật và thêm trastuzumab (cùng với hoặc không cùng với pertuzumab) trong tối đa 1 năm. Nếu sau liệu pháp tân bổ trợ mà ung thư vẫn còn hiện diện tại thời điểm phẫu thuật, thì có thể đổi trastuzumab sang một loại thuốc khác, gọi là ado-trastuzumab emtansine, được dùng 14 liều mỗi 3 tuần.
Đối với những phụ nữ có đột biến gen BRCA và ung thư vú dương tính với hormone, âm tính với HER2 đã được hóa trị tân bổ trợ mà ung thư vẫn còn hiện diện tại thời điểm phẫu thuật, thì có thể dùng thuốc nhắm trúng đích olaparib sau phẫu thuật, thường dùng trong một năm.
3.1.3. Điều trị ung thư vú giai đoạn II
Ung thư vú giai đoạn II lớn hơn ung thư giai đoạn I và/hoặc đã di căn đến một vài hạch bạch huyết lân cận.
Liệu pháp tại chỗ (phẫu thuật và xạ trị)
Ung thư giai đoạn II được điều trị bằng phẫu thuật bảo tồn vú hoặc cắt trọn vú. Các hạch bạch huyết gần đó cũng sẽ được kiểm tra, bằng cách sinh thiết hạch gác cửa hoặc cắt bỏ hạch nách.
Sau phẫu thuật bảo tồn thường là xạ trị. Xạ trị cũng được chỉ định ở những trường hợp phẫu thuật cắt trọn vú và ung thư đã xâm lấn hạch bạch huyết.
Nếu ban đầu bệnh nhân được chẩn đoán mắc ung thư vú giai đoạn II và được điều trị toàn thân như hóa trị hoặc liệu pháp hormone trước khi phẫu thuật, xạ trị vẫn có thể được khuyến nghị nếu phát hiện ung thư xâm lấn ở các hạch bạch huyết trong quá trình phẫu thuật cắt trọn vú.
Trong trường hợp bệnh nhân vẫn cần hóa trị sau phẫu thuật, thì xạ trị sẽ được hoãn lại cho đến khi hóa trị hoàn tất.
Trong một số trường hợp, tái tạo vú có thể được thực hiện ngay trong ca phẫu thuật điều trị cắt bỏ ung thư. Nhưng nếu bệnh nhân cần xạ trị sau phẫu thuật, thì nên đợi đến khi xạ trị hoàn tất mới tiến hành tái tạo.
Liệu pháp toàn thân (hóa trị và các loại thuốc khác)
Liệu pháp toàn thân được khuyến nghị cho ung thư vú giai đoạn II và có thể được tiến hành trước khi phẫu thuật (liệu pháp tân bổ trợ) hoặc sau khi phẫu thuật (liệu pháp bổ trợ) hoặc có thể cả trước và sau khi phẫu thuật. Liệu pháp tân bổ trợ phù hợp cho những phụ nữ có khối u lớn, vì có thể làm khối u nhỏ lại trước khi phẫu thuật, khi đó có khi chỉ cần phẫu thuật bảo tồn vú.
Liệu pháp tân bổ trợ cũng là một lựa chọn ưu tiên cho ung thư vú bộ ba âm tính hoặc ung thư vú dương tính với HER2 vì chọn lựa phương pháp điều trị sau phẫu thuật sẽ tùy thuộc vào tình trạng lúc phẫu thuật đánh giá tế bào ung thư còn hiện diện nhiều hay ít tại vú và hạch lân cận. Một số trường hợp ung thư giai đoạn đầu được điều trị tân bổ trợ có thể sống lâu hơn nếu ung thư biến mất hoàn toàn bằng phương pháp điều trị đó.
Để giúp quyết định trường hợp ung thư vú giai đoạn II dương tính với thụ thể hormone, âm tính với HER2 nào phù hợp với hóa trị, có thể cân nhắc làm xét nghiệm gen Oncotype DX trên mẫu khối u.
Các loại thuốc được sử dụng phụ thuộc vào tình trạng mãn kinh và kết quả xét nghiệm khối u, gồm:
- Hóa trị: Có thể dùng hóa trị trước và/hoặc sau phẫu thuật.
- Thuốc nhắm trúng đích HER2: Ung thư dương tính với HER2 sẽ được điều trị bằng hóa trị bổ trợ (sau phẫu thuật) với trastuzumab cùng với hoặc không cùng với pertuzumab trong tối đa 1 năm. Cũng có nhiều trường hợp ung thư dương tính với HER2 được điều trị tân bổ trợ trước phẫu thuật bằng trastuzumab (cùng với hoặc không cùng với pertuzumab), rồi phẫu thuật và sau đó là trastuzumab (cùng với hoặc không cùng với pertuzumab) trong tối đa một năm. Nếu sau liệu pháp tân bổ trợ, phát hiện ung thư vẫn còn sót lại tại thời điểm phẫu thuật, có thể sử dụng thuốc nhắm trúng đích ado-trastuzumab emtansine thay cho trastuzumab. Thuốc được dùng 3 tuần một lần với 14 liều. Đối với ung thư dương tính với thụ thể hormone được tìm thấy ở các hạch bạch huyết sau 1 năm điều trị bằng trastuzumab, có thể điều trị bổ sung bằng thuốc nhắm trúng đích đường uống là neratinib trong 1 năm.
- Liệu pháp hormone: Nếu ung thư dương tính với thụ thể hormone thì liệu pháp hormone (tamoxifen, thuốc ức chế aromatase) sẽ được sử dụng. Liệu pháp này có thể bắt đầu trước khi phẫu thuật, nhưng vì dùng thuốc kéo dài ít nhất 5 năm nên có thể sử dụng sau phẫu thuật.
- Liệu pháp thuốc nhắm trúng đích: Đối với phụ nữ bị ung thư vú giai đoạn đầu dương tính với thụ thể hormone, âm tính với HER2, có ung thư xâm lấn các hạch bạch huyết và có nguy cơ tái phát cao, có thể dùng thuốc nhắm trúng đích abemaciclib sau phẫu thuật cùng với tamoxifen hoặc thuốc ức chế aromatase. Đối với những phụ nữ có đột biến BRCA có ung thư vú dương tính với thụ thể hormone, âm tính với HER2, và sau hóa trị tân bổ trợ vẫn còn ung thư trong mô được phẫu thuật cắt bỏ, thuốc nhắm trúng đích olaparib có thể được dùng trong một năm để giúp giảm nguy cơ ung thư tái phát.
- Liệu pháp miễn dịch: Phụ nữ mắc ung thư vú bộ ba âm tính có thể dùng thuốc miễn dịch là pembrolizumab trước khi phẫu thuật và sau đó dùng lại sau khi phẫu thuật. Xem thêm chi tiết ở mục Điều trị ung thư vú bộ ba âm tính bên dưới.
3.1.4. Điều trị ung thư vú giai đoạn III
Ở giai đoạn III của ung thư vú, khối u lớn (hơn 5 cm) hoặc xâm lấn vào các mô lân cận (da trên vú hoặc cơ bên dưới), hoặc ung thư đã di căn đến nhiều hạch bạch huyết gần đó.
Có hai cách tiếp cận điều trị ung thư vú giai đoạn III:
Bắt đầu bằng liệu pháp tân bổ trợ
Thông thường, bệnh nhân sẽ được hóa trị trước phẫu thuật (tân bổ trợ). Đối với ung thư dương tính với HER2, trastuzumab sẽ được chỉ định sử dụng, thường dùng cùng với pertuzumab (Perjeta). Thuốc có thể làm khối u co nhỏ lại, đủ để phẫu thuật bảo tồn vú. Nếu khối u không nhỏ lại đủ, phẫu thuật cắt trọn vú sẽ được tiến hành. Các hạch bạch huyết lân cận cũng sẽ được kiểm tra xem ung thư đã xâm lấn chưa. Sinh thiết hạch gác cổng thường không phải là lựa chọn cho ung thư giai đoạn III, thường bác sĩ phải cắt bỏ hạch bạch nách.
Xạ trị thường được tiến hành sau phẫu thuật. Nếu có kế hoạch tái tạo vú, thường sẽ trì hoãn cho đến sau khi xạ trị xong. Một số trường sau phẫu thuật cũng cần hóa trị bổ sung.
Sau phẫu thuật, ung thư dương tính với HER2 sẽ được điều trị bằng trastuzumab (cùng với hoặc không cùng với pertuzumab) trong tối đa một năm. Nhiều trường hợp ung thư dương tính với HER2 sẽ được điều trị đầu tiên bằng trastuzumab (cùng với hoặc không cùng với pertuzumab), kế đến là phẫu thuật và sau đó là trastuzumab (cùng với hoặc không cùng với pertuzumab) trong tối đa một năm. Nếu sau liệu pháp tân bổ trợ, lúc đến lúc phẫu thuật vẫn còn thấy ung thư thì có thể sử dụng ado-trastuzumab emtansine thay cho trastuzumab. Thuốc được dùng 3 tuần một lần trong 14 liều. Trường hợp hạch bạch huyết có tế bào ung thư dương tính với thụ thể hormone ở bệnh nhân đã dùng trastuzumab trong một năm, có thể điều trị bổ sung trong một năm bằng thuốc nhắm trúng đích đường uống là neratinib.
Nếu ung thư vú dương tính với thụ thể hormone (tế bào ung thư có thụ thể estrogen hoặc có thụ thể progesterone) thì sẽ được điều trị bằng liệu pháp hormone bổ trợ, thường có thể dùng cùng lúc với trastuzumab.
Trường hợp ung thư vú có tế bào ung thư ở hạch bạch huyết dương tính với thụ thể hormone, âm tính với HER2 và có khả năng tái phát cao, có thể dùng abemaciclib sau phẫu thuật cùng với tamoxifen hoặc thuốc ức chế aromatase.
Đối với những phụ nữ có đột biến BRCA có ung thư vú dương tính với thụ thể hormone, âm tính với HER2, và sau hóa trị tân bổ trợ vẫn còn ung thư trong mô được phẫu thuật cắt bỏ, thuốc nhắm trúng đích olaparib có thể được dùng trong một năm để giúp giảm nguy cơ ung thư tái phát.
Liệu pháp tân bổ trợ là lựa chọn ưu tiên cho những phụ nữ ung thư vú bộ ba âm tính giai đoạn III hoặc ung thư vú dương tính với HER2 vì chọn lựa phương pháp điều trị sau phẫu thuật sẽ tùy thuộc lúc phẫu thuật đánh giá tình trạng ung thư còn hiện diện nhiều hay ít tại mô vú và hạch lân cận. Một số trường hợp ung thư giai đoạn III được điều trị tân bổ trợ có thể sống lâu hơn nếu ung thư biến mất hoàn toàn bằng phương pháp điều trị đó.
Những phụ nữ ung thư vú bộ ba âm tính có thể được chỉ định dùng thuốc miễn dịch pembrolizumab trước khi phẫu thuật và sau đó dùng lại sau phẫu thuật. Xem thêm chi tiết ở mục Điều trị ung thư vú bộ ba âm tính bên dưới.
Bắt đầu bằng phẫu thuật
Bắt đầu điều trị bằng phẫu thuật cho một số trường hợp ung thư giai đoạn III khi những khối u khá lớn và/hoặc đã xâm lấn vào các mô lân cận. Lúc đó phẫu thuật thường được chọn là cắt trọn vú. Đối với những phụ nữ có vú khá lớn, phẫu thuật bảo tồn vú có thể là một lựa chọn nếu ung thư chưa xâm lấn vào các mô lân cận. Sinh thiết hạch gác cửa có thể là một lựa chọn cho một số ít bệnh nhân, đa số sẽ cần phải cắt bỏ hạch nách. Sau phẫu thuật thường là hóa trị bổ trợ và/hoặc liệu pháp hormone và/hoặc liệu pháp thuốc nhắm trúng đích và/hoặc điều trị trường hợp có HER2 dương tính (trastuzumab, pertuzumab hoặc neratinib) tùy thuộc vào đặc điểm của tế bào ung thư. Xạ trị cũng được khuyến nghị sau phẫu thuật.
3.1.5. Điều trị ung thư vú giai đoạn IV (di căn)
Ung thư giai đoạn IV đã di căn ra ngoài vú và các hạch lân cận để đến các bộ phận khác của cơ thể. Ung thư vú thường di căn xa đến xương, gan và phổi, cũng có thể đến não hoặc các cơ quan khác.
Đối với phụ nữ bị ung thư vú giai đoạn IV, liệu pháp toàn thân là phương pháp điều trị chính, bao gồm:
- Liệu pháp hormone
- Hóa trị
- Liệu pháp nhắm trúng đích
- Liệu pháp miễn dịch
- Phối hợp giữa những liệu pháp trên
Đôi khi Phẫu thuật và/hoặc xạ trị được chỉ định trong một số trường hợp.
Điều trị giai đoạn này với mục đích làm u nhỏ lại (hoặc làm chậm sự phát triển), cải thiện các triệu chứng và sống lâu hơn. Không thể chữa dứt ung thư giai đoạn này.
Điều trị toàn thân (bằng thuốc) cho ung thư vú giai đoạn IV
Việc điều trị thường tiếp tục cho đến khi ung thư bắt đầu phát triển trở lại hoặc cho đến khi bệnh nhân không thể dung nạp các tác dụng phụ của thuốc. Khi đó, bác sĩ sẽ đổi sang loại thuốc khác. Các thuốc được chọn lựa sử dụng giai đoạn IV phụ thuộc vào tình trạng thụ thể hormone, HER2, đột biến gen, thể trạng của bệnh nhân.
- Ung thư dương tính với thụ thể hormone
Liệu pháp hormone (tamoxifen hoặc chất ức chế aromatase thường được sử dụng trước cho bệnh nhân ung thư dương tính với thụ thể hormone (estrogen hoặc progesterone). Bác sĩ có thể kết hợp với một loại thuốc nhắm trúng đích như thuốc nhóm ức chế CDK4/6.
Nếu liệu pháp hormone không còn hiệu quả, có thể kết hợp với một loại thuốc nhắm trúng đích như everolimus, chất ức chế PI3K như alpelisib (Piqray) hoặc chất ức chế AKT như capivasertib (Truqap), nếu các tế bào ung thư có một số thay đổi gen nhất định.
Phụ nữ chưa mãn kinh thường được điều trị bằng tamoxifen hoặc bằng thuốc ức chế buồng trứng sản xuất hormone cùng với các loại thuốc khác.
- Ung thư âm tính với thụ thể hormone
Hóa trị là phương pháp điều trị chính vì liệu pháp hormone không có tác dụng đối với những trường hợp này.
- Ung thư dương tính với HER2
Liệu pháp đầu tiên thường được áp dụng là hóa trị kết hợp với trastuzumab (Herceptin) và pertuzumab (Perjeta), cả hai đều là thuốc nhắm trúng đích HER2. Nếu ung thư tiến triển, các lựa chọn khác gồm:
- Thuốc nhóm liên hợp thuốc-kháng thể
- Thuốc nhóm ức chế kinase phối hợp với thuốc nhắm trúng đích HER2 hoặc với thuốc hóa trị hoặc cả hai
- Đổi sang thuốc nhắm trúng đích HER2 khác và phối hợp với hóa trị
Liệu pháp hormone có thể được phối hợp với các thuốc này nếu ung thư dương tính với thụ thể hormone.
Ung thư có lượng HER2 thấp: Đối với ung thư vú được coi là HER2 thấp và đã di căn đến các vị trí xa, liên hợp thuốc-kháng thể fam-trastuzumab deruxtecan (Enhertu) có thể là một lựa chọn.
- Ung thư HER2 âm tính ở phụ nữ có đột biến gen BRCA
Những trường hợp này thường được điều trị bằng thuốc nhắm trúng đích nhóm chất ức chế PARP, chẳng hạn như olaparib hoặc talazoparib. Thuốc hóa trị và thuốc nội tiết tố cũng có thể được sử dụng để điều trị các trường hợp này.
- Ung thư vú bộ ba âm tính
Thuốc miễn dịch kết hợp với hóa trị có thể được sử dụng cho những trường hợp ung thư vú bộ ba âm tính tiến triển có khối u tạo ra protein PD-L1. Protein PD-L1 được tìm thấy ở khoảng 1/5 trường hợp ung thư vú bộ ba âm tính. Đối với những phụ nữ ung thư vú bộ ba âm tính và có đột biến BRCA, có thể cân nhắc dùng thuốc ức chế PARP (như olaparib hoặc talazoparib).
Có thể sử dụng liệu pháp miễn dịch với pembrolizumab cho các trường hợp ung thư vú bộ ba âm tính có các biến đổi về gen hoặc protein khác.
Đối với ung thư vú bộ ba âm tính không có bất kỳ thay đổi về gen hoặc protein nào, hóa trị đơn thuần hoặc liên hợp thuốc-kháng thể sacituzumab govitecan (Trodelvy) có thể là một lựa chọn.
Điều trị tại chỗ cho ung thư vú giai đoạn IV
Mặc dù điều trị toàn thân là phương pháp điều trị chính cho ung thư vú giai đoạn IV, nhưng đôi khi các phương pháp điều trị tại chỗ như phẫu thuật, xạ trị hoặc hóa trị cục bộ cũng được sử dụng để điều trị ung thư ở một vị trí nào đó trong cơ thể, hoặc để ngăn ngừa hay điều trị các triệu chứng hoặc biến chứng do ung thư gây ra.
Xạ trị và/hoặc phẫu thuật có thể được sử dụng trong một số trường hợp nhất định, chẳng hạn như:
- Khi khối u vú gây ra vết thương hở hoặc đau ở vú
- Để điều trị ung thư di căn, ví dụ như di căn não
- Để giúp ngăn ngừa hoặc điều trị gãy xương
- Khi ung thư chèn ép tủy sống
- Để điều trị tắc mạch máu ở gan
- Để giảm đau hoặc điều trị các triệu chứng khác
Trong một số trường hợp, bệnh nhân được hóa trị cục bộ (thuốc hóa trị được đưa trực tiếp vào một vùng nhất định, như vào dịch não tủy, được gọi là hóa trị nội tủy).
Nếu bác sĩ đề nghị các phương pháp điều trị tại chỗ, bệnh nhân cần biết mục tiêu của những phương pháp điều trị này: là để điều trị ung thư hay để ngừa hoặc điều trị triệu chứng do ung thư gây nên.
Điều trị giảm nhẹ triệu chứng
Phương pháp điều trị để giảm nhẹ các triệu chứng phụ thuộc vào vị trí ung thư di căn. Ví dụ, cơn đau do di căn xương có thể được điều trị bằng thuốc nhóm bisphosphonate như pamidronate (Aredia) hoặc axit zoledronic (Zometa) hoặc thuốc denosumab (Xgeva).
Ung thư tiến triển trong quá trình điều trị
Điều trị ung thư vú tiến triển thường có thể làm giảm kích thước khối u hoặc làm chậm sự phát triển của khối u (đôi khi trong nhiều năm), nhưng sau một thời gian sẽ giảm và không còn hiệu quả. Các lựa chọn điều trị tiếp theo khi đó phụ thuộc vào nhiều số yếu tố như phương pháp điều trị trước đó, vị trí khối u, tình trạng mãn kinh của phụ nữ, tổng trạng của bệnh nhân, mong muốn tiếp tục điều trị, tình trạng thụ thể hormone và tình trạng HER2 có thay đổi trên các tế bào ung thư hay không.
- Tiến triển trong quá trình điều trị bằng hormone
Đối với các loại ung thư dương tính với thụ thể hormone (estrogen hoặc progesterone) đang được điều trị bằng liệu pháp hormone, việc chuyển sang thuốc hormone khác và/hoặc thêm một loại thuốc nhắm trúng đích đôi khi có hiệu quả. Ví dụ:
Nếu letrozole (Femara) hoặc anastrozole (Arimidex) được dùng trước, thì sử dụng exemestane, có thể kết hợp với thuốc nhắm trúng đích everolimus (Afinitor), có thể là một lựa chọn.
Một lựa chọn khác có thể là elacestrant (Orserdu), fulvestrant (Faslodex) hoặc một thuốc ức chế aromatase khác, đôi khi kết hợp với một loại thuốc nhóm ức chế CDK4/6.
Nếu ung thư có đột biến gen PIK3CA và tiến triển khi đang điều trị bằng thuốc ức chế aromatase, thì có thể cân nhắc dùng fulvestrant kết hợp với thuốc nhắm trúng đích alpelisib (Piqray).
Nếu ung thư có đột biến gen PIK3CA, AKT1 hoặc PTEN, thì có thể cân nhắc dùng fulvestrant kết hợp với thuốc nhắm trúng đích capivasertib (Truqap).
Nếu ung thư không còn đáp ứng với bất kỳ loại thuốc nội tiết nào, liệu pháp miễn dịch, hóa trị hoặc thuốc ức chế PARP có thể là những lựa chọn tiếp theo tùy thuộc vào các đặc điểm của ung thư hoặc tình trạng biến đổi gen.
- Tiến triển trong khi hóa trị
Nếu ung thư không còn đáp ứng với một phác đồ hóa trị, thì có thể đổi sang phác đồ hóa trị khác. Nhiều loại thuốc hóa trị và nhiều cách phối hợp có thể vẫn còn hiệu quả. Tuy nhiên, khi mỗi lần ung thư tiến triển trong quá trình điều trị, thì hiệu quả của phác đồ kế tiếp thường sẽ giảm đi. Nhiều khi phải phối hợp thêm các thuốc miễn dịch vào hóa trị mới có hiệu quả.
- Tiến triển trong khi điều trị bằng thuốc nhắm trúng đích HER2
Các bệnh ung thư dương tính với HER2 không còn đáp ứng với trastuzumab (Herceptin) có thể đáp ứng với các loại thuốc nhắm vào protein HER2 khác. Các lựa chọn điều trị cho ung thư dương tính với HER2 gồm:
- Pertuzumab (Perjeta) với hóa trị và trastuzumab
- Ado-trastuzumab emtansine (Kadcyla)
- Fam-trastuzumab deruxtecan (Enhertu)
- Margetuximab (Margenza) với hóa trị
- Lapatinib (Tykerb) và thuốc hóa trị đường uống capecitabine
- Lapatinib và thuốc ức chế aromatase (cho trường hợp ung thư dương tính với thụ thể hormone)
- Neratinib (Nerlynx) và thuốc hóa trị capecitabine (cho trường hợp ung thư đã di căn đến não)
- Tucatinib (Tukysa), trastuzumab và thuốc hóa trị capecitabine (cho trường hợp ung thư đã di căn đến não)
Vì các liệu pháp hiện tại rất khó điều trị hiệu quả ung thư vú đã di căn, nên nếu bệnh nhân có sức khỏe tốt, có thể cân nhắc tham gia nghiên cứu lâm sàng (nếu phù hợp) để thử nghiệm một phương pháp điều trị mới hơn.
3.1.6. Điều trị ung thư vú tái phát
Ung thư vú có thể tái phát sau khi điều trị, có khi là nhiều năm sau đó. Tái phát có thể là cục bộ (u xuất hiện ở cùng một bên vú trước đây), vùng (ở các hạch bạch huyết lân cận) hoặc xa (ở cơ quan xa vú). Nếu ung thư được tìm thấy ở bên vú đối diện mà không có bất kỳ ung thư ở nơi nào khác trong cơ thể thì nhiều khả năng không phải là ung thư tái phát mà là một loại ung thư mới cần phải được chẩn đoán và điều trị phù hợp.
Điều trị tái phát tại chỗ
Đối với những trường hợp ung thư vú tái phát tại chỗ, phương pháp điều trị phụ thuộc vào những điều trị trước đây.
- Nếu đã phẫu thuật bảo tồn vú (chỉ cắt bỏ khối u), giờ tái phát tại chỗ ở vú thì sẽ được điều trị bằng phẫu thuật cắt trọn vú.
- Nếu phương pháp điều trị ban đầu là cắt trọn vú, giờ tái phát gần vị trí cắt trọn vú thì sẽ được điều trị bằng cách cắt bỏ khối u bất cứ khi nào có thể. Thường tiếp tục bằng xạ trị nếu chưa được thực hiện trước đó.
Trong cả hai trường hợp, các liệu pháp hormone, nhắm trúng đích (như trastuzumab), miễn dịch, hóa trị hoặc kết hợp của những liệu pháp này có thể được sử dụng sau phẫu thuật và/hoặc xạ trị. Những liệu pháp này cũng có thể được sử dụng nếu phẫu thuật hoặc xạ trị không phải là lựa chọn.
Điều trị tái phát vùng
Khi ung thư vú tái phát ở các hạch bạch huyết vùng lân cận (như hạch nách dưới cánh tay hoặc quanh xương đòn), thường sẽ điều trị bằng phẫu thuật cắt bỏ các hạch này. Sau đó là xạ trị chiếu tia vào khu vực này nếu trước đó chưa thực hiện. Điều trị toàn thân (như hóa trị, liệu pháp nhắm trúng đích hoặc liệu pháp hormone) cũng có thể được cân nhắc sau phẫu thuật.
Điều trị tái phát xa
Nhìn chung, những trường hợp ung thư vú tái phát ở các cơ quan khác trong cơ thể, chẳng hạn như xương, phổi hoặc não… sẽ được điều trị theo cùng cách như ung thư vú giai đoạn IV ở các cơ quan này khi mới được chẩn đoán. Xem lại mục Điều trị ung thư vú giai đoạn IV (di căn) ở trên. Điểm khác biệt duy nhất là các liệu pháp (bao gồm thuốc) mà bệnh nhân đã dùng trước đây có thể sẽ được hoặc không được sử dụng.
Ung thư vú tái phát khó điều trị. Nếu bệnh nhân có sức khỏe tốt, có thể cân nhắc tham gia nghiên cứu lâm sàng (nếu phù hợp) để thử nghiệm phương pháp điều trị mới hơn.
3.2. Điều trị ung thư vú bộ ba âm tính
Ung thư vú bộ ba âm tính không có thụ thể estrogen hoặc progesterone và cũng tạo ra quá ít hoặc không có protein HER2. Vì các tế bào ung thư không có các protein này nên liệu pháp hormone và thuốc nhắm vào HER2 không có tác dụng. Khi đó hóa trị là lựa chọn điều trị toàn thân chính. Và mặc dù ung thư vú bộ ba âm tính thường đáp ứng tốt với hóa trị lúc đầu, nhưng nó thường tái phát hơn so với các loại ung thư vú khác.
3.2.1. Ung thư vú ba âm tính giai đoạn I-III
Phẫu thuật trước: Nếu khối u giai đoạn đầu đủ nhỏ để có thể phẫu thuật cắt bỏ, thì có thể tiến hành phẫu thuật bảo tồn vú hoặc cắt trọn vú kèm theo kiểm tra hạch bạch huyết. Trong một số trường hợp, như khối u lớn hoặc nếu phát hiện hạch bạch huyết có ung thư xâm lấn, thì có thể tiến hành xạ trị sau phẫu thuật. Bệnh nhân cũng có thể được hóa trị sau phẫu thuật (hóa trị bổ trợ) để giảm nguy cơ ung thư tái phát. Đối với những phụ nữ có đột biến BRCA và khi phẫu thuật phát hiện có:
- Khối u lớn hơn 2cm nhưng không lớn hơn 5cm hoặc
- 1 đến 3 hạch bạch huyết nách (dưới cánh tay) có ung thư
thì thuốc nhắm trúng đích mục tiêu olaparib (Lynparza) có thể được dùng trong một năm sau hóa trị bổ trợ.
Phẫu thuật sau: Hóa trị thường được dùng trước phẫu thuật (hóa trị tân bổ trợ) đơn lẻ hoặc kết hợp với pembrolizumab (Keytruda) để thu nhỏ khối u có kích thước lớn và/hoặc hạch có ung thư. Nếu tế bào ung thư vẫn còn hiện diện trong mô được cắt bỏ bằng phẫu thuật sau khi đã dùng hóa trị tân bổ trợ, thì bác sĩ có thể chỉ định:
- Hóa trị đường uống có tên capecitabine (Xeloda) trong 18 đến 24 tuần.
- Pembrolizumab sau phẫu thuật (điều trị bổ trợ) để giảm nguy cơ ung thư tái phát.
- Thuốc nhắm trúng đích olaparib trong một năm cho những phụ nữ có đột biến BRCA để giúp giảm nguy cơ ung thư tái phát.
3.2.2. Ung thư vú bộ ba âm tính giai đoạn IV
Hóa trị thường được sử dụng đầu tiên khi ung thư đã di căn đến các bộ phận khác của cơ thể (giai đoạn IV). Các loại thuốc hóa trị phổ biến được sử dụng bao gồm anthracycline, taxanes, capecitabine, gemcitabine, eribulin và các loại khác. Thuốc hóa trị có thể được sử dụng riêng lẻ hoặc kết hợp.
Đối với những phụ nữ ung thư vú bộ ba âm tính có đột biến gen BRCA và ung thư không còn đáp ứng với các loại thuốc hóa trị ung thư vú thông thường, có thể cân nhắc các loại thuốc hóa trị chứa bạch kim (như cisplatin hoặc carboplatin) hoặc các loại thuốc nhắm trúng đích khác như thuốc ức chế PARP (ví dụ olaparib [Lynparza] hoặc talazoparib [Talzenna]).
Đối với ung thư vú bộ ba âm tính tiến triển trong đó các tế bào ung thư có protein PD-L1, phương pháp điều trị đầu tiên có thể là liệu pháp miễn dịch (pembrolizumab) phối hợp với hóa trị. Protein PD-L1 được tìm thấy trong khoảng 1/5 trường hợp ung thư vú bộ ba âm tính.
Đối với ung thư vú bộ ba âm tính tiến triển trong đó ít nhất 2 phương pháp điều trị bằng thuốc khác đã được thử, có thể sử dụng nhóm liên hợp kháng thể-thuốc sacituzumab govitecan (Trodelvy).
Đối với ung thư vú bộ ba âm tính tiến triển trong đó các tế bào ung thư có biểu hiện thay đổi bất thường hay có đột biến ở một số gen cụ thể, thì liệu pháp miễn dịch pembrolizumab có thể được sử dụng.
Phẫu thuật và xạ trị cũng có thể là lựa chọn trong một số trường hợp nhất định.
3.2.3. Ung thư vú bộ ba âm tính tái phát
Nếu ung thư vú bộ ba âm tính tái phát tại chỗ, mà không thể loại bỏ bằng phẫu thuật và tế bào ung thư tạo ra protein PD-L1, thì liệu pháp miễn dịch với thuốc pembrolizumab cùng với hóa trị là một lựa chọn. Các phương pháp điều trị khác cũng có thể cân nhắc tùy thuộc vào từng trường hợp cụ thể.
Nếu ung thư tái phát ở các cơ quan khác trong cơ thể, hóa trị hoặc liên hợp kháng thể-thuốc sacituzumab govitecan (Trodelvy) có thể được sử dụng.
Bất kể đang thuộc giai đoạn ung thư nào, tham gia vào thử nghiệm lâm sàng để thử phương pháp điều trị mới cho ung thư vú bộ ba âm tính cũng là một lựa chọn tốt vì loại ung thư này không phổ biến và thường có tiên lượng kém so với các loại ung thư vú khác.
3.3. Điều trị ung thư vú dạng viêm
Ung thư vú dạng viêm là một loại ung thư vú xâm lấn không phổ biến, thường làm da ở vú đỏ và nóng, cũng có thể làm cho da vú dày lên, rỗ trông giống như vỏ cam. Những thay đổi này là do các tế bào ung thư làm tắc nghẽn các mạch bạch huyết trên da vú.
Vì ung thư vú dạng viêm đã đến các mạch bạch huyết ở da và gây ra những thay đổi ở da nên khi được chẩn đoán, nó sẽ được xếp loại ít nhất là giai đoạn III. Ung thư vú dạng viêm đã di căn đến các bộ phận khác của cơ thể được coi là giai đoạn IV. Loại ung thư này thường tiến triển nhanh và khó điều trị.
Bất kể giai đoạn ung thư nào, việc tham gia thử nghiệm lâm sàng để thử phương pháp điều trị mới cho ung thư vú dạng viêm cũng là một lựa chọn tốt vì loại ung thư này rất hiếm và thường có tiên lượng xấu.
3.3.1. Điều trị ung thư vú dạng viêm giai đoạn III
Ung thư vú dạng viêm chưa xâm lấn ra khỏi vú hoặc đến các hạch bạch huyết lân cận là giai đoạn III. Thường bắt đầu bằng hóa trị để cố gắng thu nhỏ khối u. Nếu ung thư là HER2 dương tính, liệu pháp nhắm trúng đích được phối hợp cùng với hóa trị. Sau đó là phẫu thuật (cắt trọn vú và cắt bỏ hạch bạch huyết) để loại bỏ ung thư. Xạ trị thường được tiến hành sau phẫu thuật. Đôi khi, hóa trị sau phẫu thuật có thể được chỉ định rồi mới đến xạ trị. Nếu ung thư có thụ thể hormone dương tính, có thể điều trị bằng liệu pháp hormone (thường là sau khi đã tiến hành tất cả các đợt hóa trị). Việc kết hợp các phương pháp điều trị này giúp cải thiện đáng kể thời gian sống còn của bệnh nhân.
Hóa trị (có thể kết hợp với liệu pháp nhắm trúng đích)
Sử dụng hóa trị trước khi phẫu thuật được gọi là điều trị tân bổ trợ hoặc tiền phẫu thuật. Hầu hết các trường hợp ung thư vú dạng viêm sẽ được dùng hai loại thuốc hóa trị (dùng cùng lúc hoặc trước sau):
- Anthracycline, chẳng hạn như doxorubicin (Adriamycin) hoặc epirubicin (Ellence)
- Taxane, chẳng hạn như paclitaxel (Taxol) hoặc docetaxel (Taxotere)
Cũng có thể dùng các loại thuốc hóa trị khác.
Nếu ung thư dương tính với HER2, thuốc điều trị nhắm trúng đích trastuzumab (Herceptin) thường được dùng, đôi khi dùng cùng với một loại thuốc nhắm trúng đích khác như pertuzumab (Perjeta). Những thuốc này có thể gây tác dụng phụ trên tim khi dùng cùng với anthracycline, vì vậy có thể sử dụng anthracycline trước (không dùng trastuzumab hoặc pertuzumab), sau đó mới dùng taxane và trastuzumab (cùng với hoặc không cùng với pertuzumab).
Đối với ung thư vú dạng viêm bộ ba âm tính, thuốc miễn dịch pembrolizumab có thể được dùng cùng với hóa trị trước khi phẫu thuật (điều trị tân bổ trợ) và tiếp tục dùng sau phẫu thuật (điều trị bổ trợ).
Đối với những phụ nữ có:
- đột biến BRCA VÀ
- ung thư vú dạng viêm bộ ba âm tính hoặc âm tính với HER2 VÀ
- ung thư còn sót lại trong mô đã cắt bỏ bằng phẫu thuật sau khi hóa trị tân bổ trợ
thì thuốc nhắm trúng đích olaparib (Lynparza) có thể được dùng để giảm nguy cơ ung thư tái phát. Thuốc thường được dùng trong một năm.
Phẫu thuật và các phương pháp điều trị tiếp theo
Nếu ung thư được cải thiện bằng hóa trị, phẫu thuật thường là bước tiếp theo. Phẫu thuật tiêu chuẩn là cắt trọn vú tận gốc cải tiến, khi đó toàn bộ vú và các hạch bạch huyết dưới cánh tay được cắt bỏ. Vì ung thư vú dạng viêm ảnh hưởng rất nhiều đến vú và da nên phẫu thuật bảo tồn vú và cắt trọn vú bảo tồn da không phải là lựa chọn phù hợp.
Nếu ung thư không đáp ứng với hóa trị (và vú vẫn rất sưng và đỏ), thì không thể phẫu thuật. Khi đó sẽ thử đổi sang các loại thuốc hóa trị khác hoặc xạ trị. Sau đó, nếu ung thư có đáp ứng (vú co nhỏ lại và không còn đỏ nữa), thì có thể tiến hành phẫu thuật.
Nếu không xạ trị vú trước khi phẫu thuật, thì xạ trị sẽ được thực hiện sau phẫu thuật, ngay cả khi không còn thấy sót lại tế bào ung thư. Phương pháp này được gọi là xạ trị bổ trợ, để làm giảm khả năng ung thư tái phát. Xạ trị thường được thực hiện 5 ngày trong tuần, trong vòng 6 tuần. Trong một số trường hợp, có thể áp dụng xạ trị mạnh hơn (hai lần một ngày). Tùy thuộc vào lượng khối u được tìm thấy trong vú sau phẫu thuật, xạ trị có thể bị trì hoãn cho đến khi tiến hành xong hóa trị và/hoặc liệu pháp nhắm trúng đích (như trastuzumab) sau phẫu thuật. Tái tạo vú (nếu có) thường sẽ phải đợi đến khi kết thúc xạ trị sau phẫu thuật.
Điều trị sau phẫu thuật thường bao gồm điều trị toàn thân bổ sung (bổ trợ), bao gồm hóa trị, liệu pháp nhắm trúng đích, liệu pháp hormone (tamoxifen hoặc thuốc nhóm ức chế aromatase) nếu tế bào ung thư có thụ thể hormone, thuốc hóa trị đường uống capecitabine (Xeloda) nếu ung thư là loại bộ ba âm tính, chất ức chế PARP olaparib (Lynparza) nếu phụ nữ có đột biến BRCA và/hoặc trastuzumab, pertuzumab hoặc ado-trastuzumab emtansine nếu ung thư là HER2 dương tính.
3.3.2. Điều trị ung thư vú dạng viêm giai đoạn IV
Bệnh nhân ung thư vú dạng viêm di căn (giai đoạn IV) sẽ được điều trị bằng liệu pháp toàn thân:
- Hóa trị
- Liệu pháp nội tiết tố (nếu ung thư dương tính với thụ thể nội tiết tố)
- Liệu pháp nhắm trúng đích HER2 (nếu ung thư dương tính với HER2)
- Liệu pháp miễn dịch nếu ung thư tạo ra protein PD-L1
- Liệu pháp nhắm trúng đích bằng thuốc ức chế PARP, như olaparib nếu phụ nữ có đột biến BRCA
Có thể phối hợp hai hay nhiều liệu pháp ở trên tùy từng trường hợp cụ thể.
3.4. Điều trị ung thư vú trong thời kỳ mang thai
Nếu ung thư vú được chẩn đoán trong thời kỳ mang thai thì các lựa chọn điều trị sẽ phức tạp hơn vì vừa phải điều trị ung thư vừa phải bảo vệ thai nhi. Kế hoạch điều trị sẽ cần được bàn luận, hội chẩn liên chuyên khoa, giữa ung thư và sản khoa.
Có an toàn khi điều trị ung thư vú trong thời kỳ mang thai không?
Nếu đang mang thai và bị ung thư vú, bệnh nhân có thể phải đưa ra những lựa chọn khó khăn. Do đó hãy tìm kiếm sự giúp đỡ từ các chuyên gia để có thể hiểu hết những lựa chọn của mình. Phụ nữ mang thai có thể được điều trị ung thư vú một cách an toàn, mặc dù phương pháp và thời điểm điều trị có thể bị ảnh hưởng bởi thai kỳ. Nếu bệnh nhân đang mang thai và được chẩn đoán ung thư vú, các khuyến nghị điều trị sẽ phụ thuộc vào:
- Kích thước của khối u
- Vị trí của khối u
- Tình trạng di căn: ung thư đã di căn chưa và nếu có thì di căn đến đâu
- Đang ở giai đoạn nào của thai kỳ
- Sức khỏe tổng thể của bệnh nhân
- Ưu tiên chọn lựa cá nhân của bệnh nhân
Nói chung, phẫu thuật ung thư vú trong thời kỳ mang thai là an toàn. Hóa trị có thể an toàn cho em bé nếu được thực hiện trong tam cá nguyệt thứ hai hoặc thứ ba của thai kỳ, nhưng không an toàn trong tam cá nguyệt đầu tiên. Các phương pháp điều trị ung thư vú khác, như liệu pháp hormone, liệu pháp nhắm trúng đích và xạ trị, có nhiều khả năng gây hại cho em bé và thường không được sử dụng trong thời kỳ mang thai.
Các lựa chọn điều trị có thể trở nên phức tạp nếu cần cân nhắc giữa phương pháp điều trị tốt nhất cho mẹ và sức khỏe của thai nhi. Ví dụ, nếu được chẩn đoán ung thư vú vào đầu thai kỳ và cần hóa trị ngay lập tức, thì bệnh nhân có thể được khuyên nên cân nhắc chấm dứt thai kỳ. Chuyên gia tâm lý có thể giúp hỗ trợ về mặt tinh thần trong những trường hợp này.
Chấm dứt thai kỳ hiện không còn được khuyến nghị thường xuyên. Tuy nhiên, lựa chọn này cũng có thể được cân nhắc khi xem xét tất cả các lựa chọn điều trị hiện có, đặc biệt là đối với trường hợp ung thư đã di căn (giai đoạn IV) hoặc ung thư có độ ác tính cao cần điều trị ngay lập tức (VD như ung thư vú dạng viêm).
3.4.1. Phẫu thuật ung thư vú trong thời kỳ mang thai
Phẫu thuật cắt bỏ khối u ở vú và các hạch lân cận là phương pháp điều trị chính cho trường hợp ung thư vú giai đoạn đầu và thường an toàn trong thời kỳ mang thai. Lựa chọn phẫu thuật bao gồm:
- Phẫu thuật cắt trọn vú
- Phẫu thuật bảo tồn vú (chỉ cắt bỏ khối u, một phần vú)
Bệnh nhân sẽ được chỉ định loại phẫu thuật phù hợp dựa vào mức độ diễn tiến của ung thư và thời điểm chẩn đoán ung thư trong thời kỳ mang thai.
Kiểm tra hạch bạch huyết để phát hiện ung thư di căn
Ngoài việc cắt bỏ khối u ở vú, một hoặc nhiều hạch bạch huyết ở vùng dưới cánh tay (hạch nách) cũng được cắt bỏ để kiểm tra xem ung thư đã di căn tới chưa. Cắt bỏ hạch nách hoặc sinh thiết hạch gác cửa sẽ được chọn lựa tùy thuộc vào giai đoạn mang thai và giai đoạn ung thư. Trong sinh thiết hạch gác cửa, bác sĩ cắt bỏ ít hạch hơn, nhưng chất có hoạt tính phóng xạ được sử dụng trong thủ thuật này có thể gây hại thai nhi. Do đó sinh thiết hạch gác cửa được khuyến cáo chỉ nên sử dụng trong một số trường hợp nhất định như giai đoạn sau của thai kỳ và không nên sử dụng thuốc chứa hoạt tính phóng xạ màu xanh trong quá trình thực hiện.
Gây mê lúc mang thai có an toàn không?
Phẫu thuật ung thư vú thường ít gây hại cho em bé. Nhưng có một số thời điểm nhất định trong thai kỳ mà gây mê (thuốc dùng để khiến bệnh nhân ngủ trong ca mổ) có thể gây hại cho em bé.
Bác sĩ phẫu thuật, bác sĩ gây mê, cùng với bác sĩ sản khoa cần hội chẩn để quyết định thời điểm phẫu thuật tốt nhất trong thai kỳ. Nếu phải phẫu thuật ở thời điểm muộn trong thai kỳ, bác sĩ sản khoa có thể cũng sẽ có mặt trong phòng mổ, để phòng trường hợp có bất kỳ vấn đề nào xãy ra với em bé trong quá trình phẫu thuật. Loại thuốc và kỹ thuật gây mê nào là an toàn nhất cho cả mẹ và em bé cũng sẽ được thảo luận.
3.4.2. Điều trị sau phẫu thuật
Tùy thuộc vào giai đoạn ung thư, bệnh nhân có thể cần thêm liệu pháp khác sau phẫu thuật như hóa trị, xạ trị, liệu pháp hormone và/hoặc liệu pháp nhắm trúng đích để giúp giảm nguy cơ ung thư tái phát. Trong một số trường hợp, các phương pháp điều trị này có thể phải hoãn lại cho đến sau khi bệnh nhân sinh em bé.
Hóa trị
Hóa trị có thể được sử dụng sau phẫu thuật (hóa trị bổ trợ) cho ung thư vú giai đoạn sớm và giai đoạn tiến triển.
Không được hóa trị (chống chỉ định) trong 3 tháng đầu (tam cá nguyệt đầu tiên) của thai kỳ vì phần lớn sự phát triển của em bé diễn ra trong thời gian này, và độ an toàn của hóa trị đối với thai nhi trong tam cá nguyệt đầu tiên chưa được nghiên cứu. Nguy cơ sảy thai cũng là cao nhất trong giai đoạn này.
Trong nhiều năm, nhiều người cho rằng tất cả các loại hóa trị đều sẽ gây hại cho thai nhi bất kể sử dụng trong giai đoạn nào của thai kỳ. Nhưng các nghiên cứu đã chỉ ra rằng một số thuốc hóa trị (như doxorubicin, cyclophosphamide, fluorouracil và taxane) được sử dụng trong tam cá nguyệt thứ hai và thứ ba (tháng thứ 4 đến tháng thứ 9 của thai kỳ) không làm tăng nguy cơ dị tật bẩm sinh, thai chết lưu hoặc các vấn đề sức khỏe của em bé ngay sau khi sinh, mặc dù chúng có thể làm tăng nguy cơ sinh non. Chưa biết liệu những đứa trẻ này có bị tác dụng phụ lâu dài nào về sau này không.
Nếu bệnh nhân bị ung thư vú giai đoạn đầu và cần phải hóa trị sau phẫu thuật (hóa trị bổ trợ), thì thông thường hóa trị sẽ được trì hoãn cho đến ít nhất là tam cá nguyệt thứ hai. Nếu bệnh nhân được chẩn đoán ung thư vú đang trong tam cá nguyệt thứ ba, thì hóa trị có thể được trì hoãn cho đến sau khi sinh. Một số phụ nữ có thể sinh sớm hơn vài tuần. Những cách điều trị này cũng có thể được áp dụng cho những trường hợp ung thư tiến triển.
Hóa trị thường không được khuyến khích sau 35 tuần mang thai hoặc trong vòng 3 tuần trước khi sinh vì có thể làm giảm số lượng tế bào máu của mẹ, có thể gây chảy máu và làm tăng nguy cơ nhiễm trùng khi sinh. Việc trì hoãn hóa trị trong vài tuần cuối trước khi sinh là cần thiết để tránh những biến cố này.
Các biện pháp điều trị thường được hoãn lại cho đến sau khi sinh
Một số phương pháp điều trị ung thư vú có thể gây hại cho em bé và không an toàn trong thời kỳ mang thai. Nếu cần những phương pháp điều trị này, chúng thường được lên lịch sau khi em bé chào đời.
- Xạ trị: thường được sử dụng sau phẫu thuật bảo tồn vú để giúp giảm nguy cơ ung thư tái phát. Liều lượng tia xạ cao có thể gây hại cho em bé vào mọi thời điểm trong thai kỳ, có thể gây sảy thai, dị tật bẩm sinh, thai nhi chậm phát triển hoặc nguy cơ ung thư ở trẻ em cao hơn. Vì lý do này, bác sĩ không sử dụng phương pháp xạ trị trong thai kỳ.
Đối với một số trường hợp phát hiện ung thư muộn trong thai kỳ, có thể cắt bỏ khối u và sau đó đợi đến khi em bé chào đời mới tiến hành xạ trị. Tuy nhiên cách điều trị này vẫn chưa được nghiên cứu kỹ lưỡng. Việc trì hoãn xạ trị quá lâu có thể làm tăng nguy cơ ung thư tái phát.
- Liệu pháp hormone: thường được sử dụng để điều trị sau phẫu thuật hoặc để điều trị ung thư vú tiến triển trong trường hợp ung thư vú dương tính với thụ thể hormone (estrogen hoặc progesterone). Các loại thuốc điều trị hormone được sử dụng cho ung thư vú bao gồm tamoxifen, anastrozole, letrozole và exemestane.
Không nên dùng liệu pháp hormone trong thai kỳ vì có thể ảnh hưởng đến em bé. Nên trì hoãn cho đến sau khi sinh.
- Liệu pháp nhắm trúng đích: Các loại thuốc nhắm trúng đích HER2, chẳng hạn như trastuzumab (Herceptin), pertuzumab (Perjeta), ado-trastuzumab emtansine (Kadcyla) và lapatinib (Tykerb), rất quan trọng trong điều trị ung thư vú dương tính với HER2. Ở những phụ nữ không mang thai, trastuzumab rất thường được sử dụng để điều trị sau phẫu thuật, pertuzumab có thể được sử dụng cùng với trastuzumab trước khi phẫu thuật và tất cả các loại thuốc này thường có hiệu quả trong điều trị ung thư tiến triển. Nhưng dựa trên các nghiên cứu ở phụ nữ được điều trị trong thời kỳ mang thai, không có thuốc nào trong số này được xem là an toàn cho em bé nếu dùng trong thời kỳ mang thai.
Everolimus (Afinitor) và palbociclib (Ibrance) cũng là những loại thuốc nhắm trúng đích có thể được sử dụng với liệu pháp hormone để điều trị ung thư vú tiến triển. Tuy nhiên, những loại thuốc nhắm trúng đích này cũng được cho là không an toàn để sử dụng trong thời kỳ mang thai.
Có thể cho con bú trong quá trình điều trị ung thư vú không?
Hầu hết phụ nữ vừa sinh con và sắp được điều trị ung thư vú được khuyên là nên ngừng (hoặc không bắt đầu) cho con bú. Nhiều loại thuốc hóa trị, thuốc nội tiết và thuốc nhắm trúng đích có thể đi vào sữa mẹ và vào cơ thể em bé. Không nên cho con bú nếu bệnh nhân đang được điều trị bằng thuốc toàn thân và có thể cũng không nên cho con bú lại sau khi ngưng điều trị nhiều tháng. Có trường hợp ung thư vú hormone dương tính, bệnh nhân phải dùng thuốc để ngừng sản xuất sữa mẹ.
Nếu có kế hoạch phẫu thuật vú, việc ngừng cho con bú sẽ giúp giảm lượng máu đến vú và làm cho vú nhỏ lại. Điều này có thể giúp ích cho ca phẫu thuật, giúp giảm nguy cơ nhiễm trùng vú và tránh trường hợp sữa mẹ tích tụ nhiều ở các vùng sinh thiết hoặc phẫu thuật.
Việc mang thai có ảnh hưởng đến tỷ lệ sống còn không?
Mang thai có thể khiến việc phát hiện, chẩn đoán và điều trị ung thư vú trở nên khó khăn hơn. Hầu hết các nghiên cứu đều cho thấy kết quả là như nhau giữa phụ nữ mang thai và không mang thai bị ung thư vú cùng giai đoạn.
Chấm dứt thai kỳ giúp việc điều trị trở nên đơn giản hơn. Tuy nhiên, cho đến nay vẫn chưa có bằng chứng nghiên cứu lâm sàng nào kết luận rằng chấm dứt thai kỳ giúp cải thiện tiên lượng hay khả năng sống còn của ung thư vú.
Việc trì hoãn điều trị trong thai kỳ để tránh gây hại cho thai nhi ảnh hưởng đến kết quả điều trị ung thư vú như thế nào cũng chưa được kết luận. Nhưng đây cũng là một lĩnh vực khó nghiên cứu.
Cuối cùng, không có nghiên cứu nào kết luận bản thân bệnh ung thư vú có thể gây hại cho thai nhi.
BS. Trần Quốc Hùng
Ban Biên tập Y Khoa Online
-----------------------------------
Nguồn tham khảo:
https://www.cancer.org/cancer/types/breast-cancer.html. Truy cập ngày 30/09/2024
https://www.cancer.gov/publications/dictionaries/cancer-terms/def/ki-67-score. Truy cập ngày 01/10/2024
https://www.mayoclinic.org/diseases-conditions/lobular-carcinoma-in-situ/symptoms-causes/syc-20374529. Truy cập ngày 30/09/2024
-
Ung thư
18/11/2024 09:51 GMT+7
-
Viêm mũi xoang
15/11/2024 18:38 GMT+7
-
Bướu sợi tuyến vú
24/09/2024 21:25 GMT+7
-
Sởi
29/08/2024 11:12 GMT+7
-
Ung thư gan
28/12/2023 12:56 GMT+7
-
Lymphoma
04/10/2023 14:45 GMT+7
-
Ung thư hạch
04/10/2023 14:10 GMT+7
-
Thiếu máu trên bệnh nhân u lympho
04/10/2023 13:50 GMT+7
-
Lõm xương ức
14/08/2023 16:23 GMT+7
-
Lõm ngực
14/08/2023 15:59 GMT+7
-
Tay Chân Miệng ở trẻ nhỏ
17/07/2023 15:42 GMT+7
-
Viêm kết mạc ở trẻ sơ sinh
06/07/2023 16:16 GMT+7






